Новые гепариновые частицы и способы их применения
Иллюстрации
Показать всеИзобретение относится к медицине и касается медицинского субстрата, включающего гепариновые частицы, связанные на субстрате через, по меньшей мере, одну молекулу гепарина, причем эта гепариновая частица содержит, по меньшей мере, одну гепариновую молекулу и, по меньшей мере, одну каркасную молекулу, причем связанные гепариновые частицы чувствительны к гепариназе, и эта гепариновая частица связана с субстратом: по концевой точке, либо петлеобразно, либо через концевой альдегид, либо через альдегиды по всей длине данного гепарина. Изобретение обеспечивает значительную биологическую активность гепариновых частиц после иммобилизации, стерилизации, механического сжатия и растяжения и/или хранения по сравнению с другими покрытиями медицинских субстратов. 20 з.п. ф-лы, 6 ил., 3 табл., 19 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение касается медицинских субстратов, содержащих иммобилизованные активные частицы (entities), сохраняющие свою биологическую активность после стерилизации. В частности, настоящее изобретение касается новых гепариновых частиц и способов их применения.
Уровень техники
Хорошо известны медицинские устройства, служащие заменителями кровеносных сосудов, в качестве синтетических и внутриглазных линз, электродов, катетеров и т.п. в организме и на теле или в виде экстракорпоральных устройств, предназначенных для подключения к организму для содействия при хирургических операциях или диализе. Однако применение биоматериалов в медицинских устройствах может вызывать отрицательные реакции организма, включая быстрое тромбогенное действие. В запуске отложения тромбоцитов и фибрина на поверхности биоматериалов играют роль различные белки плазмы. Эти действия ведут к сужению сосудов, которое затрудняет кровоток, а последующие воспалительные реакции могут привести к потере функции медицинского устройства. Для устройств, контактирующих с кровью, особый интерес представляют биологически активные частицы (entities), уменьшающие или ингибирующие образование тромбов на поверхности биоматериала и/или покрывающего материала. Предпочтительными антитромботическими средствами в общем являются гликозаминогликаны, причем особенно предпочтительны гепарин, аналоги и производные гепарина.
Для улучшения био- и гемосовместимости широко исследовали иммобилизацию на биоматериалах таких гликозаминогликанов, как гепарин. Считается, что механизм, ответственный за снижение тромбогенности гепаринизированных материалов, состоит в способности гепарина вызывать ускорение инактивации сериновых протеаз (ферментов свертывания крови) антитромбином III (АТIII). При этом АТIII образует комплекс с хорошо определенной пентасахаридной последовательностью в гепарине, подвергаясь конформационному изменению и тем самым усиливая способность АТIII к образованию ковалентной связи с активными центрами таких сериновых протеаз, как тромбин. Затем образовавшийся комплекс сериновая протеаза-АТIII отделяется от гепарина, оставляя его свободным для последующих циклов инактивации через каталитический процесс.
Иммобилизация на биоматериалах таких биологически активных частиц, как гепарин в биологически активной форме, включает оценку химизма частиц и биоматериала соответственно. В области медицинских устройств распространенными биоматериалами являются керамические, полимерные и/или металлические материалы. Эти материалы могут применяться для имплантируемых устройств, диагностических устройств или экстракорпоральных устройств. Для иммобилизации биологически активных частиц на биоматериале зачастую требуется модификация химического состава биоматериала. Такая модификация обычно осуществляется путем обработки поверхности биоматериала с образованием популяции химически реактивных молекул или групп с последующей иммобилизацией биологически активных частиц по соответствующей методике. Что касается других биоматериалов, то поверхность биоматериала покрывают материалом, содержащим введенные в него реактивные химические группы. Затем биологически активные частицы иммобилизируют на биоматериале через реактивные химические группы материала покрытия. Описан целый ряд схем нанесения покрытий на биоматериалы. Репрезентативные примеры биологически активных частиц, иммобилизованных на биоматериале с нанесенным покрытием, описаны в US 4,810,784; 5,213,898; 5,897,955; 5,914,182; 5,916,585; и 6,461,665.
При иммобилизации биологически активных соединений, композиций или частиц на биологической активности этих "биопрепаратов" может отрицательно сказаться процесс иммобилизации. Биологическая активность многих биопрепаратов зависит от конформации и структуры (т.е. первичной, вторичной, третичной и т.д.) биопрепарата в иммобилизованном состоянии. Наряду с тщательным выбором процесса иммобилизации могут потребоваться химические изменения биопрепарата для того, чтобы включить его в покрывающий материал с такой конформацией и структурой, которые сделают его достаточно активным для выполнения предназначенной ему функции.
Несмотря на оптимизацию схемы нанесения покрытия и иммобилизации, дополнительная обработка типа стерилизации может ухудшить биологическую активность иммобилизованного биопрепарата. Для имплантируемых медицинских устройств перед употреблением необходима стерилизация. Стерилизация также может потребоваться для диагностических устройств in vitro, чувствительных к загрязнению. Стерилизация таких устройств часто требует подвергать их высокой температуре, давлению и влажности, зачастую на протяжении нескольких циклов. В некоторых случаях в процесс стерилизации включают противомикробные стерилизаторы типа газообразного этиленоксида (EtO) или паров перекиси водорода. Наряду со стерилизацией механическое сжатие и расширение или длительное хранение иммобилизованного биопрепарата могут ухудшить его активность.
Существует потребность в медицинских устройствах с иммобилизованными на них биологически активными частицами, которые можно подвергать стерилизации, механическому сжатию и растяжению и/или хранению без существенной потери биологической активности. Такие медицинские устройства должны иметь биологически совместимые композиции или соединения, включенные вместе с иммобилизованными биологическими частицами, служащие для минимизации ухудшения биологической активности частиц при стерилизации, механическом сжатии и растяжении и/или при хранении. В некоторых случаях дополнительные биологически совместимые композиции или соединения могут увеличивать биологическую активность некоторых биологически активных частиц после процедуры стерилизации.
Раскрытие изобретения
Таким образом, настоящее изобретение охватывает медицинские субстраты, содержащие гепариновые частицы, иммобилизованные на субстрате. Гепариновые частицы по изобретению сохраняют значительную биологическую активность после иммобилизации, стерилизации, механического сжатия и растяжения и/или хранения по сравнению с другими покрытиями медицинских субстратов.
Одно воплощение изобретения составляют медицинские субстраты, содержащие гепариновые частицы, связанные с субстратом через по меньшей мере одну молекулу гепарина, причем связанные гепариновые частицы чувствительны к гепариназе. В другом воплощении субстрат выбирается из группы, состоящей из полиэтилена, полиуретана, силикона, полиамидных полимеров, полипропилена, политетрафторэтилена, пенополитетрафторэтилена, фторполимеров, полиолефинов, керамических материалов и биосовместимых металлов. В другом воплощении субстратом является пенополитетрафторэтилен. В другом воплощении биосовместимым металлом является никель-титановый сплав типа Nitinol. В другом воплощении субстрат является компонентом медицинского устройства. В другом воплощении медицинское устройство выбирается из группы, состоящей из трансплантатов, сосудистых трансплантатов, стентов, эндопротезов, раздвоенных трансплантатов, раздвоенных стентов, раздвоенных эндопротезов, пластырей, пробок, устройств для доставки лекарств, катетеров, отводов кардиостимуляторов, баллонов и вживленных сосудистых фильтров. В другом воплощении гепарин или его фрагменты после обработки гепариназой не будут обнаруживаться на субстрате.
Следующее воплощение изобретения составляют гепариновые частицы, содержащие по меньшей мере одну молекулу гепарина и по меньшей мере одну каркасную (core) молекулу таким образом, что при связывании гепариновых частиц на субстрате через по меньшей мере одну молекулу гепарина данные гепариновые частицы будут чувствительны к гепариназе. В одном воплощении каркасная молекула выбирается из группы, состоящей из белков (включая полипептиды), углеводородов, аминогликозидов, полисахаридов и полимеров. В другом воплощении гепариновые частицы связаны на субстрате через по меньшей мере одну молекулу гепарина, причем связанная молекула гепарина прикрепляется к субстрату по концевой точке. В другом воплощении гепариновые частицы связаны на субстрате через по меньшей мере одну молекулу гепарина, причем связанная молекула гепарина прикрепляется к субстрату петлеобразно.
Следующее воплощение изобретения составляют АТIII-связывающие частицы, содержащие каркасную молекулу, по меньшей мере одну полисахаридную цепь, присоединенную к каркасной молекуле, и по меньшей мере одну свободную концевую группировку альдегида на полисахаридной цепи. В одном воплощении полисахаридная цепь представлена гепарином или фрагментом гепарина. В другом воплощении каркасная молекула выбирается из группы, состоящей из белков (включая полипептиды), углеводородов, аминогликозидов, полисахаридов и полимеров. В другом воплощении субстрат выбирается из группы, состоящей из полиэтилена, полиуретана, силикона, полиамидных полимеров, полипропилена, политетрафторэтилена, пенополитетра-фторэтилена, фторсодержащих полимеров, полиолефинов, керамических материалов и биосовместимых металлов. В другом воплощении АТIII-связывающие частицы связаны на субстрате по концевой точке или петлеобразно. В другом воплощении субстрат является компонентом медицинского устройства.
Следующее воплощение изобретения составляет способ определения структуры гепариновых частиц, связанных с субстратом, который включает стадии обеспечения субстрата, содержащего гепариновые частицы, деполимеризации гепариновых частиц с образованием смеси растворимых фрагментов гепарина, выявления всех растворимых фрагментов гепарина в смеси методом колоночной хроматографии, идентификации каждого детектируемого фрагмента гепарина из предыдущей стадии, и выведения структуры гепариновых частиц из структур выявленных фрагментов гепарина. В одном воплощении деполимеризация осуществляется с помощью гепариназы. В другом воплощении колоночная хроматография представляет собой жидкостную хроматографию высокого разрешения на сильном анионообменнике (SAX-HPLC).
Следующее воплощение изобретения составляет система определения структуры гепариновых частиц, связанных с субстратом, которая включает раствор для деполимеризации, раствор метящего реагента и детектор. В другом воплощении раствор для деполимеризации содержит гепариназу. В другом воплощении раствор метящего реагента содержит толуидиновый синий и трис(4-метилтио)бензоат тербия. В другом воплощении детектор включает SAX-HPLC, эпифлуоресцентный микроскоп и абсорбционный спектроскоп.
Краткое описание чертежей
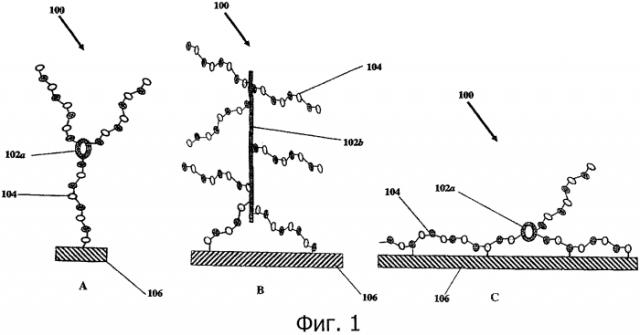
На фиг.1 представлено несколько гепариновых частиц по изобретению и способы прикрепления гепариновых частиц к субстрату.
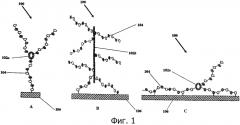
На фиг.2 представлена АТIII-связывающая способность различных альдегидсодержащих гепариновых частиц, конъюгированных на пенополитетрафторэтилене (ePTFE) и подвергавшихся множественной стерилизации ЕtO. Альдегидсодержащие гепариновые частицы классифицированы по каркасной молекуле, использовавшейся при синтезе данных гепариновых частиц. При этом колистинсульфат в качестве каркасной молекулы относится к примеру 1, неомицин - к примеру 2, поли-L-лизин - к примеру 4, капреомицин - к примеру 3, полиэтиленимин (PEI) - к примеру 5, и этилендиамин (EDA) - к примеру 6. Все столбики означают средние значения образцов по номерам, а планки погрешностей - стандартное отклонение.
На фиг.3, А и В представлены световые микрофотографии гепариновых частиц, содержащих свободные концевые альдегиды и иммобилизованных на субстрате ePTFE методом прикрепления по одному концу, до (3А) и после (3В) обработки гепариназой-1 и окрашенных толуидиновым синим. Отсутствие окраски на фиг.3, В по сравнению с 3, А свидетельствует о том, что гепариновые частицы, содержащие свободные концевые альдегиды, иммобилизованные на субстрате ePTFE методом прикрепления по одному концу, в основном подверглись деполимеризации из поверхности после обработки гепариназой-1.
На фиг.3, С представлены нормализированные изменения яркости до и после обработки гепариназой-1 для гепарина, иммобилизованного через концевой альдегид и через множественные точки прикрепления, причем гепариновые частицы содержат каркас из неомицина, иммобилизованного через концевую точку и через множественные точки прикрепления по меньшей мере к одной молекуле гепарина, и для гепарина USP, иммобилизованного через множественные точки прикрепления. Низкие нормализованные значения изменений яркости для гепарина с концевым альдегидом, для гепариновых частиц, содержащих гепарин и неомициновый каркас с концевым альдегидом, и для гепарина USP со множественными точками прикрепления к субстрату означают, что их поверхности не чувствительны к гепариназе-1 и все еще содержат много гепарина на поверхности.
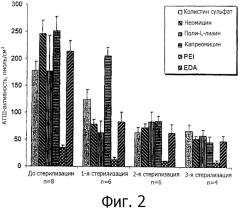
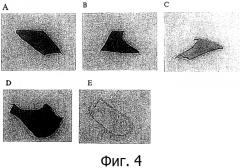
На фиг.4, А-С представлены световые микрофотографии гепариновых частицы, содержащих гепарин и каркас из EDA и иммобилизованных на субстрате ePTFE методом прикрепления по одному концу, до (4, А и 4, В) и после (4, С) обработки гепариназой-1 и окрашенных толуидиновым синим. Окрашивание образцов свидетельствуют о наличии гепариновых частиц. Образцы 4 В and 4С подвергали однократной стерилизации и промывали только деионизированной водой после стерилизации. Окраска на фиг.4С после стерилизации и обработки гепариназой-1 означает, что гепариназа-1 не распознает гепариновые частицы на поверхности.
На фиг.4, D и Е представлены световые микрофотографии гепариновых частиц, содержащих гепарин и каркас из EDA и иммобилизованных на субстрате ePTFE методом прикрепления по одному концу, до (4, D) и после (4, Е) обработки гепариназой-1 и окрашенных толуидиновым синим. Эти образцы подвергали однократной стерилизации и промывали деионизированной водой и борной кислотой после стерилизации. Отсутствие окраски на фиг.4, Е после стерилизации означает, что гепариназа-1 распознает гепариновые частицы на поверхности и подвергает их деполимеризации.
На фиг.5, А-С представлены хроматограммы SAX-HPLC при деполимеризации гепариназой-1 (А) гепарина USP, (В) гепариновых частиц, состоящих из гепарина и колистина сульфата, и (С) гепариновых частиц, состоящих из гепарина и неомицина сульфата.
На фиг.6, А и В представлены хроматограммы SAX-HPLC при деполимеризации гепариназой-1 иммобилизованных на поверхности ePTFE (А) гепарина USP, связанного по свободному концевому альдегиду, и (В) гепариновых частиц, состоящих из гепарина и колистина сульфата, связанных по свободным концевым альдегидам.
Осуществление изобретения
Настоящее изобретение касается медицинских субстратов, содержащих гепариновые частицы, иммобилизованные на субстрате. Гепариновые частицы по изобретению сохраняют значительную биологическую активность после иммобилизации и стерилизации по сравнению с другими медицинскими субстратами с покрытием.
В контексте данного изложения применяется ряд терминов. Представлены следующие определения. В настоящем изобретении и прилагаемой формуле изобретения формы единственного числа включают значения множественного числа, если только из контекста четко не вытекает иное.
В настоящем изобретении термином "гепариновые частицы (entities)" обозначаются молекулы гепарина, ковалентно присоединенные к каркасной молекуле. Такие молекулы гепарина могут присоединяться к каркасной молекуле по концевой точке (как описано ниже и в основном описано в US 4,613,665, включенном в виде ссылки на все случаи) или другими способами, известными в данной области (например, см. GT Hermanson, Bioconjugate Techniques, Academic Press, 1996; HG Garg et al., Chemistry and Biology of Heparin and Heparan Sulfate, Elsevier, 2005).
В настоящем изобретении термином "каркасная молекула" обозначается полифункциональная молекула, к которой присоединяется гепарин. В целях настоящего изобретения данная каркасная молекула и субстрат означают не одно и то же, хотя каркасная молекула и субстрат могут состоять из одного и того же материала.
В настоящем изобретении термином "существенно очищенный" обозначается то, что данная разновидность является преобладающей (т.е. в пересчете на моль она более распространена, чем любая другая индивидуальная разновидность в композиции), а предпочтительно существенно очищенной фракцией является композиция, в которой данная разновидность составляет по меньшей мере 50% (в молях) от всех присутствующих видов макромолекул. В общем, существенно очищенная композиция должна составлять более 80-90% от всех присутствующих в композиции видов макромолекул. Более предпочтительно, данная разновидность очищена практически до гомогенности (примеси в композиции не обнаруживаются обычными способами детекции), при этом композиция состоит практически из одного вида макромолекул.
В настоящем изобретении термином "гепариназа" обозначается любая энзиматическая реакция деполимеризации (т.е. расщепления) гепарина. Примеры гепариназ включают, без ограничения, гепариназу-1, гепариназу-2, гепариназу-3, гепараназы, экзосульфатазы, бактериальные экзоферменты и гликозидазы, которые способны деполимеризировать гепарин.
В настоящем изобретении термином "чувствительность к гепариназе" обозначается то, что после обработки гепариназой субстрата, содержащего гепариновые частицы, и окрашивания данного субстрата толуидиновым синим субстрат не должен заметно окрашиваться (в основном, как изображено на фиг.3, В и фиг.4, Е). Термин также означает то, что с остаточным гепарином или его фрагментами должно связываться незначительное количество толуидинового синего, а показания от детектора, способного измерить количество толуидинового синего (или других меток) на субстрате, как то спектрофотометра, люминометра, денситометра, жидкостного сцинтилляционного счетчика, гамма-счетчика и т.п., должно быть на уровне фона или незначительно отличаться от уровня фона при сравнении с субстратом без гепариновых частиц и окрашенным толуидиновым синим или же быть ниже чувствительности данного детектора при сравнении с субстратом, содержащим гепариновые частицы и окрашенным толуидиновым синим без обработки гепариназой. Термин также означает то, что метка, связывающаяся с гепарином или его фрагментами, не должна детектировать значительное количество гепарина или его фрагментов после обработки гепариназой субстрата, содержащего гепариновые частицы.
В настоящем изобретении термины "связанный", "присоединенный" или "конъюгированный" и их производные в отношении гепариновых частиц и/или гепарина означают ковалентно связанный, если не указано иначе.
Обращаясь к фиг 1, А-С, одно воплощение изобретения составляет медицинский субстрат, содержащий гепариновые частицы 100, связанные на субстрате 106 через по меньшей мере одну молекулу гепарина 104, причем связанные гепариновые частицы чувствительны к гепариназе. Подходящие материалы субстрата для иммобилизации или связывания гепариновых частиц составляют такие полимеры, без ограничения, как полиамиды, поликарбонаты, полиэфиры, полиолефины, полистирен, полиуретан, поли(эфиры уретана), поливинилхлориды, силиконы, полиэтилены, полипропилены, полиизопрены, политетрафторэтилены и пенополитетрафторэтилены (ePTFE, как описано в US 4,187,390). В одном воплощении субстратом является пено- или пористый политетрафторэтилен (ePTFE).
Дополнительные субстраты включают, без ограничения, гидрофобные субстраты, как то политетрафторэтилен, пенополитетрафторэтилен, пористый политетрафторэтилен, фторированный полиэтилен-пропилен, гексафторпропилен, полиэтилен, полипропилен, нейлон, полиэтилентерефталат, полиуретан, каучук, силиконовый каучук, полистирен, полисульфон, полиэфир, полигидроксикислоты, поликарбонат, полиимид, полиамид, полиаминокислоты, регенерированная целлюлоза и такие белки, как шелк, шерсть и кожа. Методы получения материалов из пористого политетрафторэтилена описаны в US 3,953,566 и 4,187,390, каждый из которых включен в виде ссылки. В другом воплощении данный ePTFE может быть инпрегнирован, заполнен, пропитан или покрыт по меньшей мере одним химическим соединением, вызывающим биоактивный ответ. Соединения, вызывающие биоактивный ответ, включают противомикробные (например, противобактериальные и противовирусные), противовоспалительные (например, дексаметазон и преднизон), антипролиферативные (например, таксол, паклитаксель и доцетаксель) и антикоагулирующие средства (например, абциксимаб, эптифибатид и тирофибран). В одном воплощении противовоспалительным средством является стероид. В другом воплощении стероид представлен дексаметазоном. Способы покрытия субстратов хорошо известны в данной области. В другом воплощении субстрат включает гепариновые частицы по изобретению и покрытие, содержащее соединение, вызывающее биоактивный ответ. Такой субстрат включает материалы, приведенные выше и ниже. В одном воплощении субстрат представлен ePTFE.
Другими подходящими субстратами являются, без ограничения, производные целлюлозы, агароза, альгинат, полигидроксиэтилметакрилат, поливинилпирролидон, поливиниловый спирт, полиаллиламин, полиаллиловый спирт, полиакриламид и полиакриловая кислота.
Кроме того, в качестве субстратов в настоящем изобретении могут применяться некоторые металлы и керамические вещества. Подходящими металлами являются, без ограничения, титан, нержавеющая сталь, золото, серебро, родий, цинк, платина, рубидий и медь, к примеру. Подходящими сплавами являются сплавы кобальта и хрома типа L-605, MP35N, Elgiloy, сплавы никеля и хрома (как-то Nitinol) и такие сплавы ниобия, как Nb-1% Zr и др.
Подходящими материалами для керамических субстратов являются, без ограничения, оксиды кремния, оксиды алюминия, глинозем, кремнезем, гидроксиапатиты, стекла, оксиды кальция, полисиланолы и оксиды фосфора. В другом воплощении могут применяться субстраты на основе белков типа коллагена. В другом воплощении могут применяться субстраты на основе полисахаридов типа целлюлозы.
Некоторые субстраты могут иметь множество реактивных химических групп, заполняющих по меньшей мере часть их поверхности, с которыми могут связываться гепариновые частицы по изобретению. Гепариновые частицы по изобретению ковалентно связываются с материалом субстрата через данные реактивные химические группы. Поверхности этих субстратов могут быть гладкими, неровными, пористыми, изогнутыми, плоскими, угловатыми, неправильной формы или комбинированными. В некоторых воплощениях субстраты с порами на поверхности содержат внутренние пустые пространства, простирающиеся от пористой поверхности материала вглубь материала. Эти пористые субстраты содержат внутренний материал субстрата, окаймляющий поры, который часто составляет поверхность, пригодную для иммобилизации биологически активных молекул. И пористые, и непористые субстраты могут иметь вид нитей, пленок, листов, трубочек, ячеек, сетчатых и несетчатых структур и их комбинаций.
Субстраты без реактивных химических групп на их поверхностях (или не имеющие соответствующих реактивных химических групп) могут быть покрыты, по меньшей мере частично, полимерным покрывающим материалом, несущим множество реактивных химических групп, с которыми могут связываться гепариновые частицы. Полимерные субстраты также могут быть модифицированы вдоль их поверхности или вдоль их полимерного остова различными методами, включая гидролиз, аминолиз, фотолиз, травление, плазменную модификацию, плазменную полимеризацию, введение карбенов, введение нитренов и т.д. Гепариновые частицы ковалентно прикрепляются к или связываются с полимерным покрывающим материалом через реактивные химические группы покрывающего материала или непосредственно с субстратом, подвергавшимся модификации. Полимерный покрывающий материал может образовывать по меньшей мере один слой по крайней мере на части субстрата.
Существует много других модификаций поверхности типа тех, что описаны в US 4,600,652 и US 6,642,242, на основе субстратов со слоем полиуретанмочевины, с которыми может связываться ковалентными связями гепарин, содержащий альдегидные группы после модификации путем окисления азотистой кислотой или периодатом. Подобная технология описана в US 5,032,666, в котором поверхность субстрата покрывается богатой аминами фторированной полиуретан-мочевиной перед иммобилизацией антитромбогенного агента типа активированного альдегидами гепарина. Другая антитромбогенная модификация поверхности, которую можно привести, описана в публикации WO 87/07156. Поверхность устройства подвергается модификации путем покрытия слоем лизоцима или его производного, на который налипает гепарин. Еще одна модификация поверхности для получения антитромбогенных изделий описана в US 4,326,532. В этом случае покрытая антитромбогенным слоем поверхность содержит полимерный субстрат, хитозан, связанный с полимерным субстратом, и антитробогенный агент, связанный с хитозановым покрытием. Другие сообщали об антитромбогенном гемофильтре тоже с хитозановым слоем для связывания гепарина. Другой способ получения антитромбогенных поверхностей описан в WO 97/07834, при этом гепарин смешивают с достаточным количеством периодата с тем, чтобы прореагировало не более двух сахаридных звеньев на молекулу гепарина. Эта смесь наносится на поверхность модифицированного субстрата медицинского устройства, при этом данная модификация поверхности содержит аминогруппы. Вышеприведенные способы добавления реактивных групп к субстратам составляют лишь небольшой пример того, как это может осуществляться. Вышеприведенный перечень никоим образом не является полным. Более того, ясно, что тип процесса, используемого для добавления реактивных химических групп к субстрату, зависит от свойств субстрата, известных специалистам в данной области.
В другом воплощении изобретения данный медицинский субстрат, содержащий гепариновые частицы, связанные через по меньшей мере одну молекулу гепарина, являются компонентом медицинского устройства. Медицинские устройства включают, без ограничения, трансплантаты, сосудистые трансплантаты, стенты, эндопротезы, раздвоенные трансплантаты, раздвоенные стенты, раздвоенные эндопротезы, грыжевые пластыри, грыжевые пробки, периодонтальные трансплантаты, хирургические ткани, устройства доставки лекарств, катетеры, отводы кардиостимуляторов, баллоны и вживленные фильтры. В одном воплощении стенты могут применяться в кардиологических, периферических или неврологических применениях. В другом воплощении эндопротезы могут применяться в кардиологических, периферических или неврологических применениях.
Другое воплощение изобретения составляют гепариновые частицы, содержащие по меньшей мере одну молекулу гепарина и по меньшей мере одну каркасную молекулу. Как видно из фиг.1, каркасная молекула 102 является "остовом" гепариновой частицы 100, с которым связаны молекулы гепарина 104. Каркасная молекула 102 может быть циклической (102а, фиг.1, А и 1, С), линейной (102b, фиг.1, В), разветвленной, древовидной, Y-образной, Т-образной или "звездчатой", как описано в Freudenberg U., Biomaterials, 30, 5049-5060, 2009; и Yamaguchi N., Biomacromolecules, 6, 1921-1930, 2005. В одном воплощении каркасная молекула выбирается из группы, состоящей из белков (включая полипептиды), углеводородов, липидов, аминогликозидов, полисахаридов и полимеров. Белки включают, без ограничения, антитела, ферменты, рецепторы, факторы роста, гормоны, серпины и другие глобулярные белки. Специфические белки и полипептиды включают, без ограничения, альбумин, колистин, коллаген, полилизин, антитромбин III, фибрин, фибриноген, тромбин, ламинин, кератин и т.п. В другом воплощении каркасная молекула может представлять собой полипептид. Такой полипептид необязательно является длинным и может содержать один или несколько повторов аминокислот, к примеру повторов остатков серина, глицина (например, Ser-Gly-Gly-Ser-Gly), лизина или орнитина. С другой стороны, можно использовать и другие последовательности аминокислот, к примеру колистин, полилизин и полимиксин.
Примеры полисахаридов включают, без ограничения, нейтральные полисахариды, такие как целлюлоза, крахмал, агароза, карбоксиметилцеллюлоза, нитроцеллюлоза и декстран, анионные полисахариды, такие как альгинат, гепарин, гепаринсульфат, декстрансульфат, ксантан, гиалуроновая кислота, каррагенан, гумимиарабик, трагакант, арабиногалактан и пектин; макроциклические полисахариды, такие как циклодекстрин и гидроксипропилциклодекстрин; и поликатионные полисахариды, такие как хитин и хитозан.
Примеры синтетических полимеров включают, без ограничения, полиэтиленгликоль (ПЭГ) 200, 300, 400, 600, 1000, 1450, 3350, 4000, 6000, 8000 и 20000, политетрафторэтилен, полипропиленгликоль, поли(этиленгликоль-с-пропиленгликолем), сополимеры полиэтиленгликоля, сополимеры полипропиленгликоля, сополимеры тетрафторэтилена с винилацетатом и виниловым спиртом, сополимеры этилена с винил ацетатом и виниловым спиртом, поливиниловым спиртом, полиэтиленимином, полиакриловой кислотой; полиоли, такие как поливиниловый спирт и полиаллиловый спирт; полианионы, такие как акриловая кислота и полиметакриловая кислота. Поликатионные полимеры включают полиаллиламин, полиэтиленимин, полигуанидин, поливиниламин, полиэтиленгликоль-диамин, этилендиамин и поличетвертичные амины; полиакрилонитрилы, такие как гидролизованный полиакрилонитрил, полиакриламид-с-акрилонитрилом и их сополимеры. Другие полимеры включают фторированные сополимеры, в том числе сополимеры тетрафторэтилена и винилового спирта, винил-ацетата, винилформамида, акриламида и виниламина. В другом воплощении каркасная молекула может представлять собой аминогликозид, включая, без ограничения, амикацин, арбекацин, гентамицин, канамицин, неомицин, нетилмицин, паромомицин, родо-стсрептомицин, стрептомицин, тобрамицин и апрамицин.
Гепарин - это мукополисахарид, выделенный из кишечника свиньи или легких быка, и он гетерогенен по молекулярному размеру и химической структуре. Гепарин состоит из чередующихся звеньев глюкуроновой кислоты и глюкозамина. Звенья глюкуроновой кислоты состоят из D-глюкуроновой кислоты и L-идуроновой кислоты. Они соединяются по D- и L-(1,4), соответственно, со звеньями D-глюкозамина. Большая часть остатков L-идуроновой кислоты сульфатирована в положении 2. Звенья D-глюкозамина N-сульфатированы, сульфатированы в положении 6 и соединяются по α-(1,4) с остатками уроновой кислоты. Некоторые звенья D-глюкозамина также сульфатированы в положении 3. Гепарин содержит материал с молекулярным весом в пределах от 6000 дальтон до 30000 дальтон. Гидроксильные и аминогруппы в различной степени подвергаются сульфатированию и ацетилированию. Активная последовательность гепарина, отвечающая за его антикоагулирующие свойства, представлена уникальной пентасахаридной последовательностью, которая связывается со своим лигандом антитромбином III (АТIII). Последовательность состоит из трех остатков D-глюкозамина и двух остатков уроновой кислоты. Молекулы гепарина также можно классифицировать по содержанию пентасахарида. Примерно одна треть гепарина содержит цепи с одной копией уникальной последовательности пентасахарида (см. Choay, Seminars in Thrombosis and Hemostasis 11:81-85 (1985), включено в виде ссылки) с высоким сродством к АТIII, тогда как гораздо меньшая часть (оценивается на уровне 1% от всего гепарина) состоит из цепей, содержащих более одной копии пентасахарида с высоким сродством (см. Rosenberg et al, Biochem. Biophys. Res. Comm. 86:1319-1324 (1979), включено в виде ссылки). Остальной (прибл. 66%) гепарин не содержит последовательности пентасахарида. Таким образом, так называемый "стандартный гепарин" составляет смесь из трех разновидностей: "высокоаффинный" гепарин обогащен молекулами, содержащими по меньшей мере одну копию пентасахарида, и "очень высокоаффинный" гепарин составляет около 1% молекул, содержащих более одной копии последовательности пентасахарида. Эти три разновидности можно отделить друг от друга обычными методами хроматографии, как то аффинной хроматографии через колонку с антитромбином (например, Сефарозой-АТ; например, см. Lam et al., Biochem. Biophys. Res. Comm. 69:570-577 (1976); и Homer, Biochem. J. 262:953-958 (1989), которые включены в виде ссылки).
В одном воплощении гепарин получают из животных. В другом воплощении гепарин получают из быка или свиньи. В следующем воплощении гепарин представлен синтетическим гепарином, т.е. он не происходит из животного источника (например, фондапаринукс или еноксапарин). В другом воплощении гепариновые частицы по изобретению содержат гепарин, который подвергался очистке и содержит практически чистый "высокоаффинный" гепарин. В другом воплощении гепариновые частицы по изобретению содержат гепарин, который подвергался очистке и содержит комбинацию из практически чистого "высокоаффинного" и "очень высокоаффинного" гепарина.
Другое воплощение изобретения составляет связывание гепариновых частиц с медицинским субстратом через по меньшей мере одну молекулу гепарина. Как видно из фиг.1, гепариновые частицы изобретения связываются с субстратом через по меньшей мере одну молекулу гепарина. Так, в одном воплощении связанная молекула гепарина прикрепляется к субстрату по концевой точке (как изображено на фиг.1, А и 1, В). В другом воплощении связанная молекула гепарина прикрепляется к субстрату через концевой альдегид. Это может осуществляться в основном, как описано в US 4,613,665, который включен в виде ссылки во всей полноте, и как описано ниже.
В другом воплощении гепариновые частицы связаны на субстрате через по меньшей мере одну молекулу гепарина, причем связанная молекула гепарина прикрепляется к субстрату "петлеобразно". Петлеобразное прикрепление, как показано на фиг.1, С, это такое прикрепление гепариновых частиц через по меньшей мере один гепарин, при котором гепарин слабо связан с субстратом по немногим местам, тем самым позволяя значительной части связанного гепарина подвергаться действию гепариназы (в отличие от более распространенных способов, когда гепарин тесно связан по многим местам). Более распространенные методы прикрепления гепарина к субстрату включают реакцию с большинством функциональных групп, случайным образом расположенных по всей длине молекулы гепарина (например, с помощью конденсирующих реагентов, таких как карбодиимиды, эпоксиды и полиальдегиды). Эти методы дают высокую вероятность того, что активная последовательность (уникальная пентасахаридная последовательность, описанная выше) будет связываться с субстратом, что приводит к снижению и/или потере активности. При петлеобразном прикреплении гепарина лишь небольшое количество функциональных групп гепарина реагирует и связывается с субстратом. Таким образом, существует высокая вероятность того, что активная последовательность прикрепленного гепарина не будет связываться с субстратом, что позволит ей связываться со своим лигандом. В другом воплощении изобретение охватывает гепариновые частицы с множественным прикреплением к субстрату, при этом активная последовательность не связывается с субстратом. В другом воплощении молекула гепарина, связывающая гепариновую частицу с субстратом, прикрепляется к субстрату петлеобразно.
Как изложено выше, прикрепление по концевой точке и петлеобразное прикрепление дает возможность значительной части молекул гепарина (в гепариновой частице) не связываться с субстратом. В настоящем изобретении термин "значительная часть" означает, что около 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% и 99% молекул гепарина не связываются с субстратом. В другом воплощении термин также означает то, что по меньшей мере одна молекула гепарина (в гепариновой частице) из числа связанных с субстратом связывается с субстратом не через свою активную последовательность. Таким образом, поскольку активная последовательность не связана с поверхностью субстрата, то она с большей вероятностью будет взаимодействовать со своим лигандом. Иными словами, если активная последовательность связана с поверхностью субстрата, то у гепарина будет очень мало шансов для связывания со своим лигандом.
Однако поскольку гепариновые частицы прикрепляются через гепарин посредством концевых и/или петлеобразных связей, то гепарин будет чувствителен к гепариназе. Таким образом, после обработки гепариназой н