Способ лечения заболеваний глаз, сопровождающихся окислительным стрессом
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к офтальмологии, и предназначено для лечения заболеваний глаз, сопровождающихся окислительным стрессом. Супероксиддисмутазу вводят в состав кальций-фосфатных биодеградируемых наночастиц, покрытых дисахаридами, с радиусом до 350 нм и в диапазоне ферментативной активности от 20 до 500 кЕД/мл и инсталлируют в конъюнктивальную полость глаза. Способ позволяет увеличить терапевтическую эффективность супероксиддисмутазы за счет усиления способности этого фермента снижать выраженность окислительного стресса при глазных заболеваниях. 6 пр.
Реферат
Изобретение относится к медицине, в частности к офтальмологии и фармации, и предназначено для лечения заболеваний глаз, сопровождающихся окислительным стрессом. Роль свободнорадикальных процессов в патологии впервые была установлена отечественными учеными в 60-х годах 20 века [Тарусов Б.Н. Физико-химические механизмы биологического действия ионизирующих излучений// Успехи совр. биологии, 1957, 44, 2, 171-185; Эммануэль Н.М., Липчина Л.П. Лейкоз у мышей и особенности его развития при воздействии ингибиторов цепных окислительных процессов // Доклады АН, 1958, 121, 1, 141-144]. Но и в настоящее время контроль образования свободных радикалов при лечении широкого круга заболеваний остается актуальной проблемой медицины, в том числе в офтальмологии. Свободные радикалы - это атомы или молекулы с неспаренными электронами на внешних электронных оболочках, которые обладают высокой реакционной способностью. В организме в норме процессы образования свободных радикалов строго регулируются системой антиоксидантной защиты, которая включает ферментные и неферментные антиоксиданты. К числу ферментных антиоксидантов относятся супероксиддисмутаза (СОД), каталаза, глутатион-пероксидазы.
Под окислительным стрессом понимают усиление свободнорадикальных процессов на фоне ослабления собственной антиоксидантной системы, которое приводит к повреждению практически всех компонентов тканевых структур, нарушению метаболических процессов и структуры тканей [Зенков Н.К., Ланкин В.З., Меньшикова Е.Б. Окислительный стресс: Биохимический и патофизиологический аспекты. 2001, М.: МАИК «Наука Интерпериодика»]. Высокая вероятность свободнорадикального повреждения тканей глаза обусловливается несколькими причинами. Во-первых, ткани глаза постоянно подвергаются действию света, что приводит к фотоинициированию перекисного окисления липидов (ПОЛ). Во-вторых, липиды, входящие в состав внутриглазных тканей, по своему составу являются чрезвычайно легко окисляемым субстратом для ПОЛ. Так, в мембранных структурах сетчатки более половины фосфолипидов содержат полиеновые остатки жирных кислот, восприимчивые к атаке активированными кислородными метаболитами. Кроме того, в фоторецепторах присутствует много митохондрий, в которых проходит постоянное потребление кислорода, сопровождающееся образованием активных форм кислорода, что делает их уязвимыми в отношении окислительного стресса.
Практически нет такой офтальмологической патологии, при которой не было бы установлено усиления свободнорадикальных процессов. Например, показана их важная роль в патогенезе глаукомы [Зиангирова Г.Г., Антонова О.В. Перекисное окисление липидов в патогенезе первичной открытоугольной глаукомы // Вестн. Офтальмол., 2003, 4, 54-55], катаракты [Gamer В., Davies V.J., Truscott R.J. W. Formation of hydroxyl radicals in the human lens is related to the severity of nuclear cataract // Exp. Eye Res., 2000, 70, 81-88], псевдоэксфолиативного синдрома [Koliakos G.G., Konstas A., Schlotzer-Schrehardt U., Hollo G., Katsimbris I.E., Georgiadis N., Ritch R. 8-Isoprostaglandin F2a and ascorbic acid concentration in the aqueous humour of patients with exfoliation syndrome// Br. J. Ophthalmol., 2003, 87, 3, 353-356], внутриглазных кровоизлияний [Ромащенко А.Д., Гундорова Р.А., Касавина Б.С. Роль перекисного окисления липидов в патогенезе развития травматического гемофтальма // Вестн. Офтальмол., 1981, 2, 51-53], ожоговой болезни глаз [Гулидова О.В., Любицкий О.Б., Клебанов Г.И., Чеснокова Н.Б. Изменение антиокислительной активности слезной жидкости при экспериментальной ожоговой болезни глаз. Бюлл. Экспер. Биол. Мед.// 1999, 128, 11, 571-574], диабетической ретинопатии [Булатова О.С., Кондратьев Я.Ю., Миленькая Т.М. Окислительный стресс: клинико-метаболические показатели и полиморфный маркер гена каталазы при развитии ретинопатии у больных сахарным диабетом II типа. Клин. Эндокринол.// 1999, 45, 4, 3-7]. По мнению ряда авторов для многих глазных болезней характерна активация ПОЛ на уровне всего организма [Бабенкова И.В., Теселкин Ю.О., Макашова Н.В., Гусева М.Р. Антиоксидантная активность гистохрома и некоторых лекарственных препаратов, применяемых в офтальмологии. Вестн. Офтальмол. // 1999, 4, 22-24].
В условиях окислительного стресса клетки продуцируют в очень больших количествах супероксид-анион. Супероксид - это молекулярный кислород с неспаренным электроном на внешнем уровне. Супероксид может реагировать с молекулами воды с образованием очень агрессивного гидроксильного радикала, а также с оксидом азота с образованием высокотоксичного пероксинитрита. Гидроксильные радикалы могут легко реагировать с органическими и неорганическими молекулами, способны разрушать практически все структурные и функционально активные компоненты тканей, приводят к образованию органических свободных радикалов. Образующиеся в большом количестве свободные радикалы способствуют возникновению различных нарушений в иммунной системе, а также вызывают образование токсических веществ, что приводит к усугублению нарушений микроциркуляции в тканях, приводящее к ишемизации и гипоксии тканей [CarubelliR., Nodrquist R.E., Rowsey J.J. Role of active oxygen species in corneal ulceration. Effect of hydrogen peroxide generated in situ // Cornea, 1990, 9, 161-169; Yadav U.C. S., Kalariya N.M., Ramana K.V. Emerging role of antioxidants in the protection of uveitis complications// Curr. Med. Chem., 2011, 18, 931-942].
В организме контроль концентрации супероксид-аниона, играющего важную роль в запуске окислительного стресса, в основном осуществляет антиоксидантный фермент супероксиддисмутаза (СОД). Супероксиддисмутаза катализирует реакцию дисмутации супероксидных кислородных радикалов в кислород и перекись водорода согласно следующим реакциям.
Имеется несколько изоформ СОД, которые находятся в разных клеточных структурах, а также во внеклеточном пространстве, где эти ферменты осуществляют контроль уровня супероксид-аниона.
Действие препаратов на основе СОД направлено на усиление собственной защитной реакции организма при окислительном стрессе. В данной работе предлагается применение в виде глазных капель препарата, действующим началом которого является СОД, внедренная в кальций-фосфатные наночастицы (КФЧ), с целью увеличения проникновения фермента во внутренние структуры глаза.
Известен способ того же назначения, предусматривающий инстилляции в конъюнктивальную полость антиоксидантного препарата на основе рекомбинантной супероксиддисмутазы (фармацевтический препарат «Рексод-ОФ», ЛСР-006689/10 от 15.07.10). Показаниями к его применению являются первичная открытоугольная глаукома, аденовирусное поражение глаз, вторичная кератопатия.
Известным недостатком препаратов, применяемых для закапывания в глаз, является их плохое проникновение во внутренние структуры глаза. Помимо этого, лекарственный препарат легко смывается слезой с поверхности глаза, а также поступает в носослезный канал. В среднем только около 5% от вводимого лекарственного вещества способно проникнуть через роговую оболочку и достичь внутриглазных тканей [Ahmad I., Patton Т. Importance of thenon and corneal absorption routes in topical ophthalmic drug delivery // Invest. Ophtalm. Vis. Sci., 1985, 26, 584-587]. В итоге, необходимую концентрацию лекарственной субстанции в препарате необходимо повышать, что усиливает нежелательные побочные эффекты как локальные, так и системные, связанные с последующим попаданием этих препаратов в кровоток.
Препарат Рексод-ОФ выпускается в виде лиофилизата СОД. Перед употреблением содержимое флакона 0,8 млн ЕД разводят в 2 мл воды и полученный раствор (глазные капли) хранят в холодильнике при 4-10°С в течение не более 3 дней. Данному препарату присущи все вышеперечисленные недостатки использования капельного метода введения в виде сложности создания требуемой концентрации действующего вещества во внутренних тканях глаза, что вызывает необходимость его частого закапывания - до 8 раз в сутки.
Перспективным подходом к решению проблемы проникновения лекарственного препарата внутрь глаза является использование наночастиц в качестве систем доставки, так как они способны значительно увеличивать биодоступность лекарственного препарата и повышать концентрацию вещества в тканях без изменения исходной концентрации препарата [Araujo J., Gonzalez Е., Egea М.А., Garcia M.L., Souto E.B. Nanomedicines for ocular NSAIDs: safety on drug delivery // Nanomedicine, 2009, 5, 394-401; Sahoo S.K., Dilnawaz F., Krishnakumar S. Nanotechnology in ocular drug delivery // Drug Discov. Today, 2008, 13, 144-151]. Серьезной проблемой в разработке глазных лекарственных форм на основе наночастиц является сложность получения этих препаратов. Наночастицы должны быть биосовместимы, хорошо выводиться из организма, не оказывать токсического действия. Так, при включении СОД в полимерные наночастицы на основе сшитого метокси-поли(этиленгликоль)-поли(L-лизин) блок-сополимера и целевых добавок [Патент RU 2012130852/15, 19.07.2012; Patent US 2014/0120075 A1, May 1, 2014] экспериментально было показано усиление терапевтического действия СОД. Однако с технологической точки зрения получение данного блок-сополимера, обладающего, кстати, немалой стоимостью, является достаточно сложным и трудно масштабируемым процессом. Поэтому не снят вопрос о поиске других наночастиц - носителей СОД для применения в фармации.
В качестве альтернативы органическим частицам к использованию предложены неорганические, в частности, кальций-фосфатные частицы (КФЧ). Методика получения КФЧ была впервые упомянута и запатентована в 2002 году [US Patent №6,355,271 B1, 12 March 2002]. Кальций-фосфатные наночастицы хорошо выводятся из организма и обладают хорошей биосовместимостью ввиду схожести по составу с гидроксиапатитом Са10(PO4)6(ОН)2, который является основным компонентом костей и зубов человека [Не Q., Chu T. - C, Potter D. Biodegradable Calcium Phosphate Nanoparticles as a New Vehicle for Ocular Delivery of a Potential Ocular Hypotensive Agent // J. Ocular Pharmacol, and Therap., 2002, V. 18, P. 507-514].
Была показана способность КФЧ при инсталляциях в глаз кроликов проникать во внутренние среды глаза [Шимановская Е.В., Безнос О.В., Клячко Н.Л., Кост О.А., Никольская И.И., Павленко Т.А., Чеснокова Н.Б., Кабанов А.В. Получение кальций-фосфатных наночастиц, содержащих тимолол, и оценка их влияния на внутриглазное давление в эксперименте // Вестн. Офтальмол., 2012, 3, 15-18; патент RU №: 2472471, 20.01.2013; Шимановская Е.В., Никольская И.И., Биневский П.В., Безнос О.В., Клячко Н.Л., Павленко Т.А., Чеснокова Н.Б., Кост О.А. Лизиноприл в составе кальций-фосфатных наночастиц как перспективный антиглаукомный препарат // Российские нанотехнологии. 2014, Т. 9, №3-4, 100-106]. В этих работах были продемонстрированы повышение эффективности и пролонгация эффекта снижения внутриглазного давления в экспериментах in vivo на кроликах при включении в КФЧ низкомолекулярных соединений - адреноблокатора тимолола и ингибитора ангиотензин-превращающего фермента лизиноприла.
Эксперименты по внедрению в КФЧ ингибитора карбоангидразы, который эффективно снижает ВГД, показали, что такой препарат снижает ВГД намного эффективнее не только водного раствора этого вещества, но и коммерческого препарата бринзоламида. При этом никаких побочных эффектов при использовании частиц выявлено не было [X. Zhang, W. Yaun, D. Zhau, J. Wu. Lyceum Chinense and calcium phosphate nanoparticles for ophthalmic drug delivery // Nanotech., 2008, V. 2, P. 401-404].
В настоящее время в литературе нет данных по внедрению в КФЧ ферментов различной природы.
Техническим результатом предлагаемого способа является увеличение терапевтической эффективности СОД, связанное с усилением способности СОД снижать выраженность окислительного стресса при глазных заболеваниях.
Технический результат достигается за счет инсталляций в конъюнктивальную полость СОД в составе кальций-фосфатных биодеградируемых наночастиц, покрытых дисахаридом, с радиусом 50-350 нм и в диапазоне ферментативной активности от 20 до 500 кЕД/мл.
Частицы получали по модифицированной нами методике, предложенной впервые в 2002 году [US Patent №6,355,271 B1, 12 March 2002]. В этой работе после смешивания растворов хлорида кальция и фосфата калия частицам давали состариться в течение 48 часов перед воздействием ультразвука. В этом случае помимо частиц с радиусом 50-200 нм образуются также частицы с радиусом около 500 нм и более. Мы использовали метод, при котором смешивание эквимолярных растворов хлорида кальция и фосфата калия проводилось одновременно с ультразвуковым воздействием продолжительностью 30 мин. После этого частицы оставляли стабилизироваться. В результате мы получали частицы с радиусом только до 350 нм. Для повышения стабильности частиц было использовано покрытие их 0,5% раствором целлобиозы или лактозы. Для приготовления препарата мы внедряли супероксиддисмутазу в КФЧ на стадии их получения. Была показана стабильность определяющих параметров КФЧ (размер, дзета-потенциал) при хранении в течение как минимум 6 месяцев. Показано, что активность СОД в составе КФЧ при хранении в виде водной суспензии при 4C° падает не более чем на 30% в течение 2 месяцев. Показано, что водные суспензии КФЧ, содержащие СОД, можно подвергать концентрированию на мембранных фильтрах без потери ими ферментативной активности и изменения размера и поверхностного заряда. Важно с технологической точки зрения, что СОД-содержащие КФЧ не теряют своих свойств в результате лиофилизации. Лиофильно высушенные КФЧ, содержащие СОД, могут храниться при -20°, по крайней мере, в течение полугода без изменения свойств.
Сравнительное изучение терапевтического действия СОД в растворе и СОД в составе КФЧ мы проводили на моделях воспалительного процесса, сопровождающегося окислительным стрессом, во внутренних (иммуногенный увеит - воспаление сосудистой оболочки глаза) и внешних (ожог роговицы) структурах глаза кроликов.
При увеите имеется высокая степень корреляции между выраженностью воспаления и окислительным стрессом. Ранее нами было показано, что инсталляции СОД при увеите у кроликов по своему терапевтическому действию не уступают общепринятому методу лечения увеитов с помощью дексаметазона, который вызывает много побочных эффектов. Кроме того, в отличие от дексаметазона, СОД в значительной степени снижает уровень окислительного стресса во внутренних средах глаза при увеите [Чеснокова Н.Б., Нероев В.В., Безнос О.В., Бейшенова Г.А., Никольская И.И., Кост О.А., Биневский П.В., Шехтер А.Б. Окислительный стресс при увеите и его коррекция антиоксидантным ферментом супероксиддисмутазой // Вестн. Офтальмол. 2014, т.30, №5, 30-36]. При ожоге глаза развивается воспалительный процесс, сопровождающийся значительным снижением антиоксидантного потенциала, что свидетельствует об истощении собственной антиоксидантной системы при окислительном стрессе [Гулидова О.В., Любицкий О.Б., Клебанов Г.И., Чеснокова Н.Б. Изменение антиокислительной активности слезной жидкости при экспериментальной ожоговой болезни глаз // Бюл. Эксп. Биол. Мед., 1999, 128, 11, 571-574].
Работа выполнена на 30 кроликах (60 глаз) породы шиншилла массой 2,0-2,5 кг. В первой серии экспериментов у 15 животных воспроизводили увеит путем двукратного введения нормальной лошадиной сыворотки: первую дозу (5 мл) вводили подкожно, вторую (0,07 мл) - интравитреально на 10-е сутки после первой [Нероев В.В., Давыдова Г.А., Перова Т.С. Моделирование иммуногенного увеита у кроликов // Бюл. Эксп. Биол. Мед., 2006, 142, 11, 598-600]. Во второй серии экспериментов 15 кроликам наносили дозированный ожог центральной области роговицы с помощью круга из хлопчатобумажной ткани диаметром 5 мм, пропитанного 1н. NaOH, с временем экспозиции 40 сек.
Для лечения использовали препарат Рексод-ОФ (ООО ′′НПП Ферментные технологии′′, Россия), представляющий собой рекомбинантную СОД человека (400 кЕД в 1 мг), и полученный нами препарат СОД в составе КФЧ, содержащий СОД с такой же активностью.
Кролики в каждой серии экспериментов были разбиты на 3 группы по 5 животных. Первой группе ежедневно в течение 7 дней при увеите и 14 дней при ожоге проводили инсталляции Рексод-ОФ 3 раза в день по 30 мкл в оба глаза, второй - раствор СОД в составе КФЧ в том же режиме, третьей - плацебо (буферный раствор рН 7,4).
Клиническую оценку течения увеита проводили ежедневно в течение 8 дней после начала, а ожогового процесса на 1, 3, 7, 14, 21 и 28 сутки после травмы путем биомикроскопии с помощью щелевой лампы. В условных баллах по принятой в лаборатории шкале оценивали выраженность следующих признаков: 1) при увеите - отек радужки, отек роговицы, количество фибрина в передней камере глаза, наличие задних синехий, помутнение хрусталика, интенсивность неоваскуляризации роговицы; 2) при ожоге роговицы - отек роговицы, площадь и глубину язв роговицы, интенсивность неоваскуляризации роговицы.
Результаты показали преимущество заявленного препарата СОД, внедренного в кальций-фосфатные наночастицы, по сравнению с коммерческим водным раствором СОД при местном применении при лечении заболеваний как внутренних, так и внешних структур глаза, сопровождающихся окислительным стрессом. При воспалении внутренних структур глаза, имеющем место при иммуногенном увеите у кроликов, преимущество применения СОД в КФЧ по сравнению с простым раствором СОД выражается в снижении интенсивности воспаления, снижении отека роговицы в острый период увеита в среднем на 20%, снижении на 40% количества фибриновых сгустков в передней камере глаза на протяжении всего периода наблюдения, что способствует сохранению прозрачности сред глаза и снижению вероятности возникновения осложнений, например, вторичной глаукомы вследствие закрытия фибриновыми сгустками путей оттока внутриглазной жидкости. Полученные данные могут напрямую свидетельствовать об улучшении проникновения СОД в составе КФЧ во внутренние структуры глаза (увеличение биодоступности) с сохраненной ферментативной активностью. На примере ожога роговицы глаза (оценивался воспалительный процесс во внешних структурах глаза) показана более высокая эффективность СОД в КФЧ по сравнению с простым раствором СОД, которая выражалась в более эффективном противоспалительном и противоязвенном действии, повышении прозрачности роговицы, снижении величины площади ее изъязвления в среднем на 22% и глубины язв на 27%. Полученные результаты свидетельствуют о более эффективном действии на течение постожогового воспалительного процесса СОД в КФЧ по сравнению с СОД в простом растворе, что может быть связано с лучшим проникновением СОД в составе наночастиц в ткань роговицы.
В рамках данной работы было показано, что включение в кальций-фосфатные частицы супероксиддисмутазы повышает эффективность действия фермента без повышения его концентрации. Это важно, поскольку позволяет снизить частоту закапывания препарата, а также снизить концентрацию действующей субстанции, что снижает вероятность побочного действия препарата и улучшает качество жизни пациента.
Способ осуществляют следующим образом. Суспензию СОД, внедренной в кальций-фосфатные наночастицы с радиусом 50-350 нм, в диапазоне активности от 20 до 500 кЕД/мл применяют местно в виде капель для снижения окислительного стресса (интенсивности свободнорадикальных процессов). Режим лечения зависит от вида и характера течения патологического процесса. Частота введения может варьировать от 2 до 5 закапываний в сутки. Лечение при острых процессах следует продолжать до достижения эффекта снижения клинических проявлений, а при хронических заболеваниях лечение следует проводить курсами по 2 недели 2-6 раз в год.
Апробация на экспериментальных моделях является необходимым этапом обоснования и внедрения любого нового метода лечения. Нами были выбраны модели воспалительных процессов у кроликов: в основном внешних (ожог) и в основном внутренних (увеит) структур глаза. Модель ожога глаза у кроликов воспроизводит все проявления и стадии ожоговой болезни глаз у человека, сопровождается локальным усилением свободнорадикальных процессов [Burgalassi S, Nicosia N, Monti D, Falcone G, Boldrini E, Fabiani O, Lenzi C, Pirone A, Chetoni P. Arabinogalactan as active compound in the management of corneal wounds: in vitro toxicity and in vivo investigations on rabbits // Eye Res., 2011, 36, 1, 21-28; Гулидова O.B., Любицкий О.Б., Клебанов Г.И., Чеснокова Н.Б. Изменение антиокислительной активности слезной жидкости при экспериментальной ожоговой болезни глаз // Бюл. Экспер. Биол. Мед., 1999, 128, 11, 571-574]. Патогенетические механизмы развития иммуногенного увеита у кроликов соответствуют закономерностям развития увеита у человека, и поэтому эта модель используется для обоснования новых методов лечения увеита. Показана роль окислительного стресса при увеите у кроликов и у человека [Yadav U.С.S., Kalariya N.М., Ramana К.V. Emerging role of antioxidants in the protection of uveitis complications // Curr. Med. Chem., 2011, 18, 931-942]. Поэтому полученные нами результаты экспериментального исследования, в которых было показано увеличение терапевтической эффективности СОД, внедренной в кальций-фосфатные наночастицы, по сравнению с простым раствором фермента, можно использовать для обоснования целесообразности применения этого метода доставки СОД в глаз человека.
Способ поясняется следующими примерами.
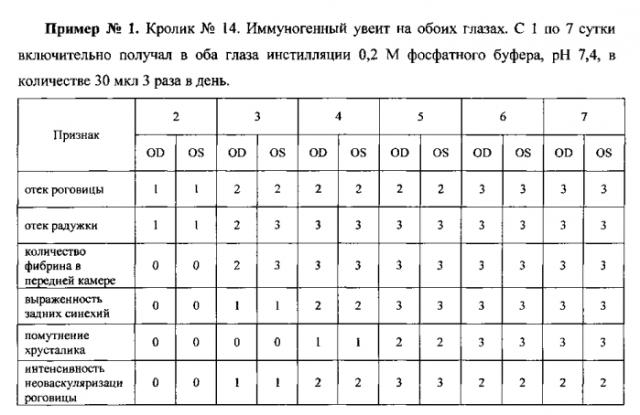
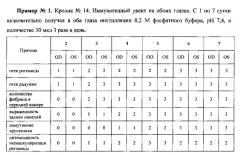
Оценка клинической картины показала, что у кролика №14 в течение всего периода наблюдения признаки увеита были ярко выражены: конъюнктива отечна и гиперемирована, развивались прогрессирующие отек роговицы, отек и гиперемия радужки, во влаге передней камеры в большом количестве обнаруживался фибрин, формировались задние синехии, в большинстве случаев круговые, хрусталик становился диффузно мутным, стекловидное тело сквозь него не визуализировалось, отмечалась выраженная неоваскуляризация роговицы.
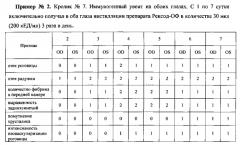
У кролика №7 признаки конъюнктивита были выражены незначительно, перикорнеальная инъекция конъюнктивы - умеренно. Отек роговицы был локальным, не резко выраженным и со временем уменьшался, как и отек радужки. Количество фибрина в передней камере и неоваскуляризация роговицы были менее выражены, чем у кролика №14. Во время лечения отмечался регресс задних синехий и частичное восстановление реакции зрачка на свет. Помутнение хрусталика было незначительным. Таким образом, лечение препаратом Рексод, содержащим фермент в виде простого водного раствора, привело к существенному снижению выраженности всех проявлений увеита по сравнению с кроликом, получавшим плацебо.
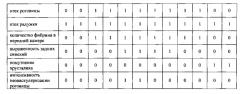
У кролика №13, получавшего инсталляции СОД в наночастицах, проявления увеита были еще меньше выражены, чем у кролика №7, получавшего фермент в растворе. Отек и гиперемия век были очень незначительны. Самые большие различия заключались в существенно меньшем содержании фибрина в передней камере глаза, что способствует лучшему сохранению прозрачности оптических сред глаза и снижению вероятности развития вторичной глаукомы вследствие закупорки путей оттока внутриглазной жидкости.
Сразу после ожога на месте нанесения травмы образовался дефект эпителия, который в течение 3-х дней закрывался, но в последующие дни вновь обнажалась строма роговицы, в которой начинался процесс ее изъязвления. Максимальная интенсивность изъязвления достигалась на 14-21 сутки, при этом на одном глазу образовалось десцеметоцеле (язва роговицы до десцеметовой базальной мембраны), создающее угрозу перфорации роговицы, а на 28 сутки на месте ожога оставалось точечное изъязвление. Наблюдался отек роговицы, рост в ней новообразованных сосудов, в обоих глазах отмечен гипопион (наличие гноя в передней камере глаза). Отмечался значительный отек век, отек и гиперемия конъюнктивы. Отек области роговицы, окружающей ожог, делал ее полностью непрозрачной.
У кролика №24, получавшего Рексод, отек век, отек и гиперемия конъюнктивы были меньше, чем у кролика №17, получавшего плацебо. Через область роговицы, окружающей ожог, можно было различить радужку, что свидетельствует о меньшей отечности этой ткани. Существенно ниже была интенсивность изъязвления роговицы, в передней камере глаза гипопиона не отмечалось. К 28 суткам формировалась рубцовая ткань без признаков изъязвления.
У кролика №29, получавшего СОД в наночастицах, на всем протяжении наблюдения отек и гиперемия век и конъюнктивы были менее выражены, чем у кролика №24, получавшего СОД в простом растворе. Степень изъязвления роговицы также снижалась и по глубине и площади не превышала умеренного уровня, на 28 сутки формировалась более нежная рубцовая ткань без признаков изъязвления. Через полупрозрачную область роговицы, окружающей ожог, хорошо просматривался рисунок радужки. Гноя в передней камере глаза не было.
Таким образом, применение супероксиддисмутазы, внедренной в кальций-фосфатные наночастицы, в виде местных инсталляций для лечения ожога глаз позволяет снизить выраженность воспалительной реакции тканей глаза, снизить интенсивность изъязвления роговицы по сравнению с применением простого раствора СОД, что приводит к образованию более нежной рубцовой ткани, что, в свою очередь, улучшает оптические свойства роговицы и позволяет лучше сохранить зрение.
Внедрение СОД в кальций-фосфатные наночастицы позволяет обеспечить усиление терапевтического эффекта при лечении заболеваний глаза, сопровождающихся окислительным стрессом как во внешних, так и внутренних структурах глаза. В данном исследовании мы сравнивали одинаковые режимы и дозы введения СОД в растворе и СОД в КФЧ. Полученные данные, свидетельствующие о большей терапевтической эффективности фермента в составе наночастиц, позволяют полагать, что его можно применять менее часто и в меньшей дозе, чем препарат в простом растворе. В то же время выбор дозы и режима применения должен зависеть от тяжести, локализации, характера течения патологии.
Показанием к применению супероксиддисмутазы в составе кальций-фосфатных наночастиц является широкий круг глазных болезней, в патогенезе которых большую роль играет усиление процессов свободнорадикального окисления. Это воспалительные процессы любой этиологии и локализации, нейродегенеративные процессы в сетчатке, включая глаукому и возрастную дистрофию сетчатки, диабетическая ретинопатия, профилактика катаракты. Метод получения СОД в составе КФЧ достаточно прост, не требует применения органических растворителей, сами частицы биосовместимы и биодеградируемы, обладают высокой биодоступностью и позволяют создать в тканях высокую концентрацию активного фермента.
Способ лечения заболеваний глаз, сопровождающихся окислительным стрессом, включающий инсталляции в конъюнктивальную полость препарата на основе супероксиддисмутазы (СОД), отличающийся тем, что СОД вводят в составе кальций-фосфатных биодеградируемых наночастиц, покрытых дисахаридами, с радиусом до 350 нм и в диапазоне ферментативной активности от 20 до 500 кЕД/мл.