Способ получения катализатора метатезисной полимеризации дициклопентадиена
Иллюстрации
Показать всеИзобретение относится к металлоорганической химии, в частности к способу производства карбенового комплекса рутения, который является катализатором полимеризации циклических олефинов, в частности дициклопентадиена. Трифенилфосфиновый комплекс рутения подвергают взаимодействию с 1,1-дифенил-2-пропин-1-олом в тетрагидрофуране или диоксане в присутствии неорганической кислоты при нагревании до температуры 65-100°С в инертной атмосфере. После удаления кислоты к полученному комплексу (3-фенилинденилид-1-ен)RuCl2(РРh3)2 добавляют хлороформенный аддукт, выбранный из группы: 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин, 3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин, 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин. Смесь нагревают до температуры 60-80°С и перемешивают в течение 2-3 ч в инертной атмосфере. Полученную смесь последовательно подвергают взаимодействию с пиридином при комнатной температуре, а затем при температуре 60-80°С с соответствующим N-замещенным 2-винилбензиламином. Изобретение обеспечивает повышение экологической безопасности технологии, в частности снижение взрыво-, пожароопасности и токсической нагрузки, упрощение технологии и сокращение времени на получение готового продукта за счет исключения промежуточных стадий выделения и очистки интермедиатов. 59 пр.
Реферат
Изобретение относится к металлоорганической химии, в частности к способу производства карбенового комплекса рутения, который является катализатором полимеризации циклических олефинов, в частности дициклопентадиена (ДЦПД).
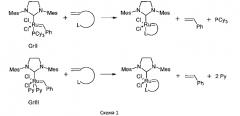
В US 2005261451 А, 24.11.2005 представлен ряд структур с контролируемой каталитической активностью, схемы синтеза которых основаны на катализаторе Граббса
второго поколения (GrII) и на его пиридиновом производном (GrIII), при этом GrII либо GrIII обрабатывается хелатирующим олефином в хлористом метилене при комнатной температуре или нагревании до 40°С:
Способ получения GrIII основан на обработке GrII пиридином. Получение GrIII как основы для синтеза катализаторов дополнительно усложняет процесс, добавляя новую стадию, на которой теряется около 15% рутения. M.S. Sanford, J.A. Love, R.H. Grubbs. A versatile precursor for the synthesis of rutherium olefin metathesis catalysts, Organometallics, 2001, v. 20, p. 5314-5318.
Недостатком способа является невысокий выход целевого продукта, который составляет от 50 до 65%, исходя из GrI. Это обусловлено многостадийностью синтеза и несовершенством методики: использованием хлорида меди для связывания трициклогексилфосфина и хлористого метилена - низкокипящего растворителя, не позволяющего в обычных условиях поднять температуру реакционной смеси выше 40°С.
Дорогостоящие GrI и GrII могут быть заменены на их более дешевые инденилиденовые аналоги: In(I.2), который быстро и с высоким выходом синтезируется при проведении реакции в диоксане или тетрагидрофуране (пат. WO 2010037550 A1, ЕР 2280033), и In(II.2), при этом синтез может проводиться в одном реакторе без выделения промежуточных продуктов.
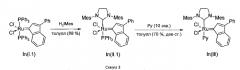
Известен также синтез инденилиденового аналога комплекса GrIII из комплекса In(I.1) без выделения промежуточного In(II.1):
Urbina-Blanco, Cesar A. et al., Design and synthesis of ruthenium indenylidene-based catalysts for olefin metathesis. Chem. Commun., 2011, v. 47, p. 5022-5024).
Общим недостатком данных способов является использование неустойчивого на воздухе и неудобного в обращении свободного карбена H2IMes.
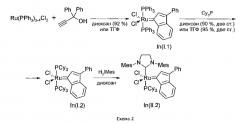
Наиболее близким к заявляемому способу является способ получения рутениевого катализатора полимеризации дициклопентадиена - RU 2462308 С1, 27.09.2012, ЕР 2280033 В1, 17.03.2011, включающий следующие стадии ведения процесса. Первая стадия - синтез инденилиденового комплекса In(I.2) по следующей схеме:
Вторая стадия включает последовательную обработку In(I.2) N-гетероциклическим карбеновым лигандом [1,3-бис-(2,4,6-триметилфенил)-2-трихлорметилимидазолидином, H2IMes(H)CCl3] и соответствующим 2-винилбензиламином с образованием целевого продукта, и осуществляется по следующей схеме:
Недостатком данного способа является двухстадийность процесса с необходимостью выделения In(I.2) и применение в качестве промежуточного вспомогательного лиганда дорогостоящего, токсичного и неустойчивого на воздухе трициклогексилфосфина.
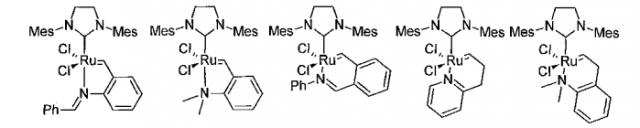
Техническая задача, решаемая заявленным изобретением, заключается в разработке упрощенного, осуществляемого в одном реакционном сосуде, способа получения катализатора метатезисной полимеризации дициклопентадиена с раскрытием цикла, с общей формулой:
где Ar - 2,4,6-триметилфенил, 2,6-диметилфенил или 2,6-диизопропилфенил и L - заместитель, выбранный из группы:
Технический результат от реализации изобретения заключается в повышении экологической безопасности технологии, в частности, снижении взрыво-, пожароопасности и токсической нагрузки, упрощении технологии и сокращении времени на получение готового продукта за счет исключения промежуточных стадий выделения и очистки интермедиатов.
Технический результат достигается тем, что трифенилфосфиновый комплекс дихлорида рутения подвергают взаимодействию с 1,1-дифенил-2-пропин-1-олом в тетрагидрофуране или диоксане в присутствии неорганической кислоты при нагревании до температуры 65-100°С в инертной атмосфере, затем кислоту удаляют и к полученному комплексу (3-фенилинденилид-1-ен)RuCl2(PPh3)2 добавляют хлороформенный аддукт, выбранный из группы:
1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин,
1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин,
1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин,
смесь нагревают до температуры 60-80°С и перемешивают в течение 2-3 ч в инертной атмосфере, после чего смесь последовательно подвергают взаимодействию с пиридином при комнатной температуре, а затем при температуре 60-80°С с N-замещенным 2-винилбензил амином, где L выбран из группы:
Способ осуществляют в одном реакторе в инертной атмосфере по следующей схеме:
где Ar - 2,4,6-триметилфенил, 2,6-диметилфенил или 2,6-диизопропилфенил и L - заместитель, выбранный из группы:
Хлорид рутения(III) взаимодействует с трифенилфосфином, образуя трифенилфосфиновый комплекс хлорида рутения. Последний взаимодействует с 1,1-дифенилпропинолом, образуя инденилиденовый комплекс рутения с трифенилфосфиновыми лигандами In(I.1). Далее In(I.1) вводят в реакцию с хлороформенным аддуктом имидазола, образуя комплекс второго поколения In(II.1). Комплекс In(II.1) взаимодействует с пиридином, образуя комплекс третьего поколения In(III), который затем обрабатывают N-замещенным 2-винилбензиламином.
Этап 1 осуществляют при кипячении хлорида рутения(III) с трифенилфосфином в растворителе, выбранном из ряда низших алифатических спиртов или их смесей, предпочтительно в этаноле или метаноле. Стадии 2-5 проводят в растворителе, выбранном из ряда простых, линейных или циклических, эфиров или диэфиров или их смесей, предпочтительно в 1,4-диоксане, тетрагидрофуране.
Этап 2 осуществляют при нагревании трифенилфосфинового комплекса хлорида рутения с 1,1-дифенилпропин-1-олом в присутствии кислого катализатора, предпочтительно летучей минеральной кислоты, наиболее предпочтительно хлористого водорода.
Этап 3 осуществляют при нагревании комплекса In(I.1) с 1,3-бис-(2,4,6-триметилфенил)-2-трихлорметилимидазолидином (H2IMes(H)CCl3).
Этап 4 осуществляют при обработке комплекса In(II.1) пиридином при комнатной температуре.
Этап 5 осуществляют при нагревании комплекса In(III) с соответствующим N-замещенным 2-винилбензил амином.
Этап 6 - выделение продукта стандартными методами: перекристаллизацией, экстракцией или колоночной хроматографией.
Выход целевого продукта составляет 70% и более.
Изобретение поясняется следующими примерами.
Пример 1
Синтез катализатора проводят в условиях, исключающих попадание влаги и воздуха в реакционную систему. Используют технику и реакторы Шленка, подсоединенные к вакуумной системе и линии сухого аргона или азота. Растворители: метанол, диэтиловый эфир, диоксан, гексан, пиридин абсолютируют по стандартным методикам и хранят в инертной атмосфере. Чистоту катализаторов оценивают на основании спектров протонного магнитного резонанса (ЯМР 1Н) и(или) тонкослойной хроматографии ТСХ (гексан-этилацетат).
В колбу Шленка на 100 мл помещают 1,3 г (5,3 ммоль) хлорида рутения(III) гидрата и 8,4 г (31,8 ммоль) трифенилфосфина, заполняют аргоном. Добавляют 65 мл метанола, и кипятят в атмосфере аргона в течение 4 ч при перемешивании. Охлаждают до комнатной температуры и удаляют жидкую фазу. К твердому остатку добавляют 1,5 г (7,2 ммоль) 1,1-дифенил-2-пропин-1-ола, 50 мл диоксана и 1,2 мл (4,8 ммоль) 4 М раствора HCl в диоксане, перемешивают в течение 0,5 ч при температуре 100°С. Далее реакционную смесь упаривают на 50%, потери компенсируют свежим растворителем. Затем добавляют 3,8 г (9 ммоль) 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидина и перемешивают в течение 3 ч при температуре 70°С в инертной атмосфере. Смесь охлаждают до комнатной температуры, добавляют 4,3 мл (53 ммоль) пиридина, перемешивают в течение 1 ч, после чего добавляют 2,5 г (13,3 ммоль) 2-(N,N-диэтиламинометил)стирола (N5) и перемешивают в течение 1 ч при температуре 70°С в инертной атмосфере. После обработки реакционной смеси получают 2,5 г (3,8 ммоль, 72%) чистого [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-диэтиламинометилфенилметилен)рутения в виде светло-зеленого порошка, чистого по ТСХ. Спектр 1Н ЯМР (CDCl3, 400 МГц), δН, м.д.: 18,73 (1Н, с); 7,41-7,53 (1Н, м); 7,08-7,18 (1H, м); 7,03 (4Н, с); 6,91-6,99 (1H, м); 6,54-6,63 (1H, м); 4,25 (2Н, уш. с); 3,95-4,16 (4Н, м); 2,87-3,04 (2Н, м); 2,67 (6Н, уш. с); 2,44 (3Н, уш. с); 2,35 (9Н, уш. с); 1,96-2,10 (2Н, м); 0,47 (6Н, т, J=7,0 Гц). Элементный анализ: для C33H43Cl2N3Ru вычислено С (60,63%), Н (6,63%), N (6,43%); найдено С (60,69%), Н (6,71%), N (6,32%).
Пример 2
В колбу Шленка на 250 мл помещают 1,3 г (5,3 ммоль) хлорида рутения(III) гидрата и 8,4 г (31,8 ммоль) трифенилфосфина, заполняют аргоном. Добавляют 65 мл этанола и кипятят в атмосфере аргона в течение 4 ч при перемешивании. Охлаждают до комнатной температуры и удаляют жидкую фазу. К твердому остатку добавляют 1,5 г (7,2 ммоль) 1,1-дифенил-2-пропин-1-ола, 125 мл ТГФ и 1,6 мл (4,8 ммоль) 3 М раствора HCl в диэтиловом эфире и перемешивают в течение 3 ч при температуре 65°С. Далее реакционную смесь частично упаривают для удаления HCl, потери компенсируют свежим растворителем. Затем добавляют 3,8 г (9 ммоль) 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидина и перемешивают в течение 3 ч при температуре 60°С в инертной атмосфере. Смесь охлаждают до комнатной температуры, добавляют 4,3 мл (53 ммоль) пиридина, перемешиваютв течение 1 ч, после чего добавляют 2,2 г (13,3 ммоль) 2-(N,N-диметиламинометил)стирола (N1) и перемешивают в течение 3 ч при температуре 60°С в инертной атмосфере. После обработки реакционной смеси получают 2,2 г (3,6 ммоль, 67%) чистого [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-диметиламинометилфенилметилен)рутения в виде темно-зеленого порошка, чистого по ТСХ. Спектр 1Н ЯМР (CD2Cl2, 300 МГц), δН, м.д.: 18,58 (1H, с); 7,38-7,50 (1H, м); 7,08-7,18 (1H, м); 6,88-7,00 (5Н, м); 6,59-6,68 (1Н, м); 4,01 (6Н, уш. с); 2,00-2,90 (18Н, м); 1.75 (6Н, с). Элементный анализ: для C31H39Cl2N3Ru вычислено С (59,51%), Н (6,28%), N (6,72%); найдено С (59,63%), Н (6,44%), N (6,59%).
Пример 3
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N4. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-бутиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 55%. Спектр 1Н ЯМР (CDCl3, 600 МГц), δН, м.д.: 18,77 (1H, с); 7,47 (1H, т, J=6,14 Гц, J=8,18 Гц); 7,12 (1H, т, J=6,14 Гц, J=8,18 Гц); 6,8-7.2 (4H, м); 6,97 (1H, д, J=6,14 Гц); 6,60 (1H, д, J=6,14 Гц); 5,39 (1H, д, J=14,3 Гц), 3,85-4.22 (4Н, м.); 3,17 (1H, м.); 3,85-4.22 (4Н, м); 3,04-2,3 (17Н, м); 2,01-1,90 (4Н, м);1,72 (3Н, уш. с); 1,60 (2Н, уш. с); 1,14-1,09 (4Н, м); 0,71 (3Н, т, J=8,1 Гц). Элементный анализ: для C34H45Cl2N3Ru вычислено С (61,16%), Н (6,79%), N (6,29%); найдено С (61,20%), Н (6,88%), N(6,15%).
Пример 4
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N14. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-бензиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 69%. Спектр 1Н ЯМР (CDCl3, 600 МГц), δН, м.д.: 18,74 (1Н, с); 7,44 (1H, т, J=6,13 Гц, J=8,18 Гц); 7.28 (5Н, м); 7,14 (1H, т, J=6,13 Гц, J=8,18 Гц); 6,95-7.10 (5Н, м); 6,88 (1H, д, J=6,13 Гц); 6,73 (1Н, д, J=6,13 Гц); 4,14 (4Н, уш. с); 2,20-2,45 (18Н, уш. с); 1,81 (3Н, уш. с); 1,52 (2Н, уш. с). Элементный анализ: для C37H43Cl2N3Ru вычислено С (63,33%), Н (6,18%), N (5,99%); найдено С (63,41%), Н (6,37%), N (5,83%).
Пример 5
Осуществляют аналогично примеру 1, но вместо 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидина взят 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-диэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 67%. Спектр 1Н ЯМР (CDCl3, 400 МГц), δН, м.д.: 18,63 (1Н, с); 7,40-7,48 (1Н, м); 7,30-7,37 (2Н, м); 7,19 (4Н, м); 7,05-7,13 (1H, м); 6,91-6,99 (1H, м); 6,51-6,59 (1H, м); 4,20 (2Н, уш. с); 3,97-4,18 (4Н, м); 2,83-3,00 (2Н, м); 2,70 (6Н, уш. с); 2,40 (6Н, уш. с); 1,92-2,06 (2Н, м); 0,46 (6Н, т, J=7,3 Гц). Элементный анализ: для C31H39Cl2N3Ru вычислено С (59,51%), Н (6,28%), N (6,72%); найдено С (59,66%), Н (6,39%), N (6,61%).
Пример 6
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N1, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-диметиламинометилфенилметилен)рутений в виде салатового порошка, чистый по данным ТСХ и ЯМР. Выход 36%. Спектр 1Н ЯМР (CDCl3, 600 МГц), δН, м.д.: 18,60 (1H, с); 7,45-7,60 (2Н, м); 7,37-7,43 (1Н, м); 7,28-7,37 (4Н, м); 7,07-7,12 (1H, м); 6,91-6,95 (1Н, м); 6,49-6,54 (1H, м); 2,77-4,44 (10Н, м); 1,99 (6Н, уш. с); 0,57-1,53 (24Н, м). Элементный анализ: для C37H51Cl2N3Ru вычислено С (62,61%), Н (7,24%), N (5,92%); найдено С (62,79%), Н (7,37%), N (5,81%).
Пример 7
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N19. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден] дихлоро(о-1-пиперидинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 52%. Спектр 1Н ЯМР (CDCl3, 400 МГц), δН, м.д.: 18,68 (1Н, с); 7,38-7,44 (1H, м); 7,06-7,12 (1H, м); 7,01 (4Н, уш. с), 6,95-7,01 (1Н, м); 6,60-6,66 (1Н, м); 4,49 (2Н, уш. с); 4,07 (4Н, уш. с); 2,19-2,73 (22Н, м); 1,41-1,66 (6Н, м). Элементный анализ: для C34H43Cl2N3Ru вычислено С (61,34%), Н (6,51%), N (6,31%); найдено С (61,41%), Н (6,64%), N (6,25%).
Пример 8
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N17. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-1-пирролидинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 65%. Спектр 1Н ЯМР (CD2Cl2, 400 МГц), δН, м.д.: 18,78 (1Н, с); 7,45-7,51 (1H, м); 7,14-7,20 (1Н, м); 7,02 (4Н, уш. с), 6,94-6,99 (1H, м); 6,66-6,71 (1Н, м); 4,21 (2Н, уш. с); 4,07 (4Н, уш. с); 2,65-2,73 (2Н, м); 2,47 (12Н, уш. с); 2,38 (6Н, уш. с); 2,04-2,13 (2Н, м); 1,40-1,49 (2Н, м); 1,21-1,32 (2Н, м). Элементный анализ: для C33H41Cl2N3Ru вычислено С (60,82%), Н (6,34%), N (6,45%); найдено С (60,98%), Н (6,47%), N (6,26%).
Пример 9
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N21. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-4-морфолинометилфенилметилен)рутений в виде синевато-зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 27%. Спектр 1Н ЯМР (CD2Cl2, 400 МГц), δН, м.д.: 18,88 (1H, с); 7,42-7,48 (1H, м); 7,17-7,23 (1H, м); 7,05 (4Н, уш. с), 7,01-7,04 (1H, м); 6,58-6,63 (1Н, м); 4,08 (6Н, уш. с); 3,49-3,56 (2Н, м); 3,11-3,19 (2Н, м); 2,95-3,04 (2Н, м); 2,33-2,64 (18Н, м); 1,96-2,02 (2Н, м). Элементный анализ: для C33H41Cl2N3ORu вычислено С (59,36%), Н (6,19%), N (6,29%); найдено С (59,53%), H (6,32%), N (6,11%).
Пример 10
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N2. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-этиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 67%. Спектр 1Н ЯМР (CD2Cl2, 400 МГц), δН, м.д.: 18,70 (1H, с); 7,46-7,53 (1Н, м); 6,86-7,25 (6Н, м); 6,58-6,63 (1H, м); 5,23 (1Н, д, J=13,9 Гц); 4,04 (4Н, уш. с); 3,15-3,26 (1Н, м); 2,92 (1H, д, J=13,9 Гц); 2,28-2,84 (15Н, м); 1,87-2,14 (4Н, м); 1,61 (3Н, с); 0,46 (3Н, т, J=7,3 Гц). Элементный анализ: для C32H41Cl2N3Ru вычислено С (60,09%), Н (6,46%), N (6,57%); найдено С (60,22%), Н (6,56%), N (6,44%).
Пример 11
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N8. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 61%. Спектр 1Н ЯМР (CDCl3, 300 МГц), δН, м.д.: 18,75 (1Н, с); 7,41-7,51 (1H, м); 6,95-7,13 (6Н, м); 6,53-6,63 (1H, м); 5,34 (1H, д, J=13,7 Гц); 3,93-4,14 (4Н, м); 3,91-3,98 (1H, м); 3,35-3,41 (1Н, м); 2,96-3.14 (6Н, м); 2.19-2.58 (18Н, м); 1.81 (3Н, с). Элементный анализ: для C33H43Cl2N3ORu вычислено С (59,18%), Н (6,47%), N (6,27%); найдено С (59,33%), Н (6,61%), N (6,13%).
Пример 12
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N12. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-фениламинометилфенилметилен)рутений в виде зеленого порошка, чистый по данным ТСХ и ЯМР. Выход 31%. Спектр 1Н ЯМР (CDCl3, 400 МГц), δН, м.д.: 18,83 (1Н, с); 7,47-7,53 (1H, м); 7,02-7,24 (9Н, м); 6,85-6,89 (1H, м); 6,68-6,71 (1Н, м); 6,65-6,68 (1Н, м); 6,12 (1H, д, J=2,8 Гц); 4,01-4,10 (2Н, м); 3,83-3,92 (2Н, м); 3,46 (1H, д, J=2,8 Гц); 2,84 (3H, с); 2,71 (3H, с); 2,41 (3H, с); 2,36 (3H, с); 2,19 (3H, с); 2,06 (3H, с); 1,96 (3H, с). Элементный анализ: для C36H41Cl2N3Ru вычислено С (62,87%), Н (6,01%), N (6,11%); найдено С (63,03%), Н (6,20%), N (5,97%).
Пример 13
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N3. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-пропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 59%. Элементный анализ: для C33H43Cl2N3Ru вычислено С (60,63%), Н (6,63%), N (6,43%); найдено С (60,77%), Н (6,89%), N (6,29%).
Пример 14
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N6. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-пропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 52%. Элементный анализ: для C34H45Cl2N3Ru вычислено С (61,16%), Н (6,79%), N (6,29%); найдено С (61,27%), Н (6,93%), N (6,13%).
Пример 15
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N7. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-дипропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 52%. Элементный анализ: для C35H47Cl2N3Ru вычислено С (61,66%), Н (6,95%), N (6,16%); найдено С (61,77%), Н (7,12%), N (6,04%).
Пример 16
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N9. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 55%. Элементный анализ: для C34H45Cl2N3ORu вычислено С (59,73%), Н (6,63%), N (6,15%); найдено С (59,81%), Н (6,79%), N (5,99%).
Пример 17
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N10. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-пропил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 47%. Элементный анализ: для C35H47Cl2N3ORu вычислено С (60,25%), Н (6,79%), N (6,02%); найдено С (60,34%), Н (6,98%), N (5,89%).
Пример 18
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N11. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-ди-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 33%. Элементный анализ: для C35H47Cl2N3O2Ru вычислено С (58,90%), Н (6,64%), N (5,89%); найдено С (59,11%), H (6,86%), N (5,72%).
Пример 19
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N13. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-фениламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 32%. Элементный анализ: для C37H43Cl2N3Ru вычислено С (63,33%), Н (6,18%), N (5,99%); найдено С (63,49%), Н (6,36%), N (5,82%).
Пример 20
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N15. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-бензиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 64%. Элементный анализ: для C38H45Cl2N3Ru вычислено С (63,77%), Н (6,34%), N (5,87%); найдено С (63,88%), Н (6,48%), N (5,79%).
Пример 21
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N16. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро(о-N-пропил-N-бензиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 57%. Элементный анализ: для C39H47Cl2N3Ru вычислено С (64,19%), Н (6,49%), N (5,76%); найдено С (64,26%), Н (6,65%), N (5,69%).
Пример 22
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N18. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро[о-2-(2,3-дигидро-1H-изоиндолил)-метилфенилметилен]рутений в виде зеленого порошка, чистый по ТСХ. Выход 44%. Элементный анализ: для C37H41Cl2N3Ru вычислено С (63,51%), Н (5,91%), N (6,01%); найдено С (63,69%), Н (6,11%), N (5,83%).
Пример 23
Осуществляют аналогично примеру 1, но вместо 2-винилбензиламина N5 взят 2-винилбензиламин N20. Получен катализатор [1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден]дихлоро[о-2-(1,2,3,4-тетрагидроизохинолинил)метилфенилметилен]рутений в виде зеленого порошка, чистый по ТСХ. Выход 39%. Элементный анализ: для C38H43Cl2N3Ru вычислено С (63,95%), Н (6,07%), N (5,89%); найдено С (64,12%), Н (6,24%), N (5,73%).
Пример 24
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N2, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-этиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 64%. Элементный анализ: для C30H37Cl2N3Ru вычислено С (58,91%), Н (6,10%), N (6,87%); найдено С (59,00%), Н (6,17%), N (6,75%).
Пример 25
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N3, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-пропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 58%. Элементный анализ: для C31H39Cl2N3Ru вычислено С (59,51%), Н (6,28%), N (6,72%); найдено С (59,59%), Н (6,44%), N (6,61%).
Пример 26
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N4, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-бутиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 51%. Элементный анализ: для C32H41Cl2N3Ru вычислено С (60,09%), Н (6,46%), N (6,57%); найдено С (60,22%), Н (6,57%), N (6,46%).
Пример 27
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N6, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-пропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 48%. Элементный анализ: для C32H41Cl2N3Ru вычислено С (60,09%), Н (6,46%), N (6,57%); найдено С (60,12%), Н (6,53%), N (6,49%).
Пример 28
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N7, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-дипропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 53%. Элементный анализ: для C33H43Cl2N3Ru вычислено С (60,63%), Н (6,63%), N (6,43%); найдено С (60,76%), Н (6,78%), N (6,32%).
Пример 29
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N8, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 59%. Элементный анализ: для C31H39Cl2N3ORu вычислено С (58,03%), Н (6,13%), N (6,55%); найдено С (58,20%), Н (6,29%), N (6,41%).
Пример 30
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N9, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 57%. Элементный анализ: для C32H41Cl2N3ORu вычислено С (58,62%), Н (6,30%), N (6,41%); найдено С (58,82%), Н (6,48%), N (6,23%).
Пример 31
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N10, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-пропил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 41%. Элементный анализ: для C33H43Cl2N3ORu вычислено С (59,18%), Н (6,47%), N (6,27%); найдено С (59,33%), H (6,64%), N (6,09%).
Пример 32
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N11, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-ди-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 36%. Элементный анализ: для C33H43Cl2N3O2Ru вычислено С (57,80%), Н (6,32%), N (6,13%); найдено С (57,93%), Н (6,47%), N (5,95%).
Пример 33
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N13, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-фениламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 27%. Элементный анализ: для C35H39Cl2N3Ru вычислено С (62,40%), Н (5,84%), N (6,24%); найдено С (62,44%), Н (5,91%), N (6,13%).
Пример 34
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N14, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-бензиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 63%. Элементный анализ: для C35H39Cl2N3Ru вычислено С (62,40%), Н (5,84%), N (6,24%); найдено С (62,49%), Н (5,98%), N (6,02%).
Пример 35
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N15, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-бензиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 65%. Элементный анализ: для C36H41Cl2N3Ru вычислено С (62,87%), Н (6,01%), N (6,11%); найдено С (63,01%), Н (6,22%), N (5,97%).
Пример 36
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N16, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-N-пропил-N-бензиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 61%. Элементный анализ: для C37H43Cl2N3Ru вычислено С (63,33%), Н (6,18%), N (5,99%); найдено С (63,47%), Н (6,35%), N (5,85%).
Пример 37
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N17, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-1-пирролидинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 59%. Элементный анализ: для C31H37Cl2N3Ru вычислено С (59,70%), Н (5,98%), N (6,74%); найдено С (59,81%), Н (6,14%), N (6,63%).
Пример 38
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N18, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-2-(2,3-дигидро-1H-изоиндолил)метилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 51%. Элементный анализ: для C35H37Cl2N3Ru вычислено С (62,59%), Н (5,55%), N (6,26%); найдено С (62,77%), Н (5,66%), N (6,12%).
Пример 39
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N20, соответственно. Получен катализатор [1,3-бис-(2,6-диметилфенил)-2-имидазолидинилиден]дихлоро(о-2-(1,2,3,4-тетрагидроизохинолинил)метилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 35%. Элементный анализ: для C35H37Cl2N3Ru вычислено С (63,06%), Н (5,73%), N (6,13%); найдено С (63,19%), Н (5,81%), N (5,98%).
Пример 40
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N2, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-этиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 39%. Элементный анализ: для C38H53Cl2N3Ru вычислено С (63,05%), Н (7,38%), N (5,81%); найдено С (63,29%), Н (7,51%), N(5,69%).
Пример 41
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N3, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-пропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 34%. Элементный анализ: для C39H55Cl2N3Ru вычислено С (63,48%), Н (7,51%), N (5,69%); найдено С (63,61%), Н (7,64%), N (5,53%).
Пример 42
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N4, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-бутиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 25%. Элементный анализ: для C40H57Cl2N3Ru вычислено С (63,90%), Н (7,64%), N (5,59%); найдено С (64,07%), Н (7,77%), N (5,43%).
Пример 43
Осуществляют аналогично примеру 1, но вместо 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидина взят 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометил имидазолидин. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-диэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 37%. Элементный анализ: для C39H55Cl2N3Ru вычислено С (63,48%), Н (7,51%), N (5,69%); найдено С (63,63%), Н (7,69%), N (5,52%).
Пример 44
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N6, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-пропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 22%. Элементный анализ: для C40H57Cl2N3Ru вычислено С (63,90%), Н (7,64%), N (5,59%); найдено С (64,02%), Н (7,71%), N (5,40%).
Пример 45
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N7, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-дипропиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 29%. Элементный анализ: для C41H59Cl2N3Ru вычислено С (64,30%), Н (7,76%), N (5,49%); найдено С (64,52%), Н (7,80%), N (5,35%).
Пример 46
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N8, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 33%. Элементный анализ: для C39H55Cl2N3ORu вычислено С (62,14%), Н (7,35%), N (5,57%); найдено С (62,32%), Н (7,49%), N (5,49%).
Пример 47
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N9, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 26%. Элементный анализ: для C40H57Cl2N3ORu вычислено С (62,57%), Н (7,48%), N (5,47%); найдено С (62,74%), Н (7,61%), N (5,29%).
Пример 48
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N10, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-пропил-N-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 20%. Элементный анализ: для C41H59Cl2N3ORu вычислено С (62,98%), Н (7,61%), N (5,37%); найдено С (63,16%), Н (7,75%), N (5,23%).
Пример 49
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N11, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N,N-ди-2-метоксиэтиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 17%. Элементный анализ: для C41H59Cl2N3O2Ru вычислено С (61,72%), Н (7,45%), N (5,27%); найдено С (61,82%), Н (7,62%), N (5,09%).
Пример 50
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N12, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-фениламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 23%. Элементный анализ: для C42H53Cl2N3Ru вычислено С (65,35%), Н (6,92%), N (5,44%); найдено С (65,56%), Н (7,01%), N (5,28%).
Пример 51
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N13, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-этил-N-фениламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 18%. Элементный анализ: для C43H55Cl2N3Ru вычислено С (65,72%), Н (7,05%), N (5,35%); найдено С (65,81%), Н (7,11%), N (5,29%).
Пример 52
Осуществляют аналогично примеру 1, но 1,3-бис-(2,4,6-триметилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N5 заменены на 1,3-бис-(2,6-диизопропилфенил)-2-трихлорометилимидазолидин и 2-винилбензиламин N14, соответственно. Получен катализатор [1,3-бис-(2,6-диизопропилфенил)-2-имидазолидинилиден]дихлоро(о-N-метил-N-бензиламинометилфенилметилен)рутений в виде зеленого порошка, чистый по ТСХ. Выход 37%. Элементный анализ: для C43H55Cl2N3Ru вычислено С (65,72%), Н (7,05%), N (5,35%