Липосомная композиция и способ ее получения
Иллюстрации
Показать всеИзобретение относится к медицине и заключается в липосомной композиции для замедленного высвобождения лекарственного средства, включающей первую липосому, содержащую внешнюю мембрану, состоящую из многослойного липидного бислоя; и множество вторых липосом, располагающихся во внутренней области первой липосомы, определенной внешней мембраной первой липосомы, где каждая из вторых липосом имеет внешнюю мембрану, состоящую из многослойного липидного бислоя, где липосомная композиция имеет внутренние области вторых липосом, каждая из которых определена внешней мембраной каждой из вторых липосом, и ионный градиент образуется по меньшей мере между каждой из внутренних областей вторых липосом и внешней средой первой липосомы. Изобретение заключается также в способе получения липосомной композиции. Технический результат заключается в замедленном высвобождении лекарственного средства, с помощью чего может быть подавлена боль, длящаяся в течение 5-7 дней после операции. 2 н. и 6 з.п. ф-лы, 5 ил., 7 табл., 15 пр.
Реферат
Область техники
[0001] Раскрыта липосомная композиция с длительным высвобождением, содержащая активный компонент, такой как лекарственное средство.
Предшествующий уровень техники
[0002] Лекарственные средства, предполагающие частое введение, являются проблемными в связи с тем, что частая госпитализация, боль от уколов и т.п. могут представлять собой тяжелую нагрузку на пациента. Кроме того, пациентам, испытывающим трудности при глотании, сложно принимать лекарственное средство через рот, поэтому желателен другой способ введения, кроме перорального. Кроме того, пациентам, нуждающимся в сиделке, таким как больные с деменциями, заболеваниями головного мозга и болезнью Паркинсона, трудно контролировать прием лекарственного средства самостоятельно. Поэтому в таких случаях желателен способ введения, отличный от перорального введения, или способ лечения, не подразумевающий частое введение. Дополнительно, для пациентов, ежедневная жизнедеятельность которых нарушается, как только заканчивается действие лекарственного средства, таких как пациенты с нарушением вегетативной регуляции, желателен терапевтический способ, при котором действие лекарственного средства не заканчивается за короткий период времени, а может продолжаться в течение длительного периода времени. Или, что касается боли после операции, пациент может испытывать невыносимую боль, как только заканчивается действие лекарственного средства, которая может влиять на реабилитацию и может вызывать задержку выписки из больницы. Поэтому, если лекарственное средство может поддерживать свое действие и подавлять боль, например, в течение пяти-семи дней после операции, считается, что послеоперационная реабилитация может быть ускорена, что, в свою очередь, может способствовать более ранней выписке из больницы.
[0003] Лекарственные формы с замедленным высвобождением, посредством которых действие лекарственного средства может поддерживаться в течение длительного времени, могут представлять собой средства для улучшения качества жизни пациента при всех видах заболеваний.
[0004] Многие лекарственные формы с замедленным высвобождением, исследованные прежде, представляют собой микросферы, создаваемые на основе сополимера полимолочной кислоты и гликолевой кислоты (PLGA). Например, как раскрыто в Biomaterials, 28 (2007), 1882-1888, были исследованы PLGA микросферы с применением донепезила гидрохлорида, активного ингредиента Aricept (зарегистрированная торговая марка; Eisai Co., Ltd.), который можно применять в качестве лекарственного средства для лечения деменции альцгеймеровского типа, и при этом были получены свойства замедленного высвобождения. В случае применения PLGA, однако, трудно осуществлять капсулирование, например, растворимого в воде лекарственного средства в высокой концентрации и с высокой эффективностью, и есть проблемы, которые необходимо решить для достижения возможности капсулирования большого количества лекарственного средства. Кроме того, при применении PLGA существует проблема в том, что применение органического растворителя в способе получения может повлечь за собой обязательное удаление органического растворителя. См., например, JP-T-2001-505224 и JP-T-2001-522870. Локальная активизация кислоты после разложения PLGA может вызывать воспаление.
[0005] Кроме вышеуказанных, также исследовали некоторые другие подходы к получению лекарственных форм с замедленным высвобождением на основе применения местного анестезирующего средства, такого как бупивакаин, где все еще не решена проблема достижения свойства замедленного высвобождения, посредством которого может быть подавлена боль, имеющая тенденцию длиться в течение пяти-семи дней после операции. См., например, Anesthesiology, 101 (2004), 133-137. Мультивезикулярная липосома (MVL) была разработана как носитель лекарственного средства с замедленным высвобождением на основе липидов для местной или системной доставки лекарственного средства. См., например, JP-T-2001-505224 и JP-T-2001-522870. Этот подход, однако, также не является удовлетворительным в отношении количества капсулируемого лекарственного средства и длительности замедленного высвобождения.
Сущность изобретения
[0006] Согласно типовому аспекту настоящего изобретения раскрыта липосомная композиция, включающая первую липосому, содержащую внешнюю мембрану, состоящую из многослойного липидного бислоя; и множество вторых липосом, располагающихся во внутренней области первой липосомы, определенной внешней мембраной первой липосомы, где каждая из вторых липосом имеет внешнюю мембрану, состоящую из липидного бислоя, где липосомная композиция имеет внутренние области вторых липосом, каждая из которых определена внешней мембраной каждой из вторых липосом, и ионный градиент образуется по меньшей мере между каждой из внутренних областей вторых липосом и внешней средой первой липосомы. Липидный бислой вторых липосом может быть многослойным.
[0007] Согласно типовому аспекту настоящего изобретения раскрыт способ получения липосомной композиции с ионным градиентом между внутренней областью и внешней областью внешней мембраны, способ, включающий смешивание первого раствора внутренней водной фазы, содержащего соединение для создания ионного градиента, с липидсодержащим смешивающимся с водой растворителем в объемном соотношении от 0,7 до 2,5 для получения первой эмульсии; смешивание второго раствора внутренней водной фазы с первой эмульсией в объемном соотношении не менее 0,7 для получения второй эмульсии; и замещение внешней водной фазы второй эмульсии водным раствором, в котором концентрация соединения для создания ионного градиента меньше, чем в первом растворе внутренней водной фазы.
Краткое описание фигур
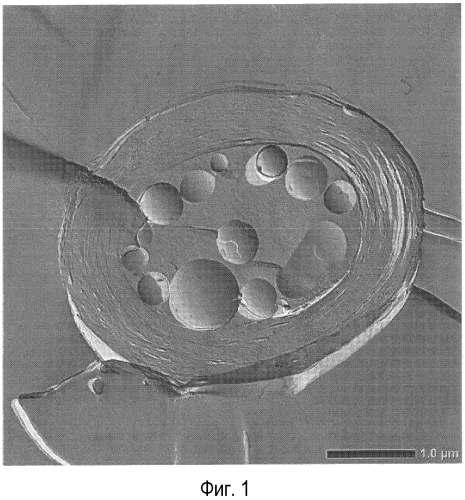
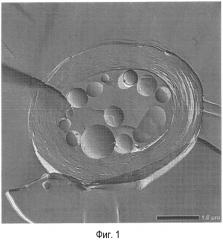
[0008] Фиг.1 представляет собой фотографию (увеличение: 32000), полученную при наблюдении части липосомной композиции при помощи трансмиссионного электронного микроскопа (TEM) после введения лекарственного средства, полученного в примере получения 2, согласно типовому варианту осуществления настоящего изобретения.
[0009] Фиг.2 представляет собой график, описывающий результаты фармакокинетического профиля липосомы донепезила (сравнительный пример 2), полученной способом экструзии 1 согласно типовому варианту осуществления настоящего изобретения.
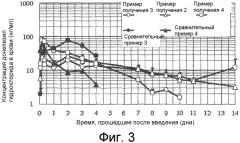
[0010] Фиг.3 представляет собой график, показывающий результаты фармакокинетического профиля липосомных композиций, полученных в примерах получения 2, 3 и 4 согласно типовому варианту осуществления настоящего изобретения.
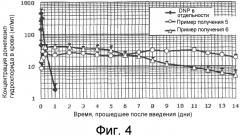
[0011] Фиг.4 представляет собой график, показывающий результаты фармакокинетического профиля липосомных композиций, полученных в примерах получения 5 и 6 согласно типовому варианту осуществления настоящего изобретения.
[0012] Фиг.5 представляет собой график, показывающий результаты фармакокинетического профиля липосомной композиции, полученной в примере получения 12 согласно типовому варианту осуществления настоящего изобретения.
Подробное описание настоящего изобретения
[0013] Согласно типовому аспекту настоящего изобретения раскрыта липосомная композиция, в которой лекарственное средство перемещается из внешней области во внутреннюю область по ионному градиенту, в которую, таким образом, лекарственное средство для капсулирования может быть введено в большом количестве с высокой эффективностью, и которая обладает свойствами замедленного высвобождения в такой степени, что эффективная концентрация может поддерживаться на клинически удовлетворительном уровне. Согласно типовому аспекту настоящего изобретения раскрыт способ получения липосомной композиции.
[0014] Раскрыты следующие типовые аспекты настоящего изобретения.
[0015] (1) Липосомная композиция, включающая первую липосому, содержащую внешнюю мембрану, состоящую из многослойного липидного бислоя; и множество вторых липосом, располагающихся во внутренней области первой липосомы, определенной внешней мембраной, где каждая из вторых липосом имеет внешнюю мембрану, состоящую из липидного бислоя, где липосомная композиция имеет внутренние области вторых липосом, каждая из которых определена внешней мембраной каждой из вторых липосом, и ионный градиент образуется по меньшей мере между каждой из внутренних областей вторых липосом и внешней средой первой липосомы. Липидный бислой вторых липосом может быть многослойным.
[0016] (2) Липосомная композиция, как описано в вышеуказанном параграфе (1), в которой ионным градиентом является градиент концентрации протонов и pH во внутренней области второй липосомы или pH во внутренней области второй липосомы и внутренней области первой липосомы меньше, чем pH во внешней среде первой липосомы.
[0017] (3) Липосомная композиция, как описано в вышеуказанном параграфе (1) или (2), в которой первая липосома имеет средний диаметр частицы в пределах диапазона 1-20 мкм.
[0018] (4) Липосомная композиция, как описано в любом из вышеуказанных параграфов (1)-(3), в которой лекарственное средство содержится во внутренней области второй липосомы или во внутренних областях второй липосомы и первой липосомы.
[0019] (5) Липосомная композиция, как описано в вышеуказанном параграфе (4), в которой лекарственное средство содержится в молярном отношении (моль/моль) не менее 0,05 по отношению к общему содержанию липидов.
[0020] (6) Липосомная композиция, как описано в любом из вышеуказанных параграфов (1)-(5), в которой каждая из липидных мембран первой липосомы и вторых липосом состоит из липида, включая фосфолипид и холестерин.
[0021] (7) Липосомная композиция, как описано в вышеуказанном параграфе (6), в которой фосфолипид представляет собой насыщенный фосфолипид.
[0022] (8) Способ получения липосомной композиции с ионным градиентом между внутренней областью и внешней областью внешней мембраны, включающий следующие стадии: смешивание первого раствора внутренней водной фазы, содержащего соединение для создания ионного градиента, с липидсодержащим смешивающимся с водой растворителем в объемном соотношении от 0,7 до 2,5 для получения первой эмульсии; смешивание второго раствора внутренней водной фазы с первой эмульсией в объемном соотношении не менее 0,7 для получения второй эмульсии; и замещение внешней водной фазы второй эмульсии водным раствором, в котором концентрация соединения для создания ионного градиента по меньшей мере меньше, чем в первом растворе внутренней водной фазы.
[0023] (9) Способ получения липосомной композиции, как описано в вышеуказанном параграфе (8), в котором ионным градиентом является градиент концентрации протонов.
[0024] (10) Способ получения липосомной композиции, как описано в вышеуказанном параграфе (8) или (9), в котором первый раствор внутренней водной фазы содержит сульфат.
[0025] (11) Способ получения липосомной композиции, как описано в вышеуказанном параграфе (10), в котором сульфатом является сульфат аммония.
[0026] (12) Способ получения липосомной композиции, как описано в любом из вышеуказанных параграфов (8)-(11), дополнительно включающий стадию введения лекарственного средства во внутреннюю часть липосомной композиции посредством движущей силы, возникающей в результате ионного градиента.
[0027] В типовом варианте осуществления настоящего изобретения описана липосомная композиция, включающая первую липосому, содержащую внешнюю мембрану, состоящую из многослойного липидного бислоя; и множество вторых липосом, располагающихся во внутренней области первой липосомы, определенной внешней мембраной, где каждая из вторых липосом имеет внешнюю мембрану, состоящую из липидного бислоя, где липосомная композиция имеет внутренние области вторых липосом, каждая из которых определена внешней мембраной каждой из вторых липосом, и ионный градиент образуется по меньшей мере между каждой из внутренних областей вторых липосом и внешней средой первой липосомы. Липидный бислой вторых липосом может быть многослойным. В типовом варианте осуществления настоящего изобретения липосомная композиция позволяет капсулирование лекарственного средства с высокой эффективностью и способна к длительному замедленному высвобождению лекарственного средства.
[0028] При помощи типового способа получения липосомной композиции возможно получение липосомной композиции, которая допускает капсулирование лекарственного средства с высокой эффективностью и способна к длительному замедленному высвобождению лекарственного средства.
Фосфолипиды
[0029] Фосфолипид может быть главным липидом, составляющим липидный бислой (в дальнейшем также иногда называемый просто липидной мембраной или мембраной липосомы) липосомной композиции согласно типовому аспекту. Фосфолипид может быть главным компонентом липидного бислоя. Например, фосфолипид представляет собой амфифильное вещество, имеющее и гидрофобную группу, составленную из длинноцепочечной алкильной группы, и гидрофильную группу, составленную из фосфатной группы в ее молекуле. Примеры фосфолипида включают глицерофосфорные кислоты, такие как фосфатидилхолин (= лецитин), фосфатидинглицерин, фосфатидная кислота, фосфатидилэтаноламин, фосфатидилсерин и фосфатидилинозитол; сфингофосфолипиды, такие как сфингомиелин; природные или синтетические дифосфатидилфосфолипиды, такие как кардиолипин и их производные; продукты гидрирования этих фосфолипидов, такие как гидрированный соевый фосфатидилхолин (HSPC), гидрированный фосфатидилхолин из яичного желтка, дистеароилфосфатидилхолин, дипальмитоилфосфатидилхолин и димиристоилфосфатидилхолин. Фосфолипиды могут быть применены как по отдельности, так и в комбинации множества из них.
Другие добавки, отличные от фосфолипидов
[0030] Липосомная композиция согласно типовому аспекту может включать другой мембранный компонент(ы) вместе с вышеуказанным типовым главным компонентом (т.е. фосфолипидом). Например, липосомная композиция может содержать другие липиды, отличные от фосфолипидов, или производные других липидов, стабилизаторы мембран, антиоксиданты и т.п., по желанию. Другие липиды, отличные от фосфолипидов, могут быть липидами, содержащими гидрофобную группу, такую как длинноцепочечная алкильная группа в своей молекуле, но не содержащими фосфатную группу в своей молекуле, и, в частности, не ограничены. Примеры других липидов включают глицерогликолипиды, сфингогликолипиды, производные стерина, такие как холестерин, и их производные, такие как продукты их гидрирования. Примеры производных холестерина включают такие стерины, которые содержат циклопентаногидрофенантреновое кольцо. Например, среди них, холестерин может содержаться в типовой липосомной композиции. Примеры антиоксидантов включают аскорбиновую кислоту, мочевую кислоту и гомологи токоферола или витамин Е. Токоферол включает четыре изомера, а именно α-, β-, γ- и δ-токоферолы, и любой из таких изомеров может быть применен.
[0031] В типовом варианте осуществления настоящего изобретения липидный бислой липосомной композиции может на 100-50% мол. состоять из фосфолипида и на 0-50% мол. из холестерина, например, на 70-50% мол. состоять из фосфолипида и 30-50% мол. из холестерина.
[0032] Липосомная композиция может включать первую липосому, содержащую внешнюю мембрану, состоящую из нескольких липидных бислоев, и множество вторых липосом, которые располагаются во внутренней области первой липосомы, определенной внешней мембраной, и каждая из которых имеет внешнюю мембрану, состоящую из липидного бислоя. Липидный бислой вторых липосом может быть многослойным. Многослойный бислой первой липосомы включает много бислоев. Например, многослойный бислой вторых липосом включает много бислоев. В липосомной композиции есть внутренние области вторых липосом, каждая из которых определена внешней мембраной каждой из вторых липосом.
[0033] Типовая липосомная композиция включает, в качестве ее вариантов, пустую липосому, в которой не содержится капсулированного лекарственного средства, и липосому, в которой капсулировано лекарственное средство.
[0034] Внешний диаметр первой липосомы может составлять 1-20 мкм, например, 3-10 мкм. Такой внешний диаметр может приводить к превосходным свойствам длительного замедленного высвобождения и обеспечивать легкое введение даже через тонкие иглы. Кроме того, внешний диаметр вторых липосом, в частности, не ограничен. Например, с точки зрения количества лекарственного средства для капсулирования и превосходных свойств длительного замедленного высвобождения внешний диаметр вторых липосом может составлять 100-800 нм.
[0035] В типовом варианте осуществления множество вторых липосом присутствует независимо друг от друга в первой липосоме, и количество вторых липосом, в частности, не ограничено.
[0036] Типовая липосомная композиция имеет ионный градиент по меньшей мере между каждой из внутренних областей вторых липосом и внешней средой первой липосомы. В дальнейшем термин "ион" относится к иону, образующему ионный градиент. В типовом варианте осуществления настоящего изобретения то, что между каждой из внутренних областей вторых липосом и внешней средой первой липосомы образуется ионный градиент, может, например, обозначать любое из следующих: (1) имеется различие в концентрации иона по разные стороны внешней мембраны второй липосомы, между внутренней областью второй липосомы и как внутренней областью первой липосомы, так и внешней средой первой липосомы; (2) имеется различие в концентрации иона по разные стороны внешней мембраны первой липосомы, между внутренней областью второй липосомы, так же как внутренней областью первой липосомы, и внешней средой первой липосомы; и (3) имеется различие в концентрации иона по разные стороны внешней мембраны второй липосомы, между внутренней областью второй липосомы и внутренней областью первой липосомы, и имеется различие в концентрации иона по разные стороны внешней мембраны первой липосомы, между внутренней областью первой липосомы и внешней средой первой липосомы (в этом случае концентрация иона во внутренней области первой липосомы имеет значение, промежуточное между концентрацией иона во внутренней области второй липосомы и концентрацией иона во внешней среде первой липосомы).
[0037] В типовом варианте осуществления настоящего изобретения, с точки зрения увеличения введения лекарственного средства, концентрация иона во внутренней области второй липосомы может быть наиболее высокой. Кроме того, может быть выполнена настройка, при которой (концентрация иона во внутренней области второй липосомы) ≥ (концентрация иона во внутренней области первой липосомы) > (концентрация иона во внешней среде первой липосомы). Например, может быть выполнена настройка, при которой (концентрация иона во внутренней области второй липосомы) > (концентрация иона во внутренней области первой липосомы) ≥ (концентрация иона во внешней среде первой липосомы). Например, может быть выполнена настройка, при которой (концентрация иона во внутренней области второй липосомы) > (концентрация иона во внутренней области первой липосомы) > (концентрация иона во внешней среде первой липосомы). Например, случай, в котором (концентрация иона во внутренней области второй липосомы) = (концентрация иона во внутренней области первой липосомы) = (концентрация иона во внешней среде первой липосомы), исключен. Тогда, когда протонный градиент (градиент pH) применен в качестве ионного градиента, высокая концентрация иона (протонная концентрация) соответствует низкому pH. Например, в этом случае pH во внутренней области второй липосомы является наиболее низким.
[0038] В типовом варианте осуществления настоящего изобретения до и после введения лекарственного средства в пустые липосомы форма и внешний диаметр первой липосомы, так же как форма и внешний диаметр вторых липосом, остаются существенно такими же. В типовом варианте осуществления настоящего изобретения у липосом, в которые введено лекарственное средство, внешний диаметр первой липосомы и внешний диаметр вторых липосом остаются существенно такими же, как у пустых липосом, в которые не вводили лекарственное средство.
[0039] В случае, когда лекарственное средство находится внутри липосомной композиции, такая липосомная композиция может содержать лекарственное средство во внутренних областях вторых липосом или во внутренних областях вторых липосом и первой липосомы.
[0040] Количество лекарственного средства, содержащегося в липосомной композиции, в частности, не ограничено и может, соответственно, регулироваться согласно применению композиции. Количество лекарственного средства, с точки зрения молярного отношения [лекарственное средство (моль)/общее содержание липидов (моль)] по отношению к общему содержанию липидов, находящихся в липосомной композиции (общая сумма липида(ов), примененных для получения липосомной композиции), может составлять не менее 0,05 и может составлять 0,06-0,14.
Способ ионного градиента
[0041] Способ ионного градиента представляет собой способ, в котором создается ионный градиент между внутренней областью и внешней средой липосомной мембраны, и лекарственное средство, добавленное во внешнюю среду, переносится через мембрану липосомы по ионному градиенту, посредством чего лекарственное средство капсулируется во внутренней части липосомы. Ионный градиент может представлять собой протонный градиент (например, градиент pH). Способом ионного градиента получают пустые липосомы, в которых не содержится капсулированное лекарственное средство, а лекарственное средство добавляют во внешнюю жидкость вокруг пустых липосом, в результате чего лекарственное средство может быть введено в липосомы.
[0042] В типовом варианте осуществления настоящего изобретения описана липосомная композиция для капсулирования лекарственного средства способом ионного градиента и липосомная композиция, в которой капсулировано лекарственное средство способом ионного градиента. Среди других может быть применен способ градиента pH, в котором градиент pH применяют в качестве ионного градиента.
[0043] В качестве типового способа получения градиента pH липосому получают с применением кислотного-pH буфера (например, раствор лимонной кислоты с pH 2-3) в качестве первой внутренней водной фазы и/или второй внутренней водной фазы, и затем pH во внешней среде первой липосомы устанавливается близким к нейтральному (например, буфер pH 6,5-7,5), посредством чего может быть осуществлен вариант, в котором градиент pH образован таким образом, что внутренняя часть вторых липосом и внутренняя часть первой липосомы имеют более низкий pH, тогда как внешняя среда первой липосомы имеет более высокий pH.
[0044] Например, градиент pH может также быть образован при помощи градиента ионов аммония. В этом случае, например, липосому получают с применением раствора сульфата аммония в качестве первой внутренней водной фазы и/или второй внутренней водной фазы и затем удаляют сульфат аммония из внешней водной фазы первой липосомы или разбавляют, в результате чего образуется градиент ионов аммония по меньшей мере между внутренней областью вторых липосом, так же как внутренней областью первой липосомы, и внешней средой первой липосомы.
[0045] Таким образом можно гарантировать, что благодаря градиенту ионов аммония, образованному таким образом, будет иметь место поток аммиака из внутренних водных фаз первой липосомы и вторых липосом во внешнюю водную фазу первой липосомы. В результате протоны, оставляемые аммиаком, накапливаются во внутренних водных фазах, в результате чего образуется градиент pH, и внутренние водные фазы в первой липосоме и вторых липосомах становятся более кислыми, чем внешняя водная фаза первой липосомы.
Лекарственное средство для капсулирования
[0046] В качестве лекарственного средства для капсулирования в липосомной композиции лекарственное средство может быть применено без каких-либо специальных ограничений. Лекарственное средство может капсулировано в липосомы способом ионного градиента. Такое лекарственное средство может быть ионизируемым амфифильным лекарственным средством, например, амфифильным слабоосновным лекарственным средством. Кроме того, с точки зрения действия, лекарственное средство может быть лекарственным средством, для которого ожидаются свойства замедленного высвобождения при местном введении, например, любое из лекарственных средств для лечения церебрально-сосудистых нарушений, болезни Паркинсона, деменции и т.д., анальгетики, местные анестетики и агенты против злокачественных опухолей. Примеры этих лекарственных средств включают донепезил, ривастигмин, галантамин, физостигмин, гептилфизостигмин, фенсерин, толсерин, симсерин, тиатолсерин, тиацимсерин, неостигмин, гуперзин, такрин, метрифонат, миноциклин, фасудилгидрохлорид, нимодин, морфин, бупивакаин, ропивакаин, левобупивакаин, трамадол, лидокаин и доксорубицин. Другие примеры включают допамин, L-DOPA, серотонин, эпинефрин, кодеин, меперидин, метадон, морфин, атропин, децикломин, метиксен, пропантелин, имипрамин, амитриптилин, доксепин, дезипрамин, хинидин, пропранолол, хлорпромазин, прометазин и перфеназин.
Первый раствор внутренней водной фазы липосомы
[0047] В типовом способе получения липосомной композиции первый раствор внутренней водной фазы, который предназначен для применения на стадии получения первой эмульсии, содержит соединение для создания ионного градиента.
[0048] Ион для создания ионного градиента может быть протоном, как указано выше. Кроме того, примеры соединения для создания ионного градиента (градиента pH) включают такие соединения, которые отдают протон, ион аммония или протонированную аминогруппу при ионизации. Примеры таких соединений включают сульфаты, такие как сульфат аммония, сульфат декстрана и сульфат хондроитина; гидроксиды; ортофосфорная кислота, глюкуроновая кислота, лимонная кислота, угольная кислота, гидрокарбонаты, азотная кислота, циановая кислота, уксусная кислота, бензойная кислота и их соли; галогениды, такие как бромиды и хлориды; неорганические или органические анионы; и анионные полимеры.
[0049] В случае, когда слабоосновное лекарственное средство (например, любое из вышеуказанных) капсулировано во внутренней водной фазе (по меньшей мере второй внутренней водной фазе) в липосомной композиции согласно типовому аспекту настоящего изобретения способом градиента pH, лекарственное средство протонируется протоном, находящимся во внутренней водной фазе, получая таким образом электрический заряд. В результате это препятствует распространению лекарственного средства за пределы липосомы, таким образом лекарственное средство удерживается во внутренней водной фазе липосомы.
[0050] В случае, когда соединение для создания ионного градиента ионизируется, анионы, такие как ионы сульфата, генерируются вместе с ионами (катионами), создавая ионный градиент, такой как протоны. В этом случае, если анион образует соль или комплекс с протонированным слабоосновным лекарственным средством, лекарственное средство может удерживаться во внутренней водной фазе более устойчиво. Другими словами, соединение для создания ионного градиента может быть соединением, которое в результате ионизации образует противоион (анион) для основного лекарственного средства, который может образовывать соль или комплекс с основным лекарственным средством. Такой противоион, в частности, не ограничен до тех пор, пока он представляет собой фармацевтически приемлемый анион. Например, противоион представляет собой ион сульфата. В качестве соединения для образования иона сульфата может быть использован сульфат аммония, но соединение также может быть выбрано из других соединений, таких как сульфат декстрана и сульфат хонтроитина. Кроме того, другие примеры противоиона включают анионы, образованные при ионизации гидроксидов, фосфатов, глюкуронатов, солей лимонной кислоты, карбонатов, гидрокарбонатов, нитратов, цианатов, ацетатов, бензоатов, бромидов, хлоридов и других неорганических или органических анионов или анионных полимеров и т.д.
[0051] В типовом варианте осуществления концентрация соединения для создания ионного градиента в первом внутреннем водном растворе фазы может составлять 50-500 мМ, например, 100-300 мМ.
[0052] В типовом способе получения липосомной композиции растворителем, применяемым для получения липидсодержащего раствора на стадии получения первой эмульсии, является смешивающийся с водой растворитель. Смешивающийся с водой растворитель обозначает растворитель, который растворяет фосфолипид(ы) и другой мембранный компонент(ы), применяемые для получения липосомной композиции согласно типовому аспекту настоящего изобретения, и который смешивается с водой. Примеры смешивающегося с водой растворителя включают этанол, метанол, изопропиловый спирт и бутанол.
[0053] В типовом варианте осуществления настоящего изобретения не применяют растворители, которые не смешиваются с водой (называемые также несмешивающиеся с водой растворители; примеры включают несмешивающиеся с водой органические растворители, такие как хлороформ). Например, когда несмешивающийся с водой растворитель применяют на стадии получения первой эмульсии, получаемая липосома не имеет такую форму, когда в большой липосоме содержится множество небольших липосом и первая внутренняя водная фаза; вместо этого получаемая липосома имеет форму, такую как так называемая мультивезикулярная липосома (MVL), в которой просто собраны индивидуальные липосомы, подобные вспененному полистиролу.
[0054] Количество липида(ов) в качестве исходного вещества для липосом (общая сумма фосфолипида(ов) и другого липида(ов)) может составлять 20-100% масс., например 20-60% масс., по отношению к смешивающемуся с водой растворителю.
[0055] В первой эмульсии (смесь липидсодержащего смешивающегося с водой растворителя и ионсодержащего раствора первой внутренней водной фазы) другой компонент(ы), отличный от компонентов, способных образовывать липидный бислой, может заполнять внутренние области вторых липосом, составляя липосомную композицию типового аспекта настоящего изобретения. Часть второго раствора внутренней водной фазы, который будет описан позже, может быть дополнительно примешана к внутренним областям вторых липосом.
[0056] Способ получения первой эмульсии, в частности, не ограничен, и может быть применен любой подходящий способ.
[0057] В случае, когда применяют способ градиента pH, pH внутренней водной фазы (первая и/или вторая внутренняя область липосомы) может быть установлен по желанию. Например, в случае, когда используется лимонная кислота в качестве соединения для создания ионного градиента в первом растворе внутренней водной фазы, градиент pH между внутренней водной фазой (внутренние области вторых липосом) и внешней водной фазой (внутренняя область первой липосомы и/или внешней средой первой липосомы) может быть создан заранее. Например, в этом случае различие в pH между внутренней водной фазой и внешней водной фазой составляет не менее трех единиц.
[0058] В случае, когда используют сульфат аммония, градиент pH образуется путем химического равновесия, при котором может оказаться ненужным предварительное установление pH раствора внутренней водной фазы. В этом случае, если тот же самый раствор как во внешней водной фазе применяется в качестве второй внутренней водной фазы, образование ионного градиента начинается со времени образования второй эмульсии, и далее градиент растет в результате замены внешней жидкости. В случае, когда тот же самый раствор сульфата аммония, как в первой внутренней водной фазе, применяют в качестве второй внутренней водной фазы, считается, что ионный градиент образуется во время замещения внешней жидкости.
[0059] Для создания липосомной композиции согласно типовому аспекту настоящего изобретения липидсодержащий смешивающийся с водой растворитель и первый раствор внутренней водной фазы, предназначенный для добавления к нему, могут быть применены в объемном соотношении (первого раствора внутренней водной фазы к смешивающемуся с водой растворителю) в диапазоне от 0,7 до 2,5, например, от 1,0 до 2,0.
Второй раствор внутренней водной фазы липосомы
[0060] В типовом варианте осуществления настоящего изобретения после получения первой эмульсии путем добавления первого раствора внутренней водной фазы к липидсодержащему смешивающемуся с водой растворителю проводят стадию добавления второго раствора внутренней водной фазы к первой эмульсии, где второй раствор внутренней водной фазы, в частности, не ограничен. Примеры второго раствора внутренней водной фазы включают такой же раствор, как первый раствор внутренней водной фазы, раствор HEPES, раствор NaCl и водные растворы сахара, такого как глюкоза и сахароза. В типовом варианте осуществления применяют такой же раствор, как для первой внутренней водной фазы. В типовом варианте осуществления первая внутренняя водная фаза и вторая внутренняя водная фаза, каждая, представляет собой водный раствор сульфата аммония. Первая эмульсия и второй раствор внутренней водной фазы, который предполагается к ней добавить, могут быть применены в объемном соотношении [второй раствор внутренней водной фазы] к [первой эмульсии (= первый раствор внутренней водной фазы + смешивающийся с водой растворитель)] не менее 0,7, например, в диапазоне от 0,7 до 2,5, например, в диапазоне от 1,0 до 1,5.
[0061] Во второй эмульсии другой компонент(ы), отличный от компонента(ов), способных образовывать липидный бислой, может заполнять внутреннюю область первой липосомы (исключая вторые липосомы), составляя липосомную композицию согласно типовому аспекту настоящего изобретения. Внутренняя область первой липосомы (исключая вторые липосомы) может содержать часть первой эмульсии.
[0062] Способ получения второй эмульсии, в частности, не ограничен, и может быть применен любой подходящий способ.
Раствор внешней водной фазы липосомы
[0063] Способ получения липосомной композиции согласно типовому аспекту настоящего изобретения включает стадию замещения внешней водной фазы второй эмульсии водным раствором с меньшей концентрацией соединения для создания ионного градиента, чем в первом растворе внутренней водной фазы.
[0064] Когда внешняя водная фаза первой липосомы после получения второй эмульсии изменяется в результате замещения второго раствора внутренней водной фазы липосомы или смешанной жидкости, содержащей первый раствор внутренней водной фазы липосомы, и второго раствора внутренней водной фазы липосомы водным раствором, в котором концентрация соединения для создания ионного градиента по меньшей мере меньше, чем в первом растворе внутренней водной фазы, гарантируется, что образуется ионный градиент по меньшей мере между каждой из внутренних областей вторых липосом и внешней средой первой липосомы, что смешивающийся с водой растворитель удаляется из системы липосомной композиции и что получаемая липосома будет иметь форму, присущую липосомной композиции согласно типовому аспекту настоящего изобретения.
[0065] В качестве замещаемой внешней водной фазы, применяемой в типовом способе получения липосомной композиции, применяют водный раствор с концентрацией соединения для создания ионного градиента по меньшей мере меньшей, чем в первом растворе внутренней водной фазы. Например, применяют раствор HEPES, раствор NaCl или водный раствор сахара, такого как глюкоза и сахароза. pH внешней водной фазы может быть настроен при помощи буфера. Принимая во внимание разложение липида и интервал pH во время введения в живой организм, pH можно контролировать в пределах диапазона pH 5,5-8,5, например, диапазона pH 6,5-7,5. Осмотическое давление внутренней водной фазы и внешней водной фазы для липосомы, в частности, не ограничено. Осмотическое давление можно регулировать в пределах таких диапазонов, чтобы липосома не разорвалась из-за различия между осмотическими давлениями. С учетом желаемой физической устойчивости липосомы меньшее различие в осмотическом давлении может быть более желательно.
[0066] Один типовой вариант осуществления замещаемой внешней водной фазы представляет собой водный раствор с меньшей концентрацией соединения для создания ионного градиент