Способ лечения глаукомной оптической нейропатии
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к способам лечения глаукомной оптической нейропатии. Проводят местную гипотензивную терапию. Осуществляют трансорбитальную низкочастотную магнитную стимуляцию. При этом амплитудное значение магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, пульсирующий режим магнитной индукции с частотой 17 Гц с плавно нарастающим фронтом и спадом импульса, длительностью 15 мс. Процедуру трансорбитальной низкочастотной магнитной стимуляции осуществляют на закрытый глаз в течение 5-7 минут. Курс лечения составляет 6-10 ежедневных процедур. Проводят четыре курса в течение года через каждые 3 месяца. Способ обеспечивает повышение эффективности лечения глаукомной оптической нейропатии за счет достоверного увеличения остроты зрения, повышения суммы показателей полей зрения по 8 меридианам, уменьшения или исчезновения относительных скотом. 3 ил., 3 табл., 3 пр.
Реферат
Изобретение относится к области медицины, в частности к неврологии, офтальмологии, и может быть использовано для лечения глаукомной оптической нейропатии.
В настоящее время лечение глаукомной оптической нейропатии (ГОН), основанное на современных знаниях о патогенезе этого заболевания, направлено на нормализацию внутриглазного давления, применение средств, улучшающих кровоснабжение и нарушенный метаболизм тканей глаза и зрительного нерва. Одной из отличительных особенностей метаболизма нервной ткани является наличие гематоэнцефалического и гематоофтальмического барьеров, которые обеспечивают избирательную проницаемость только для определенных субстратов и способствуют накоплению необходимых для метаболизма веществ в нервной ткани. Специфичный для нервной ткани метаболизм обуславливает схожесть патологических изменений при развитии дегенеративных заболеваний в различных структурах головного мозга, в том числе и структурах зрительного анализатора. В последнее время появилось много сообщений об общих патогенетических связях нейродегенеративных заболеваний и ГОН. Нарушение когнитивных функций головного мозга и светочувствительности сетчатки, прогрессирование деменции и гибель ганглиозных клеток сетчатки связывают с поражением определенных видов нейронов и одним и тем же механизмом гибели нервных клеток [Алексеев В.Н., Газизова И.Р. Новые молекулярно-биологические аспекты нейродегенерации при глаукоме // Клиническая офтальмология, 2014, №2, с. 85-90].
В комплексном лечении нейродегенеративных заболеваний и ГОН нашли применение различные по механизму действия препараты, получившие название нейропротекторы. Обычно под термином нейропротекция понимают воздействие на различные молекулярные и биохимические процессы в нервных клетках с целью предупреждения их повреждения или гибели в результате влияния различных патологических факторов. Запущенные различными неблагоприятными воздействиями, включающими в том числе хроническую компрессию аксонов нервных клеток повышенным внутриглазным давлением и ишемию, патофизиологические механизмы апоптоза и некроза приводят в итоге к незапланированной гибели нервных клеток. Своевременное и эффективное влияние на эти механизмы с целью предотвращения фатального итога и является целью нейропротекции.
В настоящее время различают первичную и вторичную нейропротекцию. Под первичной понимают воздействие на быстрые механизмы паранекроза - реакций глутамат-кальциевого каскада посредством антагонистов NMDA- и AMPA-рецепторов и блокаторов потенциал-зависимых ионных каналов. В основном эти препараты применяются при остром инсульте (например, кетамин). Большинство относится к веществам, запрещенным в медицинской практике или еще не получившим разрешение на клиническое применение или не оправдавших возлагавшихся на них надежд, так, например, за рубежом проводились многоцентровые исследования влияния антагониста NMDA-рецептора - мемантина. Несмотря на то обстоятельство, что препарат применяется при лечении деменции Альцгеймера, мемантин не оказал положительного влияния на течение ГОН [Иллариошкин С.Н. Нарушения клеточной энергетики при заболеваниях нервной системы // Нервные болезни, 2012, №1. С. 34-38].
Более широкое распространение получили методы вторичной нейропротекции, которые направлены на уменьшение выраженности отдаленных последствий ишемии. Медицинские препараты применяются с целью торможения оксидативного стресса, нормализации метаболических процессов, ингибирования апоптоза. Применяются антиоксиданты, антигипоксанты, метаболитотропные препараты и ноотропы (ретиналанин, кортексин, эмоксипин, мексидол, фезам, танакан, церебролизин и т.д.) [Егоров Е.А., Гветадзе А.А., Давыдова Н.Г. Антиоксидантный препарат в нейропротективной терапии при глаукоме // Вестник офтальмологии, 2013, №2, с. 67-69].
Помимо медикаментозных средств, в качестве нейропротекторных факторов нашли применение методы физиотерапевтического воздействия, в том числе и методы магнитотерапии. Однако в литературе о применении магнитотерапии в комплексном лечении глаукомы встречаются единичные публикации [Домашенко М.А., Червяков А.В., Максимова М.Ю., Пирадов М.А. Транскраниальная магнитная стимуляция при фуникулярном миелозе // Нервные болезни, 2014, №3, с. 43-48].
Известен способ комплексного лечения глаукомной оптической нейропатии путем введения в послеоперационном периоде в проекции трепанационного отверстия субконъюнктивально лекарственного препарата Кортексин по 0,5 мл и проведения магнитолазеростимуляции. Параметры воздействия: лазерное инфракрасное излучение, длина волны - 0,89 нм, частота - 5 Гц, мощность - 4 мВт; магнитная индукция - 10 Тл, время - 2 мин, площадь - 4 см2, непрерывный режим. Способ позволяет добиться сохранения и повышения зрительных функций путем снижения внутриглазного давления, нейропротекторного действия лекарственного препарата, депонируемого в коллагеновой гемостатической губке, и биостимулирующего эффекта магнитолазерного воздействия [RU 2308916 С1, 27.10.2007]. Однако данный способ травматичен, то есть имеется потенциальная возможность развития сосудистых или воспалительных осложнений в орбите. Кроме того, данный способ лечения используется только в послеоперационном периоде заболевания и проводится в условиях стационара, что ограничивает его использование по сравнению с амбулаторным характером лечения.
Наиболее близким техническим решением является способ лечения глаукомной оптической нейропатии путем медикаментозной терапии и физиотерапевтического лечения низкочастотным пульсирующим магнитным полем от 3 до 5 мТл с частотой 50 Гц прямоугольной формы АМТО-01 diathera. Курс лечения низкочастотной магнитотерапии составляет по 15 минут ежедневно. В зависимости от наблюдающегося объективного улучшения больные получили курс от 7 до 10 сеансов [Голикова Е.В., Маркова Е.В. Применение низкочастотной магнитотерапии в комплексном лечении глаукомной оптической нейропатии и послеоперационной кератопатии, журнал «Физиотерапевт», 2014, №2, с. 39-43]. Однако указанный способ лечения глаукомной оптической нейропатии обеспечил повышение остроты зрения только в 67% случаев и расширения границ поля зрения в 64%.
Технический результат заявленного способа заключается в повышении эффективности лечения глаукомной оптической нейропатии за счет достоверного увеличения остроты зрения с коррекцией с 0,65±0,01 до 0,93±0,01 в течение первых 7 дней наблюдения и постепенного повышения остроты зрения до 0,97±0,01 к третьему месяцу наблюдения, оставаясь при этом стабильной в течение всего срока лечения (4-х курсов через каждые 3 месяца) и наблюдения (трех лет) у всех пациентов. Кроме того, достоверно повышается сумма показателей полей зрения по 8 меридианам, уменьшаются или исчезают относительные скотомы в сроки от 1 до 6-9 месяцев (р<0,01) и с сохранением тенденции к увеличению суммы показателей к 12 месяцам наблюдений.
Технический результат достигается тем, что лечение глаукомной оптической нейропатии осуществляют путем использования медикаментозной терапии и низкочастотной магнитной стимуляции, при этом наряду с местной гипотензивной терапией проводят трансорбитальную низкочастотную магнитную стимуляцию с амплитудным значением магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, с пульсирующим режимом магнитной индукции и частотой 17 Гц, с плавно нарастающим фронтом и спадом импульса, длительностью 15 мс, при этом процедуру трансорбитальной низкочастотной магнитной стимуляции осуществляют на закрытый глаз в течение 5-7 минут, курс лечения составляет 6-10 ежедневных процедур, с проведением в течение года четырех курсов через каждые 3 месяца.
Способ осуществляется следующим образом.
Пациенту при первичном обращении проводят обследование, включающее определение остроты зрения без и с максимальной очковой коррекцией, бесконтактную компьютерную тонометрию и тонометрию по Маклакову, компьютерную статическую периметрию, биомикроскопию, гониоскопию и офтальмоскопию. При наличии у него глаукомной оптической нейропатии в качестве гипотензивных средств назначают инсталляции глазных капель, снижающих внутриглазное давление, например ксалатан на ночь и 0,5% раствор арутимола 2 раза в день. Одновременно проводят курс трансорбитальной низкочастотной магнитной стимуляции (МС), используя следующие параметры. Амплитудное значение магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, режим магнитной индукции - пульсирующий, частотой 17 Гц с плавно нарастающим фронтом и спадом импульса, длительность которого составляет 15 мс. Реализацию указанных параметров осуществляют на отечественном аппарате «Полюс-2», используя для МС индуктор прямоугольной формы. Индуктор помещают непосредственно к закрытому глазу южным полюсом. Процедуру МС осуществляют через прокладку в 2 слоя медицинской марли в течение 5-7 минут. Одновременно можно выполнять процедуру для двух глаз, страдающих глаукомной оптической нейропатией. На курс лечения проводят 6-10 ежедневных процедур. В течение года проводят 4 курса магнитной стимуляции через каждые 3 месяца.
Под наблюдением в течение трех лет находилось 32 пациента (56 глаз) с неоперированной открытоугольной глаукомой I, II и III стадии, давностью заболевания от 2 до 16 лет (в среднем 9,2±1,3 года). Исследуемая группа включала 26 пациентов с разными стадиями глаукомы, контрольная - 6 пациентов (10 глаз) с компенсированной глаукомой II стадии. В исследование были отобраны пациенты без тяжелых соматических заболеваний, при отсутствии противопоказаний к физиотерапевтическому лечению. Возраст пациентов составил от 51 до 67 лет (в среднем 61,3±2,4 года). На протяжении многих лет пациенты применяли различные гипотензивные препараты или их комбинации: растворы тимолола, бетаксолола, дорзаломида, бринзоламида, латанопроста, бримонидина, травапроста.
Пациентам исследуемой группы наряду с местными гипотензивными средствами проводили трансорбитальную низкочастотную магнитную стимуляцию. А именно всем пациентам в исследуемой и контрольной группах проводили лечение гипотензивными средствами, снижающими внутриглазное давление, например инстилляции глазных капель ксалатан на ночь и 0,5% раствора арутимола 2 раза в день. При этом пациентам в исследуемой группе (26 пациентов) дополнительно проводили курс трансорбитальной низкочастотной магнитной стимуляции при амплитудном значении магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, режиме магнитной индукции - пульсирующем, частоте 17 Гц с плавно нарастающим фронтом и спадом импульса и длительности 15 мс. Процедуру МС осуществляли через прокладку в 2 слоя медицинской марли в течение 5-7 минут как для одного, так и для двух глаз с глаукомной оптической нейропатией. Курс лечения составлял от 6 до 10 ежедневных процедур. В течение года провели 4 курса магнитной стимуляции через каждые 3 месяца.
Наблюдение за пациентами помимо общепринятых в поликлинической практике обследований производили с помощью компьютерного анализа изображений сетчатки и диска зрительного нерва (ДЗН), используя для получения изображений когерентный томограф Optipol SOCT Copernicus HR (производство Польша) и фундус-камеру Canon CX-1 (Япония). При этом в течение первых 2-х недель наблюдение осуществляли ежедневно. Проводили измерение внутриглазного давления (ВГД), остроту зрения, биомикроофтальмоскопию. На 30 день выполняли повторную компьютерную периметрию на аппарате «Периком». Подсчитывали значения градусов на периметрических картах по 8 главным меридианам, суммировали их. Контрольные осмотры и обследования, включая периметрию после очередного курса лечения, проводили каждые 3 месяца.
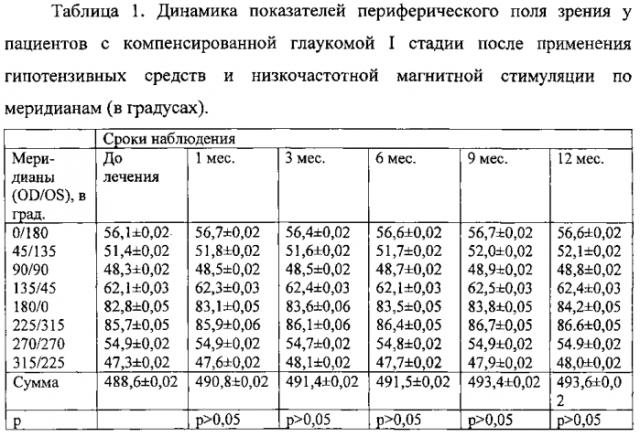
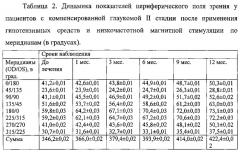
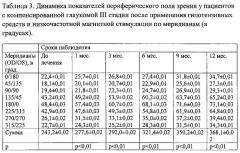
Процедуры магнитной стимуляции пациентами переносились хорошо, без каких-либо неприятных ощущений и побочных эффектов. Непосредственно сразу после первой процедуры магнитной стимуляции статистически (р>0,05) не отмечено изменение ВГД ни у одного пациента. В сроки от 2 до 5 дней у всех пациентов исследуемой группы после ежедневных процедур МС и инсталляций ксалатана и арутимола отмечено снижение ВГД до 16-21 мм рт.ст. Величины ВГД, вне зависимости от стадии заболевания, снижались у всех пациентов более чем на 30% от исходного уровня, тем самым достигнув к последнему курсу лечения значений «давления цели» (см. фиг. 1). На фигуре 1 показана динамика снижения внутриглазного давления (Po) у пациентов с открытоугольной глаукомой II и III стадий после применения трансорбитальной магнитной стимуляции (в мм рт.ст.). По сравнению с пациентами контрольной группы отмечено достоверное увеличение остроты зрения с коррекцией с 0,65±0,01 до 0,93±0,01 в течение первых 6 дней наблюдения. В дальнейшем острота зрения повысилась до 0,97±0,01 к 3 месяцу и оставалась стабильной в течение всего срока лечения и наблюдения. Повышение остроты зрения коррелировало со стабилизацией ВГД. В контрольной группе (II стадия открытоугольной глаукомы) острота зрения оставалась без изменений (см. фиг. 2). На фигуре 2 показана динамика повышения остроты зрения у пациентов с открытоугольной глаукомой II стадии после применения трансорбитальной магнитной стимуляции по сравнению с контролем (в днях). Наиболее выраженные изменения влияния МС в исследуемой группе, по сравнению с контрольной, видны по результатам исследования периферического поля зрения (см. табл. 1-3, фиг. 3). На фигуре 3 показана динамика увеличения суммарного показателя периметрии по 8 меридианам у пациентов с открытоугольной глаукомой разных стадий после применения трансорбитальной магнитной стимуляции по сравнению с контролем (выражено в градусах).
На фигуре 3 и в таблицах 1-3 отмечено достоверное увеличения суммы показателей полей зрения по 8 меридианам, уменьшение или исчезновение относительных скотом в сроки от 1 месяца до 6-9 месяцев (р<0,01) и с сохранением тенденции к увеличению суммы показателей к 12 месяцу наблюдений. Более выраженные расширения полей зрения и увеличения суммарного показателя периметрии отмечали у пациентов со II и III стадиями глаукомы. Наоборот, у пациентов с I стадией глаукомы достоверной разницы (р>0,05) в показателях полей зрения в течение всего срока наблюдения не наблюдали, однако отмечали исчезновение относительных скотом 1 и 2 порядка и положительную динамику в увеличении периферического поля зрения. У пациентов с I стадией глаукомы отмечали более выраженные изменения центрального поля зрения по сравнению с пациентами более развитых стадий глаукомы. Так, на 8 глазах (66,7%) было отмечено уменьшение интенсивности и исчезновение скотом в зоне слепого пятна и зоне Бьеррума после 2-3 курсов МС. Уменьшение интенсивности скотом в этих зонах у пациентов со II и III стадиями глаукомы отмечали на 14 (53,8%) и 7 (38,3%) глазах, соответственно, после 4 курсов МС.
Примеры осуществления способа
Пример 1
Пациентка О., 1947 года рождения, обратилась на плановый очередной прием 02.04.2013 по поводу диспансерного наблюдения с диагнозом: компенсированная открытоугольная глаукома I А стадии правого глаза, начальная катаракта обоих глаз, гиперметропия слабой степени обоих глаз. При обследовании: острота зрения правого глаза (ОД) = 0,6 с сферой + 1,5 дптр = 1,0; острота зрения левого глаза (OS) = 0,6 с сферой + 1,5 дптр = 1,0. Внутриглазное давление правого глаза PoОД = 19 мм рт.ст.; левого глаза PoOS = 18 мм рт.ст. Компьютерная статическая периметрия. Границы периферического поля зрения ОД по 8 меридианам: 56; 48; 48; 62; 83; 86; 55; 47, что в сумме составляло 485 градусов. В зоне слепого пятна - абсолютные (<0,1%) и относительные (<0,5%) скотомы. Границы периферического поля зрения OS по 8 меридианам в пределах нормы: 58; 58; 48; 65; 90; 90; 65; 48, что в сумме составляло 522 градуса. Было рекомендовано продолжать предписанное ранее гипотензивное лечение, состоящее из инсталляций глазных капель ксалаком на ночь в ОД. Пациентке был проведен курс трансорбитальной магнитной стимуляции на ОД. Использовали следующие параметры. Амплитудное значение магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, режим магнитной индукции - пульсирующий, частотой 17 Гц с плавно нарастающим фронтом и спадом импульса, длительность которого составляет 15 мс. Реализацию указанных параметров осуществляли на отечественном аппарате «Полюс-2», используя для МС индуктор прямоугольной формы. Индуктор помещали непосредственно к закрытому правому глазу южным полюсом, который на индукторе обозначен стрелкой. Процедуру МС осуществляли через прокладку в 2 слоя медицинской марли в течение 5-7 минут. На курс лечения назначали 6 ежедневных процедур. В течение всего периода лечения пациентка не испытывала каких-либо неприятных ощущений и побочных эффектов от проводимого физиотерапевтического лечения. После проведенного курса лечения на ОД показатели компьютерной статической периметрии увеличились, а именно границы периферического поля зрения ОД по 8 меридианам были следующими: 58; 49; 48; 63; 84; 87; 55; 48, что в сумме составляло 492 градуса. В зоне слепого пятна ослабление абсолютной (до <0,5%) и относительной (до <5,0%) скотом. Границы периферического поля зрения OS по 8 меридианам остались без изменений, в пределах нормы, а именно 58; 58; 48; 65; 90; 90; 65; 48, что в сумме составляло 522 градуса. Были проведены второй, третий и четвертый курсы лечения с интервалами в три месяца. После каждого курса у пациентки О. с I стадией открытоугольной глаукомы достоверно увеличивались показатели компьютерной статической периметрии, острота зрения сохранялась в пределах нормы, ВГД было стабильным. А именно после четвертого курса на ОД показатели по 8 меридианам: 58; 51; 48; 63; 90; 86; 60; 48, что в сумме составило 504 и приблизились к значениям нормы. На OS показатели периметрии в течение года не изменились и составили: 58; 60; 48; 66; 90; 90; 65; 48, что в сумме составило 525 градусов. В центральном поле зрения отмечали ослабление абсолютной и относительной скотом.
Таким образом, наблюдение в течение года показало, что ВГД оставалось стабильным в пределах значений «давления цели», острота зрения не менялась, а границы периферического поля зрения под воздействием комплексного лечения, включающего гипотензивную терапию и курсы трансорбитальной МС, имели тенденцию к увеличению.
Пример 2
Пациент К., 1963 года рождения, обратился на прием 22.04.2013 с жалобами на туман перед левым глазом. Беспокоит в течение 1-2 месяцев. При обследовании: острота зрения ОД = 1,0; OS = 0,7 не корригируется. Внутриглазное давление правого глаза PoОД = 27 мм рт.ст.; левого глаза PoOS = 31 мм рт.ст. При биомикроскопическом осмотре передний отрезок без патологических изменений, среды прозрачные, угол открыт. Диск зрительного нерва бледно-розового цвета с расширенной экскавацией до 0,5 на ОД и до 0,7 на OS. Компьютерная статическая периметрия. Границы периферического поля зрения ОД по 8 меридианам: 56; 47; 48; 61; 82; 84; 52; 45, что в сумме составляло 475 градусов. В зоне слепого пятна - относительные (<0,5%) скотомы. Границы периферического поля зрения OS по 8 меридианам: 41; 24; 43; 52; 60; 59; 41; 31, что в сумме составляло 351 градус. В зоне слепого пятна - абсолютные (<0,1%) и относительные (<0,5%) скотомы. Диагноз: ОД - открытоугольная I А глаукома, OS - открытоугольная II В глаукома. Было рекомендовано в оба глаза инсталляции глазных капель ксалатан на ночь и 0,5% раствора арутимола 2 раза в день. Пациенту был проведен курс трансорбитальной магнитной стимуляции (МС) на оба глаза. Использовали следующие параметры. Амплитудное значение магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, режим магнитной индукции - пульсирующий, частотой 17 Гц с плавно нарастающим фронтом и спадом импульса, длительность которого составляет 15 мс. Реализацию указанных параметров осуществляли на отечественном аппарате «Полюс-2», используя для МС индуктор прямоугольной формы. Индуктор помещали непосредственно к закрытому глазу южным полюсом. Процедуру МС осуществляли на обоих глазах через прокладку в 2 слоя медицинской марли в течение 5-7 минут. На курс лечения назначали 10 ежедневных процедур. В течение всего периода лечения пациентка не испытывала каких-либо неприятных ощущений и побочных эффектов от проводимого физиотерапевтического лечения. При осмотре на следующий день ВГД снизилось на ОД до 20 мм рт.ст., на OS - до 26 мм рт.ст. ВГД регистрировалось в пределах нормы: ОД - 19 мм рт.ст., OS - 23 мм рт.ст. На 4-й день ВГД на ОД - 16 мм рт.ст., на OS - 18 мм рт.ст. Острота зрения обоих глаз = 1,0 без коррекции. Таким образом, глаукома компенсирована на 4-й день после назначения местной гипотензивной терапии и трансорбитальной МС. Однако для стабилизации достигнутой компенсации был проведен через 3 месяца следующий курс лечения. При этом ВГД ОД - 14 мм рт.ст., OS - 14 мм рт.ст. Значения компьютерной статической периметрии увеличились: границы периферического поля зрения ОД по 8 меридианам: 56; 51; 47; 62; 83; 86; 58; 46, что в сумме составляло 489 градусов. В зоне слепого пятна ослабление относительной (до <2,5%) скотом. Границы периферического поля зрения OS по 8 меридианам: 44; 25; 47; 56; 67; 65; 44; 33, что в сумме составляло 381 градусов. В зоне слепого пятна ослабление абсолютной (до <0,5%) и относительной (до <2,5%) скотомы. В центральном поле зрения - ослабление абсолютной и относительной скотом. Для закрепления эффекта и его стабилизации был проведен через 3 месяца следующий курс лечения. Были получены следующие показатели периметрия: границы периферического поля зрения ОД по 8 меридианам приблизились к границам нормы: 58; 52; 48; 63; 85; 88; 60; 47, что в сумме составило 501 градус. В зоне слепого пятна - ослабление относительной (до <5,0%) скотома. Границы периферического поля зрения OS по 8 меридианам: 40; 26; 50; 58; 72; 68; 46; 35, что в сумме составило 395 градусов. В зоне слепого пятна - относительные (<0,5% и <2,5%) скотомы. После проведения четвертого курса лечения показатели оставались стабильными. Наблюдение в течение года показало, что ВГД оставалось стабильным в пределах значений «давления цели», достигнутая острота зрения в пределах нормы не изменялась. Границы периферического поля зрения под воздействием комплексного лечения, включающего гипотензивную терапию и курсы трансорбитальной МС в виде четырех курсов через каждые 3 месяца, у пациента К. со II стадией открытоугольной глаукомы увеличивались. Границы периферического поля зрения через 12 месяцев: 58; 54; 48; 63; 85; 88; 60; 47, что в сумме составило 503 градуса; на OS по 8 меридианам: 48; 35; 48; 61; 73; 71; 48; 40, что в сумме составило 424 градуса.
Пример 3
Пациентка Ш., 1951 года рождения, обратилась на прием 16.09.2013 для измерения ВГД. Страдает глаукомой обоих глаз с 2006 г. В настоящее время гипотензивная терапия состоит из инсталляций косопта 2 раза в день в оба глаза. При обследовании: острота зрения ОД = 0,4 с сферой + 1,5 = 0,6; OS = 0,6 с сферой + 1,5 = 0,9. Внутриглазное давление PoОД=32 мм рт.ст.; PoOS = 22 мм рт.ст. При биомикроскопическом осмотре передний отрезок без патологических изменений, угол открыт, помутнения хрусталика. ДЗН бледно-розового цвета с расширенной экскавацией до 0,8 на ОД и до 0,6 на OS. Компьютерная статическая периметрия. Границы периферического поля зрения ОД по 8 меридианам: 22; 18; 19; 43; 48; 42; 26; 23, что в сумме составляет 241 градусов. Границы периферического поля зрения OS по 8 меридианам: 39; 24; 37; 49; 56; 54; 29; 31, что в сумме составляет 319 градус. В зоне слепого пятна - абсолютные (<0,1%) и относительные (<0,5%) скотомы. Диагноз: ОД - открытоугольная III В глаукома, OS - открытоугольная II А глаукома. Было рекомендовано в оба глаза инстилляции глазных капель ксалатан на ночь и 0,5% раствора арутимола 2 раза в день. Пациентке был назначен курс трансорбитальной магнитной стимуляции (МС). Использовали следующие параметры. Амплитудное значение магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, режим магнитной индукции - пульсирующий, частотой 17 Гц с плавно нарастающим фронтом и спадом импульса, длительность которого составляет 15 мс. Реализацию указанных параметров осуществляли на отечественном аппарате «Полюс-2», используя для МС индуктор прямоугольной формы. Индуктор помещали непосредственно к закрытому глазу южным полюсом, который на индукторе обозначен стрелкой. Процедуру МС осуществляли на обоих глазах через прокладку в 2 слоя медицинской марли в течение 5-7 минут. На курс лечения назначали 8 ежедневных процедур. В течение всего периода лечения пациентка не испытывала каких-либо неприятных ощущений и побочных эффектов от проводимого физиотерапевтического лечения. Нормализация ВГД до значений «давления цели» было достигнуто на 5 день лечения и составило на ОД - 19 мм рт.ст., на OS - 18 мм рт.ст. Острота зрения повысилась до 0,7 с коррекцией на ОД и до 1.0 с коррекцией на OS. Таким образом, благодаря трансорбитальной МС и местной гипотензивной терапии достигнута компенсация ВГД, которая сохранялась в течение 3-х мес. Через 3 месяца для закрепления эффекта и его стабилизации был проведен через 3 месяца следующий курс лечения. После проведенного курса лечения ВГД на ОД - 28 мм рт.ст., OS - 16 мм рт.ст. Показатели компьютерной статической периметрии были следующими: границы периферического поля зрения ОД по 8 меридианам: 27; 21; 22; 54; 61; 49; 33; 25, что в сумме составляет 292 градусов. Границы периферического поля зрения OS по 8 меридианам: 41; 27; 39; 54; 58; 57; 32; 35, что в сумме составляет 343 градус. В зоне слепого пятна ослабление абсолютной (до <0,5%) и относительной (до <2,5%) скотомы. Разница в периферических полях зрения была достигнута только на обоих глазах (р<0,01). В центральном поле зрения - ослабление абсолютной и относительной скотом. Через 6 месяцев после 2 курса лечения показатели периметрии были следующими: границы периферического поля зрения ОД по 8 меридианам: 32; 27; 28; 64; 72; 62; 37; 31, что в сумме составляет 353 градусов. В зоне слепого пятна - ослабление абсолютной (до <0,5%) скотомы. Границы периферического поля зрения OS по 8 меридианам: 46; 25; 52; 60; 71; 69; 47; 34, что в сумме составляет 404 градусов. В зоне слепого пятна ослабление относительных (до <0,5% и <2,5%) скотом. После третьего и четвертого курса комплексного лечения границы периферического поля зрения ОД по 8 меридианам приблизились к границам нормы: 48; 42; 38; 53; 65; 78; 50; 37, что в сумме составило 411 градус. В зоне слепого пятна - ослабление относительной (до <5,0%) скотомы. Границы периферического поля зрения OS по 8 меридианам: 45; 31; 55; 63; 77; 68; 46; 35, что в сумме составило 420 градусов. В зоне слепого пятна - относительные (<0,5% и <2,5%) скотомы. После проведения четвертого курса лечения показатели оставались стабильными. Дальнейшие наблюдения в течение года показали, что границы периферического поля зрения под воздействием комплексного лечения, включающего гипотензивную терапию и курсы трансорбитальной МС, у пациентки Ш. со II и III стадиями открытоугольной глаукомы оставались стабильными с тенденцией к увеличению суммарного показателя. ВГД, а также ВГД оставалось компенсированным в пределах значений «давления цели» в течение всего срока наблюдения.
Способ лечения глаукомной оптической нейропатии, включающий использование медикаментозной терапии и низкочастотной магнитной стимуляции, отличающийся тем, что наряду с местной гипотензивной терапией проводят трансорбитальную низкочастотную магнитную стимуляцию с амплитудным значением магнитной индукции на рабочей поверхности индуктора - 37,5 мТл, с пульсирующим режимом магнитной индукции и частотой 17 Гц с плавно нарастающим фронтом и спадом импульса, длительностью 15 мс, при этом процедуру трансорбитальной низкочастотной магнитной стимуляции осуществляют на закрытый глаз в течение 5-7 минут, курс лечения составляет 6-10 ежедневных процедур, с проведением в течение года четырех курсов через каждые 3 месяца.