Новое имидазооксазиновое соединение или его соль
Иллюстрации
Показать всеНастоящее изобретение относится к имидазооксазиновому соединению формулы (I) или к его соли, где А, В, С и D представляют собой атом N или C-R1a, атом N или C-R1b, атом N или C-R1c, и атом N или C-R1d соответственно; R1a, R1b, R1c и R1d являются одинаковыми или отличаются друг от друга и каждый представляет собой водород, галоген, циано, С1-6алкил, который может содержать гидроксильную(ые) группу(ы) в качестве заместителя(ей), С1-6алкокси, карбонил, содержащий гидроксил, амино или моно- или ди- (С1 _ 6алкокси)амино в качестве заместителя, необязательно замещенный моно- или ди- (С1-6алкил)аминокарбонил или пиразол; R2 представляет собой фенил, пиридил или тиенил; и R3 и R4 являются одинаковыми или отличаются друг от друга и каждый представляет собой водород, гидрокси, С1-6алкил или С3-7циклоалкил, а также изобретение относится к фармацевтической композиции на основе этих соединений, обладающей противоопухолевой активностью, ингибитору АКТ, способу лечения и предупреждения рака и применению указанных соединений для получения противоракового средства.7 н. и 5 з.п. ф-лы, 6 табл., 64 пр.
,
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новому имидазооксазиновому соединению или к его соли, и к фармацевтической композиции, содержащей имидазооксазиновое соединение или его соль в качестве активного ингредиента, и в частности, к противоопухолевому лекарству, обладающему ингибирующей активностью в отношении AKT киназы. Кроме того, настоящее изобретение относится к ингибитору AKT, к способу предупреждения или лечения злокачественной опухоли, и к применению имидазооксазинового соединения или его соли для получения противоопухолевого лекарства.
Предпосылки создания настоящего изобретения
AKT представляет собой серин-треониновую киназу, идентифицированную в качестве онкогена в вирусе лейкемии мышей, и было выявлено, что ее активность важна для различных функций, таких как клеточная пролиферация, выживаемость, метаболизм, метастазирование и инвазия (непатентные документы 1 и 2). Сообщалось о трех изоформах (AKT1/PKBα, AKT2/PKBβ и AKT3/PKBγ) присутствующих у человека (непатентные документы 3 и 4). Активация AKT влечет за собой размещение в цитоплазматической мембране посредством связывания с фосфатидилинозитол-3-фосфатом, образованным PI3 киназой и фосфорилирование многочисленными киназами (непатентный документ 5). Сообщалось, что во многих случаях рака (например, при раке молочной железы, раке поджелудочной железы, раке печени, раке предстательной железы, раке желудка, раке легкого, раке яичников, раке головы и шеи, раке мочевыводящих путей и эндометриальном раке) экспрессия активированной AKT усилена посредством активации PI3 киназы вследствие мутации, и т.п., или инактивации ее отрицательного регулятора, PTEN (непатентный документ 6). Кроме того сообщалось, что усиленная экспрессия активированной AKT ассоциирована с неблагоприятными прогнозами в случаях различных видов рака (например, рака молочной железы, рака поджелудочной железы, рака печени, рака предстательной железы, рака желудка и эндометриального рака) (непатентный документ 7).
В этой связи, в случаях рака с усиленной активностью AKT ожидается, что лекарство, которое специфически ингибирует AKT, обеспечит супрессию пролиферации, выживаемости, метастазирования, инвазии и т.п. раковых клеток, при введении указанного лекарства, и предлагается в качестве нового противоракового средства, которое поспособствует увеличению продолжительности жизни и улучшению качества жизни пациентов. При существующих методах терапии, поскольку аномалия PI3 киназы, аномалия PTEN или активация AKT служат в качестве показателя для стратификации, становится возможным подбор пациентов, основанный на стратификации; поэтому, это является высоко предпочтительным с этической точки зрения.
Список процитированных документов
Непатентные документы
Непатентный документ 1: Cell, 129, p. 1261-1274 (2007)
Непатентный документ 2: Cell Cycle. 7. p. 2991-2996 (2008)
Непатентный документ 3: Proc. Natl. Acad. Sci. USA 84. p. 5034-5037 (1987)
Непатентный документ 4: J. Biol. Chem. 274. p. 9133-9136 (1999)
Непатентный документ 5: FEBS Letters. 546. p. 108-112 (2003)
Непатентный документ 6: Nature Reviews Drug Discovery, 8, p. 627-644 (2009)
Непатентный документ 7: Anticancer Research, 18, p. 861-874 (2007)
Краткое описание сущности настоящего изобретения
Техническая задача
Задача настоящего изобретения состоит в предоставлении нового имидазооксазинового соединения, обладающего ингибирующей активностью в отношении AKT1 и AKT2 киназ, а также ингибирующей активностью в отношении процессов фосфорилирования AKT и рибосомального белка S6. Кроме того, другая задача настоящего изобретения заключается в предоставлении лекарственного средства, которое применимо для предотвращения и/или лечения заболевания с участием AKT1 и AKT2 киназ, в частности рака, что обусловлено его ингибирующей активностью в отношении AKT1 и AKT2.
Решение задачи
Авторы настоящего изобретения провели обширные исследования соединений, обладающих ингибирующей активностью в отношении AKT1 и AKT2 киназ, и обнаружили, что новое имидазооксазиновое соединение, представленное формулой (I), обладает чрезвычайно высокой ингибирующей активностью в отношении AKT киназы. Настоящее изобретение было оформлено на основании полученных результатов.
Конкретно, настоящее изобретение относится к новому имидазооксазиновому соединению или к его соли, к фармацевтической композиции, содержащей имидазооксазиновое соединение или его соль в качестве активного ингредиента, к противоопухолевому лекарству, содержащему имидазооксазиновое соединение или его соль в качестве активного ингредиента, к ингибитору AKT, содержащему имидазооксазиновое соединение или его соль в качестве активного ингредиента, к способу предупреждения или лечения злокачественной опухоли и к использованию имидазооксазинового соединения или его соли для получения противоопухолевого лекарства.
(1) Имидазооксазиновое соединение, представленное формулой (I), или его соль
,
где
А, B, C и D представляют собой атом N или C-R1a, атом N или C-R1b, атом N или C-R1c, и атом N или C-R1d, соответственно;
R1a, R1b, R1c и R1d являются одинаковыми или отличаются друг от друга, и каждый представляет собой водород, галоген, циано, необязательно замещенный C1-6алкил, необязательно замещенный C1-6алкокси, замещенный карбонил или необязательно замещенную ненасыщенную гетероциклическую группу;
R2 представляет собой необязательно замещенный арил или необязательно замещенную ненасыщенную гетероциклическую группу; и
R3 и R4 являются одинаковыми или отличаются друг от друга, и каждый представляет собой водород, гидрокси, необязательно замещенный C1-6алкил или необязательно замещенный C3-7циклоалкил.
(2) Имидазооксазиновое соединение согласно пункту (1) или его соль, где
A, B, C и D представляют собой атом N или C-R1a, атом N или C-R1b, атом N или C-R1c, и атом N или C-R1d, соответственно;
R1a, R1b, R1c и R1d являются одинаковыми или отличаются друг от друга, и каждый представляет собой водород, галоген, циано, необязательно замещенный C1-6алкил, C1-6алкокси, замещенный карбонил или необязательно замещенную ненасыщенную гетероциклическую группу;
R2 представляет собой С6-10арил или 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, выбранных из группы, состоящей из N, S и O;
R3 представляет собой водород, необязательно замещенный С1-6алкил или необязательно замещенный C3-7циклоалкил; и
R4 представляет собой водород или гидрокси.
(3) Имидазооксазиновое соединение согласно пунктам (1) или (2) или его соль, где
A, B, C и D представляют собой C-R1a, C-R1b, C-R1c и C-R1d, соответственно, или один или два из A, B, C и D представляют собой атом N;
по меньшей мере, два из R1a, R1b, R1c и R1d представляют собой водород, а другой(ие) представляет(ют) собой галоген, циано, C1-6алкил, который может иметь гидроксильную(ые) группу(ы) в качестве заместителя(ей), C1-6алкокси, карбонил, содержащий гидроксил, амино или моно- или ди-(C1-6алкокси)амино в качестве заместителя, необязательно замещенный моно- или ди-(C1-6алкил)аминокарбонил или ненасыщенную гетероциклическую группу,
R2 представляет собой фенил, пиридил или тиенил;
R3 представляет собой водород, метил, этил или циклопропил; и
R4 представляет собой водород или гидрокси.
(4) Имидазооксазиновое соединение согласно пунктам (1) или (2), или его соль, где
A, B, C и D представляют собой C-R1a, C-R1b, C-R1c и C-R1d, соответственно, или один или два из A, B, C и D представляют собой атом N;
по меньшей мере, два из R1a, R1b, R1c и R1d представляют собой водород, а другой(ие) представляет(ют) собой хлор, фтор, циано, метил, гидроксиметил, метокси, этокси, амино, карбоксил, карбамоил, метиламинокарбонил, диметиламинокарбонил, этиламинокарбонил, гидроксиэтиламинокарбонил, этоксиаминокарбонил или пиразолил;
R2 представляет собой фенил, пиридил или тиенил;
R3 представляет собой водород, метил, этил или циклопропил; и
R4 представляет собой водород или гидрокси.
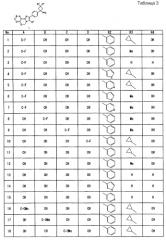
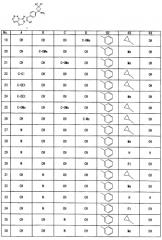
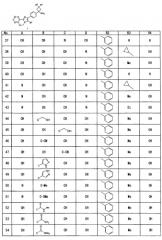
(5) Имидазооксазиновое соединение, выбранное из группы, состоящей из последующих соединений (a)-(t), или его соль:
(a) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(b) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-(пиридин-4-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(c) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(d) транс-3-амино-1-циклопропил-3-(4-(10-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(e) транс-3-амино-1-циклопропил-3-(4-(9-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(f) транс-3-амино-1-циклопропил-3-(4-(8-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(g) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(h) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-с]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(i) транс-3-амино-1-этил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-е][1,3]оксазин-2-ил)фенил)циклобутанол,
(j) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-с]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(k) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(l) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[4,3-е][1,3]оксазин-2-ил)фенил)циклобутанол,
(m) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-с]пиридо[4,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(n) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,2-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(o) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиразино[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(p) транс-3-амино-3-(4-(9-(гидроксиметил)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)-1-метилциклобутанол,
(q) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-9-карбонитрил,
(r) транс-3-амино-1-метил-3-(4-(3-фенил-9-(1H-пиразол-5-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(s) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-метил-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-8-карбоксамид, и
(t) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-этокси-3-фенил-5H-бензо[e]имидазо[1,2-е][1,3]оксазин-8-карбоксамид.
(6) Фармацевтическая композиция, содержащая эффективное количество имидазооксазинового соединения в соответствии с любым из пунктов (1)-(5) или его соли и фармацевтический носитель.
(7) Противоопухолевое лекарство, содержащее эффективное количество имидазооксазинового соединения в соответствии с любым из пунктов (1)-(5) или его соли и фармацевтический носитель.
(8) Ингибитор AKT, содержащий имидазооксазиновое соединение в соответствии с любым из пунктов (1)-(5) или его соль в качестве активного ингредиента.
(9) Ингибитор AKT в соответствии с пунктом (8), который представляет собой ингибитор AKT1 и AKT2.
(10) Способ предупреждения или лечения рака, включающий введение млекопитающему имидазооксазинового соединения в соответствии с пунктами (1) или (2) или его соли в количестве, эффективном для предупреждения рака или лечения рака.
(11) Применение имидазооксазинового соединения в соответствии с пунктами (1) или (2) или его соли для получения профилактического или терапевтического средства против рака.
(12) Имидазооксазиновое соединение в соответствии с пунктами (1) или (2) или его соль для применения в профилактике или терапии рака.
Полезные эффекты настоящего изобретения
Настоящее изобретение относится к новому соединению, представленному вышеуказанной формулой (I), или его соли, которые используются в качестве ингибитора AKT1 и AKT2 киназ.
Было выявлено, что соединение или его соль согласно настоящему изобретению обладает превосходной ингибирующей активностью в отношении AKT1 и AKT2 киназ, а также проявляет ингибирующую активность в отношении процессов фосфорилирования AKT и рибосомального белка S6. Поэтому, исходя из его превосходной ингибирующей активности в отношении AKT киназы, соединение или его соль согласно настоящему изобретению используется в качестве средства для предупреждения и/или лечения заболевания с участием AKT киназы, такого как рак.
Описание вариантов осуществления
Соединение согласно настоящему изобретению, которое представлено формулой (I), представляет собой имидазооксазиновое соединение, содержащее циклобутил в пара-положении фенильной группы в 2-положении в имидазооксазиновом скелете формулы (I), и является новым соединением, не описанным в вышеупомянутой литературе.
Например, в Can. J. Chem., Vol. 63, p. 632 (1985) имидазооксазиновое соединение представлено в качестве промежуточного соединения синтеза каннабиноидов (например, соединение 10). Тем не менее, заместитель, присутствующий в фенильной группе в 2-положении в имидазооксазиновом скелете, отличается от представленного в настоящем изобретении, и в Can. J. Chem., Vol. 63, p. 632 (1985) также не указаны противоопухолевые эффекты.
В описании настоящего изобретения, примеры «заместителей» необязательно замещенных групп включают галоген, гидроксил, циано, амино, нитро, оксо, карбокси, карбамоил, алкил, циклоалкил, алкенил, алкинил, алкокси, ацил, ацилокси, алкоксикарбонил, насыщенную гетероциклическую группу, ненасыщенную гетероциклическую группу, арил, галогеналкил, аралкил, насыщенный гетероциклический алкил, алкиламино, ациламино и аралкилокси. Если присутствуют заместители, то обычно их число составляет от 1 до 3, и, в частности, от 1 до 2.
В заместителях, примеры галогена включают хлор, бром, фтор и йод.
В заместителях, алкил предпочтительно представляет собой неразветвленную или разветвленную C1-6алкильную группу, и его примеры включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил и гексил.
В заместителях, циклоалкил предпочтительно представляет собой C3-7циклоалкильную группу, и его примеры включают циклопропил, циклобутил, циклопентил, циклогексил и циклогептил.
В заместителях, алкенил предпочтительно представляет собой C2-6алкенильную группу, содержащую двойную углерод-углеродную связь, и его примеры включают винил, аллил, метилвинил, пропенил, бутенил, пентенил и гексенил.
В заместителях, алкинил предпочтительно представляет собой C2-6алкинильную группу, содержащую тройную углерод-углеродную связь, и его примеры включают этинил и пропаргил.
В заместителях, алкокси предпочтительно представляет собой неразветвленную или разветвленную C1-6алкоксигруппу, и его примеры включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси и трет-бутокси.
В заместителях, ацил предпочтительно представляет собой C1-6алканоильную группу или C7-12ароильную группу, и его примеры включают формил, ацетил, пропионил, н-бутирил, изобутирил, валерил, изовалерил, пивалоил и бензоил.
В заместителях, ацилокси представляет собой оксигруппу, замещенную вышеупомянутой ацильной группой, и предпочтительно оксигруппа замещена C1-6алканоильной группой или C7-12ароильной группой. Ее примеры включают формилокси, ацетокси, пропионилокси, н-бутирилокси, изобутирилокси, валерилокси, изовалерилокси, пивалоилокси и бензоилокси.
В заместителях, алкоксикарбонил представляет собой карбонильную группу, замещенную вышеупомянутой алкоксигруппой, и предпочтительно карбонильную группу, замещенную C1-6алкоксигруппой. Его примеры включают метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил и трет-бутоксикарбонил.
В заместителях, насыщенная гетероциклическая группа предпочтительно представляет собой 5-10-членную моноциклическую или бициклическую насыщенную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, выбранных из группы, состоящей из N, S и O. Ее примеры включают пирролидинил, пиперидинил, пиперазинил, гексаметиленимино, морфолино, тиоморфолино, гомопиперазинил, тетрагидрофуранил, тетрагидропиранил, метилендиоксифенил, этилендиоксифенил и дигидробензофуранил.
В заместителях, ненасыщенная гетероциклическая группа предпочтительно представляет собой 5-10-членную моноциклическую или бициклическую ненасыщенную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, выбранных из группы, состоящей из N, S и O. Ее примеры включают имидазолил, тиенил, фурил, пирролил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тетразолил, пиридил, пиразил, пиримидинил, пиридазинил, индолил, изоиндолил, индазолил, бензофуранил, бензимидазолил, бензоксазолил, бензотиазолил, пуринил, хинолил, изохинолил, хиназолинил и хиноксалил.
В заместителях, арил предпочтительно представляет собой C6-14арильную группу, и его примеры включают фенил и нафтил.
В заместителях, галогеналкил представляет собой группу, в которой от одного до всех атомов водорода вышеупомянутой алкильной группы замещены описанным выше галогеном, и предпочтительно группу, в которой от одного до всех атомов водорода вышеупомянутой неразветвленной или разветвленной C1-6алкильной группы замещены описанным выше галогеном. Его примеры включают дифторметил и трифторметил.
В заместителях, аралкил предпочтительно представляет собой неразветвленную или разветвленную C1-6алкильную группу, замещенную C6-14ароматической углеводородной группой, и его примеры включают бензил, фенилэтил, фенилпропил, нафтилметил и нафтилэтил.
В заместителях, насыщенный гетероциклический алкил представляет собой вышеупомянутую алкильную группу, замещенную описанной выше насыщенной гетероциклической группой, и предпочтительно, вышеупомянутую неразветвленную или разветвленную C1-6алкильную группу, замещенную 5-7-членной моноциклической насыщенной гетероциклической группой, содержащей 1 или 2 гетероатома, выбранных из группы, состоящей из N, S и O. Его примеры включают морфолинометил и пиперидинилэтил.
В заместителях, алкиламино представляет собой аминогруппу, моно- или ди-замещенную вышеупомянутой алкильной группой, и предпочтительно, если аминогруппа моно- или ди-замещена неразветвленной или разветвленной C1-6алкильной группой. Ее примеры включают метиламино, этиламино, диэтиламино, метилэтиламино, циклобутилметиламино, диметиламино и 2-гидроксиэтил(метил)амино.
В заместителях, ациламино представляет собой аминогруппу, замещенную вышеупомянутой ацильной группой, и предпочтительно, если аминогруппа замещена C1-6алканоильной группой или C7-12ароильной группой. Ее примеры включают формиламино, ацетиламино, пропиониламино, бутириламино, 2-метилпропиониламино, пивалоиламино, пенталоиламино, 3-метилбутириламино и гексаноиламино.
В заместителях, аралкилокси представляет собой оксигруппу, содержащую вышеупомянутую аралкильную группу, и предпочтительно, если оксигруппа замещена неразветвленной или разветвленной C1-6алкильной группой, с которой связана C6-14ароматическая углеводородная группа. Ее примеры включают бензилокси, фенэтилокси, фенилпропилокси, нафтилметилокси и нафтилэтилокси.
В формуле (I) A, B, C и D представляют собой атом N или C-R1a, атом N или C-R1b, атом N или C-R1c, и атом N или C-R1d, соответственно.
Примеры галогена, представленного R1a, R1b, R1c или R1d, включают вышеупомянутый галоген, и предпочтительно хлор или фтор.
C1-6алкил «необязательно замещенного C1-6алкила», представленного R1a, R1b, R1c или R1d, представляет собой вышеупомянутую неразветвленную или разветвленную C1-6алкильную группу, и предпочтительно C1-3алкильную группу, и более предпочтительно метил. В качестве заместителя предпочтительным является гидроксил.
C1-6алкокси «необязательно замещенного C1-6алкокси», представленного R1a, R1b, R1c или R1d, представляет собой вышеупомянутую неразветвленную или разветвленную C1-6алкоксигруппу, и предпочтительно C1-3алкоксигруппу, и более предпочтительно метокси или этокси.
Заместитель «замещенного карбонила», представленного R1a, R1b, R1c или R1d, предпочтительно представляет собой гидроксил, амино, необязательно замещенный моно- или ди-(C1-6алкил)амино или моно- или ди-(C1-6алкокси)амино.
Моно- или ди-(C1-6алкил)аминокарбонил «необязательно замещенного моно- или ди-(C1-6алкил)аминокарбонила» представляет собой аминокарбонильную группу, содержащую одну или две описанные выше C1-6алкильные группы; предпочтительной является моно- или ди-(C1-3алкил)аминокарбонильная группа; и более предпочтительными являются метиламинокарбонил, диметиламинокарбонил и этиламинокарбонил. В качестве заместителя предпочтительным является гидроксил.
Моно- или ди-(C1-6алкокси)аминокарбонил представляет собой аминокарбонильную группу, содержащую одну или две описанные выше C1-6алкоксигруппы, предпочтительно моно- или ди-(C1-3алкокси)аминокарбонильную группу, и более предпочтительно этоксиаминокарбонил.
В качестве «замещенного карбонила», представленного R1a, R1b, R1c или R1d, особенно предпочтительным является карбоксил, карбамоил, метиламинокарбонил, этиламинокарбонил, гидроксиэтиламинокарбонил и этоксиаминокарбонил.
Ненасыщенная гетероциклическая группа «необязательно замещенной ненасыщенной гетероциклической группы», представленной R1a, R1b, R1c или R1d, представляет собой вышеупомянутую ненасыщенную гетероциклическую группу, и предпочтительно пиразолил.
Арил «необязательно замещенного арила», представленного R2 в формуле (1), предпочтительно представляет собой C6-14арильную группу, и более предпочтительно фенил.
Ненасыщенная гетероциклическая группа «необязательно замещенной ненасыщенной гетероциклической группы», представленной R2, представляет собой вышеупомянутую ненасыщенную гетероциклическую группу, предпочтительно 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, выбранных из группы, состоящей из N, S и O, и более предпочтительно пиридил или тиенил.
R3 и R4 являются одинаковыми или отличаются друг от друга, и каждый представляет собой водород, гидрокси, необязательно замещенный C1-6алкил или необязательно замещенный C3-7циклоалкил.
C1-6алкил «необязательно замещенного C1-6алкила», представленного R3 или R4, представляет собой вышеупомянутую неразветвленную или разветвленную C1-6алкильную группу, и предпочтительно C1-3алкильную группу; и предпочтительными являются метил и этил.
C3-7циклоалкил «необязательно замещенного C3-7циклоалкила», представленного R3 или R4, представляет собой циклопропил, циклобутил, циклопентил, циклогексил или циклогептил; предпочтительной является C3-6циклоалкильная группа; и более предпочтительным является циклопропил.
Способ получения соединения, представленного формулой (I)
Соединение согласно настоящему изобретению может быть получено, например, следующими способами получения или способами, представленными в примерах. Тем не менее, способ получения соединения согласно настоящему изобретению не ограничивается указанными примерами.
Соединение (I) согласно настоящему изобретению может быть получено, например, следующим способом получения A и способом получения B.
Способ получения A
(В формуле L1, L2, L3 и L4 являются одинаковыми или отличаются друг от друга, и каждый представляет собой уходящую группу; а другие символы определены выше).
Стадия 1
Указанная стадия представляет собой способ получения соединения 2 из альдегидного соединения 1.
Исходное соединение 1 представляет собой коммерчески доступный продукт, или оно может быть получено известным способом. Первая стадия может проводиться способом, описанным в документах (например, J. Med. Chem., Vol. 46, p. 5416, 2003; J. Org. Chem., Vol. 68, p. 5415, 2003), основанного на них способа или комбинаций указанных способов с обычными способами.
Например, при использовании в реакции водного раствора аммиака и водного раствора глиоксаля количество используемого водного раствора аммиака составляет от 1 до 10 эквивалентов относительно соединения 1. Количество используемого водного раствора глиоксаля составляет от 1 до 10 эквивалентов относительно соединения 1.
Примеры используемых растворителей включают метанол, этанол, тетрагидрофуран, этилацетат, N,N-диметилформамид, уксусную кислоту и воду. Растворители могут использоваться по отдельности или в комбинации. Время реакции составляет от 0,1 до 100 часов, и предпочтительно от 0,5 до 24 часов. Температура реакции составляет от 0°C до температуры кипения растворителя, и предпочтительно от 0 до 100°C.
Полученное таким образом соединение 2 может быть выделено и очищено известными способами разделения и очистки, такими как концентрирование, концентрирование при пониженном давлении, кристаллизация, экстрагирование растворителем, повторное осаждение и хроматография, а затем использовано на следующей стадии; или оно может быть использовано на следующей стадии без выделения и очистки.
Стадия 2
Указанная стадия представляет собой способ получения соединения 4, при котором проводят реакцию алкилирования соединения 2 соединением 3 в присутствии основания.
Соединение 3, в котором упомянуты L1 и L2, хлор, бром, йод и т.д., представляет собой коммерчески доступный продукт, или оно может быть получено известным способом.
Соединение 3 может использоваться в количестве от 1 до 100 эквивалентов, и предпочтительно от 1 до 10 эквивалентов, относительно соединения 2.
Примеры основания включают неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия и гидроксид цезия, и органические амины, такие как триметиламин, триэтиламин, трипропиламин, диизопропилэтиламин, N-метилморфолин, пиридин, 4-(N,N-диметиламино)пиридин, лутидин и коллидин. Основание может использоваться в количестве от 1 до 100 эквивалентов, и предпочтительно от 2 до 10 эквивалентов.
Примеры подходящих растворителей включают N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, тетрагидрофуран, 1,4-диоксан, N-метилпирролидин-2-он, ацетонитрил и воду. Растворители могут использоваться по отдельности или в комбинации. Время реакции составляет от 0,1 до 100 часов, и предпочтительно от 0,5 до 24 часов. Температура реакции составляет от 0°C до температуры кипения растворителя, и предпочтительно от 0 до 100°C.
Полученное таким образом соединение 4 может быть выделено и очищено известными способами разделения и очистки, а затем использовано на следующей стадии; или оно может быть использовано на следующей стадии без выделения и очистки.
Стадия 3
Указанная стадия представляет собой способ получения соединения 6 из соединения 5.
Соединение 5, в котором упомянуты L3, хлор, бром, йод и т.д., представляет собой коммерчески доступный продукт, или оно может быть получено известным способом.
Стадия 3 может проводиться тем же способом, что и стадия 1.
Стадия 4
Указанная стадия представляет собой способ получения соединения 4, при котором взаимодействие соединения 6 с формальдегидом проводят в присутствии основания.
Формальдегид может использоваться в количестве от 1 до 100 эквивалентов, и предпочтительно от 1 до 10 эквивалентов, относительно соединения 6. Формальдегид может использоваться в форме водного раствора или в форме параформальдегида.
Примеры основания включают гидроксид натрия, карбонат натрия, гидроксид калия, карбонат цезия, трет-бутоксид натрия и трет-бутоксид калия. Основание может использоваться в количестве от 1 до 100 эквивалентов, и предпочтительно от 2 до 10 эквивалентов.
Примеры используемых растворителей включают N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, тетрагидрофуран, 1,4-диоксан, N-метилпирролидин-2-он, ацетонитрил и воду. Растворители могут использоваться по отдельности или в комбинации. Время реакции составляет от 0,1 до 100 часов, и предпочтительно от 0,5 до 24 часов. Температура реакции составляет от 0°C до температуры кипения растворителя, и предпочтительно от 0 до 100°C.
Полученное таким образом соединение 4 может быть выделено и очищено известными способами разделения и очистки, а затем использовано на следующей стадии; или оно может быть использовано на следующей стадии без выделения и очистки.
Стадия 5
Указанная стадия представляет собой способ получения соединения 7 путем проведения галогенирования, например, путем осуществления воздействия галогенирующего агента на соединение 4 (L4=Cl, Br или I). Галогенирование может проводиться общеизвестным способом; например, галогенирование может проводиться в реакционном растворителе, который не оказывает негативное влияние на реакцию.
Полученное таким образом соединение 7 может быть выделено и очищено известными способами разделения и очистки, а затем использовано на следующей стадии; или оно может быть использовано на следующей стадии без выделения и очистки.
Стадия 6
Указанная стадия представляет собой способ получения соединения 8 путем осуществления взаимодействия соединения 7 с арилбороновой кислотой, сложным эфиром арилбороновой кислоты, ненасыщенной гетероциклической бороновой кислотой или сложным эфиром ненасыщенной гетероциклической арилбороновой кислоты.
Указанная стадия может проводиться общеизвестным способом (например, Chemical Reviews, Vol. 95, p. 2457, 1995); например, указанная стадия может проводиться в растворителе, который не оказывает негативное влияние на реакцию, в присутствии катализатора, содержащего металл переменной валентности, и основания.
Арилбороновая кислота, сложный эфир арилбороновой кислоты, ненасыщенная гетероциклическая бороновая кислота или сложный эфир ненасыщенной гетероциклической арилбороновой кислоты могут использоваться в количестве от 1 до 10 эквивалентов, и предпочтительно от 1 до 3 эквивалентов, относительно соединения 7.
Примеры подходящих катализаторов, содержащих металл переменной валентности, включают палладиевые катализаторы (например, ацетат палладия, хлорид палладия, тетракис(трифенилфосфин)паддалий и т.д.) и никелевые катализаторы (например, хлорид никеля и т.д.). При необходимости, могут быть добавлены лиганды (например, трифенилфосфин, три-трет-бутилфосфин и т.д.), и в качестве сокатализаторов могут использоваться оксиды металлов (например, оксид меди, оксид серебра и т.д.), и т.п. Хотя количество используемого катализатора, содержащего металл переменной валентности, изменяется в зависимости от типа катализатора, как правило, оно составляет приблизительно от 0,0001 приблизительно до 1 моль, и предпочтительно приблизительно от 0,01 приблизительно до 0,5 моль относительно соединения 7 (1 моль). Как правило, количество используемого лиганда составляет приблизительно от 0,0001 приблизительно до 4 моль, и предпочтительно приблизительно от 0,01 приблизительно до 2 моль относительно соединения 7 (1 моль). Как правило, количество используемого сокатализатора составляет приблизительно от 0,0001 приблизительно до 4 моль, и предпочтительно приблизительно от 0,01 приблизительно до 2 моль относительно соединения 7 (1 моль).
Примеры основания включают органические амины (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5.4.0]ундец-7-ен, пиридин, N,N-диметиланилин и т.д.), соли щелочных металлов (например, гидрокарбонат натрия, гидрокарбонат калия, карбонат натрия, карбонат калия, карбонат цезия, фосфат натрия, фосфат калия, гидроксид натрия, гидроксид калия и т.д.), гидриды металлов (например, гидрид калия, гидрид натрия и т.д.), алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид натрия, трет-бутоксид калия и т.д.), дисилазиды щелочных металлов (например, дисилазид лития, дисилазид натрия, дисилазид калия и т.д.). Среди них предпочтительными являются соли щелочных металлов, такие как карбонат калия, карбонат цезия, фосфат натрия и фосфат калия; алкоксиды щелочных металлов, такие как трет-бутоксид натрия и трет-бутоксид калия; органические амины, такие как триэтиламин и диизопропилэтиламин; и т.п. Количество используемого основания, как правило, составляет от 0,1 до 10 моль, и предпочтительно приблизительно от 1 приблизительно до 5 моль относительно соединения 7 (1 моль).
Могут использоваться любые растворители при условии, если они не оказывают негативное влияние на реакцию. Их примеры включают углеводороды (например, бензол, толуол, ксилол, и т.д.), галогенированные углеводороды (например, хлороформ, 1,2-дихлорэтан, и т.д.), нитрилы (например, ацетонитрил, и т.д.), эфиры (например, диметоксиэтан, тетрагидрофуран, 1,4-диоксан, и т.д.), спирты (например, метанол, этанол, и т.д.), апротонные полярные растворители (например, диметилформамид, диметилсульфоксид, гексаметилфосфорамид, и т.д.), вода и их смеси. Время реакции составляет от 0,1 до 100 часов, и предпочтительно от 0,5 до 24 часов. Температура реакции составляет от 0°C до температуры кипения растворителя, и предпочтительно от 0 до 150°C.
Полученное таким образом соединение 8 может быть выделено и очищено известными способами разделения и очистки, а затем использовано на следующей стадии; или оно может быть использовано на следующей стадии без выделения и очистки.
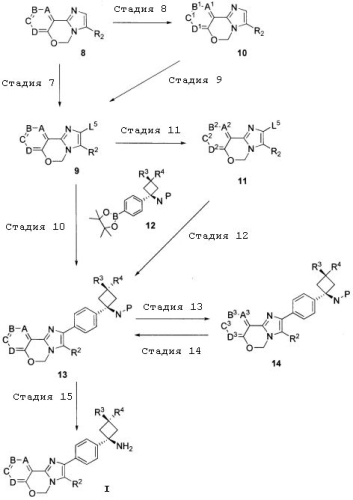
Способ получения B
(В формуле L5 являются одинаковыми или отличаются друг от друга, и каждый представляет собой уходящую группу; P представляет собой защитную группу; а другие символы определены выше).
Стадия 7
Стадия 7 может проводиться тем же способом, что и стадия 5.
Стадия 8
Указанная стадия представляет собой способ преобразования любого из A-D соединения 8 в любой из A1-D1, соответственно, путем проведения реакции сочетания и т.д. с применением общеизвестного способа.
Если любой из A-D соединения 8 содержит уходящую группу, такую как галоген, то реакцию соединения проводят в присутствии катализатора, содержащего металл переменной валентности, с получением соединения 10.
В случае преобразования уходящей группы, такой как галоген, в цианогруппу используют цианид цинка. В случае преобразования в ароматическое кольцо или гетероароматическое кольцо используют коммерчески доступную бороновую кислоту или сложный бороновый эфир, или бороновую кислоту или сложный бороновый эфир, которые могут быть получены известным способом. В случае преобразования в сложноэфирную группу использую монооксид углерода.
Полученное таким образом соединение 10 может быть выделено и очищено известными способами разделения и очистки, а затем использовано на следующей стадии; или оно может быть использовано на следующей стадии без выделения и очистки.
Стадия 9
Стадия 9 может проводиться тем же способом, что и стадия 5.
Стадия 10
Указанная стадия представляет собой способ получения соединения 13 путем осуществления реакции сочетания соединения 9 и соединения 12.
Соединение 12 может быть получено способом, описанным в документах (например, в WO2008/070016, WO2009/148877, WO2009/148916, WO2010/088177, WO2010/114780, WO2010/104933), или основанным на нем способом.
Указанная стадия может проводиться тем же способом, что и стадия 6.
Полученное таким образом соединение 13 может быть выделено и очищено известными способами разделения и очистки, а затем использовано на следующей стадии; или оно может быть использовано на следующей стадии без выделения и очистки.
Стадия 11
Указанная стадия представляет собой способ преобразования любого из A-D соединения 9 в любой из A1-D1, соответственно, путем проведения реакции преобразования функциональных групп и т.д. с применением общеизвестного способа.
Если любое из A-D соединения 9 сод