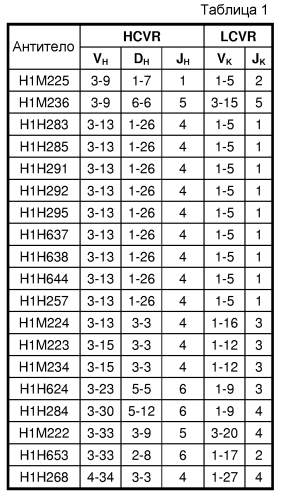
Антитела человека против ангиопоэтин-подобного белка 4 человека
Иллюстрации
Показать всеИзобретение относится к биохимии. Раскрыты антитело человека или антиген-связывающий фрагмент антитела человека, которые специфически связывают и ингибируют ангиопоэтин-подобный белок 4 человека (hANGPTL4). Описаны молекула нуклеиновой кислоты, кодидующая раскрытое антитело или антиген-связывающий фрагмент и вектор экспрессии, содержащий такую кислоту. Описан способ получения антитела, включающий использования клетки-хозяина, содержащий указанный вектор экспрессии. Также описана фармацевтическая композиция, содержащая раскрытое антитело. Представлен способ профилактики или лечения заболевания или нарушения, которое можно предотвратить, облегчить, сократить или ингибировать посредством сокращения или ингибирования активности ANGPTL4, включающий введение нуждающемуся в этом индивидууму терапевтически эффективного количества фармацевтической композиции. Изобретение можно использовать в лечении заболеваний или нарушений, связанных с ANGPTL4, таких как гиперлипидемия, гиперлипопротеинемия, дислипидемия, включая гипертриглицеридемию, гиперхолестеринемию, хиломикронемию и т.п. Далее анти-hANGPTL4 антитела можно вводить нуждающемуся в них индивидууму для профилактики или лечения заболеваний или нарушений, для которых нарушение метаболизма липидов представляет собой фактор риска. Такие заболевания или нарушения включают сердечно-сосудистые заболевания, такие как атеросклероз или атеросклеротическая болезнь сердца; острый панкреатит; неалкогольный стеатогепатит (NASH); диабет; ожирение; и т.п. 8 н. и 11 з.п. ф-лы, 7 ил., 18 табл., 13 пр.
Реферат
2420-187440RU/061
АНТИТЕЛА ЧЕЛОВЕКА ПРОТИВ АНГИОПОЭТИН-ПОДОБНОГО БЕЛКА 4 ЧЕЛОВЕКА
Область изобретения
Настоящее изобретение относится к антителам человека и антигенсвязывающим фрагментам антител человека, которые специфично связывают ангиопоэтин-подобный белок 4 человека (hANGPTL4), и к терапевтическим способам применения этих антител.
Связанные области
Липопротеинлипаза (LPL) играет центральную роль в метаболизме липопротеинов, поддерживая нормальные уровни липопротеинов в крови и, посредством тканеспецифической регуляции их активности, определяя, когда и в каких тканях высвобождаются триглицериды (TG). Опубликовано, что ANGPTL4 ингибирует LPL и замедляет катаболизм липопротеинов у людей и грызунов. Нулевые по ANGPTL4 мыши демонстрируют значительное снижение сывороточного уровня TG. И наоборот, инъекция мышам ANGPTL4 вызывает быстрое повышение уровней циркулирующих липидов, более интенсивное, чем при инъекции ангиопоэтин-подобного белка 3 (ANGPTL3) (Yoshida et al., 2002, J Lipid Res 43:1770-1772). Показано, что для ингибирования активности LPL и, таким образом, для индикации гипертриглицеридемии важна N-концевая суперспиральная область, а не C-концевой фибриноген-подобный домен белка ANGPTL4. Эти наблюдения показывают, что ингибирование ANGPTL4 может оказаться эффективным для лечения заболеваний, которые характеризуются повышенными уровнями липидов, включая первичную дислипидемию и гипертриглицеридемию, связанную с ожирением, метаболический синдром, диабет II типа и т.п. ANGPTL4 также играет роль в ангиогенезе и образовании злокачественных опухолей (Galaup et al., 2006, PNAS 103(49):18721-18726; Kim et al., 2000, Biochem J 346:603-610; и Ito et al., 2003, Cancer Res 63(20):6651-6657).
Последовательности нуклеиновых кислот и аминокислотные последовательности ANGPTL4 человека представлены в SEQ ID NO:475 и 476, соответственно. Антитела против ANGPTL4 описаны, например, в WO 2006/074228 и WO 2007/109307.
КРАТКАЯ СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В первом аспекте изобретение относится к полностью моноклональным антителам (mAb) человека и их антигенсвязывающим фрагментам, которые специфически связывают ANGPTL4 (hANGPTL4) человека и нейтрализуют его активность.
Антитела (Ab) могут быть полноразмерными (например, антитела IgG1 или IgG4) или могут содержать только антигенсвязывающий участок (например, фрагмент Fab, F(ab')2 или scFv), и их можно модифицировать с изменением функциональности, например, для устранения конечных эффекторных функций (Reddy et al., 2000, J. Immunol. 164:1925-1933).
В одном из вариантов осуществления изобретение включает антитело или антигенсвязывающий фрагмент антитела, содержащие вариабельную область тяжелой цепи (HCVR), выбранную из группы, состоящей из SEQ ID NO: 2, 18, 22, 26, 42, 46, 50, 66, 70, 74, 90, 94, 98, 114, 118, 122, 138, 142, 146, 162, 166, 170, 186, 190, 194, 210, 214, 218, 234, 238, 242, 258, 262, 266, 282, 286, 290, 306, 310, 314, 330, 334, 338, 354, 358, 362, 378, 382, 386, 402, 406, 410, 426, 430, 434, 450, 454, 458, 466, 468 и 487 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или, по меньшей мере на 99%. В другом варианте осуществления антитело или его антигенсвязывающий фрагмент содержат HCVR с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:26, 42, 46, 487, 74, 90, 94, 122, 138, 142, 146, 162 и 166. В еще одном варианте осуществления антитело или его фрагмент содержат HCVR, содержащую SEQ ID NO:42, 487, 90, 138 или 162.
В одном из вариантов осуществления антитело или антигенсвязывающий фрагмент антитела содержат вариабельную область легкой цепи (LCVR), выбранную из группы, состоящей из SEQ ID NO: 10, 20, 24, 34, 44, 48, 58, 68, 72, 82, 92, 96, 106, 116, 120, 130, 140, 144, 154, 164, 168, 178, 188, 192, 202, 212, 216, 226, 236, 240, 250, 260, 264, 274, 284, 288, 298, 308, 312, 322, 332, 336, 346, 356, 360, 370, 380, 384, 394, 404, 408, 418, 428, 432, 442, 452 и 456 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или, по меньшей мере на 99%. В другом варианте осуществления антитело или антигенсвязывающий участок антитела содержат LCVR с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:34, 44, 48, 82, 92, 96, 130, 140, 144, 154, 164 и 168. В еще одном варианте осуществления антитело или его фрагмент содержат LCVR, содержащую SEQ ID NO:44, 92, 140 или 164.
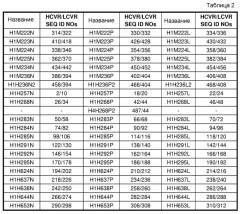
В дополнительных вариантах осуществления антитело или его фрагмент содержат пару последовательностей HCVR и LCVR (HCVR/LCVR), выбранную из группы, состоящей из SEQ ID NO:2/10, 18/20, 22/24, 26/34, 42/44, 487/44, 46/48, 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 98/106, 114/116, 118/120, 122/130, 138/140, 142/144, 146/154, 162/164, 166/168, 170/178, 186/188, 190/192, 194/202, 210/212, 214/216, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 266/274, 282/284, 286/288, 290/298, 306/308, 310/312, 314/322, 330/332, 334/336, 338/346, 354/356, 358/360, 362/370, 378/380, 382/384, 386/394, 402/404, 406/408, 410/418, 426/428, 430/432, 434/442, 450/452, 454/456, 458/394, 466/404 и 468/408. В одном из вариантов осуществления антитело или его фрагмент содержат HCVR и LCVR, выбранные из пар аминокислотных последовательностей SEQ ID NO:26/34, 42/44, 487/44, 46/48, 74/82, 90/92, 94/96, 122/130, 138/140, 142/144, 146/154, 162/164 и 166/168. В другом варианте осуществления антитело или его фрагмент содержат пару HCVR/LCVR, содержащую SEQ ID NO:42/44, 487/44, 90/92, 138/140 или 162/164.
Во втором аспекте изобретение предоставляет антитело или антигенсвязывающий фрагмент антитела, содержащие аминокислотную последовательность определяющей комплементарность области тяжелой цепи 3 (HCDR3), выбранную из группы, состоящей из SEQ ID NO: 8, 32, 56, 80, 104, 128, 152, 176, 200, 224, 248, 272, 296, 320, 344, 368, 392, 416, 440 и 464 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или, по меньшей мере на 99%; и аминокислотную последовательность легкой цепи CDR3 (LCDR3), выбранную из группы, состоящей из SEQ ID NO:16, 40, 64, 88, 112, 136, 160, 184, 208, 232, 256, 280, 304, 328, 352, 376, 400, 424 и 448 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или, по меньшей мере на 99%. В одном из вариантов осуществления антитело или его фрагмент содержат пару аминокислотных последовательностей HCDR3/LCDR3, содержащую SEQ ID NO:32/40, 80/88, 128/136 или 152/160. В другом варианте осуществления антитело или его фрагмент содержат пару аминокислотных последовательностей HCDR3/LCDR3, содержащую SEQ ID NO:32/40 или 80/88.
В дополнительном варианте осуществления антитело или его фрагмент дополнительно содержат аминокислотную последовательность тяжелой цепи CDR1 (HCDR1), выбранную из группы, состоящей из SEQ ID NO:4, 28, 52, 76, 100, 124, 148, 172, 196, 220, 244, 268, 292, 316, 340, 364, 388, 412, 436 и 460 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%; и аминокислотную последовательность тяжелой цепи CDR2 (HCDR2), выбранную из группы, состоящей из SEQ ID NO:6, 30, 54, 78, 102, 126, 150, 174, 198, 222, 246, 270, 294, 318, 342, 366, 390, 414, 438 и 462 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или, по меньшей мере на 99%; и необязательно дополнительно содержат аминокислотную последовательность легкой цепи CDR1 (LCDR1), выбранную из группы, состоящей из SEQ ID NO:12, 36, 60, 84, 108, 132, 156, 180, 204, 228, 252, 276, 300, 324, 348, 372, 396, 420 и 444 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%; и/или аминокислотную последовательность легкой цепи CDR2 (LCDR2), выбранную из группы, состоящей из SEQ ID NO:14, 38, 62, 86, 1 10, 134, 158, 182, 206, 230, 254, 278, 302, 326, 350, 374, 398, 422 и 446 или в значительной степени сходных последовательностей, идентичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%.
Альтернативно, изобретение предоставляет антитело или антигенсвязывающий фрагмент антитела, содержащие комбинацию HCDR1/HCDR2/HCDR3, выбранную из группы, состоящей из SEQ ID NO: 4/6/8, 28/30/32, 52/54/56, 76/78/80, 100/102/104, 124/126/128, 148/150/152, 172/174/176, 196/198/200, 220/222/224, 244/246/248, 268/270/272, 292/294/296, 316/318/320, 340/342/344, 364/366/368, 388/390/392, 412/414/416, 436/438/440 и 460/462/464; и/или комбинацию LCDR1/LCDR2/LCDR3, выбранную из группы, состоящей из SEQ ID NO:12/14/16, 36/38/40, 60/62/64, 84/86/88, 108/110/112, 132/134/136, 156/158/160, 180/182/184, 204/206/208, 228/230/232, 252/254/256, 276/278/280, 300/302/304, 324/326/328, 348/350/352, 372/374/376, 396/398/400, 420/422/424 и 444/446/448.
В одном из вариантов осуществления HCDR1, HCDR2 и HCDR3 выбраны из группы, состоящей из SEQ ID NO:28/30/32, 76/78/80, 124/126/128, и 148/150/152; и/или LCDR1, LCDR2 и LCDR3 выбраны из группы, состоящей из SEQ ID NO:36/38/40, 84/86/88, 132/134/136 и 156/158/160. В еще одном варианте осуществления аминокислотные последовательности тяжелой и легкой цепи CDR содержат комбинацию последовательностей CDR, выбранную из группы, состоящей из SEQ ID NO:28/30/32/36/38/40, 76/78/80/84/86/88, 124/126/128/132/134/136 и 148/150/152/156/158/160. В еще одном варианте осуществления антитело или его антигенсвязывающий фрагмент содержат последовательности CDR тяжелой и легкой цепи SEQ ID NO: 28/30/32/36/38/40 или 76/78/80/84/86/88.
В связанном варианте осуществления изобретение содержит антитело или антигенсвязывающий фрагмент антитела, которые специфически связываются с hANGPTL4, где антитело или его фрагмент содержат домены CDR тяжелой и легкой цепи, содержащиеся в паре HCVR/LCVR, выбранной из группы, состоящей из SEQ ID NO:2/10, 18/20, 22/24, 26/34, 42/44, 487/44, 46/48, 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 98/106, 114/116, 118/120, 122/130, 138/140, 142/144, 146/154, 162/164, 166/168, 170/178, 186/188, 190/192, 194/202, 210/212, 214/216, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 266/274, 282/284, 286/288, 290/298, 306/308, 310/312, 314/322, 330/332, 334/336, 338/346, 354/356, 358/360, 362/370, 378/380, 382/384, 386/394, 402/404, 406/408, 410/418, 426/428, 430/432, 434/442, 450/452, 454/456, 458/394, 466/404 и 468/408. Способы и техника обнаружения CDR в аминокислотных последовательностях HCVR и LCVR известны в данной области, и их можно применять для обнаружения CDR в определенных аминокислотных последовательностях HCVR и/или LCVR, описываемых в настоящем документе. Общепринятые определения, которые можно применять для определения границ CDR, включают определение по Kabat, определение по Chothia и определение AbM. Вкратце, определение по Kabat основано на вариабельности последовательности, определение по Chothia основано на определении местоположения структурных петлевых участков, а определение AbM совмещает подходы по Kabat и по Chothia. См., например, Kabat, "Sequences of Proteins of Immunological Interest", National Institutes of Health, Bethesda, Md. (1991); Al-Lazikani et al., J. Mol. Biol. 273:927-948 (1997); и Martin et al., Proc. Natl. Acad. Sci. USA 86:9268-9272 (1989). Также для обнаружения последовательностей CDR в антителе можно использовать общедоступные базы данных. В одном из вариантов осуществления антитело или его фрагмент содержат последовательности CDR, содержащиеся в паре HCVR и LCVR, выбранной из группы, состоящей из пар аминокислотных последовательностей SEQ ID NO:26/34, 42/44, 487/44, 46/48, 74/82, 90/92, 94/96, 122/130, 138/140, 142/144, 146/154, 162/164 и 166/168. В другом варианте осуществления антитело или его фрагмент содержат последовательности CDR, содержащиеся в паре последовательностей HCVR и LCVR SEQ ID NO:42/44, 487/44, 90/92, 138/140 или 162/164.
В другом связанном варианте осуществления изобретение относится к антителу или его антигенсвязывающему фрагменту, которые конкурируют за специфическое связывание с hANGPTL4 с антителом или антигенсвязывающим фрагментом, содержащим последовательности CDR тяжелой и легкой цепи SEQ ID NO:28/30/32/36/38/40, 76/78/80/84/86/88, 124/126/128/132/134/136, или 148/150/152/156/158/160. В одном из вариантов осуществления антитело или антигенсвязывающий фрагмент по изобретению конкурирует за специфическое связывание с hANGPTL4 с антителом, содержащим пару последовательностей HCVR/LCVR SEQ ID NO:42/44, 487/44, 90/92, 138/140 или 162/164.
В другом связанном варианте осуществления изобретение относится к антителу или его антигенсвязывающему фрагменту, связывающим тот же эпитоп на hANGPTL4, который распознается антителом или его фрагментом, содержащим последовательности CDR тяжелой и легкой цепи SEQ ID NO:28/30/32/36/38/40, 76/78/80/84/86/88, 124/126/128/132/134/136 или 148/150/152/156/158/160. В одном из вариантов осуществления антитело или антигенсвязывающий фрагмент по изобретению распознают эпитоп на hANGPTL4, который распознается антителом, содержащим пару последовательностей HCVR/LCVR SEQ ID NO:42/44, 487/44, 90/92, 138/140 или 162/164.
В третьем аспекте изобретение относится к молекулам нуклеиновой кислоты, кодирующим антитела против ANGPTL4 или их фрагменты, в частности, описанные выше. Рекомбинантные векторы экспрессии, несущие нуклеиновые кислоты по изобретению, и клетки-хозяева, например, бактериальные клетки, такие как E. coli, или клетки млекопитающих, такие как клетки CHO, в которые встраивают такие векторы, также включены в изобретение, наряду со способами получения антител посредством культивирования клеток-хозяев в условиях, обеспечивающих получение антител и извлечение полученных антител.
В одном из вариантов осуществления изобретение относится к антителу или его фрагменту, содержащим HCVR, кодируемую нуклеиновой кислотой с последовательностью, выбранной из группы, состоящей из SEQ ID NO:1, 17, 21, 25, 41, 45, 49, 65, 69, 73, 89, 93, 97, 113, 117, 121, 137, 141, 145, 161, 165, 169, 185, 189, 193, 209, 213, 217, 233, 237, 241, 257, 261, 265, 281, 285, 289, 305, 309, 313, 329, 333, 337, 353, 357, 361, 377, 381, 385, 401, 405, 409, 425, 429, 433, 449, 453, 457, 465, 467 и 486 или в значительной степени сходных последовательностей, гомологичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%. В другом варианте осуществления антитело или его фрагмент содержат HCVR, кодируемую нуклеиновой кислотой с последовательностью, выбранной из группы, состоящей из SEQ ID NO:25, 41, 45, 73, 89, 93, 121, 137, 141, 145, 161, 165 и 486. В еще одном варианте осуществления антитело или его фрагмент содержат HCVR, кодируемую нуклеиновой кислотой с последовательностью SEQ ID NO: 41, 89, 137, 161 или 486.
В одном из вариантов осуществления антитело или его антигенсвязывающий фрагмент содержат LCVR, кодируемую нуклеиновой кислотой с последовательностью, выбранной из группы, состоящей из SEQ ID NO:9, 19, 23, 33, 43, 47, 57, 67, 71, 81, 91, 95, 105, 115, 119, 129, 139, 143, 153, 163, 167, 177, 187, 191, 201, 211, 215, 225, 235, 239, 249, 259, 263, 273, 283, 287, 297, 307, 311, 321, 331, 335, 345, 355, 359, 369, 379, 383, 393, 403, 407, 417, 427, 431, 441, 451 и 455 или в значительной степени сходных последовательностей, гомологичных по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%. В другом варианте осуществления антитело или его фрагмент содержат LCVR, кодируемую нуклеиновой кислотой с последовательностью, выбранной из группы, состоящей из SEQ ID NO:33, 43, 47, 81, 91, 95, 129, 139, 143, 153, 163 и 167. В еще одном варианте осуществления антитело или его фрагмент содержат LCVR, кодируемую нуклеиновой кислотой с последовательностью SEQ ID NO: 43, 91, 139 или 163.
В дополнительных вариантах осуществления антитело или его фрагмент содержат пару последовательностей HCVR и LCVR (HCVR/LCVR), кодируемую парой нуклеиновых кислот с последовательностями, выбранными из группы, состоящей из SEQ ID NO: 1/9, 17/19, 21/23, 25/33, 41/43, 486/43, 45/47, 49/57, 65/67, 69/71, 73/81, 89/91, 93/95, 97/105, 113/115, 117/119, 121/129, 137/139, 141/143, 145/153, 161/163, 165/167, 169/177, 185/187, 189/191, 193/201, 209/211, 213/215, 217/225, 233/235, 237/239, 241/249, 257/259, 261/263, 265/273, 281/283, 285/287, 289/297, 305/307, 309/311, 313/321, 329/331, 333/335, 337/345, 353/355, 357/359, 361/369, 377/379, 381/383, 385/393, 401/403, 405/407, 409/417, 425/427, 429/431, 433/441, 449/451, 453/455, 457/393, 465/403 и 467/407. В одном из вариантов осуществления антитело или его фрагмент содержат пару последовательностей HCVR/LCVR, кодируемую парой нуклеиновых кислот с последовательностями, выбранными из группы, состоящей из SEQ ID NO:25/33, 41/43, 486/43, 45/47, 73/81, 89/91, 93/95, 121/129, 137/139, 141/143, 145/153, 161/163 и 165/167. В еще одном варианте осуществления антитело или его фрагмент содержат пару HCVR/LCVR, кодируемую парой нуклеиновых кислот с последовательностями SEQ ID NO:41/43, 486/43, 89/91, 137/139 или 161/163.
В одном из вариантов осуществления изобретение относится к антителу или антигенсвязывающему фрагменту антитела, содержащим домен HCDR3, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из SEQ ID NO:7, 31, 55, 79, 103, 127, 151, 175, 199, 223, 247, 271, 295, 319, 343, 367, 391, 415, 439 и 463 или в значительной степени сходными последовательностями, гомологичными по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%; и домен LCDR3, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из SEQ ID NO:15, 39, 63, 87, 111, 135, 159, 183, 207, 231, 255, 279, 303, 327, 351, 375, 399, 423 и 447 или в значительной степени сходными последовательностями, гомологичными по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%. В другом варианте осуществления антитело или его фрагмент содержат пару последовательностей HCDR3 и LCDR3, кодируемых парой нуклеиновых кислот с последовательностями SEQ ID NO:31/39, 79/87, 127/135 или 151/159. В еще одном варианте осуществления антитело или его фрагмент содержат пару последовательностей HCDR3 и LCDR3, кодируемых парой нуклеиновых кислот с последовательностями SEQ ID NO:31/39 или 79/87.
В дополнительном варианте осуществления антитело или его фрагмент дополнительно содержат домен HCDR1, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из SEQ ID NO:3, 27, 51, 75, 99, 123, 147, 171, 195, 219, 243, 267, 291, 315, 339, 363, 387, 411, 435 и 459 или в значительной степени сходными последовательностями, гомологичными по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%; и домен HCDR2, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из SEQ ID NO:5, 29, 53, 77, 101, 125, 149, 173, 197, 221, 245, 269, 293, 317, 341, 365, 389, 413, 437 и 461 или в значительной степени сходными последовательностями, гомологичными по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%; и необязательно дополнительно содержит домен LCDR1, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из SEQ ID NO:11, 35, 59, 83, 107, 131, 155, 179, 203, 227, 251, 275, 299, 323, 347, 371, 395, 419 и 443 или в значительной степени сходными последовательностями, гомологичными по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%; и/или домен LCDR2, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из SEQ ID NO:13, 37, 61, 85, 109, 133, 157, 181, 205, 229, 253, 277, 301, 325, 349, 373, 397, 421 и 445 или в значительной степени сходными последовательностями, гомологичными, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99%.
Альтернативно, изобретение относится к антителу или антигенсвязывающему фрагменту антитела, содержащим комбинацию HCDR1/HCDR2/HCDR3, кодируемую комбинацией нуклеотидных последовательностей, выбранной из группы, состоящей из SEQ ID NO:3/5/7, 27/29/31, 51/53/55, 75/77/79, 99/101/103, 123/125/127, 147/149/151, 171/173/175, 195/197/199, 219/221/223, 243/245/247, 267/269/271, 291/293/295, 315/317/319, 339/341/343, 363/365/367, 387/389/391, 411/413/415, 435/437/439 и 459/461/463; и/или комбинацию LCDR1/LCDR2/LCDR3, кодируемую комбинацией нуклеотидных последовательностей, выбранной из группы, состоящей из SEQ ID NO:11/13/15, 35/37/39, 59/61/63, 83/85/87, 107/109/111, 131/133/135, 155/157/159, 179/181/183, 203/205/207, 227/229/231, 251/253/255, 275/277/279, 299/301/303, 323/325/327, 347/349/351, 371/373/375, 395/397/399, 419/421/423 и 443/445/447.
В одном из вариантов осуществления HCDR1, HCDR2 и HCDR3 кодируются комбинацией нуклеотидных последовательностей, выбранной из группы, состоящей из SEQ ID NO:27/29/31, 75/77/79, 123/125/127 и 147/149/151; и/или LCDR1, LCDR2 и LCDR3 кодируются комбинацией нуклеотидных последовательностей, выбранной из группы, состоящей из SEQ ID NO:35/37/39, 83/85/87, 131/133/135, и 155/157/159. В еще одном варианте осуществления антитело или его фрагмент содержат последовательности CDR тяжелой и легкой цепи, кодируемые комбинацией нуклеотидных последовательностей, выбранной из группы, состоящей из SEQ ID NO: 27/29/31/35/37/39; 75/77/79/83/85/87; 123/125/127/131/133/135; и 147/149/151/155/157/159. В другом варианте осуществления антитело или его антигенсвязывающий участок содержат последовательности CDR тяжелой и легкой цепи, кодируемые комбинацией нуклеотидных последовательностей SEQ ID NO: 27/29/31/35/37/39; или 75/77/79/83/85/87.
Четвертый аспект изобретение относится к выделенному антителу или антигенсвязывающему фрагменту антитела, которые специфически связываются с hANGPTL4 и содержат HCDR3 и LCDR3, где HCDR3 содержит аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18-X19-X20 (SEQ ID NO:471), где X1 представляет собой Ala, X2 представляет собой Arg или Lys, X3 представляет собой Gly или Glu, X4 представляет собой Gly, Asp или пропуск, X5 представляет собой Asp или пропуск, X6 представляет собой Leu, Arg или пропуск, X7 представляет собой Arg или Ser, X8 представляет собой Phe, Gly или Arg, X9 представляет собой Leu, His или Asn, X10 представляет собой Asp, Pro или Tyr, X11 представляет собой Trp, Tyr или Phe, X12 представляет собой Leu, Phe, Val или Asp, X13 представляет собой Ser, Tyr или Gly, X14 представляет собой Ser, Tyr или Asp, X15 представляет собой Tyr, X16 представляет собой Phe или Gly, X17 представляет собой Leu или пропуск, X18 представляет собой Asp, X19 представляет собой Tyr, Val или Phe и X20 представляет собой Trp; и LCDR3 содержит аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8-X9-X10 (SEQ ID NO:474), где X1 представляет собой Gln, X2 представляет собой Asn или Gln, X3 представляет собой Tyr или Leu, X4 представляет собой Asn, His, Ser или Asp, X5 представляет собой Thr или Ser, X6 представляет собой Ala или Tyr, X7 представляет собой Pro, Ser или Phe, X8 представляет собой Leu или Arg, X9 представляет собой Thr и X10 представляет собой Phe.
В дополнительном варианте осуществления антитело или его фрагмент дополнительно содержит последовательность HCDR1, содержащую аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8 (SEQ ID NO:469), где X1 представляет собой Gly, X2 представляет собой Gly или Phe, X3 представляет собой Ser или Thr, X4 представляет собой Phe, X5 представляет собой Ser, X6 представляет собой Ile, Ser или Thr, X7 представляет собой His или Tyr и X8 представляет собой His, Gly или Asp; последовательность HCDR2, содержащую аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8 (SEQ ID NO:470), где X1 представляет собой Ile, X2 представляет собой Asn, Ser или Gly, X3 представляет собой His, Phe, Ser или Val, X4 представляет собой Arg, Asp или Ala, X5 представляет собой Gly, X6 представляет собой Gly или пропуск, X7 представляет собой Ser, Asn или Asp и X8 представляет собой Thr или Lys; последовательность LCDR1, содержащую аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6 (SEQ ID NO:472), где X1 представляет собой Gln, X2 представляет собой Gly или Ser, X3 представляет собой Ile, X4 представляет собой Ser или Asn, X5 представляет собой Asp, Ser или Arg и X6 представляет собой Tyr или Trp; и последовательность LCDR2, содержащую аминокислотную последовательность формулы X1-X2-X3 (SEQ ID NO:473), где X1 представляет собой Ala или Lys, X2 представляет собой Ala и X3 представляет собой Ser. Выравнивания последовательностей моноклональных антител H1H268P, H1H284P, H1H291P и H1H292P показаны на фиг. 1 (HCVR) и фиг. 2 (LCVR).
В пятом аспекте изобретение относится к антителу человека против ANGPTL4 или его антигенсвязывающему фрагменту, содержащим вариабельную область тяжелой цепи (HCVR), кодируемую сегментами нуклеотидной последовательности, полученными из последовательностей зародышевых линий VH, DH и JH, и вариабельную область легкой цепи (LCVR), кодируемую сегментами нуклеотидной последовательности, полученными из последовательностей зародышевых линий VK и JK, где HCVR и LCVR кодируются сегментами нуклеотидной последовательности, полученными из комбинаций генов зародышевых линий, выбранных из группы, состоящей из: (i) VH3-30, DH5-12, JH6, VK1-9 и JK4; (ii) VH4-34, DH3-3, JH4, VK1-27 и JK4; и (iii) VH3-13, DH1-26, JH4, VK1-5 и JK1.
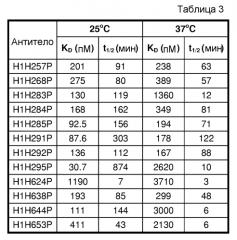
В шестом аспекте изобретение относится к антителу или его антигенсвязывающему фрагменту, которые специфически связываются с hANGPTL4 с константой диссоциации (KD), составляющей приблизительно 1 нМ или менее, как показано посредством поверхностного плазмонного резонанса (например, BIACORE™). В определенных вариантах осуществления антитело по изобретению характеризуется KD, составляющей приблизительно 500 пМ или менее; приблизительно 400 пМ или менее; приблизительно 300 пМ или менее; приблизительно 200 пМ или менее; приблизительно 150 пМ или менее; приблизительно 100 пМ или менее; или приблизительно 50 пМ или менее.
В седьмом аспекте настоящее изобретение относится к антителу против hANGPTL4 или его антигенсвязывающему фрагменту, которые связывают белок hANGPTL4 SEQ ID NO:476, но не проявляют перекрестной реактивности в отношении родственного белка, такого как ангиопоэтин-подобный белок 3 человека (hANGPTL3; SEQ ID NO:485), как показано, например, посредством ELISA, поверхностного плазмонного резонанса или способа LUMINEX® XMAP®, как описано в настоящем документе. ANGPTL3 представляет собой другой секретируемый белок, который, как показано, сокращает активность LPL и содержит N-концевой суперспиральный участок и C-концевой фибриноген-подобный домен (Ono et al., 2003, J Biol Chem 43:41804-41809). В связанных вариантах осуществления изобретение относится к антителу против hANGPTL4 или его антигенсвязывающему фрагменту, которые связывают белок hANGPTL4 и проявляют перекрестную реактивность в отношении белка hANGPTL3. В определенных вариантах осуществления аффинность связывания антитела hANGPTL4 или его фрагмента с белком hANGPTL3 составляет приблизительно 75% или менее, или приблизительно 50% или менее от аффинности связывания антитела или его фрагмента с белком hANGPTL4. В другом связанном варианте осуществления изобретение относится к антителу против hANGPTL4 или его антигенсвязывающему фрагменту, которые не проявляют перекрестной реактивности в отношении ANGPTL4 мыши (mANGPTL4: SEQ ID NO:478), но проявляют перекрестную реактивность в отношении ANGPTL4 яванского макака (Macaca fascicularis; аминокислотная последовательность N-концевых 1-148 остатков и последовательности кодирующих ДНК показаны в SEQ ID NO:490 и 489, соответственно) и/или ANGPTL4 макака-резуса (Macaca mulatta; аминокислотная последовательность N-концевых 1-148 остатков и последовательности кодирующих ДНК показаны в SEQ ID NO:492 и 491, соответственно).
Настоящее изобретение относится к антителам против hANGPTL4, характеризующимся модифицированным паттерном гликозилирования. В некоторых областях применения модификацию можно применять для удаления нежелательных участков гликозилирования, или например, для удаления составной группы фукозы для усиления антитело-зависимой клеточной цитотоксичности (ADCC) (см. Shield et al. (2002) JBC 277:26733). В других областях применения удаление N-участка гликозилирования может уменьшать нежелательный иммунный ответ на терапевтические антитела или повышать аффинность антител. В других областях применения можно применять модификацию галактозилирования для модифицирования обусловленной комплементом цитотоксичности (CDC).
В восьмом аспекте изобретение относится к фармацевтической композиции, содержащей рекомбинантное антитело человека или его фрагмент, которые специфически связываются с hANGPTL4, и фармацевтически приемлемый носитель. В одном из вариантов осуществления изобретение относится к композиции, которая представляет собой комбинацию антитела или его антигенсвязывающего фрагмента по изобретению и второго терапевтического средства. Второе терапевтическое средство может представлять собой одно или несколько из таких средств как (1) ингибиторы 3-гидрокси-3-метилглутарил-кофермент A (HMG-CoA) редуктазы, такие как церивастатин, аторвастатин, симвастатин, питавастатин, розувастатин, флувастатин, ловастатин, правастатин и т.п.; (2) ингибиторы захвата холестерина и/или повторного всасывания желчной кислоты; (3) ниацин, который усиливает катаболизм липопротеинов; (4) фибраты или амфипатические карбоновые кислоты, которые снижают уровень липопротеинов низкой плотности (LDL), увеличивают уровень липопротеинов высокой плотности (HDL) и TG и снижают частоту возникновения несмертельного инфаркта миокарда; и (5) активаторы фактора транскрипции LXR, участвующего в разрушении холестерина, такие как 22-гидроксихолестерол, или фиксированные комбинации, такие как эзетимиб плюс симвастатин; статин с секвестрантами желчных кислот (например, холестирамин, колестипол, колесевелам), фиксированная комбинация ниацин плюс статин (например, ниацин с ловастатином); или с другими гиполипидемическими средствами, такими как сложные эфиры омега-3-жирных кислот (например, омакор). Кроме того, второе терапевтическое средство может представлять собой один или несколько других ингибиторов ANGPTL4, а также ингибиторы других молекул, таких как ANGPTL3, ANGPTL5, ANGPTL6 и пропротеинконвертаза субтилизин/кексин типа 9 (PCSK9), которые вовлечены в метаболизм липидов, в частности, в гомеостаз холестерина и/или триглицеридов. Ингибиторы этих молекул включают низкомолекулярные соединения и антитела, которые специфически связываются с этими молекулами и блокируют их активность.
В связанных вариантах осуществления второе терапевтическое средство может представлять собой одно или несколько противоопухолевых средств, таких как химиотерапевтические средства, антиангиогенные средства, ингибирующие рост средства, цитотоксические средства, апоптозные средства и другие средства, хорошо известные в данной области как средства для лечения злокачественной опухоли или других пролиферативных заболеваний или нарушений, а также другие терапевтические средства, такие как анальгетики, противовоспалительные средства, включая нестероидные противовоспалительные лекарственные средства (NSAIDS), такие как ингибиторы Cox-2 и т.п., позволяющие облегчить и/или сократить симптомы, сопутствующие злокачественной опухоли.
В девятом аспекте изобретение предоставляет способы ингибирования активности hANGPTL4 с применением антитела к hANGPTL4 или антигенсвязывающего участка антитела по изобретению, где терапевтические способы включают введение терапевтически эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент антитела по изобретению и необязательно одно или несколько дополнительных терапевтических средств, описанных выше. Заболевание или нарушение, подлежащее лечению, представляет собой любое заболевание или состояние, которое можно облегчить, ослабить, ингибировать или предотвратить или сократить частоту возникновения по сравнению с отсутствием лечения с применением антитела к hANGPTL4 (например, ANGPTL4-обусловленные заболевания или нарушения), посредством ингибирования или снижения активности ANGPTL4. Примеры заболеваний или нарушений, которые можно лечить способами по изобретению, в качестве неограничивающих примеров включают заболевания и нарушения, затрагивающие метаболизм липидов, такие как гиперлипидемия, гиперлипопротеинемия и дислипидемия, включая атерогенную дислипидемию, диабетическую дислипидемию, гипертриглицеридемию, включая тяжелую гипертриглицеридемию с TG > 1000 мг/дл, гиперхолестеринемию, хиломикронемию, смешанную дислипидемию (ожирение, метаболический синдром, диабет и т.д.), липодистрофию, липоатрофию и т.п., которые вызываются, например, сниженной активностью LPL и/или дефицитом LPL, сниженной активностью рецепторов LDL и/или дефицитом рецепторов LDL, нарушениями ApoC2, дефицитом ApoE, повышенным ApoB, повышенным выделением и/или сниженным разрушением липопротеинов с очень низкой плотностью (VLDL), воздействием определенного лекарственного средства (например, дислипидемия, вызванная лечением глюкокортикоидами), любой генетической предрасположенностью, питанием, образом жизни и т.п. Способы по изобретению также могут предотвращать или лечить заболевания или нарушения, связанные с или вызванные гиперлипидемией, гиперлипопротеинемией и/или дислипидемией, включая в качестве неограничивающих примеров сердечно-сосудистые заболевания или нарушения, такие как атеросклероз, аневризмы, гипертензия, ангина, инсульт, цереброваскулярная болезнь, застойная сердечная недостаточность, ишемическая болезнь сердца, инфаркт миокарда, заболевания периферических сосудов и т.п.; острый панкреатит; неалкогольный стеатогепатит (NASH); нарушения, связанные с содержанием сахара в крови, такие как диабет; ожирение и т.п.
Другие примеры заболеваний или нарушений, которые можно лечить способами по изобретению, включают злокачественную опухоль, а также не неопластические ангиогенез-связанные заболевания или нарушения, включая глазные ангиогенные заболевания или нарушения, такие как связанная с возрастом дегенерация желтого пятна, окклюзия центральной вены сетчатки или окклюзия ветки вены сетчатки, диабетическая ретинопатия, ретинопатия недоношенных и т.п., воспалительные заболевания или нарушения, такие как артрит, ревматоидный артрит (RA), псориаз и т.п.
Другие варианты осуществления предоставлены в приведенном ниже подробном описании.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На фиг. 1 представлено выравнивание последовательностей вариабельных областей тяжелой цепи (HCVR) антител H1H268P, H1H284P, H1H291P и H1H292P.
На фиг. 2 представлено выравнивание последовательностей вариабельных областей легкой цепи (LCVR) антител H1H268P, H1H284P, H1H291P и H1H292P.
На фиг. 3A и 3B показан фармакокинетический клиренс антител против ANGPTL4 у мышей дикого типа (фиг. 3A) и у трансгенных мышей, экспрессирующих ANGPTL4 человека [мыши hAngptl4(+/+); или "гуманизированные ANGPTL4 мыши"] (фиг. 3B). H4H268P2 (□); H4H284P (▲); и контрольные hIgG4 (●).
На фиг. 4 показано воздействие антител против ANGPTL4, H4H268P2, на сывороточный уровень триглицеридов (TG) у гуманизированных ANGPTL4 мышей, скрещенных с нулевыми по ApoE мыши. Показан процент (%) изменений сывороточного уровня TG, вызванных H4H268P2, по сравнению с контрольным антителом с неподходящей специфичностью. Контрольные Ab (○); и H4H268P2 (■).
На фиг. 5 показано воздействие антитела против ANGPTL4 H4H268P2 и снижающего уровень TG лекарственного средства фенофибрат, как по отдельности, так и в комбинации, на сывороточный уровень TG у гуманизированных ANGPTL4 мышей.
На фиг. 6 представлены результаты этапа I пилотного исследования воздействия антител против ANGPTL4 на снижение сывороточного уровня TG, а также других липидов, у страдающих ожирением макак-резусов (Macaca mulatta). Все обезьяны получали носитель (10 мМ гистидин, pH 6) внутривенным вливанием на сутки -5 и либо H4H268P2 (n=3) (●), либо H4H284P (n=3) (□) в дозе 10 мг/кг внутривенно на сутки 0. Образцы сыворотки собирали, начиная с исходного периода по сутки 35 после лечения. Средние исходные уровни для каждого животного определяли на основе образцов, собранных на сутки -7, -5 и 0, и для каждой группы Ab определяли и усредняли процент (%) изменений сывороточных уровней TG по сравнению с исходными значениями.
На фиг. 7 представлены результаты этапа II пилотного исследования воздействия антитела против ANGPTL4 H4H268P2 на снижение сывороточного уровня TG у страдающих ожирением обезьян, как описано для фиг. 6, за исключением того, что этап введения носителя не проводили. Для каждой обезьяны получали средние исходные уровни на основе образцов, собранных на сутки -7, -3 и 0. Обезьян разделяли на группы на основе их исходных уровней: A. TG<150 мг/дл (n=3;□); B. 150 мг/дл<TG<500 мг/дл (n=4; ●); и C. TG>1000 мг/дл (n=1; ∇). Процент (%) изменений уровней TG после голодания по сравнению с исходными значениями определяли для каждой обезьяны и усредняли для каждой группы.
Величины ошибок во всех графах представлены в виде средних значений ± SEM.
ПОДРОБНОЕ ОПИСАНИЕ
Прежде, чем настоящее изобретение будет детально описано, следует понимать, что это изобретение не ограничено конкретными описанными способами и экспериментальными условиями, поскольку эти способы и условия могут варьировать. Также следует понимать, что терминология, применяемая в настоящем документе, предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения, поскольку объем настоящего изобретения ограничен только приложенной формулой изобретения.
Если не определено иначе, все технические и научные термины, применяемые в настоящем документе, имеют те же значения, что и традиционно применяемые специалистами в данной области, к которой относится это изобретение. Хотя в практическом осуществлении или исследованиях по настоящему изобретению можно использовать любые способы и материалы, сходные или эквивалентные описываемым в настоящем документе, описаны предпочтительные способы и материалы.
Определения
Как используют в настоящем документе, термин "ангиопоэтин-подобный белок 4 человека" или "hANGPTL4" относится к hANGPTL4 с последовательностью нуклеиновой кислоты SEQ ID NO:475 и аминокислотной последовательностью SEQ ID NO:476 или его биологически активному фрагменту.
Как используют в настоящем документе, термин "антитело", предназначен для обозначения молекул иммуноглобулина, состоящих из четырех полипептидных цепей, двух тяжелых (H) цепей и двух легких (L) цепей, связанных дисульфидными связями. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (HCVR) и константной области тяжелой цепи (CH; состоит из доменов CH1, CH2 и CH3). Каждая легкая цепь состоит из вариабельной области легкой цепи (LCVR) и константной области легкой цепи (CL). HCVR и LCVR могут дале