Анксиолитическое средство и фармацевтическая композиция анксиолитического действия
Иллюстрации
Показать всеГруппа изобретений относится к медицине, в частности к разработке и применению нового анксиолитического средства. Предложены применение гексапептида Thr-Gly-Glu-Asn-His-Arg-NH2 в качестве анксиолитического средства и новый состав анксиолитического средства, содержащий активное вещество в виде указанного гексапептида (2-10 г/л), консервант в виде нипагина (0,95-1,05 г/л), хлорид натрия (10,0 г/л) и вода дистиллированная - остальное. Состав высокоэффективен в низких дозах и прост в применении: используется в виде капель в нос. Предлагаемая фармацевтическая композиция может найти применение в клинической практике для коррекции психических и неврологических расстройств. Противотревожный эффект препарата сопоставим, а по некоторым показателям и превосходит аналогичный эффект препаратов сравнения - диазепама (500 мкг/кг) и гептапептида селанка (300 мкг/кг). 2 н.п. ф-лы, 7 ил., 1 табл., 2 пр.
Реферат
Изобретение относится к медицине, в частности к разработке и применению нового анксиолитического средства. Предложено применение гексапептида Thr-Gly-Glu-Asn-His-Arg-NH2 в качестве анксиолитического средства. Предложен новый состав анксиолитического средства, содержащий: активное вещество в виде указанного гексапептида (2-10 г/л), консервант в виде нипагина (0,95-1,05 г/л), хлорид натрия (10,0 г/л) и вода дистиллированная - остальное. Состав высокоэффективен в низких дозах и прост в применении: используется в виде капель в нос. Предлагаемая фармацевтическая композиция может найти применение в клинической практике для коррекции психических и неврологических расстройств.
Изобретение относится к медицине, а именно к разработке и применению нового анксиолитического средства. Может быть использовано для лечения направленного на повышение мотивационной устойчивости и адекватного адаптивного поведения при психиатрических и неврологических заболеваниях для коррекции страха, тревоги, составляющих патогенетическую основу многих психоэмоциональных расстройств для повышения адаптационных возможностей здорового человека в экстремальных ситуациях.
Актуальность разработки препарата определяется возрастанием стрессовых ситуаций в современной жизни, связанных с техногенными и природными катастрофами, ухудшающейся экологической обстановкой, нестабильностью экономической обстановки в современном обществе и недостаточностью в современной медицине анксиолитиков, не обладающих побочными эффектами.
Известны в качестве анксиолитиков различные транквилизаторы, преимущественно бенздиазепинового ряда, нашедшие широкое применение в клинической практике. Однако они характеризуются большим числом побочных эффектов: седация, миорелаксация, гипно-седативное, снотворное действие, нарушение обучения, феномен отмены и другие.
Новым направлением в области создания эффективных и безопасных лекарственных средств для адекватного купирования страха, тревоги является создание анксиолитиков на основе эндогенных регуляторных пептидов, высокоэффективных и обладающих низкой токсичностью. Известен гексапептид общей формулы (Thr-Gly-Glu-Asn-His-Arg-NH2) в качестве нейропротекторного и ноотропного средства, направленного на профилактику и лечение болезни Альцгеймера и ишемического инсульта (заявка на патент Российской Федерации №2014130894. «Пептид, обладающий нейропротекторной и ноотропной активностью, и фармацевтическая композиция на его основе», приоритет от 25.07.2014). Однако возможность использовать его в качестве лекарственного препарата анксиолитического действия неизвестна. Техническим результатом, достигаемым при реализации изобретения, является обнаружение у известного пептида Thr-Gly-Glu-Asn-His-Arg-NH2, обладающего нейропротекторной и ноотропной активностью, анксиолитической активностью, что определяет возможность его использования в низких дозах в качестве анксиолитического средства в виде удобной для применения лекарственной формы без нежелательных побочных эффектов, характерных для транквилизаторов, с хорошей переносимостью.
Выраженность анксиолитического действия этого нового лекарственного препарата в дозах 100-300 мкг/кг более сопоставима с действием диазепама (0.5 мг/кг), феназепама (0.1 мг/кг), альпразолама (0.2 мг/кг) - любой из которых можно рассматривать в качестве прототипа предлагаемого нового лекарственного препарата. Однако в отличие от вышеперечисленных транквилизаторов, которые рассматриваются в качестве прототипа, увеличение дозы нового лекарственного препарата в 200-500 раз в различных тестах не сопровождается развитием нежелательных побочных эффектов.
Вышеописанный технический результат достигается тем, что известный гексапептид общей формулы: Thr-Gly-Glu-Asn-His-Arg-NH2, применяется в качестве анксиолитического средства.
В лекарственном составе анксиолитического средства, содержащего активное вещество, хлорид натрия и дистиллированную воду, в качестве активного вещества содержится гексапептид Thr-Gly-Glu-Asn-His-Arg-NH2, хлорид натрия и дополнительно консервирующее вещество нипагин при следующем соотношении компонентов, г/л:
| Гексапептид Thr-Gly-Glu-Asn-His-Arg-NH2 | 2-10 |
| Нипагин - 0,95 | 1,05 |
| Хлорид натрия | 10 |
| Вода дистиллированная | Остальное |
Лекарственной форме присвоено название Анксилит.
Предложенный в качестве анксиолитического средства гексапептид Thr-Gly-Glu-Asn-His-Arg-NH2 известен как стимулятор памяти и нейропротектор. Проведенные исследования на различных видах животных показали, что у интактных животных в условиях центрального и системного введения Thr-Gly-Glu-Asn-His-Arg-NH2 наблюдается улучшение формирования и сохранения долговременной памяти. Эти свойства отличают фармакологическое действие гексапептида от фармакологического действия транквилизаторов, обладающих в качестве побочного действия седативным эффектом и снижением когнитивных функций.
Пример 1. Изучение влияния субхронического системного введения пептида Thr-Gly-Glu-Asn-His-Arg-NH2 на поведение мышей линий BALB/c неинвазивным методом в тестах «крестообразный лабиринт».
В опытах на мышах была использована модифицированная методика приподнятого крестообразного лабиринта (ПКЛ). Установка ПКЛ для мышей представляет собой две взаимопересекающиеся под прямым углом горизонтальные дорожки 45×5 см. Два противоположных отсека имеют непрозрачные вертикальные стенки высотой 30 см. Лабиринт приподнят от пола на 40 см. В месте перекрестья плоскостей находится открытая центральная платформа 5×5 см. Методика ПКЛ основана на врожденном страхе открытого пространства и высоты у грызунов. Сущность метода заключается в анализе соотношения реакции страха животных в незнакомом пространстве и высоты, с одной стороны, и поисковой активности в новой обстановке, с другой. В соответствии с характеристиками для лабораторных мышей и крыс формами поведения реакция страха определяется стремлением животных находиться в закрытых рукавах лабиринта, снижением двигательной активности. Поисковая активность определяется пребыванием животных в открытых рукавах, увеличением двигательной активности. Для исследования предполагаемого анксиолитического эффекта гексапептида Thr-Gly-Glu-Asn-His-Arg-NH2 эксперименты проводили на инбредных мышах линии BALB/c, характеризующихся повышенным врожденным уровнем тревожности.
Эксперимент проводили в условиях дневного освещения. В начале тестирования животное помещали в центр лабиринта, головой к открытому рукаву. Фиксировали следующие показатели поведения в ПКЛ в течение 300 с: время нахождения в открытых рукавах; время нахождения в закрытых рукавах; время нахождения на центральной площадке; число заходов в открытые рукава; число заходов в закрытые рукава; число свешиваний с открытых рукавов ПКЛ. В качестве базового критерия анксиолитического действия использовали показатель времени, проведенного в открытых рукавах установки. Число пересечений центральной платформы (сумма заходов в темный и светлый рукава лабиринта) использовали для оценки влияния соединений на двигательную активность мышей. Каждая группа состояла из 16 мышей. Все препараты вводили ежедневно в течение 5 суток. Раствор пептида Thr-Gly-Glu-Asn-His-Arg-NH2 применяли интраназально в дозах 100 и 300 мкг/кг/день. В качестве препаратов сравнения были выбраны бензодиазепиновый транквилизатор диазепам (0,5 мг/кг/день, внутрибрюшинно), а также препарат пептидной структуры селанк (0,3 мг/кг/день, интраназально).
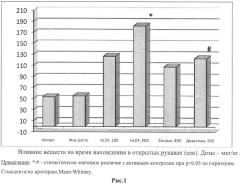
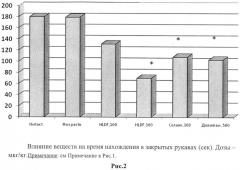
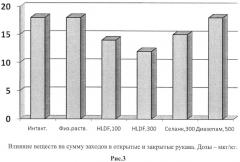
Установлено, что уже в дозе 100 мкг/кг амидная форма гексапептида Thr-Gly-Glu-Asn-His-Arg-NH2 увеличивала время пребывания мышей в открытых рукавах ПКЛ до 233% относительно группы активного контроля (физраствор). В этой дозе анксиолитическая активность Thr-Gly-Glu-Asn-His-Arg-NH2 была сравнима с аналогичным эффектом для препаратов сравнения - диазепама и селанка, введенным в значительно большей дозе (Рис. 1). Увеличение дозы гексапептида Thr-Gly-Glu-Asn-His-Arg-NH2 до 300 мкг/кг сопровождалось существенным возрастанием времени нахождения, более чем в 3 раза (Рис. 1), что свидетельствует о высоком противотревожном эффекте гексапептида. Соответственно этому происходило уменьшение времени нахождения мышей в закрытых рукавах лабиринта (Рис. 2). При этом значимых признаков изменения двигательной активности у животных под влиянием препаратов не отмечалось (Рис. 3). Также был проведен анализ влияния пептида Thr-Gly-Glu-Asn-His-Arg-NH2 и препаратов сравнения на латентный период первого захода (Рис. 4) и время нахождения на центральной площадке (Рис. 5). Дополнительным подтверждением наличия у дозы 300 мг/кг гексапептида противотревожной (анксиолитической) активности является сопоставимое с селанком и диазепамом увеличение количества свешиваний с открытых рукавов (Рис. 6). Для всех исследованных экспериментов было показано, что в дозе 300 мкг/кг/день исследуемый препарат превосходит анксиолитический эффект препаратов сравнения - диазепама (500 мкг/кг) и гептапептида Селанк (300 мкг/кг). При этом значимых признаков изменения двигательной активности у животных под влиянием пептида Thr-Gly-Glu-Asn-His-Arg-NH2 не отмечалось.
Пример 2. Изучение влияния хронического системного введения пептида Thr-Gly-Glu-Asn-His-Arg-NH2, на поведение мышей линий BALB/c в тесте «открытое поле»
Для исследования анксиолитической активности пептида Thr-Gly-Glu-Asn-His-Arg-NH2 в тесте «открытое поле» были использованы мыши-самцы линии Balb/c, полученные из питомника РАН «Пущино» и содержавшиеся в условиях вивария при температуре 20-22°С, световом режиме 12/12 (свет с 7 до 19 часов), пищевом и питьевом режиме adlibitum. После 2 недель акклиматизации к условиям вивария животные были разбиты на 5 групп по 15 в каждой. Первая группа мышей оставалась интактной, мышам второй группы интраназально (и/н) вводили физраствор (ф/р) в объеме 8 мкл, следующие 2 группы получали и/н пептид в дозировке 0.3 и 1.6 мг/кг в том же объеме ф/р, животным последней группы пептид в дозировке 0.3 мг/кг вводили внутрибрюшинно (в/б) в 200 мкл ф/р. Препараты вводили в течение 4 недель ежедневно 5 дней в неделю. В конце 1-й, 2-й и 3-й недели по 5 животных из каждой группы через 30 мин после инъекций тестировали в системе «открытое поле».
«Открытое поле» представляет собой ярко освещенную круглую площадку диаметром 1 м, которая ограничена высокими бортами и разлинована концентрическими окружностями и центральными лучами на сегменты. Периферическими сегментами считаются те, которые находятся около бортов установки, остальные - центральные. Переход животного в новый сегмент засчитывался в том случае, когда оно всеми 4 лапами пересекало его границы. Животных помещали в один из периферических сегментов, засекали время нахождения его в первом сегменте (латентный период), затем в течение 5 мин тестировали количество посещенных периферических и центральных сегментов, количество стоек, а также количество болюсов и уринаций.
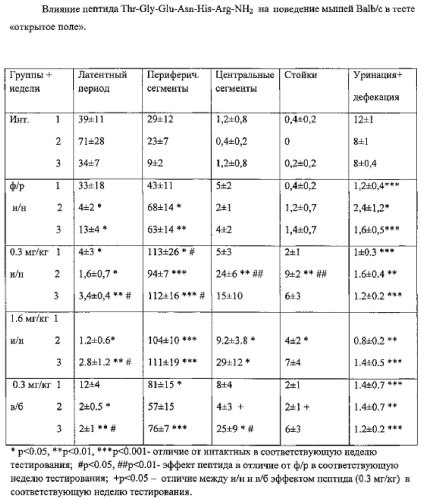
Мыши линии Balb/c характеризуются высокой тревожностью. Это выражается в относительно продолжительном латентном периоде при их попадании в новую обстановку, низкой периферической активности, практическом отсутствии выходов в центральные сегменты и стоек, а также повышенном количестве дефекаций и уринаций (соматическая реакция на эмоциональный стресс). Именно такое поведение было характерно для интактных животных на всех 3 неделях тестирования (таблица). На этом фоне процедурные воздействия, сопровождающие и/н введение ф/р, существенно снижают тревожность мышей. На первой неделе это сказывается на достоверном снижении числа дефекаций и уринаций (таблица). При 2-м и 3-м тестировании к этому добавляется снижение латентного периода замирания мышей при попадании в «открытое поле» и увеличении их двигательной активности в периферических сегментах.
Тестирование мышей линии Balb/c в «открытом поле» показало, что хроническое введение исследуемого пептида в дозе, эквивалентной человеческой терапевтической, оказывает анксиолитическое действие. Фармакологически значимый эффект развивается в течение 2-3 недель. Выход животных в центральные сегменты «открытого поля» может рассматриваться как снижение их тревожности, так и как повышение поисковой активности, т.е. увеличение когнитивных функций. По этому параметру достоверный эффект пептида обнаружен после 2 недель и/н введения (р<0.01) и после 3 недель в/б инъекций (р<0.05) (таблица, рис. 6). Причем фармакологическое действие пептида более выражено и наступает быстрее при интраназальном, чем при внутрибрюшинном введении, о чем свидетельствует достоверное (р<0.05) отличие центральной активности мышей, получавших одну и ту же дозу пептида этими двумя способами в течение 3 недель (рис. 7). Результаты исследования в тесте «открытое поле» свидетельствуют о том, что хроническое введение тестируемого препарата на основе пептида Thr-Gly-Glu-Asn-His-Arg-NH2 не вызывает изменений во внутренних органах мышей Balb/c в дозе, эквивалентной человеческой терапевтической, с учетом пересчета для данного вида животных и пятикратной терапевтической дозе.
Таким образом, результаты теста «приподнятый крестообразный лабиринт» и «открытое поле» свидетельствуют, что амидная форма гексапептида Thr-Gly-Glu-Asn-His-Arg-NH2 обладает анксиолитическими свойствами, наиболее выраженными в дозе 300 мкг/кг/день. При этом противотревожный эффект препарата сопоставим, а по некоторым показателям и превосходит, аналогичный эффект препаратов сравнения - диазепама (500 мкг/кг) и гептапептида селанка (300 мкг/кг). Обнаружение дополнительного вида психотропной активности делает гексапептид Thr-Gly-Glu-Asn-His-Arg-NH2 перспективным в плане внедрения в клиническую практику для коррекции психических и неврологических расстройств.
1. Применение гексапептида Thr-Gly-Glu-Asn-His-Arg-NH2 в качестве анксиолитического средства.
2. Фармацевтическая композиция анксиолитического действия, содержащая активное вещество и дистиллированную воду, отличающаяся тем, что в качестве активного вещества содержит гептапептид формулы Thr-Gly-Glu-Asn-His-Arg-NH2, хлорид натрия и дополнительно консервирующее вещество нипагин при следующих соотношениях компонентов, г/л:
| Гексапептид указанной формулы | 2-10 |
| Нипагин | 0,95-1,05 |
| Хлорид натрия | 10,0 |
| Дистиллированная вода | Остальное |