Стабильные композиции антигенов neisseria meningitidis rlp2086
Иллюстрации
Показать всеГруппа изобретений относится к стабильным композициям антигенов подсемейства B Neisseria meningitidis rLP2086, а также к способам стабилизации эффективности полипептида подсемейства В LP2086 (fHBP) в составе иммуногенной композиции. Группа изобретений раскрывает иммуногенную композицию, содержащую полисорбат 80 и полипептид подсемейства В LP2086 (fHBP) в молярном соотношении полисорбат 80:белок менее 10:1 и дополнительно содержащую полипептид подсемейства A LP2086 (fHBP) и алюминий, где более 95% полипептида подсемейства В связано с алюминием и где композиция не является лиофилизированной и имеет pH 6,5 или менее, и способы стабилизации эффективности полипептида в ее составе. При использовании группы изобретений достигается длительная стабильность. 3 н. и 74 з.п. ф-лы, 29 ил., 5 табл., 8 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композициям антигенов подсемейства B Neisseria meningitidis rLP2086 в иммуногенных композициях, которые описаны в данном документе. Настоящее изобретение также относится к способам сохранения конформации антигенов Neisseria meningitidis rLP2086 и к способам определения эффективности антигенов Neisseria meningitidis rLP2086.
Предшествующий уровень техники
rLP2086 представляет собой рекомбинантный липопротеин 28 кДа, который индуцирует перекрестно-реагирующие бактериальные антитела против целого ряда штаммов Neisseria meningitidis. На основе установленной гомологии аминокислотных последовательностей были идентифицированы два разных подсемейства rLP2086, A и B. Эти два подсемейства были использованы в приготовлении образцов вакцины MnB-rLP2086, содержащих 20, 60, 120 и 200 мкг/мл, каждые в 10 мМ гистидине (pH 6,0), 150 мМ NaCl и 0,5 мг/мл алюминия с варьирующими уровнями Полисорбата 80 (PS-80). Полисорбат 80, также известный как TWEEN 80, является неионным поверхностно-активным веществом и эмульгатором, получаемым из сорбита, и его часто используют в фармацевтических композициях в качестве эмульгатора, солюбилизатора и стабилизатора. Полагают, что присутствие Полисорбата 80 в иммуногенной композиции MnB rLP2086 предотвращает агрегацию в процессе приготовления, обработки, фильтрации, заполнения и транспортировки, снижает адсорбцию на мембране фильтра и снижает адсорбцию в трубопроводах.
Краткое изложение сущности изобретения
В некоторых воплощениях настоящего изобретения предложена стабильная иммуногенная композиция, где эффективность полипептида подсемейства B LP2086 сохраняется в течение по меньшей мере примерно 1-12 месяцев, примерно 6-18 месяцев, примерно 12-24 месяцев, примерно 24-36 месяцев или примерно 36-48 месяцев. В некоторых воплощениях иммуногенная композиция дополнительно содержит полипептид подсемейства ALP2086.
В некоторых воплощениях иммуногенная композиция дополнительно содержит детергент. В некоторых воплощениях молярное отношение детергент:белок составляет от примерно 0,5:1 до примерно 10:1; от примерно 1:1 до примерно 5:1; или от примерно 1,4:1 до 4,2:1. В некоторых воплощениях молярное отношение детергент:белок составляет примерно 2,8:1. В некоторых воплощениях количество детергента является достаточным для снижения связывания полипептида с кремнием в контейнере, таком как шприц или флакон. В некоторых воплощениях детергент представляет собой неионный детергент, такой как полисорбатный детергент. В некоторых воплощениях детергент представляет собой Полисорбат 80.
В некоторых воплощениях иммуногенная композиция дополнительно содержит многовалентный катион. В некоторых воплощениях многовалентным катионом является кальций или алюминий. В некоторых воплощениях иммуногенная композиция содержит фосфат кальция. В некоторых воплощениях иммуногенная композиция содержит алюминий в виде фосфата алюминия, гидроксида алюминия, сульфата алюминия или квасцов. В некоторых воплощениях концентрация алюминия составляет от примерно 0,1 мг/мл до 1,0 мг/мл. В некоторых воплощениях концентрация алюминия составляет примерно 0,5 мг/мл.
В некоторых воплощениях иммуногенная композиция дополнительно содержит гистидин. В некоторых воплощениях концентрация гистидина составляет от примерно 2 мМ до примерно 20 мМ или от примерно 5 мМ до примерно 15 мМ. В некоторых воплощениях концентрация гистидина составляет примерно 10 мМ. В некоторых воплощениях pH гистидина составляет от примерно 5,0 до примерно 8,0 или от примерно 5,8 до примерно 6,0. В некоторых воплощениях концентрация гистидина составляет 10 мМ, pH 6,0.
В некоторых воплощениях иммуногенная композиция дополнительно содержит сукцинат. В некоторых воплощениях концентрация сукцината составляет от примерно 2 мМ до примерно 10 мМ или от примерно 3 мМ до примерно 7 мМ. В некоторых воплощениях концентрация сукцината составляет примерно 5 мМ. В некоторых воплощениях pH сукцината составляет от примерно 5,0 до примерно 8,0 или от примерно 5,8 до примерно 6,0. В некоторых воплощениях концентрация сукцината составляет 5 мМ, pH 6,0.
В некоторых воплощениях иммуногенная композиция является лиофилизированной. В некоторых воплощениях лиофилизированная композиция ресуспендирована в буфере, содержащем алюминий. В некоторых воплощениях алюминий присутствует в виде фосфата алюминия, гидроксида алюминия, сульфата алюминия или квасцов.
В некоторых воплощениях иммуногенная композиция содержит Полисорбат 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 10 мМ гистидина pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства B LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 10 мМ гистидина pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства A rLP2086 (fHBP), 200 мкг/мл полипептида подсемейства B LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 10 мМ гистидина pH 6,0 и 150 мМ NaCl.
В некоторых воплощениях иммуногенная композиция содержит Полисорбат 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 5 мМ сукцината pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства В LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 5 мМ сукцината pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства A rLP2086 (fHBP), 200 мкг/мл полипептида подсемейства B LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 5 мМ сукцината pH 6,0 и 150 мМ NaCl.
В другом аспекте изобретения предложен способ стабилизации эффективности полипептида подсемейства В LP2086 в иммуногенной композиции путем хранения полипептида подсемейства В LP2086 в буфере с молярным отношением детергент:белок от примерно 0,5:1 до 10:1; от примерно 1:1 и примерно 5:1; или от примерно 1,4:1 до примерно 4,2:1. В некоторых воплощениях молярное отношение детергент:белок составляет примерно 2,8:1. В некоторых воплощениях количество детергента является достаточным для снижения связывания полипептида с кремнием в контейнере, таком как шприц или флакон. В некоторых воплощениях детергент представляет собой неионный детергент, такой как полисорбатный детергент. В некоторых воплощениях детергент представляет собой Полисорбат-80.
В некоторых воплощениях буфер дополнительно содержит многовалентный катион. В некоторых воплощениях многовалентным катионом является кальций или алюминий. В некоторых воплощениях буфер содержит фосфат кальция. В некоторых воплощениях буфер содержит алюминий в виде фосфата алюминия, гидроксида алюминия, сульфата алюминия или квасцов. В некоторых воплощениях концентрация алюминия составляет от примерно 0,1 мг/мл до 1,0 мг/мл. В некоторых воплощениях концентрация алюминия составляет примерно 0,5 мг/мл.
В некоторых воплощениях буфер дополнительно содержит гистидин. В некоторых воплощениях концентрация гистидина составляет от примерно 2 мМ до примерно 20 мМ или от примерно 5 мМ до примерно 15 мМ. В некоторых воплощениях концентрация гистидина составляет примерно 10 мМ. В некоторых воплощениях рН гистидина составляет от примерно 5,0 до примерно 8,0 или от примерно 5,8 до примерно 6,0. В некоторых воплощениях концентрация гистидина составляет 10 мМ, pH 6,0.
В некоторых воплощениях буфер дополнительно содержит сукцинат. В некоторых воплощениях концентрация сукцината составляет от примерно 2 мМ до примерно 10 мМ или от примерно 3 мМ до примерно 7 мМ. В некоторых воплощениях концентрация сукцината составляет примерно 5 мМ. В некоторых воплощениях pH сукцината составляет от примерно 5,0 до примерно 8,0 или от примерно 5,8 до примерно 6,0. В некоторых воплощениях концентрация сукцината составляет 10 мМ, pH 6,0.
В некоторых воплощениях иммуногенная композиция является лиофилизированной. В некоторых воплощениях лиофилизированная композиция ресуспендирована в буфере, содержащем алюминий. В некоторых воплощениях алюминий присутствует в виде фосфата алюминия, гидроксида алюминия, сульфата алюминия или квасцов.
В некоторых воплощениях буфер по существу состоит из Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 10 мМ гистидина pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства B LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 10 мМ гистидина pH 6,0 и 150 мМ NaCl.
В некоторых воплощениях буфер по существу состоит из Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 5 мМ сукцината pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства B LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 5 мМ сукцината pH 6,0 и 150 мМ NaCl.
В другом аспекте изобретения предложен способ стабилизации эффективности полипептида подсемейства A LP2086 и полипептида подсемейства B LP2086 в иммуногенной композиции путем хранения полипептида подсемейства A LP2086 и полипептида подсемейства В LP2086 в буфере с алюминием в количестве от примерно 0,1 мг/мл до примерно 10 мг/мл и с молярным отношением детергент:белок от примерно 0,5:1 до 10:1. В некоторых воплощениях молярное отношение детергент:белок составляет от примерно 1:1 до примерно 5:1 или от примерно 1,4:1 до примерно 4,2:1. В некоторых воплощениях молярное отношение детергент:белок составляет примерно 2,8:1. В некоторых воплощениях количество детергента является достаточным для снижения связывания полипептида с кремнием в контейнере, таком как шприц или флакон. В некоторых воплощениях детергент представляет собой неионный детергент, такой как полисорбатный детергент. В некоторых воплощениях детергент представляет собой Полисорбат 80.
В некоторых воплощениях алюминий присутствует в виде фосфата алюминия, гидроксида алюминия, сульфата алюминия или квасцов. В некоторых воплощениях концентрация алюминия составляет примерно 0,5 мг/мл.
В некоторых воплощениях буфер дополнительно содержит гистидин. В некоторых воплощениях концентрация гистидина составляет от примерно 2 мМ до примерно 20 мМ или от примерно 5 мМ до примерно 15 мМ. В некоторых воплощениях концентрация гистидина составляет примерно 10 мМ. В некоторых воплощениях рН гистидина составляет от примерно 5,0 до примерно 8,0 или от примерно 5,8 до примерно 6,0. В некоторых воплощениях концентрация гистидина составляет 10 мМ, pH 6,0.
В некоторых воплощениях буфер дополнительно содержит сукцинат. В некоторых воплощениях концентрация сукцината составляет от примерно 2 мМ до примерно 10 мМ или от примерно 3 мМ до примерно 7 мМ. В некоторых воплощениях концентрация сукцината составляет примерно 5 мМ. В некоторых воплощениях pH сукцината составляет от примерно 5,0 до примерно 8,0 или от примерно 5,8 до примерно 6,0. В некоторых воплощениях концентрация сукцината составляет 10 мМ, pH 6,0.
В некоторых воплощениях иммуногенная композиция является лиофилизированной. В некоторых воплощениях лиофилизированная композиция ресуспендирована в буфере, содержащем алюминий. В некоторых воплощениях алюминий присутствует в виде фосфата алюминия, гидроксида алюминия, сульфата алюминия или квасцов.
В некоторых воплощениях буфер по существу состоит из Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 10 мМ гистидина pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства A LP2086 (fHBP), 200 мкг/мл полипептида подсемейства B LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 10 мМ гистидина pH 6,0 и 150 мМ NaCl.
В некоторых воплощениях буфер по существу состоит из Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 5 мМ сукцината pH 6,0 и 150 мМ NaCl. В некоторых воплощениях иммуногенная композиция по существу состоит из 200 мкг/мл полипептида подсемейства A LP2086 (fHBP), 200 мкг/мл полипептида подсемейства B LP2086 (fHBP), Полисорбата 80 в молярном отношении к белку примерно 2,8:1, 0,5 мг/мл алюминия в виде AlPO4, 5 мМ сукцината pH 6,0 и 150 мМ NaCl.
В другом аспекте изобретения предложен способ определения эффективности полипептида подсемейства A rLP2086 и/или полипептида подсемейства B rLP2086, включающий следующие стадии: (а) связывание первого и второго функционального моноклонального антитела, распознающего конформационные эпитопы на белке каждого подсемейства с иммуногенной композицией, и (б) количественное определение связывания антитела с полипептидами. В некоторых воплощениях количественное определение осуществляют электрохемилюминисценцией. В некоторых воплощениях определяют количество полипептидов, презентирующих эпитопы, распознаваемые обоими антителами. В некоторых воплощениях первое антитело конъюгировано с меткой, такой как биотин. В некоторых воплощениях первое антитело выделяют соединением, которое связывает конъюгированную метку, таким как стрептавидиновые гранулы или стрептавидиновая колонка. В некоторых воплощениях второе антитело связывают количественной меткой. В некоторых воплощениях эффективность иммуногенной композиции сравнивают с эффективностью эталонного вещества.
Краткое описание графических материалов
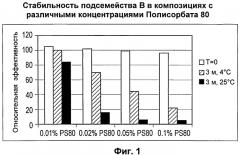
Фиг.1: Стабильность подсемейства B в композициях с различными концентрациями Полисорбата 80.
200 мкг/мл каждого из подсемейств A и В готовили в 10 мМ гистидиновом буфере при pH 6,3 с 0,5 мг/мл алюминия и различными концентрациями Полисорбата 80. Композиции заполняли в BD шприцы и хранили при 2-8°C или 25°C. Показаны значения эффективности для подсемейства В в начальной точке времени и в точке времени 3 месяца.
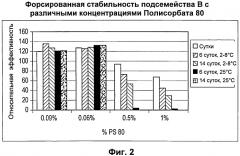
Фиг.2: Форсированная стабильность подсемейства B с различными концентрациями Полисорбата 80.
Лекарственное вещество на основе подсемейства B, приготовленное в виде композиции с 0,09% Полисорбата 80, 10 мМ гистидина, pH 6,5, разводили Полисорбатом 80, варьируя его концентрацию, для оценки влияния Полисорбата 80 на стабильность. Образцы хранили при 2-8°C или 25°C, и эффективность оценивали в начальной точке времени, в точке времени 6 суток и в точке времени 14 суток.
Фиг.3: Эффективность подсемейства B при 200 мкг/мл в течение 28 суток.
Подсемейства A+B MnB rLP2086 готовили в дозировке 200 мкг/мл каждого с 0,5 мг/мл алюминия в виде фосфата алюминия в присутствии различных концентраций Полисорбата 80 (A=0%, B=0,02%, C=0,005% и D=0,01%) и хранили либо при 2-8°C, либо при 25°C. Молярные соотношения Полисорбат 80 : белок A, B, C и D равны 0, 1,1, 2,7 и 5,3 соответственно. Эффективность белка подсемейства B затем тестировали в точках времени 0, 7, 14 и 28 суток. В каждой точке времени перед тестированием образцы перемешивали в течение 24 часов.
Фиг.4: Эффективность подсемейства B при 20 мкг/мл в течение 28 суток.
Подсемейства A+B MnB rLP2086 готовили в дозировке 20 мкг/мл каждого с 0,5 мг/мл алюминия в виде фосфата алюминия в присутствии различных концентраций Полисорбата 80 (A=0%, B=0,0005% и C=0,001%) и хранили либо при 2-8°C, либо при 25°C. Молярные соотношения Полисорбат 80 : белок A, B и C равны 0, 2,7 и 5,3 соответственно. Эффективность белка подсемейства B затем тестировали в точках времени 0, 7, 14 и 28 суток. В каждой точке времени перед тестированием образцы перемешивали в течение 24 часов.
Фиг.5: Результаты по эффективности для 200 мкг/мл с разными молярными отношениями.
Подсемейства A+B MnB rLP2086 готовили в дозировке 200 мкг/мл с молярными отношениями Полисорбат 80 : белок 1,4, 2,3, 3,4, 3,9, 4,3, 4,7, 10,7 для партий 50A, 50B, 50C, 50D, 50E, 50F, 50G, соответственно. T-0, T-10 и T-20 означают точки времени 0, 10 и 20 суток, соответственно. На верхней диаграмме представлены результаты по эффективности для подсемейства A, а на нижней диаграмме представлены результаты по эффективности для подсемейства B. В каждой точке времени перед тестированием образцы перемешивали в течение 24 часов.
Фиг.6: Результаты по эффективности для 20 мкг/мл с разными молярными отношениями.
Подсемейства A+B MnB rLP2086 готовили в дозировке 20 мкг/мл с молярными отношениями Полисорбат 80 : белок 1,4, 2,3, 3,4, 3,9, 4,3, 4,7, 10,7 для партий 53A, 53B, 53C, 53D, 53E, 53F, 53G, соответственно. T-0, T-10 и T-20 означают точки времени 0, 10 и 20 суток, соответственно. На верхней диаграмме представлены результаты по эффективности для подсемейства A, а на нижней диаграмме представлены результаты по эффективности для подсемейства B. В каждой точке времени перед тестированием образцы перемешивали в течение 24 часов.
Фиг.7: Связывание белка с фосфатом алюминия при pH 6,5.
Подсемейства A+В MnB rLP2086 готовили в дозировке 400 мкг/мл в 10 мМ гистидиновом буфере с 150 мМ NaCl и концентрацией Полисорбата 80 0,02% при pH 6,5. Ось X отображает содержание алюминия в композиции, а ось Y отображает процент связанного белка, измеренный анализом методом IEX HPLC.
Фиг.8: Связывание подсемейств A и B MnB rLP2086 в зависимости от pH.
Композиции подсемейств А+В MnB в дозировке белков подсемейств A и В 200 мкг/мл каждого готовили с 0,5 мг/мл алюминия в виде фосфата алюминия в 10 мМ гистидиновом буфере с 150 мМ NaCl при разных pH. Множество партий представляют собой композиции, приготовленные с различными партиями DS (лекарственное вещество), как показано на Фиг.8.
Фиг.9: Влияние pH, буфера и концентрации белка на связывание подсемейств A и B rLP2086.
Одиннадцать композиций подсемейств A+B MnB с белками подсемейств A+B были приготовлены в дозировке 200 мкг/мл каждого с 0,5 мг/мл алюминия в виде фосфата алюминия в 10 мМ гистидиновом буфере с 150 мМ NaCl и 0,02% PS-80 при разных pH (F1-F3 каждая с 200 мкг/мл белка и 0,02% Полисорбата 80); с разными концентрациями Полисорбата 80 от 0,01% до 0,005% (F4-F5); с разной белковой концентрацией до 250 мкг/мл для каждого белка подсемейства (F6-F8); с разными концентрациями гистидинового буфера: 5 мМ и 20 мМ (F9 и F10); с добавлением 10 мМ MgCl2 (F11).
F1: pH 6,0; F2: pH 5,8; F3: pH 5,6; F4: pH 6,0, 0,01% PS 80; F5: pH 6,0, 0,005% PS 80; F6: pH 6,0, 0,25 мг белка; F7: pH 5,8, 0,25 мг белка; F8: pH 5,6, 0,25 мг белка; F9: pH 6,0, 5 мМ His; F10: pH 6,0, 20 мМ His; F11: pH 6,0, 10 мМ MgCl2; общее: 10 мМ His, 0,15 М NaCl, 0,5 мг/мл Al, 0,2 мг белка, 0,02% PS80.
Фиг.10: Внешний вид композиций rLP2086 без фосфата алюминия.
Фотография двух композиций белков A+B rLP2086 в дозировке 200 (слева) и 20 (справа) мкг/мл без фосфата алюминия с различными концентрациями Полисорбата 80, выраженными в процентах, указанными сверху (1=0%, 2=0,002%, 3=0,005%, 4=0,01%, 5=0%, 6=0,0005%, 7=0,001%). Все пробирки инкубировали при 5°C в течение 14 суток и перемешивали в течение 2 часов перед тестированием. Вода и стандарт мутности 50 NTU (нефелометрические единицы мутности) включены на каждом конце для визуального сравнения; вода показывает прозрачность, а 50 NTU показывает внешний вид мутного раствора. Примечание: аналогичные результаты были также получены после инкубирования в течение 1, 7 и 28 суток.
Фиг.11: Измерения OD (оптическая плотность) образцов внешнего вида, 2-8°C.
Измерения оптической плотности образцов, приготовленных без фосфата алюминия при λ=320 нм для композиций rLP2086 200 мкг/мл, обозначение 15С (0,005% Полисорбата 80), в течение одного месяца при 5°C. Перемешанные образцы указаны красными квадратиками, а образцы без перемешивания указаны синими ромбиками.
Фиг.12: Результаты по эффективности для подсемейства A для композиций с и без AlPO4.
Подсемейства A+B MnB rLP2086, приготовленные в дозировке 200 мкг/мл каждого подсемейства. Композиции были приготовлены в гистидин-забуференном физиологическом растворе с и без AlPO4 и с разными уровнями Полисорбата 80. На верхней диаграмме представлены композиции без AlPO4, а на нижней диаграмме представлены композиции с 0,5 мг/мл алюминия в виде фосфата алюминия. Четыре группы в левой половине диаграммы представляют собой образцы без перемешивания, а остальные четыре группы на правой половине представляют собой образцы с перемешиванием, как отмечено на каждой диаграмме внизу по оси X. Ось Y отображает относительную эффективность в процентах. Концентрации Полисорбата в конечных композициях следующие: 0%, 0,0005%, 0,001% и 0,01% для партии 15A или 13A, 15B или 13B, 15C или 13С и 15D или 13D, соответственно. Образцы хранили при 2-8°C и 25°C. T-0, T-7 с, T-14 с и Т-28 с означают ноль, 7, 14 и 28 суток. Каждый столбик отображает данные для каждой точки времени.
Фиг.13: Результаты по эффективности для подсемейства B для композиций с и без AlPO4.
Подсемейства A+B MnB rLP2086, приготовленные в дозировке 200 мкг/мл каждого подсемейства. Композиции были приготовлены в гистидин-забуференном физиологическом растворе с и без AlPO4 и с разными уровнями Полисорбата 80. На верхней диаграмме представлены композиции без AlPO4, а на нижней диаграмме представлены композиции с 0,5 мг/мл алюминия в виде фосфата алюминия. Четыре группы в левой половине диаграммы представляют собой образцы без перемешивания, а остальные четыре группы на правой половине представляют собой образцы с перемешиванием, как отмечено на каждой диаграмме внизу по оси X. Ось Y отображает относительную эффективность в процентах. Концентрации Полисорбата в конечных композициях следующие: 0%, 0,0005%, 0,001% и 0,01% для партии 15A или 13A, 15B или 13B, 15C или 13C и 15D или 13D, соответственно. Образцы хранили при 2-8°C и 25°C. T-0, T-7 с, T-14 с и T-28 с означают ноль, 7, 14 и 28 суток. Каждый столбик отображает данные для каждой точки времени.
Фиг.14: Результаты по Полисорбату 80 в rLP2086 Плацебо с 0,5 мг/мл алюминия.
Фиг.15: Результаты по Полисорбату 80 для подсемейства A.
Фиг.16: Результаты по Полисорбату 80 для подсемейства B.
Фиг.17: Корреляция эффективности и связанного молярного отношения для подсемейства B.
Фиг.18: Результаты по молярному отношению для подсемейства A.
Фиг.19: Результаты по молярному отношению для подсемейства B.
Фиг.20: Результаты по молярному отношению для композиций rLP2086 приблизительно 400 мкг/мл.
Фиг.21: Результаты по Полисорбату 80 для лекарственного продукта rLP2086 в разные моменты времени.
Фиг.22: Результаты по связанному молярному отношению для лекарственного продукта rLP2086 в разные моменты времени.
Фиг.23: Результаты по эффективности и связанному молярному отношению для подсемейства A.
Фиг.24: Результаты по эффективности и связанному молярному отношению для подсемейства B.
Фиг.25: Связывание подсемейства A с AlPO4 в сукцинатном и гистидиновом буферах.
Связывание белка подсемейства A из препаратов бивалентных композиций MnB, приготовленных в дозировке 200 мкг/мл каждого белка с 0,5 мг/мл алюминия в виде фосфата алюминия в 10 мМ гистидиновом буфере с 150 мМ NaCl и 0,02% PS-80 при разных pH (F1-F3 каждая с 200 мкг/мл белка и 0,02% PS-80); с разными концентрациями полисорбата PS-80 0,01, 0,05 (F4-F5); с разной белковой концентрацией до 250 мкг/мл (F6-F8); с разными концентрациями гистидинового буфера 5 мМ и 20 мМ (F9 и F10); с добавлением 10 мМ MgCl2 (F11).
Фиг.26: Связывание подсемейства B с AlPO4 в сукцинатном и гистидиновом буферах.
Связывание белка подсемейства B из препаратов бивалентных композиций MnB, приготовленных в дозировке 200 мкг/мл каждого белка с 0,5 мг/мл алюминия в виде фосфата алюминия в 10 мМ гистидиновом буфере с 150 мМ NaCl и 0,02% PS-80 при разных pH (F1-F3 каждая с 200 мкг/мл белка и 0,02% PS-80); с разными концентрациями полисорбата PS-80 0,01, 0,05 (F4-F5); с разной концентрацией белка до 250 мкг/мл (F6-F8); с разными концентрациями гистидинового буфера 5 мМ и 20 мМ (F9 и F10); с добавлением 10 мМ MgCl2 (F11).
Фиг.27: Сравнение связывания в сукцинатном, гистидиновом и фосфатном буфере.
Фиг.28: pH-зависимое связывание подсемейства A с AlPO4.
Фиг.29: pH-зависимое связывание подсемейства B с AlPO4.
Подробное описание изобретения
Если не дано иного определения, все использованные в данном описании технические и научные термины имеют общепринятые значения, понятные специалисту в области техники, к которой относится данное изобретение. Хотя способы и вещества, подобные или эквивалентные способам и веществам, описанным в данном документе, могут быть использованы на практике или при тестировании настоящего изобретения, подходящие способы и вещества описаны ниже. Вещества, способы и примеры являются только иллюстративными и не предназначены для ограничения. Все публикации, патенты и другие документы, упомянутые в данном документе, во всей их полноте включены посредством ссылки.
По всему тексту данного документа слово "содержать" или его варианты, такие как "содержит" или "содержащий", подразумевают включение указанного целого или групп целых, но не исключение никакого другого целого или группы целых.
Определения
Использованные в данном документе формы единственного числа включают определяемые объекты во множественном числе, если контекст четко не диктует иное. Так, например, ссылка на "способ" включает один или более способов и/или стадий описанного здесь типа, и/или которые станут очевидными специалисту в данной области при прочтении этого описания, и тому подобное.
Использованные в данном документе формы множественного числа включают объекты в единственном числе, если контекст четко не диктует иное. Так, например, ссылка на "способы" включает один или более способов и/или стадий описанного здесь типа, и/или которые станут очевидными специалисту в данной области при прочтении этого описания, и т.д.
В данном документе "примерно" означает, что значение параметра находится в пределах статистически значимого диапазона значения, такого как указанный диапазон концентраций, период времени, молекулярная масса, температура или pH. Такой диапазон может быть в пределах порядка величины, обычно в пределах 20%, в более типичных случаях в пределах 10% и даже еще более типично в пределах 5% от данного значения или диапазона. Допустимый разброс, охватываемый термином "примерно", будет зависеть от конкретной исследуемой системы и может быть легко определен специалистом в данной области. В любом месте в данной заявке, где указан диапазон, каждое целое число в этом диапазоне также предусмотрено в качестве воплощения данного изобретения.
Термин "адъювант" относится к соединению или смеси, которое(ая) усиливает иммунный ответ на антиген, как дополнительно описано и проиллюстрировано в данном описании. Не являющиеся ограничивающими примеры адъювантов, которые могут быть использованы в вакцине по настоящему изобретению, включают адъювантную систему RIBI (Ribi Inc., Hamilton, Mont.), квасцы, минеральные гели, такие как гель гидроксида алюминия, эмульсии масло-в-воде, эмульсии вода-в-масле, такие как, например, полный и неполный адъюванты Фрейнда, блок-сополимер (CytRx, Atlanta Ga.), QS-21 (Cambridge Biotech Inc., Cambridge Mass.), SAF-M (Chiron, Emeryville Calif), адъювант AMPHIGEN(R), сапонин, Quil A или другая сапониновая фракция, монофосфориллипид A и липид-аминный адъювант Avridine.
Термин "связывание алюминия с белком" относится к проценту молекул белка в композиции, который связан с алюминием. Связывание алюминия с белком может быть определено с использованием методов, описанных в данном описании, или известных в данной области.
Используемый в данном документе термин "эффективное иммуногенное количество" относится к количеству полипептида или композиции, содержащей полипептид, которое является эффективным в вызывании иммунного ответа у позвоночного носителя. Например, эффективное иммуногенное количество белка rLP2086 по данному изобретению представляет собой количество, которое является эффективным в вызывании иммунного ответа у позвоночного носителя. Конкретная "эффективная иммуногенная дозировка или количество" будет зависеть от возраста, массы тела и медицинского состояния носителя, а также от способа введения. Подходящие дозы без труда смогут определить специалисты в данной области.
Используемый в данном документе термин "молярное отношение" относится к отношению количества молей двух разных компонентов в композиции. В некоторых воплощениях молярное отношение представляет собой отношение молей детергента к молям белка. В некоторых воплощениях молярное отношение представляет собой отношение молей Полисорбата 80 к молям белка. Исходя из концентраций белка и Полисорбата 80, молярное отношение вычисляют, используя следующее уравнение:
Например, композиция, содержащая 0,01% Полисорбата 80 и 200 мкг, имеет молярное отношение детергент:белок 10,8:1 [(0,01/0,2)×216]. Отношение 3 молей Полисорбата 80 к 2 молям белка может быть выражено как молярное отношение PS-80 : белок 3:2. Кроме того, если молярное отношение указано как одно число, то оно относится к отношению этого одного числа к 1. Например, отношения Полисорбат 80 : белок 0,5, 2 и 10 относятся к отношениям 0,5:1, 2:1 и 10:1 соответственно. Используемые в данном документе термины молярное отношение "детергент:белок" и молярное отношение "Полисорбат 80 : белок" относятся в общем к молярному отношению детергента (или Полисорбата 80) к белковым антигенам, в частности антигенам Р2086. На основе сведений, раскрытых в данном описании, специалист в данной области будет способен определить, как вычислить молярные отношения для других детергентов и оптимальное молярное отношение для композиций с другими детергентами. В данном документе "низкое" молярное отношение относится обычно к молярному отношению детергент : белковый антиген в иммуногенной композиции, которое меньше, чем "высокое" молярное отношение. "Высокое" молярное отношение относится обычно к молярному отношению детергент : белковый антиген в иммуногенной композиции, которое больше, чем "низкое" молярное отношение. В некоторых воплощениях "высокое молярное отношение" детергента к белку относится к молярному отношению больше 10:1. В некоторых воплощениях "низкое молярное отношение" детергента к белку относится к молярному отношению от 0,5:1 до 10:1.
Используемый в данном документе термин "ORF2086" относится к открытой рамке считывания 2086 из бактерий вида Neisseria. ORF2086 Neisseria, кодируемые белки из нее, фрагменты этих белков и иммуногенные композиции, содержащие эти белки, известны в данной области и описаны, например, в публикациях патентных заявок США №№ US 20060257413 и US 20090202593, полное содержание каждой из которых включено в данное описание посредством ссылки. Термин "Р2086" обычно относится к белку, кодируемому ORF2086. Белки Р2086 по изобретению могут быть липидированными или нелипидированными. "LP2086" и "Р2086" обычно относятся к липидированной и нелипидированной формам белка 2086 соответственно. Белок Р2086 по изобретению может быть рекомбинантным. "rLP2086" и "rP2086" обычно относятся к липидированной и нелипидированной формам рекомбинантного белка 2086 соответственно.
Используемый в данном документе термин "фармацевтически приемлемый носитель" охватывает любые и все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и задерживающие абсорбцию агенты и т.п., совместимые с введением людям или другим позвоночным хозяевам. Типично, фармацевтически приемлемый носитель представляет собой носитель, использованием которого разрешено регулирующим ведомством Федеральным, правительственным или другим регулирующим ведомством, или указанный в Фармакопее США или другой общепризнанной фармакопее в списке для использования у животных, включая людей, а также млекопитающих, не являющихся людьми. Термин "носитель" относится к разбавителю, адъюванту, эксципиенту или наполнителю, с которым вводят фармацевтическую композицию. Такими фармацевтическими носителями могут быть стерильные жидкости, такие как вода и масла, включая масла нефтяного, животного, растительного или синтетического происхождения. Воду, солевые растворы и водные растворы декстрозы и глицерина можно использовать в качестве жидких носителей, в частности, для инъецируемых растворов. Подходящие фармацевтические эксципиенты включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое снятое молоко, глицерин, пропилен, гликоль, воду, этанол и т.п. Композиция, если желательно, может также содержать небольшие количества увлажняющих, увеличивающих объем, эмульгирующих агентов или pH буферных агентов. Эти композиции могут принимать форму растворов, суспензий, эмульсий, препаратов длительного высвобождения и т.п. Примеры подходящих фармацевтических носителей описаны в "Remington's Pharmaceutical Sciences" by E.W. Martin. Композиция должна соответствовать способу введения. Подходящий носитель будет очевиден специалистам в данной области и будет зависеть от пути введения.
Термин "эффективность" относится к способности антигена вызывать иммунный ответ. В некоторых воплощениях эффективность измеряют способностью эпитопов связываться с антителом. Эффективность может исчезать или снижаться со временем вследствие потери целостности антигена или эпитопа или изменения конформации антигена или эпитопа. Эффективность может исчезать или снижаться под воздействием факторов, включающих, без ограничения, свет, температуру, циклы замораживания/оттаивания, перемешивание и pH. Эффективность может быть измерена способами, раскрытыми в данном описании, и анализами, известными в данной области. Такие анализы для определения эффективности включают, без ограничения, модели вакцинации животных, сывороточные бактерицидные анализы (SBA), проточную цитометрию и анализы эффективности in vitro. Предпочтительными методами определения эффективности являются SBA и анализы эффективности in vitro. Более предпочтительным методом определения эффективности является SBA. В некоторых воплощениях эффективность может быть определена с использованием по меньшей мере одного моноклонального антитела, направленного против по меньшей мере одного эпитопа, который вовлечен в иммунный ответ. В некоторых воплощениях эффективность тестируемого образца сравнивают с эффективностью эталонного образца. В некоторых воплощениях эталонный образец представляет собой тестируемый образец в момент времени T0. В некоторых воплощениях эталонный образец представляет собой иммуногенную композицию без детергента. В некоторых воплощениях эталонный образец представляет собой иммуногенную композицию с молярным отношением детергент:белок выше 10:1.
"Защитный" иммунный ответ относится к способности иммуногенной композиции вызывать иммунный ответ, либо гуморальный, либо клеточно-опосредованный, который служит для защиты субъекта от инфекции. Обеспечиваемая защита не обязательно является абсолютной, т.е. инфекция не обязательно полностью предотвращена или искоренена, когда имеет место статистически значимое улучшение по сравнению с контрольной популяцией субъектов, например инфицированных животных, которым не вводили вакцину или иммуногенную композицию. Защита может ограничиваться уменьшением тяжести симптомов инфекции или быстроты их появления. Как правило, "защитный иммунный ответ" может включать вызывание увеличения уровней антител, специфичных к конкретному антигену, у по меньшей мере 50% субъектов, включая уровень измеряемых функциональных антительных ответов на каждый антиген. В конкретных ситуациях "защитный иммунный ответ" может включать вызывание двукратного увеличения уровней антител или четырехкратного увеличения уровней антител, специфичных конкретному антигену, у по меньшей мере 50% субъектов, включая уровень измеряемых функциональных антительных ответов на каждый антиген. В некоторых воплощениях опсонизирующие антитела коррелируют с защитным иммунным ответом. Так, защитный иммунный ответ можно проанализировать путем измерения снижения процента количества бактерий в анализе опсонофагоцитоза, например как описано ниже. В некоторых воплощениях имеет место снижение количества бактерий по меньшей мере на 10%, 25%, 50%, 65%, 75%, 80%, 85%, 90%, 95% или более по сравнению с количеством бактерий в отсутствие иммуногенной композиции.
Термины "белок", "полипептид" и "пептид" относятся к полимеру из аминокислотных остатков и не ограничены минимальной длиной продукта. Так, пептиды, олигопептиды, димеры, мультимеры и т.п. охвачены данным определением. Как полномерные белки, так и их фрагменты охвачены данным определением. Эти термины также охватывают модификации, такие как делеции, присоединения и замещения (обычно консервативные по характеру, но которые могут быть неконсервативными), нативной последовательности, предпочтительно такие, при которых белок сохраня