Антибактериальное лекарственное средство в форме мази для лечения глазных болезней у животных
Иллюстрации
Показать всеИзобретение относится к области ветеринарной медицины, а именно к офтальмологии, и предназначено для лечения глаз сельскохозяйственных и домашних животных, а также пушных зверей в условиях животноводческих ферм, личных фермерских хозяйств, питомников, ветеринарных клиник и станций по борьбе с болезнями животных. Лекарственное средство в форме мази содержит (в мас.%): азитромицин - 0,5-2,0; нетилмицин - 0,1-0,7; нафазолин - 0,0005-0,05; ланолин безводный - 1,0-70,0; жидкий парафин - 1,0-70,0; вазелин белый - 1,0-70,0; кислоту лимонную - 0,01-5,0; нипагин - 0,05-0,4; нипазол - 0,05-0,4 и воду для инъекций - до 100. Использование изобретения позволяет повысить эффективность и безопасность лечения широкого ряда заболеваний глаз животных. Лекарственное средство не обладает аллергизирующим действием и практически не имеет противопоказаний при применении. 1 з.п. ф-лы, 2 табл., 9 пр.
Реферат
Изобретение относится к области ветеринарной медицины, в частности к офтальмологии, и может быть использовано в ветеринарной практике для лечения глаз сельскохозяйственных и домашних животных, а также пушных зверей в условиях животноводческих ферм, личных фермерских хозяйств, питомников, ветеринарных клиник и станций по борьбе с болезнями животных.
Заболевания глаз инфекционной, реже - неинфекционной этиологии, широко распространены у животных разных видов. Так по данным совместного эпидемиологического анализа, проведенного с 2000 по 2014 год на кафедре незаразных болезней МГУПП, в ветеринарной клинике «Эскулап» и в Глазном центре доктора Шилкина А.Г., животные с воспалительными заболеваниями занимают первое место на амбулаторном офтальмологическом приеме. На их долю приходится до 60% всей глазной патологии. Преимущественным местом локализации глазной инфекции у мелких животных является конъюнктива, а наиболее опасными в плане прогноза и осложнений являются поражения роговицы (септическая язва, инфицированная травма роговицы) и внутренних оболочек глаза (эндофтальмит, панофтальмит). Более 90% всех инфекционных глазных заболеваний вызваны грамположительными и грамотрицательными бактериями, причем в ряде случаев, в ассоциации с хламидиями и микоплазмами. Для лечения таких различных нозологических форм глазных заболеваний у животных на ветеринарном рынке сегодня присутствует крайне малое количество офтальмоантибиотиков. Это левомицетин в составе глазных капель «Барс» и «Лакримин»; гентамицин в составе глазных капель «Ирис» и «Декта-2»; ципрофлоксацин в составе глазных капель «Ципровет».
Однако в последнее время наблюдается тенденция роста резистентности бактерий к применяющимся местно в офтальмологической практике антибактериальным лекарственным препаратам различных групп, в частности, к традиционно используемым аминогликозидам, тетрациклинам и фторхинолонам, что приводит к снижению клинической эффективности данных препаратов.
Так более половины штаммов микроорганизмов (57%), выделяемых при воспалительных заболеваниях глаз у собак и кошек, не чувствительны к левомицетину и около 20% не чувствительны к гентамицину.
К ципрофлоксацину устойчивость пока выражена значительно меньше, но и его клинический эффект также начал снижаться. Особенно отчетливо эта тенденция проявляется у животных с тяжелыми хроническими формами заболеваний. Кроме того, ограниченное количество антибактериальных препаратов для применения в ветеринарной офтальмологии крайне затрудняет лечение животных с непереносимостью или аллергическими реакциями к ципрофлоксацину, гентамицину и левомицетину.
В соответствии с изложенным разработка антибактериальных лекарственных препаратов для местного применения в офтальмологической практике является актуальной задачей.
При оценке действия различных антибиотиков на выделенные от заболевших животных возбудители инфекций, заявителем установлено, что к таким антибиотикам, как нетилмицин и азитромицин, высокочувствительны 66 (49%) из 135 выделенных микрооргнаизмов. Помимо этого, из оставшихся 69 микроорганизмов высоко чувствительными и чувствительными к одному из данных антибиотиков были 63 микроорганизма. Таким образом, комбинация из нетилмицина и азитромицина подавляет 129 (96%) из 135 выделенных микроорганизма.
Учитывая широкий спектр действия и высокую антибактериальную активность нетилмицина и азитромицина, а также выраженное их действие против хламидий и микоплазм, было принято решение создать препарат на основе данных антибиотиков.
Известно использование азитромицина в ветеринарной офтальмологии при хламидийных конъюнктивитах у кошек с эпифорой (см., например, Гречиха А.Ю. «Сравнительная характеристика схем лечения хламидийного конъюнктивита у кошек», автореферат диссертации на соиск. уч. степ. канд. вет. наук, Москва, 2013). Однако азитромицин в данном способе лечения вводят перорально, и автор отмечает, что изолированное применение азитромицина при хламидийном конъюнктивите имеет невысокую эффективность, и поэтому пероральное введение азитромицина в ветеринарной офтальмологии без местного лечения нецелесообразно.
Известен гель для лечения глазных заболеваний бактериальной природы, содержащий азитромицин и вспомогательные компоненты (см., например, Гусов P.M. Разработка состава и технологии офтальмологических капель и геля азитромицина, автореферат диссертации на соискание ученой степени кандидата фармацевтических наук, Пятигорск, 2011).
Данный препарат является наиболее близким заявленному.
Известный препарат обладает высокой эффективностью и широким спектром действия, однако он предназначен для использования в медицинской офтальмологии.
Задачей настоящего изобретения является создание антибактериального офтальмологического лекарственного средства для животных на основе антибиотиков, высокоэффективного против широкого спектра бактериальной флоры, активного в отношении хламидий и микоплазм, обладающего возможностью быстро проникать и накапливаться в тканях глаза, отличающегося низкой токсичностью и отсутствием местных реакций со стороны глаза.
Поставленная задача решается тем, что антибактериальное лекарственное средство в форме мази для лечения глазных болезней у животных, согласно изобретению, содержит (в мас.%): азитромицин - 0,5-2,0; нетилмицин - 0,1-0,7; нафазолин - 0,0005-0,05; ланолин безводный - 1,0-70,0; жидкий парафин - 1,0-70,0; вазелин белый - 1,0-70,0; кислоту лимонную - 0,01-5,0; нипагин - 0,05-0,4; нипазол - 0,05-0,4 и воду для инъекций - до 100.
Также поставленная задача решается и тем, что антибактериальное средство в форме мази для лечения глазных болезней животных может дополнительно содержать в своем составе либо дексаметазон в количестве 0,03-0,5 мас.%, либо преднизолон в количестве - 0,1-1,0 мас.%, либо гидрокортизон в количестве 0,1-1,0 мас.%.
Техническим результатом заявленного изобретения является то, что полученное лекарственное средство обладает высокой антибактериальной активностью широкого спектра действия, эффективно при лечении животных с инфекционно-воспалительными заболеваниями век, конъюнктивы, роговицы и сосудистой оболочки глаза, отличается низкой токсичностью и отсутствием местных реакций со стороны глаза.
Заявленное изобретение иллюстрируется следующими примерами выполнения, которые, однако, не ограничивают объем притязаний заявителя.
Пример 1. Приготовление глазной мази.
В реактор-смеситель загружают расчетное количество жидкого парафина, нагревают и при перемешивании последовательно добавляют навески ланолина безводного, вазелина, нипагина, нипазола, перемешивают до полного расплавления компонентов.
Во вспомогательных емкостях отдельно готовят следующие смеси:
а) в расчетное количество воды для инъекций добавляют навеску нетилмицина, перемешивают до полного растворения (Смесь №1);
б) в расчетное количество воды для инъекций добавляют навеску нафазолина, перемешивают до полного растворения (Смесь №2);
в) в расчетное количество воды для инъекций добавляют навеску кислоты лимонной, перемешивают до полного растворения (Смесь №3);
г) в расчетное количество воды для инъекций добавляют навеску азитромицина, перемешивают, добавляют смесь №3, перемешивают до полного растворения (Смесь №4).
В реактор-смесить при перемешивании и температуре смеси 60°С добавляют смесь №4, перемешивают до однородности, далее последовательно добавляют смеси №1 и №2, перемешивают и эмульгируют.
После окончания перемешивания, отбора проб для анализа и получения положительного заключения, мазь передают на розлив.
Получают глазную мазь следующего состава (в мас.%):
| Азитромицин | 1,5 |
| Нетилмицин | 0,5 |
| Нафазолин | 0,025 |
| Ланолин безводный | 10,0 |
| Жидкий парафин | 18,0 |
| Вазелин белый | 70,0 |
| Кислота лимонная | 2,5 |
| Нипагин | 0,2 |
| Нипазол | 0,2 |
| Вода для инъекций | остальное |
Полученный продукт - мазь мягкой консистенции, однородная, без видимых признаков физической нестабильности, белого цвета с желтоватым оттенком, полупрозрачная.
Пример 2. Мазь глазную получают аналогично примеру 1, но дополнительно в состав мази вводят дексаметазон в количестве 0,3 мас.%.
Пример 3. Мазь глазную получают аналогично примеру 1, но дополнительно вводят в состав мази преднизолон в количестве 0,5 мас.%.
Пример 4. Мазь глазную получают аналогично примеру 1, но дополнительно в состав мази вводят гидрокортизон в количестве 0,5 мас.%.
Пример 5. Обоснование подобранной концентрации комбинации нетилмицина и азитромицина в мази глазной.
Для определения оптимальной терапевтической концентрации комбинации нетилмицина и азитромицина в глазной мази использовали модель экспериментального конъюнктивита на кроликах. В опытах были использованы кролики-альбиносы калифорнийской породы массой 2-2,5 кг и две культуры микроорганизмов: S. intermedius КМ-1К (суспензия с концентрацией 125 млн. микр. клеток) и Е. coli КМ-2D (суспензия 250 млн. микр. клеток), выделенные из клинического материала.
Каждую суспензию микроорганизмов вводили с помощью микрошприца и иглы двум кроликам в конъюнктиву каждого глаза в объеме 0,1 мл S. intermedius КМ-1К (суспензия с концентрацией 125 млн. микр. клеток) и Е. coli КМ-2D (суспензия 250 млн. микр. клеток). Заражение производили субконъюнктивально. Наблюдение за животными проводили в течение 10 суток, после чего оценивали проявление патологического процесса по трехбалльной шкале: 0 - отсутствие патологического процесса, 1 - слабо выраженный, 2 - выраженный и 3 - ярко выраженный процесс.
Лечение глаз у кроликов начинали при проявлении выраженного конъюнктивита, спустя 12 ч после заражения. Каждой концентрацией:
1) нетилмицин 0,1%, азитромицин 0,5%
2) нетилмицин 0,3%, азитромицин 1%
3) нетилмицин 0,5%, азитромицин 1,5%
4) нетилмицин 0,7%, азитромицин 2%
мази глазной лечили двух кроликов (4 глаза), зараженных эшерихиями, и двух кроликов (4 глаза), зараженных стафилококком. Препарат вводили в нижний конъюнктивальный свод - полоску длиной 1 см четыре раза в сутки до клинического выздоровления, но не более 10 дней. По два кролика, зараженных разными микроорганизмами, оставили без лечения (контроль).
Степень патологических проявлений кератоконъюнктивита во время лечения оценивали по трехбалльной шкале.
0 баллов - отсутствие реакции или невозможность ее оценки;
1 балл - слабо выраженный процесс;
2 балла - выраженный процесс;
3 балла - ярко выраженный процесс.
В результате проведенных исследований установлено, что при применении мази глазной с концентрацией нетилмицина 0,3% и азитромицина 1% для лечения экспериментального конъюнктивита у кроликов, вызванного Е. coli, полное клиническое выздоровление наступало к 9-10 дню после заражения, а при заражении S. Intermedius - к 8-9 дню.
При применении мази глазной с концентрацией нетилмицина 0,5% и азитромицина 1,5% выздоровление животных, зараженных Е. coli и S. intermedius, наступало на 7 день. При этом отек и гиперемия конъюнктивы исчезали уже на 4-5 день.
При применении мази глазной с концентрацией нетилмицина 0,7% и азитромицина 2%, исчезновение гнойной экссудации происходило в те же сроки, как и в предыдущей группе животных. Однако на протяжении всего времени лечения отмечены отек и интенсивная гиперемия конъюнктивы, что свидетельствует о раздражающем действии данной концентрации лекарственных веществ на ткани конъюнктивы.
При применении мази глазной с концентрацией нетилмицина 0,1% и азитромицина 0,5% для лечения экспериментального конъюнктивита, выздоровление животных происходило к 10 дню (при заражении S. Intermedius), как и в контрольной группе, зараженной S. Intermedius, а при заражении Е. coli на 10 день отмечали незначительную гнойную экссудацию, гиперемию и отек конъюнктивы. Эти симптомы соответствовали таковым у животных в контрольной группе, зараженных Е. coli.
На основании полученных данных можно заключить, что оптимальной концентрацией действующих веществ для мази глазной является концентрация нетилмицина 0,5% и азитромицина 1,5%, так как снижение концентрации до 0,3% и 1% соответственно приводит к замедлению выздоровления у животных, а повышение концентрации нетилмицина до 0,7% и азитромицина до 2% не сокращает сроки выздоровления и вызывает раздражение конъюнктивы.
Пример 6. Синергидное действие нетилмицина и азитромицина при одновременном использовании.
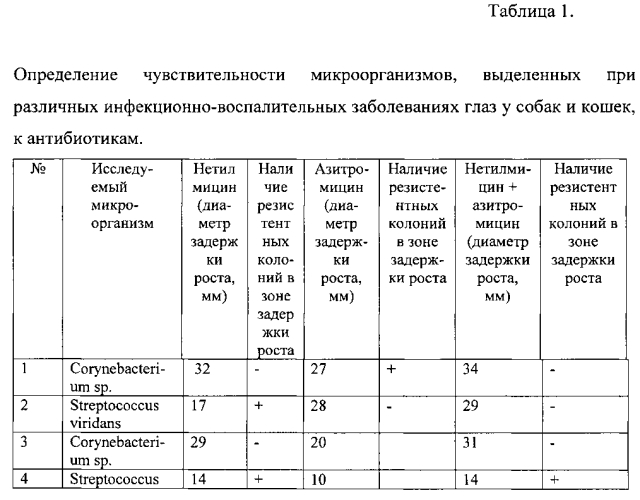
Исследование чувствительности микроорганизмов, выделенных при различных инфекционно-воспалительных заболеваниях глаз у животных, проводили методом радиальной диффузии на агаровом геле. Для этого использовали диски с антибиотиками фирмы Хаймедиа. В работе использовали следующие диски: нетилмицин (30 мкг), азитромицин (30 мкг) и диск с комбинацией антибиотиков нетилмицин (30 мгк) и азитромицин (30 мкг). Для работы использовали агар Мюллера-Хинтона, разлитый в чашки Петри с толщиной пластинки 4-5 мм. Выращенную бульонную культуру исследуемого микроорганизма наносили на агар в объеме 0,1 мл, тщательно распределяли шпателем по всей поверхности, и после впитывания устанавливали диски по периферии среды на одинаковом удалении друг от друга. Посевы с дисками инкубировали при температуре 37±1°С в течение суток. Результаты учитывали по диаметру задержки роста микроорганизма и выражали в буквенном обозначении: ВЧ - высокочувствительный, Ч - чувствительный, СЧ - переходный (слабочувствительный) и У - резистентный (устойчивый). Результаты исследования представлены в таблице 1.
Данные, представленные в таблице 1, свидетельствуют о том, что комбинация антибиотиков нетилмицина и азитромицина в 11% случаев увеличивает диаметр задержки роста микроорганизмов на 1 мм и в 6,6% случаев - на 2 мм. Кроме того, количество резистентных колоний, обнаруживаемых в зоне задержки роста, при использовании комбинации азитромицина и нетилмицина составляло 30%, что значительно ниже, чем при подтитровке каждого антибиотика по отдельности. Так было выявлено, что при определении чувствительности к азитромицину, количество культур бактерий, у которых в зоне задержки роста присутствуют резистентные микроорганизмы, составило 46%, а при определении чувствительности к нетилмицину - 48%.
Таким образом, полученные результаты позволяют сделать вывод о наличии синергидного действия у нетилмицина и азитромицина при одновременном использовании.
Пример 7. Исследование острого аллергизирующего действия глазной мази.
Исследование проводили на кроликах-альбиносах.
В конъюнктивальную полость правого глаза вводили полоску мази, приготовленной по примеру 1, длиной 0,7 см каждые 2 часа восьмикратно. В конъюнктивальную полость левого глаза инсталлировали по 2 капли 0,9% раствора натрия хлорида каждые 2 часа восьмикратно.
Учет результатов проводили каждые 2 ч перед введением очередной порции препарата восьмикратно, затем через 10 и 24 часа после последнего введения.
Во время и после исследования конъюнктива контрольных и опытных глаз оставалась бледно розового цвета, отека, экссудации и окулярного дискомфорта не отмечено, роговица оставалась прозрачной, гладкой, влажной, без признаков отека и воспаления.
Пример 8. Исследование хронического аллергизирующего действия глазной мази.
В течение 14 дней в конъюнктивальную полость правого глаза вводили полоску препарата, полученного по примеру 1, длиной 0,7 см 4 раза в день (опыт). В конъюнктивальную полость левого глаза инсталлировали по 2 капли 0,9% раствора натрия хлорида 4 раза в день (контроль).
Состояние конъюнктивы и роговицы исследовали путем биомикроскопии при помощи ручной щелевой лампы. Учет результатов проводили ежедневно в течение 14 дней опыта, затем на 3-й и 7-й дни после окончания опыта.
Во время и после исследования конъюнктива контрольных и опытных глаз оставалась бледно-розового цвета, отека, экссудации и окулярного дискомфорта не отмечено, роговица оставалась прозрачной, гладкой, влажной, без признаков отека и воспаления.
Пример 9. Клиническая эффективность заявленного препарата.
Всем животным четыре раза в день назначали препарат, полученный по примеру 1. Длительность лечения - от 10 до 14 дней. С 14 по 21 день вели наблюдение за животными после отмены лечения.
Интенсивность симптомов оценивали по 5-балльной шкале. Самая высокая степень выраженности симптомов заболевания оценивалась в 5 баллов, отсутствие симптомов - 0 баллов.
Площадь язвы роговицы указана в миллиметрах.
Как следует из данных, представленных в таблице 2, заявленное изобретение - мазь глазная - обладает высокой антибактериальной активностью при лечении широкого ряда заболеваний глаз животных: при инфекционно-воспалительных заболеваниях век, конъюнктивы, роговицы и сосудистой оболочки глаза, отличается низкой токсичностью и отсутствием местных реакций со стороны глаза.
Так как глазная мазь относится к лекарственным формам, обладающим пролонгированным действием, она имеет ряд преимуществ перед капельной формой офтальмологических препаратов, а именно:
- действующие вещества глазной мази равномерно всасываются в ткани переднего отрезка глаза, поддерживая терапевтическую концентрацию лекарственных веществ как непосредственно в конъюнктивальном мешке на поверхности конъюнктивы и роговицы, так и в тканях век, конъюнктивы и роговицы на протяжении длительного интервала времени. Поэтому кратность применения глазной мази - 2-4 раза в день - значительно реже, чем у глазных капель, обеспечивает выраженный клинический эффект при минимальной затрате времени владельцев животного;
- глазная мазь на классической гидрофобной основе (вазелин, ланолин, жидкий парафин) покрывает поверхность роговицы и конъюнктивы, препятствует испарению водной фракции слезной пленки, обеспечивая оптимальные условия увлажнения при синдроме сухого глаза на протяжении длительного времени - до 6 часов);
- глазная мазь может быть нанесена локально и длительно удерживаться на поверхности век, обеспечивая поступление действующего вещества непосредственно к очагу воспаления при таких заболеваниях как блефариты, мейбомеиты, халазионы, а также травмы век, заживающие по вторичному натяжению.
Однако глазная мазь, как лекарственная форма, имеет и недостатки, к которым можно отнести следующие:
- действующие вещества глазной мази в меньшем объеме проникают во влагу передней камеры, радужную оболочку и стекловидное тело, что ограничивает применение мазевой формы при интраокулярных воспалительных процессах;
- жировая основа глазной мази при непосредственном контакте со стромой роговицы приводит к некоторому набуханию коллагеновых волокон, а также ограничивает поступление кислорода к ее тканям. Эти особенности ограничивают применение глазной мази при язвах и травмах роговицы.
С учетом перечисленных выше преимуществ и недостатков глазной мази, заявленная лекарственная форма, имеющая в своем составе нетилмицин и азитромицин, имеет следующие показания для применения:
- синдром сухого глаза;
- хронические и субхронические формы катаральных, гнойно-катаральных и гнойных конъюнктивитов;
- хронические и субхронические формы кератоконъюнктивитов и кератитов (сосудистый и пигментозный);
- хронические и субхронические блефариты, мейбомеиты, халазионы;
- травмы век, конъюнктивы;
- воспаление Гарднеровой железы третьего века;
- эписклериты.
При испытаниях составов глазной мази, полученной по примерам 2-4, установлено, что при добавлении к базисному составу глазной мази гормонов - дексаметазона, или преднизолона, или гидрокортизона - помимо антимикробных, препарат приобретает выраженное противоаллергическое, противовоспалительное, потивоотечное и иммуносупресивное действие.
В связи с этим к показаниям к применению глазной мази добавляются:
- аллергические реакции;
воспалительные реакции, сопровождающиеся бактериальным инфицированием.
Но одновременно с расширением области применения мази, у нее появляется ряд противопоказаний. Мазь глазную, полученную по примерам 2-4, не рекомендуется использовать при вирусном кератите (язвенный и древовидный кератит); при вирусных заболеваниях роговицы и конъюнктивы; при инфекциях глаз, вызванных грибами, в частности малассезией; при острых гнойных заболеваниях глаз с поражением эпителия роговицы; при эпителиопатии роговицы; при повышенном внутриглазном давлении; при хирургических вмешательствах при травмах и язвах роговицы.
Кроме того, при назначении животным глазной мази, содержащей в своем составе дексаметазон, или преднизолон, или гидрокортизон, необходимо учитывать, что длительное применение таких препаратов может стать причиной возникновения вторичной глаукомы, стероидной катаракты и стероидной язвы роговицы.
1. Антибактериальное лекарственное средство в форме мази для лечения глазных болезней у животных, отличающееся тем, что содержит азитромицин, нетилмицин, нафазолин, ланолин безводный, жидкий парафин, вазелин белый, кислоту лимонную, нипагин, нипазол и воду для инъекций при следующем соотношении компонентов (в мас.%):
| азитромицин | 0,5-2,0 |
| нетилмицин | 0,1-0,7 |
| нафазолин | 0,0005-0,05 |
| ланолин безводный | 1,0-70,0 |
| жидкий парафин | 1,0-70,0 |
| вазелин белый | 1,0-70,0 |
| кислота лимонная | 0,01-5,0 |
| нипагин | 0,05-0,4 |
| нипазол | 0,05-0,4 |
| вода для инъекций | до 100. |
2. Антибактериальное лекарственное средство в форме мази по п. 1, отличающееся тем, что дополнительно содержит в своем составе либо дексаметазон в количестве 0,03-0,5 мас.%, либо преднизолон в количестве 0,1-1,0 мас.%, либо гидрокортизон в количестве 0,1-1,0 мас.%.