Алкалоидные производные на основе сложных аминоэфиров и композиции лекарственных средств, содержащие их
Иллюстрации
Показать всеИзобретение относится к области органической химии, а именно к алкалоидным производным на основе сложных аминоэфиров общей формулы (I) и к их фармацевтически приемлемым солям, где R1 представляет собой фенил, необязательно замещенный одним-тремя заместителями, выбранными из группы, состоящей из атомов галогена, СООН; R2 представляет собой фенил, необязательно замещенный одним заместителем, выбранным из группы, состоящей из атомов галогена; W выбирают из группы, состоящей из фенила, нафталенила и гетероарила (выбранного из дигидробензодиоксинила, дигидробензодиоксепинила, дигидробенз-оксазинила и тиофенила), при этом каждый из фенила и нафталенила необязательно замещен одним или двумя заместителями, одинаковыми или различными, выбранными из группы, состоящей из атомов галогена, -NO2, -CN, (C1-C6)алкила, (C1-C6)алкокси, галоген(C1-C6)алкила, галоген (С1-С6)алкокси, гетероциклила (выбранного из пирролидинила, морфолинила), фенила, фенилокси, галогенфенила, (C1-C6)алкил-NHCO -(C1-C6)алкила, -OR3, -N(R3)2, -SR3, -OSO2R3, -CO2R3, -OCOR3, -CON(R3)2, -NHCOR3, -NHCO2R3, -NHSO2R3, -NHCO-(С1-С6)алкил-СООН, -CO2-(C1-C6)алкил-N (R3)2 и -СО-морфолинила; R3 представляет собой H или выбран из группы, состоящей из (С1-С6)алкила; А- представляет собой физиологически приемлемый анион, выбранный из Cl-, Br-, TFA-. Также изобретение относится к применению соединения формулы (I). Технический результат: получены новые гетероциклические соединения, полезные в качестве антагонистов мускариновых рецепторов. 2 н. и 8 з.п. ф-лы, 12 табл., 39 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к алкалоидным производным на основе сложных аминоэфиров, действующим в качестве антагонистов мускариновых рецепторов, к способам их получения, к композициям, содержащим их, и к их терапевтическому применению.
Уровень техники
Соли четвертичного аммония, действующие в качестве лекарственных средств, являющихся антагонистами мускариновых (M) рецепторов, в настоящее время используют в терапии для индуцирования бронходилатации для лечения респираторных заболеваний. Примеры хорошо известных антагонистов M-рецепторов представлены, например, ипратропием бромидом и тиотропием бромидом.
Несколько химических классов селективных антагонистов M3-рецепторов, действующих в качестве лекарственных средств, разработаны для лечения воспалительных или обструктивных заболеваний дыхательных путей, таких как астма и хроническое обструктивное заболевание легких (COPD).
Карбаматные производные хинуклидина и их применение в качестве антагонистов M3 описаны, например, в WO 02/051841, WO 03/053966 и WO 2008/012290.
Указанные антагонисты M- и M3-рецепторов в настоящее время вводят посредством ингаляции, чтобы доставлять лекарственные средства непосредственно в место их действия, ограничивая, таким образом, системное экспонирование и любое нежелательное побочное воздействие из-за системного поглощения.
По этой причине, является в высшей степени желательным создание антагонистов M3-рецепторов, способных действовать локально, имея в то же время высокую эффективность и продолжительное время действия. Указанные лекарственные средства, после поглощения, деградируют до неактивных соединений, которые не обладают какими-либо системными побочными воздействиями, типичными для антагонистов мускариновых рецепторов.
Одновременно рассматриваемая заявка WO 2010/072338, описывает азонийбицикло[2.2.2]октановые соединения, действующие в качестве антагонистов мускариновых рецепторов, дополнительно обладающие указанными выше терапевтически желательными характеристиками.
В настоящее время неожиданно обнаружено, что соединения, отличающиеся присутствием замещенной оксоэтильной группы на азонийбицикло[2.2.2]октановом кольце, обладают высокой нестабильностью в плазме и более продолжительным временем действия, чем соответствующие соединения, не имеющие такой группы.
Таким образом, соединения по настоящему изобретению действуют как мягкие лекарственные средства, поскольку они способны оказывать более устойчивое бронходилатационное воздействие в легких, но они более единообразно и быстро преобразуются в неактивные метаболиты после перехода в плазму человека.
Такое поведение дает большие преимущества с точки зрения безопасности.
Сущность изобретения
Таким образом, настоящее изобретение относится к алкалоидным производным на основе сложных аминоэфиров общей формулы (I) с замещенной оксоэтильной группой на азонийбицикло[2.2.2]октане, действующим в качестве антагонистов мускариновых рецепторов, к способам их получения, к композициям, содержащим их, к их терапевтическим применениям и к их комбинациям с другими фармацевтически активными ингредиентами, среди них присутствуют, например, те, которые в настоящее время используют при лечении респираторных расстройств, например, бета2-агонисты, кортикостероиды, ингибиторы P38 MAP киназы, IKK2, ингибиторы HNE, ингибитор PDE4, лейкотриеновые модуляторы, NSAID и средства регуляции клеток слизистых.
Подробное описание изобретения
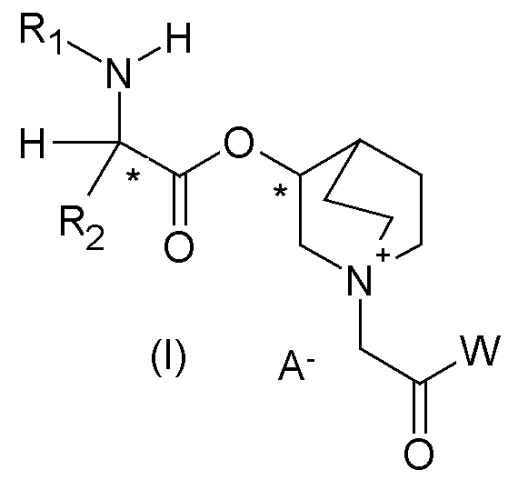
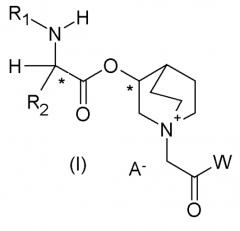
В частности, настоящее изобретение направлено на алкалоидные производные на основе сложных аминоэфиров общей формулы (I)
где:
R1 представляет собой арил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из атомов галогена, OH, SH, NO2, CN, COOH, (C1-C6)алкоксикарбонила, (C1-C6)алкилсульфанила, (C1-C6)алкилсульфинила, (C1-C6)алкилсульфонила, (C1-C6)алкила, (C1-C6)галогеналкила, (C1-C6)алкокси и (C1-C6)галогеналкокси;
R2 представляет собой арил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из атомов галогена, OH, SH, NO2, CN, COOH, (C1-C6)алкоксикарбонила, (C1-C6)алкилсульфанила, (C1-C6)алкилсульфинила, (C1-C6)алкилсульфонила, (C1-C6)алкила, (C1-C6)галогеналкила, (C1-C6)алкокси и (C1-C6)галогеналкокси;
W выбирают из группы, состоящей из (C1-C6)алкила, арила, -NH-гетероциклила и гетероарила, каждый из которых является необязательно замещенным одним или несколькими заместителями, одинаковыми или различными, выбранными из группы, состоящей из атомов галогена, оксо, -NO2, -CN, (C1-C6)алкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)галогеналкокси, (C3-C8)циклоалкила, гетероциклила, арила, арилокси, галогенарила, (C1-C6)алкил-NCO-(C1-C6)алкила, -OR3, -N(R3)2, -SR3, -OSO2R3, -COR3, -CO2R3, -OCOR3, -CON(R3)2, -NHCOR3, -NHCO2R3, -NHSO2R3, -NHCO-(C1-C6)алкил-COOH, -CO2-(C1-C6)алкил-N(R3)2 и -CO-гетероциклила;
R3 представляет собой H или выбран из группы, состоящей из (C1-C6)алкила и гетероарила, необязательно замещенного одним или несколькими заместителями, выбранными из группы, состоящей из фенила, атомов галогена, OH, оксо, SH, NO2, CN, CONH2 и COOH;
A- представляет собой физиологически приемлемый анион;
и их фармацевтически приемлемые соли.
В настоящем описании, если не указано иное, термин "галоген" включает атомы фтора, хлора, брома и йода.
Термин "(C1-C6)алкил", относится к алкильным группам с прямой или разветвленной цепью, где количество атомов углерода составляет от 1 до 6. Примеры указанных групп представляют собой метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил и, тому подобное.
Термин "(C1-C6)алкокси" относится к алкил-окси (например, алкокси) группам. Примеры указанных групп могут, таким образом, включать метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, пентокси, гексокси, и тому подобное.
Подобным же образом, выражение "(C1-C6)алкоксикарбонил" относится к указанным выше (C1-C6)алкокси группам, дополнительно несущим карбонильную группу, среди которых находится, например, ацетокси (например, ацетилоксикарбонил), трет-бутоксикарбонил и тому подобное.
Выражения "(C1-C6)галогеналкил" и "(C1-C6)галогеналкокси", относится к указанным выше группам "(C1-C6)алкил" и "(C1-C6)алкокси", где один или несколько атомов водорода заменены одним или несколькими атомами галогена, которые могут быть одинаковыми или отличаться друг от друга.
Примеры указанных (C1-C6)галогеналкильных и (C1-C6)галогеналкокси групп могут, таким образом, включать галогенированные, полигалогенированные и полностью галогенированные алкильные и алкокси группы, где один или несколько атомов водорода замещены атомами галогена, например, трифторметильную или трифторметокси группы.
Подобным же образом, выражение "(C1-C6)алкилсульфанил", "(C1-C6)алкилсульфинил" или "(C1-C6)алкилсульфонил" относится, соответственно, к алкил-S-, алкил-SO- или алкил-SO2-группам.
Выражение "(C3-C8)циклоалкил" относится к циклическим неароматическим углеводородным группам с 3-8 атомами углерода. Примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и тому подобное.
Выражение "арил" относится к моно-, или би-, или трициклическим кольцевым системам, которые имеют 6-20 атомов в кольце, предпочтительно 6-15, и где по меньшей мере одно кольцо является ароматическим.
Выражение "гетероарил" относится к моно-, би- или трициклическим кольцевым системам с 5-20 атомами в кольце, предпочтительно с 5-15, где по меньшей мере одно кольцо является ароматическим и где по меньшей мере один атом в кольце представляет собой гетероатом или гетероароматическую группу (например, N, NH, S или O).
Примеры соответствующих арильных или гетероарильных моноциклических систем включают, например, тиофеновый, бензольный, пиррольный, пиразольный, имидазольный, изоксазольный, оксазольный, изотиазольный, тиазольный, пиридиновый, имидазолидиновый, фурановый радикалы, и тому подобное.
Примеры соответствующих арильных или гетероарильных бициклических систем включают нафталиновый, бифениленовый, пуриновый, птеридиновый, бензотриазольный, хинолиновый, изохинолиновый, индольный, изоиндольный, бензотиофеновый, дигидробензодиоксиновый, дигидробензодиоксепиновый, дигидробензооксазиновый радикалы, и тому подобное.
Примеры соответствующих арильных или гетероарильных трициклических систем включают флуореновые радикалы, а также бензоконденсированные производные указанных выше гетероарильных бициклических систем.
Выражение "арилокси" относится к арил-окси группам.
Примеры указанных групп могут, таким образом, включать фенилокси, и тому подобное.
Выражение "галогенарил" относится к арильным группам, где один или несколько атомов водорода заменены атомами галогена.
Выражение "гетероциклил" относится к насыщенной, частично ненасыщенной или полностью ненасыщенной 3-8-членной гетероциклической кольцевой системе, где по меньшей мере один атом в кольце представляет собой гетероатом или гетероароматическую группу (например, N, NH, S или O).
Примеры включают пирролидинил, пиперидинил, пиридинил, морфолинил, фурил и имидазолил, и тому подобное.
Из указанного выше ясно, что при упоминании полностью ненасыщенного гетероциклического кольца, указанное выше определение также охватывает указанные выше гетероарильные группы.
Преимущественно, физиологически приемлемые анионы A- включают анионы, выбранные из хлорида, бромида, йодида, трифторацетата, формиата, сульфата, фосфата, метансульфоната, нитрата, малеата, ацетата, цитрата, фумарата, тартрата, оксалата, сукцината, бензоата и п-толуолсульфоната, предпочтительно, хлорида, бромида и трифторацетата.
Наряду с присутствием аниона A-, когда в соединениях формулы (I) присутствуют другие основные амино группы, могут присутствовать дополнительные физиологически приемлемые анионы, из тех, которые указаны ранее. Подобным же образом, в присутствии кислотных групп, таких как группы COOH, могут присутствовать также соответствующие физиологические катионные соли, содержащие, например, ионы щелочных или щелочноземельных металлов.
Первая предпочтительная группа соединений общей формулы (I) является такой, где R1 и R2 независимо представляют собой арильные группы, необязательно замещенные одним или несколькими атомами галогенов или группами -COOH; а W и A- имеют указанные выше значения.
Еще более предпочтительными, в этом классе, являются соединения общей формулы (I), где R1 и R2 независимо представляют собой фенильные группы, необязательно замещенные одним или несколькими атомами галогена или группами -COOH.
Другая предпочтительная группа соединений общей формулы (I) является такой, где W представляет собой арил или гетероарил, каждый из которых является необязательно замещенным одним или несколькими заместителями, одинаковыми или различными, выбранными из группы, состоящей из атомов галогена, -OR3, оксо, -SR3, -OSO2R3, -NO2, -COR3, -CO2R3, OCOR3, -CON(R3)2, -CN, -N(R3)2, -NHCOR3, -NHCO2R3, -NHSO2R3, (C1-C6)алкила, (C1-C6)галогеналкила, (C1-C6)алкокси, (C1-C6)галогеналкокси (C3-C8)циклоалкила, (C3-C8)гетероциклила, арила, -NHCO-(C1-C6)алкил-COOH, -CO2-(C1-C6)алкил-N(R3)2, (C1-C6)алкил-NCO-(C1-C6)алкила и -CO-гетероциклила; и R1, R2 и A- являются такими, как определено выше.
Еще более предпочтительными, в этом классе, являются соединения формулы (I), где W выбирают из группы, состоящей из фенила, тиофенила, дигидробензодиоксепина, дигидробензодиоксина, дигидробензооксазина, нафталенила или пирролидинилфенила, каждое из которых является необязательно замещенным, как указано выше; и R и R2 и A- являются такими, как указано выше.
Еще более предпочтительными, в этом классе, являются соединения формулы (I), где W представляет собой фенил, необязательно замещенный одной или несколькими группами, выбранными из атомов галогена, -CN, -NO2, -CF3, -OCH3, -OCF3, -OH, -CONH2, метила, этила, этокси, фенокси, этоксикарбонила, бутоксикарбонила, -COOH, -NH2, -N(CH3)2, (C1-C6)алкила, ацетамидопропила, -SCH3, фенила, фторфенила, морфолинила, морфолинкарбонила, изопропоксикарбонила, диметиламиноэтокси, метилсульфонилокси, ацетокси, бутирамидила, пиваламидила, карбоксипропанамидила, метилсульфонамидила и пирролидинила; и R1, R2, R3 и A- являются такими, как определено выше.
Еще более предпочтительными являются соединения формулы (I), где W выбирают из группы, состоящей из дигидробензодиоксепина, дигидробензодиоксина, дигидробензооксазина, нафталенила или пирролидинилфенила, необязательно замещенного одной или несколькими группами, выбранными из атомов галогена, -COOH и этила.
Другая предпочтительная группа соединений формулы (I) является такой, где W представляет собой -NH-гетероциклил; и R1, R2 и A- являются такими, как определено выше.
Еще более предпочтительными, в этом классе, являются соединения формулы (I), где W представляет собой пиридин-2-иламино; и R1, R2, R3 и A- являются такими, как определено выше.
В соответствии с конкретными вариантами осуществления настоящего изобретения, конкретные примеры соединений общей формулы (I) приводятся ниже:
| Соединение | Химическое наименование |
| C20 | (R)-1-(2-(3-цианофенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C21 | (R)-1-(2-(бифенил-4-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C22 | (R)-1-(2-(2-нитрофенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C23 | (R)-1-(2-(3-метоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C24 | (R)-1-(2-(2-метоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C25 | (R)-1-(2-(2,5-диметоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C26 | (R)-1-(2-(3,4-диметоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C27 | (R)-1-(2-(3-карбамоил-4-гидроксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C28 | (R)-1-(2-(2-гидроксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C29 | (R)-1-(2-(3-хлорфенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C30 | (R)-1-(2-оксо-2-(4-(трифторметокси)фенил)этил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C31 | (R)-1-(2-(5-фтор-2-гидроксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C32 | (R)-1-(2-(2,3-дигидробензо[b][1,4]диоксин-6-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C33 | (R)-1-(2-(3,4-дигидро-2H-бензо[b][1,4]диоксепин-7-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C34 | (R)-1-(2-оксо-2-(4-(пирролидин-1-ил)фенил)этил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C35 | (R)-1-(2-(4-карбоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C36 | (R)-1-(2-(3-нитрофенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C37 | (R)-1-(2-(4-(3-ацетамидопропил)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C38 | (R)-1-(2-оксо-2-(3-оксо-3,4-дигидро-2H-бензо[b][1,4]оксазин-6-ил)этил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C39 | (R)-1-(2-(3-аминофенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)-ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C40 | (R)-1-(2-(2-аминофенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C44 | (3R)-3-(2-(3-фторфенил)-2-(3,4,5-трифторфениламино)ацетокси)-1-(2-оксо-2-(тиофен-2-ил)этил)-1-азонийбицикло[2.2.2]октан хлорид |
| C46 | (R)-1-(2-(5-этилтиофен-3-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C47 | (R)-1-(2-(нафталин-2-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C48 | (R)-1-(2-(4-фтор-2-гидроксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C49 | (R)-1-(2-(4-(метилтио)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C50 | (R)-1-(2-(3,4-дигидроксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C51 | (R)-1-(2-(3-хлор-4-фторфенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C52 | (R)-1-(2-(4-морфолинофенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C53 | (R)-1-(2-(3-фтор-4-гидроксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C54 | (R)-1-(2-(4-(диэтиламино)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C55 | (R)-1-(2-оксо-2-(4-(трифторметил)фенил)этил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C56 | (R)-1-(2-(4-(этоксикарбонил)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C57 | (R)-1-(2-(4-(бутоксикарбонил)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C58 | (R)-1-(2-оксо-2-o-толилэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C59 | ((R)-1-(2-оксо-2-м-толилэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C60 | (R)-1-(2-(5-этилтиофен-2-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан хлорид |
| C61 | (R)-1-(2-(4-этоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C62 | (R)-1-(2-(2,5-дихлортиофен-3-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан хлорид |
| C63 | (R)-1-(2-оксо-2-(4-феноксифенил)этил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C64 | (R)-1-(2-(бифенил-3-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C65 | (R)-1-(2-(4'-фторбифенил-4-ил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C66 | (R)-1-(2-оксо-2-(пиридин-2-иламино)этил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан хлорид |
| C67 | (R)-1-(2-(4-карбоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C68 | (R)-1-(2-(4-(морфолин-4-карбонил)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C69 | (R)-1-(2-(4-(изопропоксикарбонил)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C70 | (R)-1-(2-(4-((2-(диметиламино)этокси)карбонил)-фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат 2,2,2-трифторацетат анион |
| C72 | (R)-1-(2-(4-(метилсульфонилокси)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C73 | (R)-1-(2-(4-ацетоксифенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C75 | (R)-1-(2-(4-бутирамидофенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C76 | (R)-1-(2-оксо-2-(4-пиваламидофенил)этил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C77 | (R)-1-(2-(4-(3-карбоксипропанамидо)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C78 | (R)-1-(2-(4-(метилсульфонамидо)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C79 | (R)-1-(2-(4-(этоксикарбониламино)фенил)-2-оксоэтил)-3-((R)-2-фенил-2-(фениламино)ацетокси)-1-азонийбицикло[2.2.2]октан бромид |
| C80 | (3R)-3-(2-(3-карбоксифениламино)-2-фенилацетокси)-1-(2-оксо-2-фенилэтил)-1-азонийбицикло[2.2.2]октан хлорид |
| C81 | (R)-3-((S)-2-(4-фторфениламино)-2-фенилацетокси)-1-(2-(4-гидроксифенил)-2-оксоэтил)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C82 | (R)-3-((R)-2-(4-фторфениламино)-2-фенилацетокси)-1-(2-(4-гидроксифенил)-2-оксоэтил)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C83 | (R)-3-((R)-2-(4-фторфениламино)-2-фенилацетокси)-1-(2-(3-гидроксифенил)-2-оксоэтил)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
| C84 | (R)-3-((R)-2-(4-фторфениламино)-2-фенилацетокси)-1-(2-(2-гидроксифенил)-2-оксоэтил)-1-азонийбицикло[2.2.2]октан 2,2,2-трифторацетат |
Соединения общей формулы (I) имеют по меньшей мере два хиральных центра, которые представлены атомами углерода со звездочками, как указано ниже:
Кроме того, в зависимости от значений R1, R2 и W, будет ясно, что в соединениях формулы (I) могут присутствовать дополнительные асимметричные центры. По этой причине, настоящее изобретение также включает любой из его оптических стереоизомеров, диастереомеров и их смесей, в любой пропорции.
В одном из предпочтительных вариантов осуществления хиральный центр на хинуклидиновом кольце показывает R-конфигурацию.
В настоящем изобретении, поскольку абсолютная конфигурация диастереомеров не определена, они указаны в примерах, как диастереомер 1, 2 или их смеси.
Настоящее изобретение также предоставляет фармацевтические композиции, содержащие одно или несколько соединений формулы (I), необязательно, в комбинации или в смеси с одним или несколькими фармацевтически приемлемыми носителями и/или эксципиентами.
Настоящее изобретение также предоставляет фармацевтические композиции, пригодные для введения посредством ингаляции, такие, например, как порошки для ингаляции, содержащие пропелленты, дозирующие упаковки аэрозолей или препараты для ингаляции, не содержащие пропеллентов.
Настоящее изобретение также предоставляет соединения формулы (I) для применения в качестве лекарственного средства.
Настоящее изобретение также предоставляет соединения формулы (I) для применения при лечении бронхообструктивных или воспалительных заболеваний, предпочтительно, астмы или хронического бронхита, или хронического обструктивного заболевания легких (COPD).
В другом аспекте настоящее изобретение предоставляет применение соединений формулы (I) для получения лекарственного для предотвращения и/или лечения бронхообструктивных или воспалительных заболеваний, предпочтительно астмы или хронического бронхита или хронического обструктивного заболевания легких (COPD).
Настоящее изобретение также предоставляет способ для предотвращения и/или лечения бронхообструктивных или воспалительных заболеваний, предпочтительно астмы или хронического бронхита или хронического обструктивного заболевания легких (COPD), который включает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I).
Настоящее изобретение также относится к устройству для введения указанной выше фармацевтической композиции, которое может представлять собой однодозовый или многодозовый ингалятор для сухого порошка, ингалятор с отмериванием дозы и небулайзер типа soft mist, содержащие соединения формулы (I).
Настоящее изобретение также относится к набору, содержащему указанные выше фармацевтические композиции, в соответствующем флаконе или контейнере, и устройство, которое может представлять собой однодозовый или многодозовый ингалятор для сухого порошка, ингалятор с отмериванием дозы и небулайзер типа soft mist, адаптируемый для удерживания указанных выше флакона или контейнера.
Соединения формулы (I) могут быть получены в соответствии с известными или обычными способами.
Настоящее изобретение также направлено на способ получения соединений общей формулы (I), где способ включает:
(a) алкилирование соединения общей формулы (III), где R1 является таким, как определено выше
соединением общей формулы (II)
где R2 является таким, как определено выше, LG представляет собой соответствующую уходящую группу, и K представляет собой карбоксильную группу, либо как есть, либо в необязательно защищенной форме, либо ацилгалогенидную группу, с получением соединения общей формулы (IV)
(b) необязательное удаление защиты карбоксильной группы с соединения общей формулы (IV) и его сочетание с соединением формулы (V)
с получением соединения общей формулы (VI)
(c) реакцию алкилирования соединения общей формулы (VI) алкилирующим агентом общей формулы (VII)
где A представляет собой соответствующую уходящую группу, и W является таким, как определено выше, с тем, чтобы получить соединение общей формулы (I); и необязательно
(d) преобразование соединения общей формулы (I) в другое соединение общей формулы (I) и/или в его фармацевтически приемлемую соль.
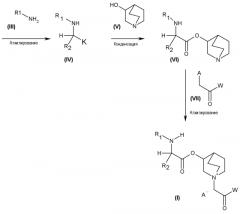
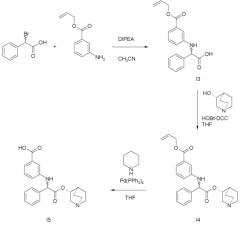
Рабочие условия, которые можно использовать в способе по настоящему изобретению, описаны более подробно ниже и дополнительно приводятся в следующей далее Схеме 1.
Исходные материалы для получения соединений формулы (I), то есть соединения формулы (II) и (III), а также любой реагент способа, являются известными или легко получаются в соответствии с известными процедурами.
Схема 1
Процедура получения соединений формулы (I)
В соответствии со стадией (a) способа, соединения формулы (IV) могут быть получены посредством алкилирования амина формулы (III) соединением формулы (II), где LG представляет собой соответствующую уходящую группу (например, галогенид, такой как бром), и K представляет собой карбоксильную группу в необязательно защищенной форме.
Как правило, LG представляет собой атом галогена, а более предпочтительно, представляет собой атом брома. K может представлять собой карбоксильную группу либо саму по себе, либо в необязательно защищенной форме, как правило, включающей группы карбоксиалкиловых сложных эфиров (например, K=COO(C1-C6)алкил), предпочтительно, карбоксиметил (например, COOMe).
Реакция алкилирования может быть ускорена присутствием основания, например, амина, выбранного из группы, состоящей из триэтиламина, пиридина и 4-диметиламинопиридина, либо как есть, либо в соответствующем растворителе (например, в ацетонитриле). Эту реакцию обычно осуществляют в диапазоне температур от примерно 0°C до примерно 130°C в течение периода от примерно 1 часа до примерно 74 часов. Реакцию можно осуществлять при обычном нагревании (с использованием масляной бани) или при микроволновом нагревании. Реакцию можно осуществлять в открытой емкости или в герметичной пробирке.
В соответствии со стадией (b) способа, соединения общей формулы (VI) затем могут быть получены посредством сочетания спирта формулы (V) с соединением формулы (IV), полученным на стадии стадии (a).
Рабочие условия выбирают на основе химической активности соединения (IV) по отношению к спирту (V) и совместимости других групп, присутствующих в обоих реагентах (относительно общей ссылки на указанную выше реакцию и ее рабочие условия, см., например, Carey, F.A. and Sundeberg, R.J. Advanced Organic Chemistry, Third Edition (1990), Plenum Press, New York and London, pg 145).
В частности, когда K представляет собой защищенную карбоксильную группу, защитная группа должна сначала удаляться до того, как будет иметь место реакция сочетания. Когда K представляет собой фрагмент сложного эфира карбоновой кислоты (например, K=COOMe), удаление защитной группы осуществляют в условиях гидролиза, как правило, в присутствии любого водного раствора соответствующего основания, выбранного из группы, состоящей из гидроксида натрия, лития и калия. Реакцию осуществляют в любом пригодном растворителе, например, в присутствии тетрагидрофурана или диоксана, при комнатной температуре (RT) и в течение периода от примерно 1 часа до примерно 36 часов.
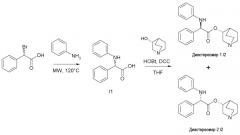
Альтернативно, когда начинают с соединения формулы (IV), где K представляет собой карбоксил, для получения соединения формулы (VI) могут применяться стандартные условия амидирования и пептидного сочетания. Указанные условия включают, например, активирование промежуточного соединения (IV) посредством одного или нескольких эквивалентов коммерчески доступного конденсирующего агента, такого как карбодиимид (например, Ν,Ν'-дициклогексилкарбодиимид (DCC), и тому подобное) в присутствии N-гидроксибензотриазола (HOBt). Органическое основание, такое как триэтиламин, также может присутствовать в реакционной смеси. Активированное промежуточное соединение может быть либо выделено, либо предварительно получено, либо образовано in situ, а затем соответствующим образом взаимодействовать со спиртом формулы (V). Соответствующие растворители для реакции сочетания включают, но не ограничиваясь этим, галогенуглеродные растворители (например, дихлорметан), тетрагидрофуран, диоксан и ацетонитрил. Реакция происходит при температуре, находящейся в пределах от примерно 0°C до примерно 170°C, в течение периода времени в пределах от примерно 1 часа до примерно 72 часов. Реакцию можно осуществлять при обычном нагревании (с использованием масляной бани) или при микроволновом излучении. Реакцию можно осуществлять либо в открытой емкости, либо в герметичной пробирке.
Альтернативно, соединение формулы (IV), где K=COOH, может быть сначала активировано с помощью других коммерчески доступных активирующих агентов, таких как бромтрипирролидинофосфоний гексафторфосфат (PyBrOP) или карбонилимидазол, в соответствующем апротонном растворителе (например, в дихлорметане, тетрагидрофуране), примерно при комнатной температуре, чтобы затем взаимодействовать с соединением (V).
В дополнение к этому, соединения формулы (VI) также могут быть эффективно получены посредством конденсации между карбоновыми кислотами (IV) и спиртом (V) при типичных условиях Мицунобу (Kumara Swamy, K.C., Chem. Rev. 2009, 109, 2551-2651). Например, кислота (IV) и спирт (V) взаимодействуют в присутствии соответствующего фосфина (например, трифенилфосфина) и сложного азадикарбоксилатного эфира (например, диэтилазадикарбоксилата или диизопропилазадикарбоксилата) в апротонном растворителе, таком как тетрагидрофуран. Реакцию, как правило, осуществляют в диапазоне температур от примерно 0°C до примерно 100°C, в течение времени в пределах от примерно 30 минут до примерно 72 часов.
В некоторых вариантах осуществления настоящего изобретения, карбоновую кислоту (IV), где K=COOH, удобнее всего, можно преобразовать в соответствующий ацилгалогенид (IV), где K=COCl. Это активирование может быть осуществлено в соответствии с одной из нескольких стандартных процедур, опубликованных в литературе. Они включают, например, обработку кислоты (IV), где K=COOH, одним или несколькими эквивалентами оксалилхлорида в присутствии каталитического количества диметилформамида (DMF) в галогенуглеродном растворителе, таком как дихлорметан, при температуре, находящейся в пределах от примерно 0°C до примерно 35°C.
Наконец, ацилхлорид (IV) (K=COCl) непосредственно взаимодействует со спиртом (V), с использованием известных или обычных способов. Реакция может быть ускорена под действием основания, такого как триэтиламин, пиридин и 4-диметиламинопиридин, и осуществляться в соответствующем растворителе (например, дихлорметане). Эту реакцию осуществляют в диапазоне температур от примерно 0°C до примерно 130°C в течение периода от примерно 1 до примерно 74 часов. Реакцию можно осуществлять при обычном нагревании (с использованием масляной бани) или при микроволновом нагревании. Реакцию можно осуществлять в открытой емкости или в герметичной пробирке.
Из указанного выше ясно, что альтернативные обычные способы синтеза также могут применяться для получения соединений формулы (VI) из реагентов (IV) и (V).
В частности, карбоксильные производные формулы (IV) могут быть удобным образом преобразованы in situ в соответствующие ацилгалогениды, которые затем должны взаимодействовать со спиртом (V). Например, спирты (V) взаимодействуют с кислотами (IV), где K=COOH, в присутствии трифенилфосфина и галогенуглеродного растворителя, такого как четыреххлористый углерод или дихлорметан, примерно при комнатной температуре, через максимальный период времени, составляющий 16 часов (Lee, J.B. J.Am.Chem.Soc, 1966, 88, 3440).
После получения, соединения общей формулы (VI) могут быть получены либо как отдельный диастереомер, либо как смесь диастереомеров. Например, когда спирт (V) имеет R конфигурацию, соответствующие соединения формулы (VI) могут быть получены как в S-R конфигурации, так и в R-R конфигурации, а также как смесь диастереомеров (конфигураций R-R и S-R).
Смесь диастереомеров может быть преобразована в соединения формулы (I), как с помощью стадии (c) способа, или, удобнее всего, может быть разделена с получением двух отдельных диастереомеров, которые, в свою очередь, могут быть преобразованы в соединения формулы (I). Это разделение может быть осуществлено с использованием известных процедур. Эти процедуры включают, но не ограничиваясь этим, хроматографию, очистку, очистку с помощью препаративной ВЭЖХ и кристаллизацию. Например, два диастереомера могут быть разделены с помощью флэш-хроматографии на силикагеле, с элюированием с помощью соответствующих растворителей или с помощью смеси растворителей, таких как DCM (дихлорметан) и метанол, и тому подобное. В другом способе по настоящему изобретению, разделение диастереомеров можно осуществлять посредством использования колонки, заполненной хиральной стационарной фазой, например, Chiralpack AY, или Chiralcel OD, или Chiralcel OZ, и элюирования например, ацетонитрилом и/или смесями ацетонитрила и спирта. Альтернативно, разделение диастереомеров удобнее всего можно осуществлять посредством кристаллизации из удобного растворителя (например, простого этилового эфира), в виде свободного основания, либо после образования соответствующей соли (например, (+)-винной кислоты)).
В соответствии со стадией (c) способа, соединения формулы (VI) затем алкилируют с помощью агента формулы (VII) с получением соединений формулы (I).
Этот вид реакции в основном описан в литературе при нескольких различных условиях. Например, реакцию можно осуществлять как есть или в соответствующем растворителе, выбранном из группы, состоящей из ацетонитрила, этилацетата, диметилформамида (DMF), диметилсульфоксида (DMSO) и тетрагидрофурана (THF). Реакцию, как правило, осуществляют в диапазоне температур от примерно 0°C до примерно 170°C, в течение времени в пределах от нескольких минут до примерно 72 часов. Реакцию можно осуществлять при обычном нагревании (с использованием масляной бани) или при микроволновом излучении. Реакцию можно осуществлять либо в открытой емкости, либо в герметичной пробирке.
В соответствии со стадией (d) способа, соединения формулы (I) могут либо рассматриваться как конечные продукты,