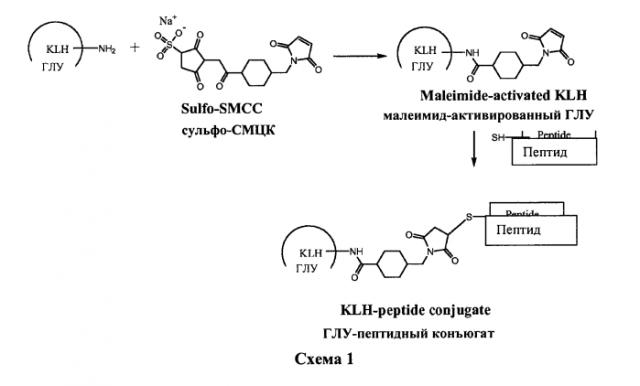
Композиции вакцин
Иллюстрации
Показать всеНастоящая группа изобретений относится к способу получения конъюгата ГЛУ-EGFRvIII, включающему объединение ГЛУ с линкером и предоставление возможности ГЛУ и линкеру взаимодействовать на протяжении периода времени в диапазоне от 30 до 60 минут; добавление пептида, включающего SEQ ID NO:1, к активированному продукту ГЛУ, полученному на предыдущей стадии с получением конъюгата ГЛУ-EGFRvIII, причем молярное соотношение линкер:ГЛУ находится в диапазоне от 75:1 до 325:1, а также конъюгату ГЛУ-EGFRvIII, полученному данным способом. Группа изобретений раскрывает эффективные способы производства и технологии приготовления лекарственного средства. 2 н. и 5 з.п. ф-лы, 26 ил., 8 табл., 7 пр.
Реферат
Данная заявка претендует на приоритет предварительной заявки на патент США № 61/289083, поданной 22 декабря 2009 г., содержание которой включено в данный документ в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее раскрытие относится к композиции вакцин, в частности, ГЛУ-пептидным конъюгатам и способам создания таких композиций. Настоящее раскрытие относится также к способам снижения аномального роста клеток с использованием композиций, описанных здесь.
УРОВЕНЬ ТЕХНИКИ
В настоящее время разрабатывается лекарственное средство CDX-110 для лечения пациентов, страдающих от мультиформной глиобластомы, типа рака мозга. Значительная часть пациентов с этим заболеванием экспрессирует на поверхности раковых клеток вариант рецептора эпидермального фактора роста (EGFR, РЭФР). Этот вариант, известный как EGFRvIII, образуется из соединения мутаций, ведущих к уникальной пептидной последовательности (как правило, из 13 аминокислот) на поверхности раковых клеток. Так как этот вариант не экспрессируется на нормальных клетках, последовательность EGFRvIII является хорошей мишенью для противоракового лечения.
EGFR представляет собой белок, который был хорошо проверен в качестве мишени для терапии раковых заболеваний. В отличие от EGFR, тем не менее, EGFRvIII не присутствует в нормальных тканях, выдвигая в качестве предположения, что эта мишень будет способствовать развитию опухоль-специфической терапии для больных раком. Более того, EGFRvIII является трансформирующим онкогеном, который может прямо способствовать росту раковых клеток. Хотя экспрессия EGFRvIII первоначально была обнаружена при мультиформной глиобластоме (МГБ), наиболее распространенной и агрессивной форме рака мозга, она наблюдается также при различных других видах раковых заболеваний, таких как рак молочной железы, рак яичников, метастатический рак предстательной железы, колоректальный рак и рак головы и шеи.
CDX-110 является конъюгатом вакцины, образованным при помощи ковалентной связи EGFRvIII пептида, к которому был добавлен С-концевой цистеин с белком-носителем гемоцианином лимфы улитки (ГЛУ) (см., например, патенты США под номерами 5401828, 6224868 и WO 2007/056061). ГЛУ также действует как иммунный стимулятор для повышения иммунных ответов против EGFRvIII пептида. Химическая связь пептида EGFRvIII и ГЛУ достигается за счет использования бифункционального линкера, сульфосукцинимидил-4-[N-малеимидометил]циклогексан-1-карбоксилата (сульфо-СМЦК).
Предыдущие процессы по производству CDX-110 и технология приготовления лекарственного средства имели несколько препятствий для использования в коммерческих условиях. Например, такие недостатки включали отсутствие полной растворимости линкера (СМЦК), что приводило в результате к реакции, которую трудно контролировать; неприемлемые уровни примесей внутри процесса; методологию процесса, которая не поддается масштабированию; отсутствие достаточного контроля основных биофизических характеристик, таких как соотношение пептид:ГЛУ-носитель, неоднородность размера, образование геля и частиц, и нестабильность продуктов. ГЛУ представляет собой очень большой белок-носитель, который ранее продемонстрировал большие трудности в конъюгации и составлении рецептуры в соответствии с высокими фармацевтическими стандартами. Соответственно, существует необходимость совершенствования способов производства и технологии приготовления лекарственного средства, которые обеспечивают композиции ГЛУ-пептидных конъюгатов, которые направлены на устранение этих недостатков.
СУЩНОСТИ ИЗОБРЕТЕНИЯ
Другие особенности и преимущества настоящего раскрытия будут видны из последующего подробного описания и примеров, которые не должны рассматриваться как ограничивающие. Содержание всех ссылок, фигур, записей GenBank, патентов и опубликованных патентных заявок, цитированных напротяжении всего текста настоящего описания, в точности введено в настоящее изобретение с помощью ссылки во всей их полноте.
В одном аспекте раскрытие обеспечивает композицию, включающую ГЛУ-пептидный конъюгат, калий-фосфатный буфер, дисахарид, а также поверхностно-активное вещество. В одном из вариантов воплощения калий-фосфатный буфер присутствует в концентрации в диапазоне от 5 мМ до 30 мМ, например, от 5 мМ до 20 мМ, от 5 мМ до 15 мМ, от 7 мМ до 13 мМ, от 8 мМ до 12 мМ, от 9 мМ до 11 мМ или от 9,5 мМ до 10,5 мМ. В другом варианте воплощения калий-фосфатный буфер присутствует в концентрации, равной 10 мМ. В дополнительном варианте воплощения калий-фосфатный буфер присутствует в такой концентрации, как после хранения в течение 12 недель при температуре 40°C, концентрация ГЛУ-пептидного конъюгата в указанной композиции, измеренная в мг/мл, изменилась менее чем на 15% по сравнению с исходной концентрацией.
В дополнительном варианте воплощения дисахарид в композиции представляет собой трегалозу. В одном варианте воплощения трегалоза присутствует в концентрации в диапазоне от 45 мг/мл до 150 мг/мл, от 70 мг/мл до 120 мг/мл, от 80 мг/мл до 100 мг/мл или от 85 мг/мл до 95 мг/мл. В другом варианте воплощения трегалоза присутствует в концентрации, равной 90 мг/мл. В другом варианте воплощения трегалоза присутствует в такой концентрации, как после хранения в течение 12 недель при температуре 40°C, концентрация ГЛУ-пептидного конъюгата в указанной композиции, измеренная в мг/мл, изменилась менее чем на 15% по сравнению с исходной концентрацией.
В дополнительном варианте воплощения поверхностно-активное вещество в композиции представляет собой полисорбат 80. Например, в одном варианте воплощения полисорбат 80 присутствует в концентрации в диапазоне от 0,01 мг/мл до 0,3 мг/мл, от 0,05 мг/мл до 0,25 мг/мл, от 0,1 мг/мл до 0,25 мг/мл или от 0,15 мг/мл до 0,25 мг/мл. В одном варианте воплощения полисорбат 80 присутствует в концентрации, равной 0,2 мг/мл. В дополнительном варианте воплощения полисорбат 80 присутствует в такой концентрации, как после хранения в течение 12 недель при температуре 40°C, концентрация ГЛУ-пептидного конъюгата в указанной композиции, измеренная в мг/мл, изменилась менее чем на 15% по сравнению с исходной концентрацией.
В одном аспекте настоящее раскрытие обеспечивает любые композиции, как описано выше, в которых пептид, конъюгированный с ГЛУ в ГЛУ-пептидном конъюгате, включает, состоит в основном из или состоит из SEQ ID №:1. В дополнительном варианте воплощения пептид, конъюгированный с ГЛУ в ГЛУ-пептидном конъюгате, включает, состоит в основном из или состоит из SEQ ID №:2. В одном варианте воплощения пептид, конъюгирован с ГЛУ сульфо-СМЦК линкером.
В одном аспекте настоящее раскрытие обеспечивает любую из ГЛУ-пептидных композиций, описанных здесь, в которой плотность эпитопа находится в диапазоне от 20 до 80. Например, в одном варианте воплощения плотность эпитопа находится в диапазоне от 25 до 75, от 25 до 70, от 25 до 65, от 30 до 60, от 30 до 55, от 35 до 50, от 40 до 50. В дополнительном варианте воплощения плотность эпитопа составляет 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59 или 60.
В дополнительном аспекте настоящее раскрытие обеспечивает любую из композиций, описанных здесь, в которой количество ГЛУ-пептидного конъюгата, присутствующего в форме димера находится в диапазоне от 45 масс.% до 65 масс.% от общей массы композиции, как определено посредством гель-фильтрационной хроматографии. Например, в одном варианте воплощения количество в форме димера находится в диапазоне от 50 масс.% до 60 масс.%, от 51 масс.% до 59 масс.%, от 52 масс.% до 58 масс.%, от 53 масс.% до 57 масс.% или от 54 масс.% до 56 масс.%. В дополнительном варианте воплощения количество ГЛУ-пептидного конъюгата в форме димера составляет 50 масс.%, 51 масс.%, 52 масс.%, 53 масс.%, 54 масс.%, 55 масс.%, 56 масс.%, 57 масс.%, 58 масс.%, 59 масс.% или 60 масс.% от общей массы композиции, как определено посредством гель-фильтрационной хроматографии. В дополнительном варианте воплощения количество ГЛУ-пептидного конъюгата в форме димера составляет более чем 80 масс.% по массе от общей массы композиции, как определено посредством гель-фильтрационной хроматографии. Например, в одном варианте воплощения количество в форме димера составляет более чем 85 масс.%, более чем 90 масс.%, более чем 95 масс.%, более чем 96 масс.%, более чем 97 масс.%, более чем 98 масс.% или более чем 99 масс.%.
В дополнительном аспекте настоящее раскрытие обеспечивает любую из композиций, описанных в настоящем документе, в которой, когда она подвергается гель-фильтрационной хроматографии с определением УФ-поглощения, пик, соответствующий форме димера в ГЛУ-пептидном конъюгате, составляет от 45% до 65% от общей площади под кривой. Например, в одном варианте воплощения пик, соответствующий форме димера, составляет от 50% до 60%, от 51% до 59%, от 52% до 58%, от 53% до 57% или от 54% до 56% от общей площади под кривой. В дополнительном варианте воплощения пик, соответствующий форме димера, составляет 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59% или 60% от общей площади под кривой. В дополнительном варианте воплощения пик, соответствующий форме димера, составляет более чем 80% от общей площади под кривой. Например, в одном варианте воплощения пик, соответствующий форме димера, составляет более чем 85%, более чем 90%, более чем 95%, более чем 96%, более чем 97%, более чем 98% или более чем 99% от общей площади под кривой.
В дополнительном аспекте настоящее раскрытие обеспечивает любую из композиций, описанных здесь, в которой количество ГЛУ-пептидного конъюгата, присутствующего в форме мономера, находится в диапазоне от 15 масс.% до 40 масс.% от общей массы композиции, как определено посредством гель-фильтрационной хроматографии. Например, в одном варианте воплощения форма димера находится в диапазоне от 20 масс.% до 35 масс.%, от 21 масс.% до 34 масс.%, от 22 масс.% до 33 масс.%, от 23 масс.% до 32 масс.%, от 24 масс.% до 31 масс.% или от 25 масс.% до 30 масс.%. В дополнительном варианте воплощения количество ГЛУ-пептидного конъюгата в форме мономера составляет18 масс.%, 19 масс.%, 20 масс.%, 21 масс.%, 22 масс.%, 23 масс.%, 24 масс.%, 25 масс.%, 26 масс.%, 27 масс.%, 28 масс.%, 29 масс.% или 30 масс.% от общей массы композиции, как определено посредством гель-фильтрационной хроматографии. В дополнительном варианте воплощения количество ГЛУ-пептидного конъюгата в форме мономера составляет более чем 80 масс.% от общей массы композиции, как определено посредством гель-фильтрационной хроматографии. Например, в одном варианте воплощения количество формы мономера составляет более чем 85 масс.%, более чем 90 масс.%, более чем 95 масс.%, более чем 96 масс.%, более чем 97 масс.%, более чем 98 масс.% или более чем 99 масс.%.
В дополнительном аспекте настоящее раскрытие обеспечивает любую из композиций, описанных здесь, в которой, когда она подвергается гель-фильтрационной хроматографии с определением УФ-поглощения, пик, соответствующий форме мономера ГЛУ-пептидного конъюгата, составляет от 15% до 40% от общей площади под кривой. Например, в одном варианте воплощения пик, соответствующий форме мономера, составляет от 20% до 35%, от 21% до 34%, от 22% до 33%, от 23% до 32%, от 24% до 31% или от 25% до 30% от общей площади под кривой. В дополнительном варианте воплощения пик, соответствующий форме мономера, составляет 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29% или 30% от общей площади под кривой. В дополнительном варианте воплощения пик, соответствующий форме мономера, составляет более чем 80% от общей площади под кривой. Например, в одном варианте воплощения пик, соответствующий форме мономера, составляет более чем 85%, более чем 90%, более чем 95%, более чем 96%, более чем 97%, более чем 98% или более чем 99% от общей площади под кривой.
Настоящее раскрытие дополнительно обеспечивает любую из композиций ГЛУ-пептидного конъюгата, описанную здесь, где композиция представляет собой водную фармацевтическую композицию. В одном варианте воплощения уровень pH вышеупомянутой композиции находится в диапазоне от 6 до 8. В дополнительном варианте воплощения уровень pH композиции находится в диапазоне от 6,5 до 7,5. В дополнительном варианте воплощения уровень pH композиции составляет 6,5, 6,6, 6,7, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4 или 7,5. В дополнительном варианте воплощения уровень pH представляет собой такое значение, как после хранения в течение 12 недель при температуре 40°C, концентрация ГЛУ-пептидного конъюгата в указанной композиции, измеренная в мг/мл, изменилась менее чем на 15% по сравнению с исходной концентрацией.
В дополнительном аспекте настоящее раскрытие обеспечивает жидкую композицию, содержащую ГЛУ-пептидный конъюгат, калий-фосфатный буфер, трегалозу и полисорбат 80, где: пептид, конъюгированный с ГЛУ, включает, состоит в основном из или состоит из SEQ ID №:1 или SEQ ID №:2; ГЛУ-пептидный конъюгат имеет плотность эпитопа в диапазоне от 30 до 65; буфер присутствует в концентрации в диапазоне от 9 мМ до 11 мМ; уровень pH композиции находится в диапазоне от 7,3 до 7,5; трегалоза присутствует в концентрации в диапазоне от 85 мг/мл до 95 мг/мл; полисорбат 80 присутствует в концентрации в диапазоне от 0,1 мг/мл до 0,3 мг/мл; и где дополнительно количество ГЛУ-пептидного конъюгата, присутствующего в форме мономера, находится в диапазоне от 18 масс.% до 35 масс.% от общей массы композиции, а количество ГЛУ-пептидного конъюгата, присутствующего в форме димера, находится в диапазоне от 50 масс.% до 65 масс.% от общей массы композиции, как определено посредством гель-фильтрационной хроматографии. Например, в одном варианте воплощения буфер присутствует в концентрации, равной 10 мМ, уровень pH композиции составляет 7,4, трегалоза присутствует в концентрации, равной 90 мг/мл, и полисорбат 80 присутствует в концентрации, равной 0,2 мг/мл. Более того, например, вышеупомянутая жидкая композиция была подготовлена путем восстановления лиофилизированной композиции при помощи воды.
Настоящее раскрытие дополнительно обеспечивает лиофилизированную композицию, включающую, состоящую в основном из или состоящую из ГЛУ-пептидного конъюгата, калий-фосфатного буфера, дисахарида и поверхностно-активного вещества. В одном варианте воплощения вышеупомянутая лиофилизированная композиция, при восстановлении при помощи воды, имеет уровень pH в диапазоне от 6 до 9. В одном варианте воплощения дисахарид представляет собой трегалозу, а поверхностно-активное вещество представляет собой полисорбат 80. В дополнительном варианте воплощения трегалоза присутствует в количестве в диапазоне от 80 мг до 110 мг на мг ГЛУ-пептидного конъюгата; и полисорбат 80 присутствует в количестве в диапазоне от 0,01 до 0,3 мг на мг ГЛУ-пептидного конъюгата. В дополнительном варианте воплощения трегалоза присутствует в количестве, равном 90 мг на мг ГЛУ-пептидного конъюгата; а полисорбат 80 присутствует в количестве, равном 0,2 мг на мг ГЛУ-пептидного конъюгата.
В одном аспекте раскрытие обеспечивает жидкую композицию, содержащую ГЛУ-EGFRvIII конъюгат, где после хранения в течение 12 недель при температуре 40°C концентрация вышеназванного конъюгата в указанной жидкой композиции, измеренная в мг/мл, изменилась менее чем на 15%, менее чем на 13%, менее чем на 11%, менее чем на 10%, менее чем на 8% или менее чем на 5% по сравнению с исходной концентрацией.
В дополнительном аспекте раскрытие обеспечивает способы уменьшения аномального роста клеток у млекопитающих, нуждающихся в этом, включающие этап введения указанному млекопитающему любой композиции, описанной здесь. В одном варианте воплощения аномальный рост клеток является раковым. В дополнительном варианте воплощения рак представляет собой глиобластому.
В дополнительном аспекте раскрытие обеспечивает способы уменьшения аномального роста клеток у млекопитающих, нуждающихся в этом, включающие этапы: a) смешивание любой композиции, описанной здесь, с адъювантом и b) введение указанному млекопитающему полученной в результате смеси. В дополнительном аспекте раскрытие обеспечивает способы уменьшения аномального роста клеток у млекопитающих, нуждающихся в этом, включающие введение любой композиции, описанной здесь, в комбинации по меньшей мере с одним адъювантом. В одном варианте воплощения адъювант представляет собой гранулоцитарно-макрофагальный колониестимулирующий фактор.
Настоящее раскрытие дополнительно обеспечивает способы уменьшения аномального роста клеток у млекопитающих, нуждающихся в этом, включающие: a) предоставление любой из лиофилизированных композиций, описанных здесь, b) добавление воды в лиофилизированную композицию для того, чтобы обеспечить восстановленную композицию и c) введение указанному млекопитающему восстановленной композиции.
Настоящее раскрытие дополнительно обеспечивает способы уменьшения аномального роста клеток у млекопитающих, нуждающихся в этом, включающие: a) предоставление любой из лиофилизированных композиций, описанных здесь, b) добавление воды в лиофилизированную композицию для того, чтобы обеспечить восстановленную композицию, c) смешивание восстановленной композиции с адъювантной композицией и d) введение указанному млекопитающему полученной в результате смеси. В одном варианте воплощения указанный адъювант представляет собой гранулоцитарно-макрофагальный колониестимулирующий фактор.
Настоящее раскрытие дополнительно обеспечивает использование любой из композиций, описанных здесь, в производстве лекарственного средства для лечения аномального роста клеток у млекопитающих.
Настоящее раскрытие дополнительно обеспечивает способы получения лиофилизированной композиции, включающей ГЛУ-пептидный конъюгат, включающий подвергание любой из жидких композиций, описанных здесь, воздействию температуры равной -20°C или ниже, -30°C или ниже, -40°C или ниже, -50°C или ниже или-60°C или ниже, и воздействию условий вакуума.
Настоящее раскрытие дополнительно обеспечивает способы получения жидких композиций, включающие добавление воды к любой из лиофилизированных композиций, описанных здесь.
Настоящее раскрытие дополнительно обеспечивает способы приготовления ГЛУ-EGFRvIII конъюгата, включающие: a) объединение ГЛУ с линкером и предоставление возможности ГЛУ и линкеру взаимодействовать на протяжении периода времени в диапазоне от 30 до 60 минут, от 35 до 55 минут, от 40 до 50 минут или 45 минут; и b) добавление пептида, включающего, состоящего в основном из или состоящего из SEQ ID №:1 или SEQ ID №:2, к активированному продукту ГЛУ, полученному в результате этапа a), чтобы предоставить ГЛУ-EGFRvIII конъюгат. В одном варианте воплощения этап b) осуществляется в системе фильтрации в тангенциальном потоке. В дополнительном варианте воплощения скорость течения ретентата находится в диапазоне от 10 мл/мин до 1000 мл/мин, например, от 50 мл/мин до 500 мл/мин, например, от 100 мл/мин до 500 мл/мин, и далее, например, 50 мл/мин, 100 мл/мин, 150 мл/мин, 200 мл/мин, 250 мл/мин, 300 мл/мин, 350 мл/мин, 400 мл/мин, 450 мл/мин или 500 мл/мин.
В одном варианте воплощения линкер объединяют с ГЛУ в молярном соотношении линкер:ГЛУ, которое находится в диапазоне от 75:1 до 325:1. Например, в одном варианте воплощения вышеупомянутое молярное соотношение линкер:ГЛУ находится в диапазоне от 100:1 до 300:1, от 150:1 до 250:1 или от 175:1 до 225:1. Например, в одном варианте воплощения вышеупомянутое молярное соотношение линкер:ГЛУ составляет 175:1, 180:1, 185:1, 190:1, 195:1, 200:1, 205:1, 210:1, 215:1, 220:1 или 225:1.
Настоящее раскрытие дополнительно обеспечивает жидкую композицию, содержащую ГЛУ-EGFRvIII-конъюгат, где после хранения в течение 26 недель при температуре 5°C число частиц по размеру больше или равных 10 мкм, как измерено согласно USP <788>, увеличилось менее чем на1000%, менее чем на 750%, менее чем на 500%, менее чем на 400%, менее чем на 300%, менее чем на 200% или менее чем на 100%.
Настоящее раскрытие дополнительно обеспечивает жидкую композицию, содержащую ГЛУ-EGFRvIII-конъюгат, где после хранения в течение 26 недель при температуре 5°C число частиц по размеру больше или равных 25 мкм, как измерено согласно USP <788>, увеличилось менее чем на 1000%, менее чем на 750%, менее чем на 500%, менее чем на 400%, менее чем на 300%, менее чем на 200% или менее чем на 100%.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
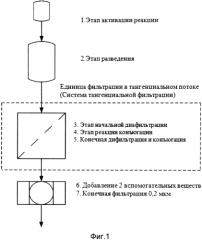
Фигура 1 демонстрирует общую схему процесса одного из примеров проведения реакции конъюгации ГЛУ-пептида.
Фигура 2A демонстрирует краткое изложение ключевых рабочих параметров, используемых в ходе реакции активации в различных экспериментах поперечного потока.
Фигура 2B демонстрирует краткое изложение ключевых рабочих параметров, используемых в ходе этапа начальной диафильтрации в различных экспериментах поперечного потока.
Фигура 2C демонстрирует краткое изложение ключевых рабочих параметров, используемых в ходе этапа конъюгации в различных экспериментах поперечного потока.
Фигуры 3A, 3B, 3C и 3D демонстрируют краткое изложение аналитических результатов для экспериментов фильтрации в поперечном потоке.
Фигуры 4A, 4B и 4C демонстрируют краткое изложение реакционных параметров, которые использовались в различных экспериментах.
Фигура 5 демонстрирует репрезентативную ГФХ ВЭЖХ хроматограмму для конъюгата CDX-110 ГЛУ-EGFRvIII, показывающую примерное время удержания пяти пиков.
Фигура 6 демонстрирует график, показывающий влияние соотношения сульфо-СМЦК на плотность эпитопа.
Фигура 7 демонстрирует график, показывающий влияние времени активации на плотность эпитопа.
Фигуры 8A (димер) и 8B (мономер) демонстрируют графики, показывающие влияние соотношения сульфо-СМЦК на гетерогенность ГФХ.
Фигуры 9A (димер) и 9B (мономер) демонстрируют графики, показывающие влияние времени активации на гетерогенность ГФХ.
Фигура 10 демонстрирует сравнение плотности эпитопа при использовании суспензии линкера и растворенного в ДМСО линкера.
Фигуры 11A (димер) и 11B (мономер) демонстрируют графики, показывающие влияние ДМСО на профиль ГФХ реакции активации.
Фигуры 12A и 12B демонстрируют статистический анализ результатов плотности эпитопа, показывающий взаимодействие соотношения сульфо-СМЦК:ГЛУ и концентрации белка.
Фигуры 13A и 13B демонстрируют статистический анализ результатов димера, показывающий взаимодействие соотношения сульфо-СМЦК:ГЛУ и концентрации белка.
Фигура 14 демонстрирует краткое изложение реакционных параметров, используемых для оригинального и оптимизированного процесса приготовления CDX-110.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее раскрытие основывается на открытии новых композиций ГЛУ-пептидных конъюгатов, которые обеспечивают полезные свойства, такие как снижение образования частиц и геля и повышение стабильности конъюгата. Композиции, описанные здесь, могут быть лиофилизированы и восстановлены, обеспечивая дополнительные преимущества для транспортировки и длительного хранения. Такие полезные свойства и другие, которые будут очевидны специалистам в данной области техники, описаны здесь более подробно. Более того, в соответствии с настоящим раскрытием было разработано улучшение процессов для производства вакцин ГЛУ-EGFRvIII-пептидного конъюгата. Новые процессы, описанные здесь, обеспечивают оптимальные условия реакции, которые подчиняются крупномасштабным производственным протоколам и которые в результате приводят к улучшению профиля чистоты и контроля основных биофизических характеристик, таких как соотношение пептидов/ГЛУ и гетерогенность размера.
Для того, чтобы настоящее раскрытие могло быть более понятным, некоторые термины вначале определены. Дополнительные определения приведены на протяжении всего текста подробного описания изобретения.
Если здесь не оговорено иначе, научные и технические термины, используемые в связи с настоящим изобретением, должны иметь значения, которые обычно понимаются обычными специалистами в данной области. Кроме того, если по контексту не требуется иначе, термины в единственном числе должны включать формы во множественном числе, а термины во множественном числе должны включать формы единственного числа. Как правило, использованная номенклатура и описанные здесь технические приемы, касающиеся выращивания клеток и ткани, молекулярной биологии, иммунологии, микробиологии, генетики и химии, и гибридизации белков и нуклеиновых кислот, являются общеизвестными и обычно используемыми в данной области техники.
Способы и технические приемы, согласно настоящему изобретению, обычно выполняются в соответствии со стандартными способами, общеизвестными в данной области и как описано в различных общих и более специфических ссылках, которые цитируются и рассматриваются в настоящем описании, если не указано иначе. Такие ссылки включают, например, Sambrook and Russell, Molecular Cloning, A Laboratory Approach, Cold Spring Harbor Press, Cold Spring Harbor, NY (2001), Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, NY (2002), and Harlow and Lane Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY (1990). Ферментативные реакции и технические приемы по очистке проводят согласно инструкциям производителя, как обычно выполняется в данной области или как описано здесь. Использованная номенклатура, лабораторные методики и технические приемы, касающиеся аналитической химии, синтетической органической химии и медицинской, и фармацевтической химии, описанные здесь, являются общеизвестными и обычно используемыми в данной области техники. Стандартные способы применяются для химического синтеза, химического анализа, фармацевтического изготовления, разработки состава и доставки, и лечения пациентов.
Как используется здесь, каждый из следующих терминов имеет значение, связанное с ним в этом разделе.
Неопределенные артикли и формы единственного числа используются в документе для обозначения одного или нескольких (то есть по меньшей мере одного) грамматического объекта статьи. К примеру, "элемент" означает один элемент или более одного элемента.
Используемые здесь двадцать главных аминокислот и их аббревиатуры имеют общепринятое использование. См. публикацию Immunology - A Synthesis (2nd Edition, E.S. Golub and D.R Gren, Eds., Sinauer Associates, Sunderland, Mass. (1991)).
Используемый в данном описании термин "ГЛУ" относится к белку гемоцианину лимфы улитки, состоящему из множества субъединиц, переносящему кислород металлопротеину, обнаруженному в гемолимфе улиток (Megathura crenulata), или к его фрагменту или субъединице.
Используемый здесь термин "ГЛУ-пептидный конъюгат" относится к ГЛУ белку или к его фрагменту или субъединице, который ковалентно связан с полипептидом, не имеющим отношения к ГЛУ. Такая ковалентная связь, как правило, достигается за счет использования соответствующего химического линкера.
Используемый здесь термин "плотность эпитопа", со ссылкой на ГЛУ-пептидный конъюгат, относится к среднему число пептидов, которые связаны с каждой субъединицей ГЛУ. Плотность эпитопа можно определить с помощью анализа аминокислотной композиции, как описано здесь.
Термин "дисахарид", используемый здесь, относится к соединению, которое после гидролиза дает две моносахаридные молекулы (например, глюкозы, фруктозы, маннозы и др.). Подходящие дисахариды включают, не ограничиваясь этим, сахарозу, лактозу и трегалозу.
Используемый здесь термин "поверхностно-активное вещество" относится к вспомогательному веществу, которое может изменять поверхностное натяжение жидкой композиции ГЛУ-пептидного конъюгата. Как указывается далее здесь, примеры поверхностно-активных веществ включают, не ограничиваясь этим, полисорбатные поверхностно-активные вещества, полоксамеры (например, полоксамер 18 и 407), тритонные поверхностно-активные вещества, такие как Тритон Х-100®, а также полисорбатные поверхностно-активные вещества, такие как Твин 20® и Твин 80®, среди многих других, которые известны специалистам в данной области техники.
Термины "лиофилизация", "лиофилизированный" и "сублимированный" относятся к процессу, при помощи которого материал, который должен быть высушен, сначала замораживают, а затем удаляют лед или замороженный растворитель при помощи сублимации в вакуумной среде.
Используемый здесь термин "EGFRvIII" относится к пептиду, который является представителем варианта мутанта III, который присутствует в рецепторе эпидермального фактора роста РЭФР, и обычно включает в себя или состоит из аминокислотной последовательности, изложенной как SEQ ID №:1 или 2 или по меньшей мере включает аминокислотную последовательность "Lys-Lys-Gly-Asn-Tyr".
Термин "аномальный рост клеток", используемый в данном описании, если не указано иное, относится к росту клеток, который является независимым от нормальных регуляторных механизмов (например, потеря контактного ингибирования), в том числе к аномальному росту нормальных клеток и росту аномальных клеток. Этот термин включает, не ограничиваясь этим, аномальный рост: опухолевых клеток (опухолей), например, мезотелиомы, гепатобилиарной опухоли (печеночной и желчевыводящих протоков), первичных или вторичных опухолей ЦНС (центральной нервной системы), первичных или вторичных опухолей головного мозга, рака легких (немелкоклеточного рака легких (НМРЛ) и мелкоклеточного рака легких (МРЛ)), рака костей, рака поджелудочной железы, рака кожи, рака головы и шеи, кожной или внутриглазной меланомы, рака яичников, рака толстой кишки, рака прямой кишки, рака анальной области, рака желудка, желудочно-кишечного тракта (желудка, толстой кишки, и двенадцатиперстной кишки), рака молочной железы, рака матки, рака фаллопиевых труб, рака эндометрия, рака шейки матки, рака влагалища, рака вульвы, болезни Ходжкина, рака пищевода, рака тонкого кишечника, рака эндокринной системы, рака щитовидной железы, рака паращитовидных желез, рака надпочечников, саркомы мягких тканей, рака уретры, рака полового члена, рака предстательной железы, тестикулярного рака, хронического или острого лейкоза, хронического миелоидного лейкоза, лимфоцитарной лимфомы, рака мочевого пузыря, рака почек или мочеточников, почечно-клеточной карциномы, рака почечной лоханки, опухолей центральной нервной системы (ЦНС), первичной лимфомы ЦНС, неходжкинской лимфомы, опухолей спинальной оси, глиомы ствола головного мозга, аденомы гипофиза, рака коры надпочечников, рака желчного пузыря, множественной миеломы, холангиокарциномы, фибросаркомы, нейробластомы, ретинобластомы или комбинации из одного или более вышеназванных видов рака.
Используемый здесь термин "лечебный" или "лечение" относится как к терапевтическому лечению, так и к профилактическим или превентивным мерам, где есть объект для предотвращения или замедления (уменьшения) целевого патологического состояния или состояний. Те, кто нуждаются в лечении, включают тех, у кого уже существует указанное состояние, а также тех, которые предрасположены иметь это состояние, или тех, у кого такое состояние должно быть предотвращено.
Термин "терапевтически эффективное количество" композиции относится к количеству, которое является эффективным в дозировках и в течение периодов времени, необходимых для достижения желаемого терапевтического результата, который включает лечение или профилактическое предупреждение аномального роста клеток. Следует отметить, что значения дозы могут изменяться в зависимости от тяжести состояния, которое должно быть облегчено. В дальнейшем необходимо понимать, что для любого конкретного субъекта, конкретные схемы дозирования должны быть скорректированы с течением времени, в зависимости от индивидуальных потребностей и профессиональной оценки лица, которое вводит или осуществляет контроль за введением композиций, и что диапазоны доз, изложенные здесь, являются только иллюстративными и не предназначены для ограничения объема или осуществления заявленной композиции. Аналогично терапевтически эффективное количество композиции может варьироваться в зависимости от таких факторов как состояние заболевания, возраст, пол и масса индивидуума, способности терапевтической композиции вызвать желаемый ответ у индивидуума и желаемого пути введения. Терапевтически эффективное количество также является таким, в котором терапевтически благоприятное воздействие превосходит любые токсичные или нежелательные эффекты композиции.
Термин "фармацевтическая композиция" относится к лекарственным средствам, которые находятся в такой форме, которая позволяет биологической активности действующих веществ быть эффективной.
"Фармацевтически приемлемыми вспомогательными веществами" (транспортными средствами, добавками) являются те, которые могут быть введены разумно (т.е. безопасно) субъекту, чтобы обеспечить эффективную дозу применяемого активного ингредиента. Термин "вспомогательное вещество" или "носитель", используемый здесь, относится к инертному веществу, которое обычно используется в качестве растворителя, транспортного средства, консерванта, связующего вещества или стабилизирующего вещества для лекарственных средств. Используемый здесь термин "разбавитель" относится к фармацевтически приемлемому (безопасному и нетоксичному при введении человеку) растворителю и является пригодным для приготовления жидких лекарственных форм, описанных здесь. Примерные растворители включают, не ограничиваясь этим, стерильную воду и бактериостатическую воду для инъекций (БВДИ).
Если не указано иное, концентрации и значения рН различных компонентов композиции, описанные здесь, представляют собой концентрации в условиях окружающей среды (т. е. при температуре 25°С и атмосферном давлении). Когда концентрации и значения рН находятся в диапазонах, перечисленных здесь, такие диапазоны, которые занимают промежуточное положение в подробно процитированных диапазонах, также предназначены для того, чтобы быть частью настоящего раскрытия. Например, диапазоны значений, использующие комбинацию любого из значений как верхнего, так и/или нижнего пределов предназначены для включения.
В соответствии с настоящим раскрытием было обнаружено, что для ГЛУ-пептидного конъюгата формирование частиц и/или геля может быть уменьшено, и стабильность конъюгата может быть улучшена путем объединения конъюгата с калий-фосфатным буфером, дисахаридом, таким как трегалоза, и поверхностно-активным веществом, таким как Твин 80. Более того, было обнаружено, что когда эти компоненты используются в определенных количествах, становится возможной лиофилизация (с последующим восстановлением в виде водного раствора) и одновременная минимизация формирования частиц и геля, и поддержание стабильности и биофизических характеристик конъюгата.
Не желая быть связанными какой-либо конкретной теорией, предполагается, что композиции настоящего раскрытия способствуют повышению стабильности и уменьшению формирования твердых частиц и/или геля ГЛУ-пептидных конъюгатов путем уменьшения частоты одного или нескольких из перечисленного: ГЛУ-пептидной агрегации, фрагментации, окисления, нестабильности замораживания/оттаивания, нестабильности, связанной с доставкой или транспортировкой из одного места в другое, изменения цвета и/или деамидирования. Таким образом, настоящее раскрытие обеспечивает композиции ГЛУ-пептидного конъюгата, обладающие улучшенной химической и/или физической стабильностью по сравнению с ранее раскрытыми композициями.
Таким образом, в некоторых аспектах настоящее раскрытие обеспечивает композицию, включающую ГЛУ-пептидный конъюгат, калий-фосфатный буфер, дисахарид, а также поверхностно-активное вещество. В других аспектах вышеупомянутая композиция может включать в себя дополнительные фармацевтически приемлемые вспомогательные вещества, в том числе, но не ограничиваясь этим, буферы, соли, антиоксиданты, вещества для тоничности, поверхностно-активные вещества и их смеси. Таким образом, данное раскрытие предлагает новые композиции для ГЛУ-пептидных конъюгатов.
ГЛУ-пептидные конъюгаты
ГЛУ представляет собой комплексный мультимерный белок, который может быть использован в качестве носителя для антигенных пептидов. Такие пептиды могут быть конъюгированными с ГЛУ, а полученный в результате ГЛУ-пептидный конъюгат может быть использован в качестве вакцины для стимулирования иммунного ответа, направленного на антигенный пептид.
В одном аспекте раскрытия антигенный пептид конъюгирован с ГЛУ путем химического поперечного сшивания, обычно с использованием гетеробифункционального поперечносшивающего линкера. Несколько гетеро-бифункциональных поперечно сшивающих линкеров известны в данной области техники. В некоторых вариантах воплощения гетеро-бифункциональный поперечно сшивающий линкер содержит функциона