Способ нейтронно-фотонной терапии больных раком молочной железы
Иллюстрации
Показать всеИзобретение относится к медицине, лучевой терапии в онкологии. Для получения оптимального терапевтического эффекта при местнораспространенном раке молочной железы комбинируют нейтронную и фотонную терапию, где нейтронная терапия предшествует курсу фотонной. Молочную железу локализуют с помощью болюса из тканеэквивалентного материала в виде прозрачных пластин с возможностью изменения и фиксации расстояния между ними. Далее ежедневно проводят облучение нейтронами дозой от 0,2 до 0,4 Гр до СОД 2,0 Гр. Затем проводят гамма-облучение дозой от 1,0 до 2,0 Гр за один сеанс до СОД от 45 до 47 Гр. Способ обеспечивает полную регрессию опухоли при отсутствии лучевых осложнений за счет расширения и оптимизации режимов и доз сочетанного лучевого воздействия со снижением лучевой нагрузки при сохранении высокой эффективности терапии, включающей вклад нейтронов в облучение 17-30%. 3 пр., 3 ил., 2 табл.
Реферат
Изобретение относится к медицине, а именно к лучевой терапии. Предложенный метод может быть использован при сочетанной нейтронно-фотонной терапии злокачественных новообразований, в частности местнораспространенных форм рака молочной железы.
Разнообразие способов лечения местнораспространенных форм рака молочной железы (МРРМЖ), когда используются многокомпонентные схемы лечения с неоадъювантной и адъювантной химиотерапией в сочетании с предоперационными курсами лучевой терапии быстрыми электронами, тормозным или гамма-излучением, изложено в работе Харченко В.П., Паньшин Г.А., Хмелевский Е.В. Многокомпонентные схемы лечения операбельного местнораспространенного рака молочной железы // Проблемы современной онкологии. Тез. докладов IV Всероссийского съезда онкологов. - Ростов-на-Дону, 1995. В приведенных схемах лечения указан процент (9,4%) местно-регионарных рецидивов в результате использования редкоионизирующего фотонного излучения при местнораспространенных формах рака молочной железы.
Известен способ нейтронной терапии больных с местно-распространенными и неоперабельными опухолями молочной железы [Catterall М., Errington R.D., Bewley D.K. Fast neutrons in the treatment of locally advanced breast cancer. // Eur. J. Surg. Oncol. - 1987, Aug. - V. 13. - No 4. - P. 315-319]. В рассматриваемом способе проводили облучение молочной железы нейтронами циклотрона со средней энергией 8 МэВ, используя большие размеры полей облучения, от 10×10 до 16×16 см2 и тангенциальное направление пучка нейтронов. Нейтронную терапию проводили за 12 сеансов в течение 26-28 дней. Разовая очаговая доза (РОД) нейтронов варьировала от 1 до 2,5 Гр, суммарная очаговая доза (СОД) между 13,3 и 25,3 Гр. Нейтронная терапия привела к полной регрессии опухолей в 95% случаев.
Недостатком способа лечения были выраженные ранние лучевые реакции кожи - влажный эпидермит. У трех пациенток из 17 имели место некротические поражения кожи. Причиной осложнений были высокие дозы нейтронов и недостаточно адекватное физическое сопровождение нейтронной терапии.
Известен способ комбинированного лечения местнораспространенных форм РМЖ T3-4N1-3M0 с использованием гамма-нейтронной терапии: быстрыми нейтронами 1,0 МэВ реактора БР-1O, РОД - 0,2 Гр (ОБЭ-5) (ОБЭ - относительная биологическая эффективность), 5 раз в неделю, СОД - 2,0 Гр и гамма-излучением РОД - 1,0 Гр на патологический очаг и зоны лимфооттока, с двухнедельным перерывом в середине курса лечения, до суммарной дозы 50 Гр и последующей операцией [Кузин А.Н. Гамма-нейтронная терапия в комплексном лечении местнораспространенных форм рака молочной железы // Труды Всесоюзной конф. "Быстрые нейтроны в лучевой терапии злокачественных опухолей". - Томск, 1992. - С. 122-124].
Недостатком данного способа является длительность курса лучевой терапии, которая составляет, включая 2-недельный перерыв, 1,5-2 месяца. Кроме того, после окончания гамма-нейтронной терапии в 98,2% случаев развивался влажный эпидермит, что препятствовало выполнению операции непосредственно после облучения и увеличивало сроки до начала операции.
Известен способ комбинированного лечения больных местнораспространенными формами рака молочной железы с использованием гамма-нейтронной терапии, когда облучение проводилось в режиме: первая фракция - 1,0 Гр гамма-терапии на патологический очаг, вторая - через 4-5 ч быстрыми нейтронами 0,2 Гр (ОБЭ-5) реактора БР-10 со средней энергией нейтронов 1 МэВ, суммарная очаговая доза - 50 Гр гамма- и 2 Гр нейтронного излучения за 1-1,5 месяца, с последующей операцией [Изотова И.А. Комбинированное лечение больных раком молочной железы с использованием гамма-нейтронной терапии // Проблемы современной онкологии. Тез. докладов IV Всероссийского съезда онкологов. - Ростов-на-Дону, 1995. - С. 1522].
Недостатком данного способа является длительность предоперационного курса облучения, обусловленная использованием методики расщепления разовой очаговой дозы на 2 фракции в день с перерывом в 4-8 ч, что в два раза повышает стоимость предоперационного курса гамма-нейтронной терапии рака молочной железы.
Известен «Способ лечения местнораспространенного рака молочной железы» по патенту RU 2186591. В рассматриваемом способе проводят курс предоперационной нейтронной терапии быстрыми нейтронами со средней энергией 6,3 МэВ разовой очаговой дозой 1,8-2,7 Гр 3-5 фракциями с интервалом 48-72 ч за 8-12 дней. Облучение проводят с двух тангенциальных полей на область молочной железы с опухолевым узлом, размеры которого превышают 9 см в диаметре. Размеры полей облучения варьируют в зависимости от размеров опухолевого узла - от 8·10 см до 10·12 см. Расстояние источник - поверхность (РИП) - 110 см. Величина суммарной дозы предоперационного курса быстрых нейтронов в предлагаемом способе составляет 7,5-9 Гр на молочную железу или 40 Гр·Экв стандартного курса облучения. На следующий день после окончания облучения проводят операцию мастэктомии. В послеоперационном периоде на зоны регионарного метастазирования проводят курс дистанционной гамма-терапии в стандартном режиме до суммарной очаговой дозы 40-45 Гр.
Недостатками данного способа являются высокие дозы нейтронов, которые приводят к поздним лучевым повреждениям в парастернальной области, попадающей в поле облучения.
Прототипом предлагаемого технического решения является способ сочетанной нейтронно-фотонной терапии больных местнораспространенными опухолями молочной железы [J Halpern, М Н Maor, D Н Hussey, G С Henkelmann, V Sampiere, М D McNeese Locally advanced breast cancer treated with neutron beams: long-term follow-up in 28 patients. Int. J. Radiat. Oncol. Biol. Phys 1990; 18(4): 825-31]. В данном способе проводили вначале курс нейтронной терапии в течение 2-х недель - 3 сеанса РОД от 1, 2 до 1,5 Гр в неделю до СОД 7,5-9 Гр, что соответствует 30-36 Гр·Экв (с учетом ОБЭ нейтронов ≈4.0). После завершения нейтронной терапии проводили курс фотонной терапии в стандартном режиме по 2 Гр за сеанс 5 раз в неделю до СОД 62-72 Гр·Экв. Таким образом, вклад нейтронной компоненты в полном курсе радиотерапии составил 50-60%.
Недостатками данного способа являются ранние лучевые реакции и поздние лучевые повреждения, появившиеся у значительного числа больных, что связано с высоким вкладом нейтронов в СОД.
Технический результат предлагаемого изобретения заключается в повышении эффективности (оптимизации) сочетанной нейтрон-фотонной терапии рака молочной железы.
Ключевым моментом в проведении лучевой терапии с использованием излучения, отличающегося от стандартного фотонного излучения (гамма-излучения), является относительная биологическая эффективность нового вида излучения по сравнению с фотонным. Типичная зависимость, представленная на фиг. 3, отражает основные закономерности биологического действия нейтронов: наличие максимума ОБЭ при энергии нейтронов 0,3-0,5 МэВ и возрастание ОБЭ с уменьшением дозы нейтронов (или гамма-излучения, при которой определяют ОБЭ=Dγ/Dn) [Биологические эффекты нейтронов разных энергий / Е.А. Жербин, С.П. Капчигашев., А.Г. Коноплянников и др. М.:, Энергоатомиздат, 1984]. Значения величины клинической ОБЭ для нейтронов используемого терапевтического пучка выбирали на основании величины радиобиологической ОБЭ (Фиг. 3), литературных данных и клинического опыта других онкологических центров, собственных клинических результатов.
Сущность предлагаемого изобретения, включающего сочетанное нейтронно-фотонное облучение молочной железы со злокачественным новообразованием, проводят с использованием болюса, который размещают на облучаемую молочную железу и изменяют конфигурацию органа для формирования оптимального распределения дозы облучения в опухоли. При этом вначале проводят облучение нейтронами в режиме РОД от 0,2 до 0,4 Гр до СОД 2,0-2,5 Гр, а затем проводят курс дистанционной гамма-терапии ежедневно РОД от 1,0 до 2,0 Гр до СОД 45-47 Гр. Величина СОД радикального курса сочетанной нейтронно-фотонной терапии с учетом ОБЭ нейтронов составляет до 60 Гр. При планировании лечения оптимальный вклад нейтронной компоненты с учетом ОБЭ в суммарном курсе сочетанной терапии выбирают от 17 до 30%.
Перечень фигур.
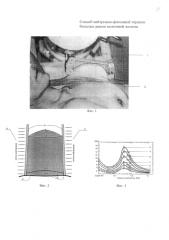
Фиг. 1. Размещение болюса при лечении больной раком молочной железы: 1 - болюс, 2 - молочная железа;
Фиг. 2. Схема распределения дозы нейтронов в области молочной железы: 3, 4 - направления пучка нейтронов, 5 - пластины болюса, 6 - молочная железа, 7 - кривые распределения изодоз нейтронов.
Фиг. 3. Зависимость ОБЭ нейтронов от их энергии по суммарной частоте аберраций хромосом в лимфоцитах человека: 8 - при дозе гамма-излучения 0,25 Гр, 9 - при дозе гамма - излучения 0,50 Гр, 10 - при дозе гамма-излучения 1,0 Гр, 11 - при дозе гамма-излучения 2,0 Гр, 12 - при дозе гамма-излучения 3,0 Гр, 13 - при дозе гамма-излучения 5,0 Гр.
Порядок реализации способа. При выборе курса лечения, как правило, анализируют историю болезни пациентки, планируют условия облучения, выбирая оптимальное соотношение при воздействии нейтронной и фотонной компоненты в суммарную очаговую дозу. Во время подготовки больной к облучению вначале устанавливают специально разработанный нами болюс и формируют поле облучения. Болюс выполнен в виде пластин из тканеэквивалентного прозрачного материала. Расстояние между пластинами регулируют с помощью винтов в соответствии с облучаемым объектом (см. фиг. 1). Он содействует лучшему распределению дозы (см. фиг. 2), а также снижает лозовую нагрузку на поверхность кожи молочной железы и окружающие нормальные ткани.
Облучение больных с первичным МРРМЖ вначале проводят нейтронами в режиме от 0,2 до 0,4 Гр до СОД 2,0-2,5 Гр. При этом разовые дозы делят на 2 равные фракции и облучают молочную железу с обеих сторон с минимальным перерывом между фракциями (<5 мин). После окончания курса нейтронной терапии проводят курс дистанционной гамма-терапии в стандартном режиме 2 Гр 5 раз в неделю до СОД 45-47 Гр. Величина СОД радикального курса сочетанной нейтронно-фотонной терапии с учетом ОБЭ нейтронов составляет до 60 Гр.
Клинические примеры реализации способа
Пример №1
Больная Гур-ва 1934 года рождения. Находилась на лечении в отделении лучевого и хирургического лечения заболеваний торакальной области с диагнозом - рак правой молочной железы T4N2M0 инфильтративно-отечная форма. Проведена подготовительная процедура с болюсом. Радикальный курс нейтронно-фотонной терапии проведен в режиме: облучение молочной железы проводили с обеих сторон нейтронами в РОД 0,2 Гр до СОД 2,0 Гр. После окончания курса нейтронной терапии проводят курс дистанционной гамма-терапии в режиме 2 Гр 5 раз в неделю до СОД 47 Гр. Величина СОД радикального курса сочетанной нейтронно-фотонной терапии с учетом ОБЭ нейтронов составляет до 60 Гр.
После окончании лечения был отмечен влажный эпидермит. Проявившаяся реакция препятствовала выполнению операции непосредственно после облучения. В конечном итоге лечение перенесла удовлетворительно.
Пример №2
Больная Неч-ва 1927 года рождения. Находилась на лечении в отделении лучевого и хирургического лечения заболеваний торакальной области с диагнозом - рак левой молочной железы T4N2M0, инфильтративно-язвенная форма. Проведена подготовительная процедура с болюсом. Радикальный курс нейтронно-фотонной проведен в режиме: облучение молочной железы проводили с обеих сторон нейтронами в РОД 0,4 Гр 5 сеансов в неделю до СОД 2 Гр. После окончания курса нейтронной терапии проводят курс дистанционной гамма-терапии в режиме 2 Гр 5 раз в неделю до СОД 47 Гр. Величина СОД радикального курса сочетанной нейтронно-фотонной терапии с учетом ОБЭ нейтронов составляет до 60 Гр.
По окончании лечения была отмечена 100% регрессия опухоли и регрессия лимфоузлов более чем на 50%. Лечение перенесла удовлетворительно. Через 5 недель после курса нейтронно-фотонной терапии проведена операция радикальной мастэктомии слева. Послеоперационный период без осложнений.
Пример №3
Больная Кут-ва, 1946 года рождения. Находилась на лечении в отделении лучевого и хирургического лечения заболеваний торакальной области с диагнозом - рак левой молочной железы T4N2M0, отечно-инфильтративная форма. Перед сеансом был установлен болюс и сформировано поле облучения опухоли. Облучение проводили с двух сторон в целях уменьшения нагрузки на кожу. При этом разовую дозу облучения делили на две равные доли. Радикальный курс лучевой терапии проведен в режиме: облучение молочной железы нейтронами в РОД 1,0 Гр 3 сеанса в неделю до СОД 3 Гр. После окончания курса нейтронной терапии проводят курс дистанционной гамма-терапии в стандартном режиме 2 Гр 5 раз в неделю до СОД 48 Гр. Величина СОД радикального курса сочетанной нейтронно-фотонной терапии с учетом ОБЭ нейтронов составляет 60 Гр.
По окончании лечения была отмечена 100% регрессия опухоли. Лечение перенесла удовлетворительно.
Через 1 месяц после курса нейтронно-фотонной терапии проведена операция радикальной мастэктомии слева. Послеоперационный период без осложнений. Наблюдается по настоящее время (2014 г.).
Подтверждение достижения технического результата. В работе представлены две группы больных раком молочной железы, получивших сочетанный курс нейтронно-фотонной терапии: 1-ая группа (44 больных) - на первом этапе проводили облучение быстрыми нейтронами в разовой очаговой дозе от 0,2 до 0,4 Гр пять раз в неделю до суммарной очаговой дозы 2,0 Гр. На основе радиобиологических исследований (см. фиг. 3) и клинического опыта ОБЭ нейтронов для данной разовой/ очаговой дозы принимали равным 5. В дальнейшем продолжали облучение молочной железы на гамма-установках по 2 Гр 5 раз в неделю до СОД 47 Гр. Величина СОД радикального курса сочетанной нейтронно-фотонной терапии с учетом ОБЭ нейтронов составляла до 60 Гр. Таким образом, вклад нейтронной компоненты в этой группе составил 17%.
2-ая группа (51 больная): на первом этапе облучали быстрыми нейтронами в разовой очаговой дозе 1 Гр три раза в неделю до СОД 3 Гр. С учетом зависимости уменьшения ОБЭ от дозы ее величину в данном режиме облучения принимали равной 4, т.е. эквивалентная доза гамма-облучения составляла 12 Гр.
При таком режиме облучения нейтронная компонента составляла 30 ед. ВДФ. В дальнейшем продолжали облучение на гамма-установках до СОД 60 Гр с учетом ОБЭ. Вклад нейтронной компоненты составлял 27%.
Таким образом, в обеих группах вклад нейтронной компоненты в суммарном курсе радикальной сочетанной нейтронно-фотонной терапии составлял 17-27%. В прототипе указанный вклад нейтронов составлял 50-60%, т.е. был почти в два раза выше, чем в предлагаемом способе.
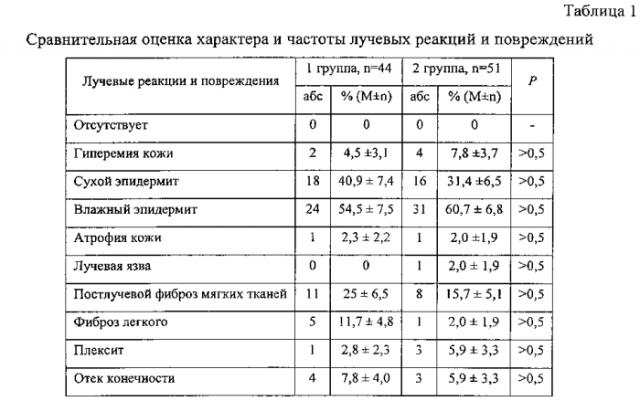
Распределение больных раком молочной железы в зависимости от распространенности процесса в обеих группах больных существенно не различались между собой. Метастатические поражения регионарных лимфоузлов в первой группе наблюдалось в 91,2%, во второй в 98,1% случаев. Не отличались группы и по другим показателям. В таблице 1 представлена сравнительная оценка характера и частоты лучевых реакций и повреждений. Полученные данные свидетельствуют, что существенные различия в характере и частоте лучевых реакций и повреждений не выявлены. Следует, однако, отметить, что во второй группе у одной больной была лучевая язва и несколько чаще развивался лучевой плексит. Величина и степень лучевых реакций и повреждений существенно ниже, чем в прототипе, когда вклад нейтронной компоненты составлял 50-60%
В таблице 2 представлена общая погодовая безрецидивная выживаемость больных, получивших радикальный курс сочетанной нейтронно-фотонной терапии, из которой видно, что выживаемость во все сроки наблюдения в двух группах не отличалась (Р<0,005).
Приведенные данные свидетельствуют, что по используемым критериям ранних реакций и поздних лучевых повреждений, безрецидивной выживаемости отсутствуют статистически значимые различия между результатами радикального курса сочетанной нейтронно-фотонной терапии местнораспространенного рака молочной железы с вкладом нейтронов в суммарную очаговую дозу 17 и 27%.
Таким образом, предложенный способ позволяет снизить величину нейтронной компоненты в курсе лучевой терапии до оптимальных значений, 17-30% по сравнению с 50-60% в прототипе при сохранении всех положительных результатов лечения и повышении качества жизни.
Способ нейтронно-фотонной терапии больных раком молочной железы, включающий локализацию железы с помощью болюса, изготовленного из тканеэквивалентного материала в виде прозрачных пластин с возможностью изменения и фиксации расстояния между ними, облучение нейтронами до СОД 2,0 Гр, а также гамма-облучение, отличающийся тем, что облучение нейтронами проводят ежедневно дозой от 0,2 до 0,4 Гр в комбинации с гамма-облучением дозой от 1,0 до 2,0 Гр за один сеанс до СОД от 45 до 47 Гр.