Способ определения полисорбата
Иллюстрации
Показать всеНастоящее изобретение относится к области аналитической химии и касается способа определения полисорбата в пробе, содержащей белок. Способ по настоящему изобретению включает предварительную обработку пробы посредством щелочного гидролиза с последующим колориметрическим определением на основе металлокомплекса, определяемого при анализе вещества с тиоцианатным реагентом, при этом указанный комплекс экстрагируют несмешивающимся с водой органическим растворителем. Щелочной гидролиз приводит к удалению мешающих белков и повышению селективности относительно поверхностно-активных веществ, подобных определяемому при анализе веществу, например селективности по Tween 80 относительно Triton X-100. 2 н. и 13 з.п. ф-лы, 6 ил., 3 табл., 8 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу определения полисорбата в пробе, содержащей белок. Способ по настоящему изобретению включает в себя предварительную обработку пробы посредством щелочного гидролиза с последующим определением полисорбата колориметрическим методом.
Предшествующий уровень техники
Вирусная безопасность представляет собой ключевое требование в отношении белков, применяемых в терапии, особенно в случае лекарственных препаратов, получаемых из плазмы. За последние годы в вирусной безопасности был достигнут существенный прогресс, в результате которого почти полностью исключается риск передачи вирусов. Специальные стадии, имеющие целью удаление или инактивацию вирусов, были разработаны, одобрены и введены в процессы получения используемых в терапевтических целях белков плазмы. Процессы изготовления факторов свертывания крови, подобных фактору VIII или фактору IX, ингибиторов протеиназ плазмы, таких как антитромбин, антитрипсин или С1-ингибитор, а также альбумина и иммуноглобулинов должны включать по меньшей мере одну стадию инактивации, эффективную в отношении вирусов с липидной оболочкой и соответствующую требованиям безопасности, а национальные и международные регулирующие органы установили всеобъемлющие правила для обеспечения соблюдения и дополнительного улучшения вирусной безопасности. Например, научный Комитет по запатентованным лекарственным препаратам (СРМР), как орган Европейского агентства по лекарственным средствам (ЕМА), издал методические указания, касающиеся вирусной безопасности биологических препаратов. Для сведения к минимуму риска передачи вирусов с получаемыми из плазмы лекарственными препаратами методические указания СРМР, помимо других профилактических действий на уровне исходного материала плазмы, строго рекомендуют включать в производственный процесс две независимые процедуры инактивации вирусов.
Сведения о полезности детергентов для целей вирусной инактивации, наряду с возможностью использования хроматографических способов очистки белка, указали путь к вирусной инактивации путем использования детергентов в ходе обработки белков плазмы. Все основные вирусы: HIV, HBV и HCV являются вирусами с липидной оболочкой. Следовательно, для эффективной инактивации вирусов разумно использовать преимущество вирусной восприимчивости к детергентам, используемым отдельно или в ходе общепринятой процедуры с использованием смеси растворитель-детергент (S/D). Воздействие всех указанных процедур заключается в специфическом разрушении вирусной липидной оболочки, при относительно слабом влиянии на целостность терапевтических белков, за исключением липопротеинов.
Неионогенный детергент моноолеат полиоксиэтиленсорбитана (полисорбат 80, Tween™ 80) представляет собой наиболее широко используемый вирулицидный детергент на основе полисорбатов. После стадии вирусной инактивации способ изготовления должен включать в себя стадию очистки, эффективную для целей удаления средств, используемых при инактивации, такую как, например, хроматографическую адсорбцию белка. Однако для осуществления контроля эффективности процедуры удаления детергента, а также для проверки соответствия процесса установленным и действующим требованиям по предельным концентрациям детергентов, измерение количества детергента после инактивации вирусов должно осуществляться в присутствии варьирующихся, и в некоторых случаях довольно высоких, концентраций белков, таких как белки плазмы. Разнообразие химического состава и структурное многообразие полисорбатов, подобных полисорбату 80, низкая реакционная способность этих соединений, матрица белок/буфер, а также возможное присутствие других, схожих по физико-химическим свойствам детергентов, таких как, например, простые эфиры алкилфенолов, подобные продукту Triton™ Х-100, с переменными количествами этиленоксидных фрагментов, делают измерение особенно трудным. Обеспокоенность по поводу рисков, связанных с губчатой энцефалопатией крупного рогатого скота (BSE), привела к внедрению формы полисорбата 80 растительного происхождения, изготовленной из растительных жиров, вместо топленого говяжьего жира. Невзирая на их одинаковую вирулицидную эффективность, упомянутые полисорбаты, предположительно имеющие различные профили жирных кислот, могут отличаться по аналитической чувствительности.
Прежний вариант колориметрического анализа, основанный на образовании комплекса полисорбата 80 с крахмалом и измерении избытка свободного крахмала по его реакции с иодом, адаптирован для сред и вакцин, приготовленных на культуре ткани и содержащих аминокислоты, сахара и белок. Другой вариант колориметрического анализа, основанный на образовании комплекса полиоксиэтиленовых цепей с тиоцианатом кобальта (II) и экстрагировании комплекса хлороформом, первоначально был разработан для определения концентрации эфиров полиэтиленгликоля и жирных кислот в водных растворах. С тех пор его применение было распространено на другие полиэтоксилированные неионные поверхностно-активные вещества, такие как, например, полиоксиэтиленовые эфиры п-изооктилфенола (поставляемые различными производителями под торговыми наименованиями Triton™ X-100, Igepal™ СА-630, Nonidet™ P40 или Tergitol™ NP40), с диэтиловым эфиром, метиленхлоридом или хлороформом в качестве экстрагента.
Однако применение данного способа для биологических препаратов ограничено присутствием белков, оказывающих сильное воздействие на анализ. Таким образом, белки необходимо удалить перед проведением анализа. Для преодоления связанных с белками эффектов матрицы были введены такие способы разделения, как стадия осаждения холодным этанолом для удаления белка центрифугированием перед проведением колориметрии с использованием тиоцианата кобальта (II), эксклюзионная хроматография с постколоночной колориметрической дериватизацией, эксклюзионная хроматография с базовой концентрацией полисорбата 80 выше критической мицеллярной концентрации для предотвращения мицеллярной агрегации с УФ-детектированием при 235 нм, сопровождаемая обеднением по белку хроматография несвязанного полисорбата с улавливанием белка в ионообменной ВЭЖХ-колонке, твердофазная экстракция с делипидизацией, колориметрическая дериватизация и отделение комплекса тиоцианата кобальта (II) при использовании гельпроникающей хроматографии, кислотный гидролиз с использованием ВЭЖХ или определение жирной кислоты методом ГХ, или мягкое омыление с определением методом ВЭЖХ выделяющейся жирной кислоты, тонкослойная хроматография или жидкостная экстракция с отделением при помощи метода ВЭЖХ и масс-спектрометрическое детектирование. Осуществление последних из указанных подходов, которые опираются на жирнокислотный фрагмент полисорбата, затруднено вследствие вариаций в составах жирных кислот определяемого при анализе вещества. В соответствии с другим современным подходом измеряют флуоресцентную поляризацию 5-додеканоиламинофлуоресцеина, включенного в состав мицелл полисорбата. Однако такие способы являются либо очень длительными, либо страдают от ограниченной скорости обработки пробы, либо требуют оснащения сложными приборами и отдельной проверки каждой стадии.
Таким образом, существует острая необходимость в способе определения полисорбата в содержащих белок пробах методом колориметрического анализа, в котором мешающее воздействие белка можно было бы устранить быстрым и простым образом. Такой способ должен давать возможность для определения актуальной концентрации детергента, например во время вирусной инактивации, а также в готовых концентратах очищенных белков.
Указанная необходимость может быть удовлетворена с использованием вариантов осуществления настоящего изобретения, охарактеризованных в формуле изобретения.
Раскрытие изобретения
Настоящее изобретение относится к способу определения полисорбата в содержащей белок пробе, основанному на предварительной обработке пробы путем щелочного гидролиза с последующим определением колориметрическим методом.
Подробное описание изобретения
Настоящее изобретение относится к способу определения полисорбата в содержащей белок пробе, включающему в себя следующие стадии:
(a) осуществление щелочного гидролиза пробы;
(b) нейтрализацию пробы после щелочного гидролиза;
(c) необязательно удаление осадка денатурированного белка из нейтрализованной пробы;
(d) добавление водной смеси тиоцианатного металлокомплекса к необязательно профильтрованной пробе с образованием тиоцианатного металлокомплекса полиоксиэтиленсорбитана;
(e) экстрагирование упомянутого тиоцианатного металлокомплекса полиоксиэтиленсорбитана, образовавшегося на стадии (d), органическим растворителем, не смешивающимся с водой;
(f) измерение поглощения экстракта, полученного на стадии (е), для определения количества упомянутого тиоцианатного металлокомплекса полиоксиэтиленсорбитана, образовавшегося на стадии (d); и
(g) расчет количества содержащегося в пробе полисорбата на основе количества упомянутого тиоцианатного металлокомплекса полиоксиэтиленсорбитана, определенного на стадии (f).
Термин «полисорбат», используемый в настоящем документе, относится к любым полиоксиэтиленсорбитановым эфирам жирных кислот (полисорбатам). Предпочтительные полисорбаты включают в себя полисорбат 20, 40, 60 и 80. Полисорбат 80 является особенно предпочтительным. Упомянутый полисорбат 80 может иметь животное или растительное происхождение.
Термин «содержащая белок проба», используемый в настоящем изобретении, относится к любой пробе, содержащей по меньшей мере один белок. Такая проба, например, может быть получена в процессе приготовления рекомбинантных белков, при этом указанная проба может быть отобрана на любой стадии упомянутого процесса, или может быть конечным продуктом упомянутого процесса. Кроме того, такая проба может, например, быть приготовлена в процессе получения белков, извлекаемых из плазмы крови, при этом такая проба может быть отобрана на любой стадии данного процесса или может быть конечным продуктом упомянутого процесса. Предпочтительно, пробу отбирают после стадии инактивации вирусов в процессе получения белков, извлекаемых из плазмы крови. Соответственно, белок (белки), содержащийся в пробе, может быть одним или несколькими из белков плазмы крови. Более того, проба, содержащая белок, может представлять собой плазму крови. Кроме того, проба, содержащая белок, может быть пробой, содержащей вакцины и/или пептиды.
Проба, содержащая белок, может дополнительно иметь в своем составе полиоксиэтиленовый эфир изооктилфенола (Triton™ Х-100) и/или три-н-бутилфосфат (ТНБФ), которые могут быть добавлены, например, на стадии инактивации вирусов в процессе приготовления белков, полученных из плазмы крови.
Большие молекулы, подобные белкам, могут содержать структурные единицы, сформированные из набора гидрофобных и гидрофильных аминокислот, которые могут обладать свойствами, имитирующими характеристики детергента. Они тоже могут мешать детектированию в некоторых количественных анализах. Связывание детергента с белковыми структурами также может влиять на измерение из-за предотвращения образования комплекса, что в результате приводит к достижению более низких степеней извлечения вещества, определяемого при анализе. Таким образом, для предотвращения указанного мешающего воздействия сопутствующие белки должны быть разрушены до стадии колориметрического определения с целью получения неискаженных результатов. Осаждение белков с использованием растворителя, подобного этанолу, представляет собой один из возможных путем удаления белков перед осуществлением количественного анализа. Однако с учетом того, что сложные смеси белков могут также содержать и белки с низкой молекулярной массой, такие как аполипопротеин А1, или белки, подобные α1-кислому гликопротеину, которые с трудом осаждаются при используемых концентрациях этанола, область применения данной стадии приготовления пробы в известной степени оказывается ограничена. Вместо этого в настоящем изобретении используется предварительная обработка пробы на основе щелочного гидролиза, более конкретно при повышенных температурах. В таких условиях, как показано далее ниже в примерах, белки будут разрушаться в такой степени, что они больше не смогут оказывать воздействие на количественный анализ. Хотя применяемый гидролиз и не приводит к полному разложению белка на аминокислоты, неожиданно обнаружилось, что он являлся достаточно жестким, чтобы исключить возможность ложноположительных реакций, а также связывания детергента.
Предпочтительно, стадия (а) способа по настоящему изобретению, т.е. осуществление щелочного гидролиза пробы, включает в себя обработку пробы щелочным реагентом при повышенных температурах в течение определенного периода времени. Предпочтительно, щелочной реагент выбирают из группы, состоящей из NaOH, KOH, LiOH, Ва(ОН)2, Sr(OH)2, Ca(OH)2, гидроксида тетраметиламмония, гидроксида тетраэтиламмония, гидроксида тетрапропиламмония, гидроксида тетрабутиламмония, а также гомологических и гетерологических замещенных четвертичных алкил- и циклоалкиламмоний гидроксидов. Более предпочтительно, щелочной реагент представляет собой NaOH, предпочтительно по меньшей мере 3N раствор NaOH, более предпочтительно примерно 10N раствор NaOH. Повышенная температура предпочтительно не превышает 100°C и составляет по меньшей мере около 80°C, более предпочтительно по меньшей мере около 90°C, наиболее предпочтительно по меньшей мере около 95°C. В особенно предпочтительном варианте осуществления изобретения щелочной гидролиз осуществляют при температуре от около 95°C до примерно 100°C. Продолжительность щелочного гидролиза предпочтительно составляет по меньшей мере около 15 минут, более предпочтительно по меньшей мере около 30 минут, наиболее предпочтительно по меньшей мере около 45 минут. Кроме того, продолжительность щелочной обработки предпочтительно не превышает 120 минут, более предпочтительно не превышает 90 минут. В особенно предпочтительном варианте осуществления изобретения продолжительность щелочной обработки составляет от примерно 45 до примерно 90 минут, более предпочтительно от примерно 45 минут до 75 минут, более предпочтительно от примерно 50 минут до 70 минут, а наиболее предпочтительно 60 минут.
Стадия (b) способа по настоящему изобретению, т.е. нейтрализация пробы по завершении щелочного гидролиза, предпочтительно включает в себя нейтрализацию пробы кислотой, например уксусной кислотой, до уровня pH от примерно 7 до около 8. Другие кислоты, которые можно использовать в данной операции, включают муравьиную кислоту, пропионовую кислоту, масляную кислоту, молочную кислоту, гидроксимасляную кислоту, алкан- и циклоалканмонокарбоновые кислоты, дикарбоновые кислоты и трикарбоновые кислоты.
Предпочтительно, стадию (с) способа настоящего изобретения, т.е. удаление осадка денатурированного белка из нейтрализованной пробы, если ее вообще осуществляют, можно осуществить посредством фильтрации или центрифугирования, в зависимости от конкретного раствора белка, и она включает в себя центрифугирование пробы или фильтрацию пробы с помощью фильтра, который не связывает полиоксиэтиленсорбитан. В предпочтительном варианте осуществления изобретения фильтр представляет собой гидрофильный фильтр, например фильтр, изготовленный из ацетата целлюлозы. Размер пор фильтра никак не ограничивается, до тех пор пока он в достаточной мере удерживает осадок, и может составлять, например, 0,22 мкм.
Металлокомплекс тиоцианата, добавляемый на стадии (d), предпочтительно представляет собой водную смесь Со(NO3)2·6 Н2О и NH4SCN, а образующийся тиоцианатный металлокомплекс полиоксиэтиленсорбитана является полиоксиэтиленсорбитановым комплексом тиоцианатокобальтата (II).
Водная смесь Со(NO3)2·6 H2O и NH4SCN, предпочтительно добавляемая к профильтрованной пробе на стадии (d) способа по настоящему изобретению, предпочтительно содержит от около 1% (масс./об.) до примерно 4% (масс./об.), предпочтительно от около 1,5% (масс./об.) до примерно 4% (масс./об.), более предпочтительно от около 2% (масс./об.) до примерно 4% (масс./об.), и наиболее предпочтительно 3% (масс./об.) Со(NO3)2·6 Н2О и от примерно 10% (масс./об.) до около 30% (масс./об.), предпочтительно от 15% (масс./об.) до примерно 25% (масс./об.), более предпочтительно около 20% (масс./об.) NH4SCN в дистиллированной воде.
Предпочтительно, не смешивающийся с водой органический растворитель, используемый на стадии (е) способа по настоящему изобретению для экстракции тиоцианатного металлокомплекса полиоксиэтиленсорбитана, образующегося на стадии (d), выбран из группы, состоящей из хлороформа, метиленхлорида, о-дихлорбензола, бромоформа и трихлорэтилена, из которых особенно предпочтительным является метиленхлорид.
Затем на стадии (f) измеряют поглощение экстракта, полученного на стадии (е) способа по настоящему изобретению, предпочтительно в диапазоне от около 300 нм до примерно 340 нм, более предпочтительно от около 310 нм до примерно 330 нм, наиболее предпочтительно примерно при 324 нм. Методы измерения поглощения пробы при одной или нескольких конкретных длинах (длине) волн известны специалистам в данной области техники и включают в себя, например, использование стандартного UV/VIS-спектрометра.
Кроме того, методы осуществления стадии (g) способа по настоящему изобретению, т.е. расчет содержащегося в пробе количества полисорбата, исходя из количества упомянутого тиоцианатного металлокомплекса полиоксиэтиленсорбитана, определенного на стадии (f), известны специалистам в данной области техники.
В предпочтительном варианте осуществления изобретения после стадии (а) и перед стадией (b) способ по настоящему изобретению дополнительно включает стадию охлаждения пробы после щелочного гидролиза, предпочтительно до комнатной температуры. Кроме того, после стадии (b) и перед стадией (с) способ по настоящему изобретению может заключать стадию выдерживания пробы при комнатной температуре в течение по меньшей мере 15 минут, предпочтительно по меньшей мере 30 минут, для обеспечения условий для образования возможного осадка денатурированного белка в полном объеме.
Для того чтобы избежать потерь определяемого при анализе вещества вследствие неспецифической адсорбции полисорбата на поверхности емкости, используемой для пробы, например на пластиковой поверхности, способ по настоящему изобретению может включать стадию смешивания пробы с раствором белка, например раствором альбумина, перед щелочным гидролизом. Такая адсорбция, в частности, может иметь место в случае проб с низким содержанием белка, например с содержанием белка ниже 1 мг/мл.
Кроме того, способ по настоящему изобретению может включать стадию построения калибровочной кривой с использованием проб с известными концентрациями полисорбата, а также одного или нескольких белков для калибровки измерений поглощения. Методы построения соответствующих калибровочных кривых известны специалистам в данной области техники.
На чертежах показано следующее:
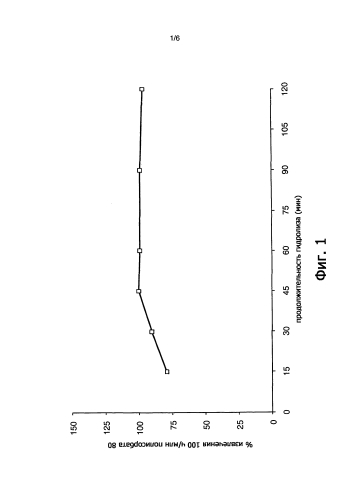
На фиг.1 представлены результаты колориметрического определения полисорбата после гидролиза при 100°C в течение периодов времени от 15 до 120 мин. Экспериментальные точки представляют собой среднее значение для двух независимых реакционных смесей гидролиза, которые отличались менее чем на 4%, когда щелочной гидролиз осуществляли в течение по меньшей мере 60 минут.
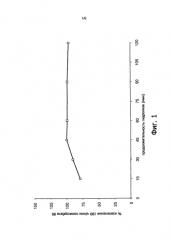
На фиг.2 приведены результаты 21 измерения, относящиеся к контрольной пробе, содержащей 100 ч./млн полисорбата 80, для установления точности и линейности анализа. Указан интервал в два стандартных отклонения от среднего значения.
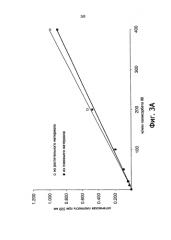
На фиг.3 продемонстрированы калибровочные графики проб с внесенным полисорбатом 80, полученным из говяжьего и овощного исходного материала, соответственно, с предварительной обработкой каждой пробы (В) или без такой обработки (А).
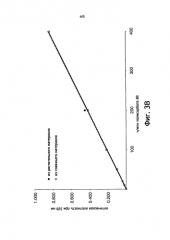
На фиг.4 представлены калибровочные кривые для полисорбата 80 и продукта Triton™ Х-100 без предварительной обработки пробы (А), а также калибровочные кривые для полисорбата 80 и смеси полисорбата 80, три-н-бутилфосфата (ТНБФ) и продукта Triton™ X-100 после щелочного гидролиза (В).
Настоящее изобретение будет дополнительно разъяснено на следующих ниже примерах без какого-либо ограничения его объема.
Примеры
Материалы:
Все использованные химические реагенты имели марку ч.д.а, если конкретно не указано иное. NaOH, 96%-ная уксусная кислота, гексагидрат нитрата кобальта (Co(NO3)2·6 H2O), метиленхлорид (Lichrosolv™), Triton™ X-100, три-н-бутилфосфат (ТНБФ) и тиоцианат аммония (NH4SCN) были приобретены у фирмы Merck (Германия). Две партии полисорбата 80 (Tween™ 80) из говяжьего, а также овощного исходного материала были приобретены у фирмы ICI (США). Водные растворы детергента с содержанием 1% (масс./об.) были приготовлены и впоследствии использованы для анализа.
Влияние некоторых белков плазмы на точность анализа исследовали с использованием промежуточных продуктов фракционирования белков плазмы и концентратов от фирмы Baxter BioScience (Вена, Австрия). Вкратце, для исследования пригодности предварительной обработки пробы посредством щелочного гидролиза использовали следующие концентраты белков плазмы человека: альбумин, иммуноглобулин, антитромбин, протеин С, экспериментальный концентрат активированного и неактивированного протромбинового комплекса (аРСС и РСС), концентрат фактора IX высокой чистоты и орозомукоид (α1-кислый гликопротеин). Наконец, способ также осуществляли в случае цельной плазмы с использованием лиофилизованной эталонной плазмы человека, поставляемой фирмой Baxter (Baxter BioScience Diagnostics Division, Вена, Австрия).
Непосредственно щелочной гидролиз проводили в полипропиленовых трубках 100×15 мм с навинчивающимися колпачками (фирма Greiner, Австрия), а последующее колориметрическое определение проводили в стеклянных трубках с навинчивающимися колпачками. Использованные фильтры представляли собой фильтры MINISART 0,22 мкм (фирма Sartorius, Германия). Колориметрическое измерение осуществляли на спектрометре LKB Ultrospec K4053 с использованием 1 см кварцевых ячеек Suprasil с навинчивающимися колпачками (фирма Hellma, Германия). Комнатную температуру (20-25°C) поддерживали в течение всех стадий способа, за исключением гидролиза.
Пример 1: Щелочной гидролиз
В полипропиленовую трубку, содержащую 1 мл исследуемой пробы, стандартной или контрольной пробы, с содержанием полисорбата менее 400 мг/л = 400 ч/млн, добавляли 0,5 мл 10 М раствора NaOH. Полученный раствор выдерживали на кипящей водяной бане в течение 60±10 мин. После охлаждения до комнатной температуры щелочные гидролизаты нейтрализовали до уровня pH ~ 7-8 с использованием 0,5 мл 10 М раствора уксусной кислоты при контроле уровня pH с помощью индикаторных полосок (фирма Merck, Германия). После нейтрализации пробы выдерживали при комнатной температуре в течение по меньшей мере 30 мин. В зависимости от раствора белка выпадал осадок, который удаляли путем фильтрации с использованием фильтра Minisart 0,22 мкм перед процедурой колориметрического определения. Пробы с содержанием белка менее 1 мг/мл смешивали с раствором альбумина перед гидролизом с целью исключения потерь определяемого при анализе вещества вследствие неспецифической адсорбции на пластиковых поверхностях, которые могут произойти в ходе данной процедуры. Оказалось, что добавление 0,1 мл раствора альбумина человека с концентрацией 200 мг/мл к 1 мл соответствующей пробы является эффективным для предотвращения неспецифических потерь полисорбата 80. Такое разбавление пробы необходимо учитывать при расчете концентрации полисорбата в пробе.
Пример 2: Колориметрическое измерение
Колориметрическое определение осуществляли следующим образом. Вкратце, 1 мл нейтрализованного гидролизата белка или водного раствора полисорбата, по существу не содержащий белка, смешивали с 3 мл реагента тиоцианатокобальтата. Данный реагент содержал 3% (масс./об.) Со(NO3)2·6 Н2О и 20% (масс./об.) NH4SCN, растворенных в дистиллированной воде, и его готовили заново каждый день. Затем добавляли 2 мл метиленхлорида. После энергичного встряхивания фазам давали разделяться по меньшей мере в течение 30 мин при 20-25°C. Наконец, проводили спектрофотометрические измерения фазы метиленхлорида в сравнении с чистым метиленхлоридом в кюветах с навинчивающимися колпачками при 320 нм.
Пример 3: Калибровка для количественного анализа
Калибровку для количественного анализа осуществляли посредством проведения анализа на стандартных разбавленных растворах, охватывающих диапазон концентраций полисорбата 80 от 10 до 400 ч./млн. Указанные стандартные растворы готовили путем внесения в раствор белка водных растворов полисорбата. Поскольку описанные в настоящем документе условия гидролиза, фактически, сводят к нулю воздействие любого испытанного до сих пор растворенного белка, для анализа подходит любой раствор белка, включая цельную плазму. Однако, следуя принципу сравнения подобного с подобным, был выбран раствор белков плазмы, максимально схожий с представляющим интерес раствором. Таким образом строили стандартную кривую, охватывающую диапазон от 10 до 400 ч./млн полисорбата 80, включающую концентрации 5, 10, 20, 50, 100, 200 и 400 ч./млн, с использованием экспериментального концентрата РСС. При осуществлении количественного анализа определение каждый раз проводили дважды.
Пример 4: Оптимизация продолжительности гидролиза
С целью установления подходящей продолжительности гидролиза в качестве белковой матрицы был выбран экспериментальный концентрат аРСС (концентрат активированного протромбинового комплекса), поскольку известно, что такой раствор существенно мешает колориметрическому определению полисорбата 80. Хотя указанная матрица по сути не содержала никакого детергента, при анализе данного раствора после попытки удаления белка посредством осаждения этанолом наблюдали ложную положительную реакцию. В указанную матрицу с концентрацией белка около 25 мг/мл, содержащую широкий спектр различных белков плазмы, таких как протромбин, ингибитор интер-α-трипсина, комплемент и витронектин, вносили 100 ч./млн полисорбата 80. Щелочной гидролиз осуществляли, как описано в настоящем документе, выдерживая пробы в течение периода от 15 до 120 мин на кипящей водяной бане. Дальнейшие операции выполняли, как описано выше.
Результаты колориметрического измерения полисорбата после гидролиза при 100°C в течение периодов времени длительностью от 15 до 120 мин представлены на фиг.1. Выбранная матрица белка, которая, как известно, содержала компоненты, дающие при определении ложноположительную реакцию после осаждения белка этанолом, не показывала никакой ложноположительной реакции даже после очень коротких периодов проведения гидролиза. После осуществления гидролиза при 100°C в течение 15 минут добавленные 100 ч./млн полисорбата 80 не удавалось извлечь полностью и было обнаружено только 79% от внесенного количества. Указанная степень извлечения была наиболее низкой из обнаруженных в данном исследовании и, кроме того, сопровождалась более высоким стандартным отклонением, по сравнению со всеми другими степенями извлечения, достигаемыми после длительного гидролиза. Таким образом, кратковременный щелочной гидролиз был недостаточен для полного устранения мешающего воздействия белка и наблюдалась более низкая степень извлечения, указывающая на то, что, вероятно, относительно прочная ассоциация между белком и детергентом предотвращала участие детергента в колориметрическом определении. Однако щелочной гидролиз, проводимый в течение 30 мин, приводил к степени извлечения 90%, а последующие пробы, проанализированные после 45, 60, 90 и 120 мин гидролиза, соответственно, показывали степени извлечения, равные 100%, 99%, 99% и 97% соответственно, при этом каждая величина характеризовалась коэффициентом вариации ниже 2,5%. В соответствии с указанными полученными данными для всех дальнейших экспериментов была выбрана продолжительность гидролиза 60±10 мин.
Пример 5: Точность количественного анализа в матрицах различных белков плазмы
В официальных методических указаниях по аттестации способов измерения определено, что точность аналитической процедуры выражает степень согласованности между истинной и обнаруженной величинами. Существует несколько подходов для оценки точности аналитического метода. Поскольку не имеется никакого сертифицированного эталонного материала для полисорбата 80 в присутствии белков плазмы, использовали метод привнесения в чистую эталонную пробу известной концентрации определяемого при анализе вещества. Указанный подход привнесения соответствующих растворов белков был выбран вследствие заведомо известного влияния белков на анализ. В результате различий в первичной, вторичной и третичной структурах стойкость белков в отношении обработки щелочью может в значительной мере варьироваться. При этом описываемая процедура, применяемая для определения полисорбата 80, является менее радикальной, чем полный щелочной гидролиз, включающий нагрев в течение 15 часов при 120°C.
С целью исследования того, являются ли используемые в настоящем документе условия щелочного гидролиза достаточными для обеспечения возможности проведения точного анализа содержания полисорбата 80 в весьма различных белковых матрицах, для проверки извлечения полисорбата 80 использовали растворы белков плазмы, включающие альбумин, иммуноглобулин, орозомукоид, антитромбин, белок С и факторы свертывания крови, а также цельную плазму. Концентрация белка в исследованных пробах находилась в пределах 1 до 50 мг/мл. Таблица 1 включает результаты экспериментов с внесением добавок, в которых к чистым матрицам добавляли 10 ч./млн, 50 ч./млн, 100 ч./млн или 200 ч./млн полисорбата 80.
| Таблица 1 | |||||
| Извлечение полисорбата 80 (р80) в растворах различных белков плазмы | |||||
| Извлечение полисорбата 80 [% от добавленного количества] | |||||
| Белок плазмы | Концентрация [мг/мл] | 10 ч./млн р80 | 50 ч./млн р80 | 100 ч./млн р80 | 200 ч./млн р80 |
| Плазма | 30 | -*) | - | 106 | 104 |
| активированный РСС | 30 | 94 | - | 104 | - |
| активированный РСС | 10 | 100 | - | 106 | - |
| альбумин | 20 | - | - | 102 | 100 |
| IgG | 20 | - | - | 90 | 93 |
| РСС | 30 | - | - | 98 | 96 |
| антитромбин | 20 | - | 99 | 98 | - |
| белок С | 6 | - | 99 | - | - |
| орозомукоид | 50 | - | 99 | - | - |
| конц. фактор IX | 1 | - | 102 | - | - |
| *) -: не определялось |
Во всех исследованных растворах белков степени извлечения составили от 90% до 106% в расчете на добавленное количество полисорбата 80. При этом все испытанные пробы удовлетворяли критериям для данных по степени извлечения в зависимости от концентрации вещества, определяемого при анализе, опубликованным ассоциацией АОАС (Американская ассоциация химиков-аналитиков). Согласно упомянутым техническим требованиям, для обеспечения достоверного результата 100 ч./млн, определяемого при анализе вещества, должны быть извлечены со степенью от 90% до 107%, тогда как пределы извлечения 10 ч./млн составляют от 80% до 110%. Полученные авторами результаты демонстрируют, что используемые условия гидролиза подходят для устранения воздействия белка, безотносительно типа белка при по меньшей мере исследованных концентрациях белка. Это было показано даже в случае матрицы из плазмы, которая, как известно, является очень сложной и содержит несколько сотен различных белков, а также компоненты с низкой молекулярной массой. Добавленные 100 ч./млн, а также 200 ч./млн полисорбата 80 удалось извлечь с отклонениями менее 6%. Кроме того, ни один из очищенных белков, в который привносили полисорбат, не препятствовал успешному извлечению, хотя испытаниям подвергались несхожие по своей структуре белки, взятые с различными концентрациями. Таким образом, например, высокогликозилированный белок орозомукоид, очень кислый белок с изоэлектрической точкой ниже 3, который, как известно, связывает лекарственные средства разного типа, а также альбумин, который может связывать жирные кислоты, не мешали определению даже при высоких концентрациях. Даже при внесении 10 ч./млн полисорбата 80, что является нижним пределом количественного определения, количественный анализ давал точный результат, независимо от имеющейся концентрации белка. В экспериментальный продукт аРСС с концентрациями 10 и 30 мг белка/мл вносили 10 ч./млн полисорбата, и безотносительно концентрации белка при анализе были достигнуты степени извлечения 94% и 100%, что, таким образом, снова соответствует приведенным выше рекомендациям ассоциации АОАС.
Пример 6: Прецизионность и линейность количественного анализа
Согласно официальным методическим указаниям по аттестации аналитических методов прецизионность метода представляет собой степень согласованности между собой результатов отдельных испытаний из множества определений для серий проб, тогда как линейность аналитической процедуры описывает ее способность давать результат испытания, прямо пропорциональный концентрации в пробе определяемого при анализе вещества. С целью описания этих важных рабочих параметров анализа использовали контрольную пробу со 100 ч./млн полисорбата 80 в экспериментальном продукте РСС. Результаты анализа показаны на фиг.2. При использовании 21 определения в контрольной пробе средний результат для пробы характеризовался относительным стандартным отклонением (sd) 4,0% и 3,7% для случаев меж- и внутрисерийной прецизионности соответственно. Обе величины отклонения соответствуют рекомендациям, данным ассоциацией АОАС, составляющим 5,3% для прецизионности в пределах дня или между днями при измерении 100 ч./млн определяемого при анализе вещества. Лишь одно из 21 определения дало величину вне интервала удвоенного стандартного отклонения, но попало в интервал ±3 sd от среднего значения. На приведенном графике также показан разброс в пределах одной серии измерений, отмеченный планками погрешностей. Прецизионность анализа дополнительно изучали при концентрации 20 ч./млн, при этом значение прецизионности составило 3,0%. Анализ пробы, отобранной в ходе процесса инактивации при высокой концентрации 150 г полисорбата 80/л, происходил со средним стандартным отклонением 2,9% (n=6), подтверждая, тем самым, что данный способ подходит также и для измерения высоких концентраций, имеющих место в ходе процесса инактивации вирусов.
Калибровочные графики анализа, охватывающие диапазон от 5 до 400 ч./млн полисорбата 80, демонстрируют хорошую линейность, давая средний коэффициент корреляции r=0,999 (n=21) между концентрацией и измеренной экстинкцией при 320 нм. Наклон линии характеризовался разбросом в пределах одной серии измерений, равным 7,7% (n=21), и было обнаружено, что предел количественного определения (LOQ) составил 10 ч./млн ± 0,4 ч./млн, как было вычислено в соответствии с рекомендациями ICH.
Пример 7: Сравнение полисорбатов различного происхождения
Для оценки того, оказывает ли влияние происхождение полисорбата 80 на показатели анализа, сравнивали партии из растительного и говяжьего исходного материала. Обе формы анализировали в присутствии описанного выше раствора белка после одинаковой процедуры щелочного гидролиза. В дополнение к этому, в отсутствие белков колориметрическое определение осуществляли с использованием реагента тиоцианата кобальта без предварительной обработки пробы, имитируя таким образом условия, имеющие место после осаждения этанолом для удаления белка.
Препараты полисорбата 80, используемые для инактивации вирусов, первоначально получали из топленого говяжьего жира. С появлением губчатой энцефалопатии крупного рогатого скота (BSE) стало необходимо исключить говяжий материал из процесса изготовления терапевтических белков и заменить его н