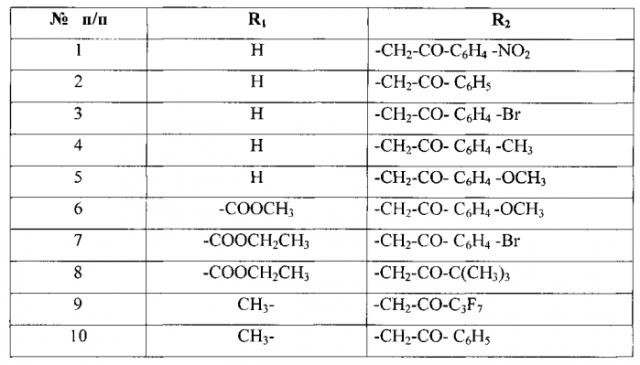
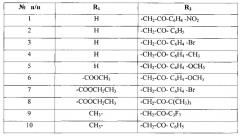
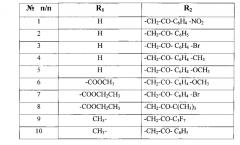
Использование тиосалицилоилгидразонов ароилуксусных альдегидов в качестве веществ, обладающих антистафилококковой активностью
Иллюстрации
Показать всеИзобретение относится к области использования тиосалицилоилгидразонов ароилуксусных альдегидов в качестве антистафилококковых агентов. Предложено применение производных 1,3,4-бензотиадиазепин-5(2Н)-она формулы (I) против штаммов рода Staphylococcus. Технический результат состоит в подавлении роста стафилококка и в расширении ассортимента соединений, обладающих антистафилококковой активностью, в медицине и ветеринарии. 2 табл.
I
Реферат
Изобретение относится к области использования тиосалицилоилгидразонов ароилуксусных альдегидов в качестве антистафилококковых агентов.
С целью получения соединений, обладающих антистафилококковой активностью взаимодействием меркаптосалицилоилгидразида с ароилуксусными альдегидами, были синтезированы соответствующие 2-меркаптобензоилгидразоны, которые в кристаллическом состоянии имеют циклическое строение формулы:
, где
Соединения были испытаны по отношению к бактериям, а именно к четырем штаммам Staphylococcus aureus, методом погружения в агар, а именно методом цилиндриков, при различных разведениях.
Данные экспериментов показали, что полученные соединения обладают антистафилококковой активностью, зоны задержки роста микроорганизмов составляют:
для 2-[2-(4-метоксифенил)-2-оксоэтил]-3,4-дигидро-1,3»4-бензотиадиа-зепин-5(2Н)-она (соединение 5):
для штамма №1:
- при разведении 1:1 - 48 мм;
- при разведении 1:2 - 24 мм;
- при разведении 1:4 - 12 мм;
- при разведении 1:8 - 6 мм;
- при разведении 1:16 - 6 мм,
для штамма №2:
- при разведении 1:1 - 64 мм;
- при разведении 1:2 - 32 мм;
- при разведении 1:4 - 16 мм;
- при разведении 1:8 - 8 мм,
для штамма №3:
- при разведении 1:1 - 68 мм;
- при разведении 1:2 - 34 мм;
- при разведении 1:4 - 17 мм;
- при разведении 1:8 - 8,5 мм,
для штамма №4:
- при разведении 1:1 - 80 мм;
- при разведении 1:2 - 40 мм;
- при разведении 1:4 - 20 мм;
- при разведении 1:8 - 10 мм;
- при разведении 1:16 - 6 мм,
для 2-[2-(4-метоксифенил)-2-оксоэтил]-2-метокси-3,4-дигидро-1,3,4-бензотиадиазепин-5(2Н)-она (соединение 6):
для штамма №1:
- при разведении 1:1 - 48 мм;
- при разведении 1:2 - 24 мм;
- при разведении 1:4 - 12 мм;
- при разведении 1:8 - 6 мм;
- при разведении 1:16 - 6 мм,
для штамма №2:
- при разведении 1:1 - 48 мм;
- при разведении 1:2 - 24 мм;
- при разведении 1:4 - 12 мм;
- при разведении 1:8 - 6 мм;
- при разведении 1:16 - 6 мм,
для штамма №3:
- при разведении 1:1 - 64 мм;
- при разведении 1:2 - 32 мм;
- при разведении 1:4 - 16 мм;
- при разведении 1:8 - 8 мм;
- при разведении 1:16 - 8 мм,
для штамма №4:
- при разведении 1:1 - 64 мм;
- при разведении 1:2 - 32 мм;
- при разведении 1:4 - 16 мм;
- при разведении 1:8 - 8 мм;
- при разведении 1:16 - 6 мм,
для 2-[2-(1,2,3-гептафторопропил)-2-оксоэтил]-3,4-дигидро-1,3,4-бензотиадиазепин-5(2Н)-она (соединение 9):
для штамма №1:
- при разведении 1:1 - 56 мм;
- при разведении 1:2 - 28 мм;
- при разведении 1:4 - 14 мм;
- при разведении 1:8 - 7 мм;
- при разведении 1:16 - 6 мм;
- при разведении 1:32 - 6 мм,
для штамма №2:
- при разведении 1:1 - 56 мм;
- при разведении 1:2 - 28 мм;
- при разведении 1:4 - 14 мм;
- при разведении 1:8 - 11 мм;
- при разведении 1:16 - 7 мм;
- при разведении до 1:64 - 6 мм,
для штамма №3:
- при разведении 1:1 - 56 мм;
- при разведении 1:2 - 28 мм;
- при разведении 1:4 - 14 мм;
- при разведении 1:8 - 7 мм;
- при разведении до 1:128 - 6 мм,
для штамма №4:
- при разведении 1:1 - 48 мм;
- при разведении 1:2 - 24 мм;
- при разведении 1:4 - 12 мм;
- при разведении 1:8 - 6 мм;
- при разведении 1:16 - 6 мм.
Способ получения
Пример 1. Получение 2-[2-(4-метоксифенил)-2-оксоэтил]-3,4-дигидро-1,3,4-бензотиадиа-зепин-5(2Н)-она (соединение 5)
К раствору 0,445 г (2,5 ммоль) 1,3-кетоальдегида в 5 мл этанола прибавляют при перемешивании 0,420 г (2,5 ммоль) гидразида 2-меркаптобензойной кислоты в 15 мл горячей воды и выдерживают на водяной бане при постоянном перемешивании при температуре около 50°C в течение 2 часов. Образовавшиеся после охлаждения кристаллы фильтруют, перекристаллизовывают из этанола и сушат. Выход 0,460 г (56%), Тплав 157-158°C.
Аналогичным способом получены и другие соединения данного ряда, их характеристики представлены в таблице 1.
Пример 2. Определение антистафилококковой активности
Испытания антистафилококковой активности проводили по отношению к 4 штаммам Staphylococcus aureus. С этой целью на агар Сабуро был произведен посев чистых культур методом сплошного газона. Последующее нанесение 0,02% водно-спиртовых растворов испытуемых веществ осуществлялось методом погружения в агар ("методом цилиндриков"). Культивирование микроорганизмов производилось при pH среды 5,6 и температуре 37°C в термостате в течение 3 дней. Измерение зон задержки роста микроорганизмов осуществлялось в мм.
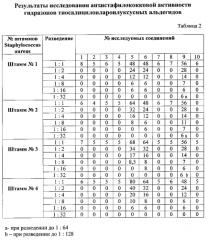
Определение чувствительности проводилось методом двукратных серийных разведений. В качестве стандарта сравнения использовали 0,02% раствор нитрофурала, который показал некоторую активность в отношении Staphylococcus aureus. Результаты антистафилококковой активности 2-меркаптобензоилгидразонов ароилуксусных альдегидов представлены в таблице 2.
Источники информации
1. В.В. Пакальнис, И.В. Зерова, С.И. Якимович, А.Ю. Ершов, И.В. Лагода. Гетероциклы на основе ароилуксусных альдегидов и SH-содержащих гидразидов. Журнал органической химии, 2009, т. 45, вып. 2, С. 295-300.
2. А.Ю. Ершов, И.В. Лагода, С.И. Якимович, В.В. Пакальнис, В.В. Шаманин. Кольчато-цепная таутомерия продукта конденсации ацетона с гидразидом тиосалициловой кислоты. Журнал органической химии, 2007, т. 43, вып. 11, С. 1742.
3. С.И. Якимович, К.Н. Зеленин, В.Н. Николаев, Н.В. Кошмина, В.В. Алексеев, В.А. Хрусталев. Таутомерия тиобензоилгидразонов ароилацетонов и аромлуксусных альдегидов. Журнал органической химии, 1983, т. 19, вып. 2, С. 1875-1881.
Применение тиосалицилоилгидразонов ароилуксусных альдегидов формулы , где: в качестве веществ, обладающих антистафилококковой активностью.