Химерные гены ospa, белки и способы их применения
Иллюстрации
Показать всеИзобретение относится к области биохимии, в частности к полипептиду, способному вызывать специфичный иммунный ответ против бактерий рода Borrelia, а также полинуклеотиду, его кодирующему. Также раскрыты экспрессионный вектор, содержащий вышеуказанный полинуклеотид, клетка-хозяин, его содержащая, а также способ получения пептида путем культивирования вышеуказанной клетки-хозяина. Изобретение также относится к композициям, содержащим вышеуказанные полинуклеотиды или полипептиды, для вызова специфичного иммунного ответа против бактерий рода Borrelia. Изобретение позволяет эффективно лечить или проводить профилактику инфекции Borrelia или лаймской болезни. 12 н. и 12 з.п. ф-лы, 24 ил., 9 табл., 22 пр.
Реферат
Область техники
Изобретение в общем относится к химерным полипептидам OspA, нуклеиновым кислотам, кодирующим полипептиды, композициям, содержащим такие молекулы, и способам их применения.
Известный уровень техники
Лаймская болезнь представляет собой переносимую клещами болезнь, вызываемую Borrelia burgdorferi sensu lato (s.l.). Болезнь типично характеризуется появлением распространяющейся красной сыпи на месте укуса клеща, за которой могут последовать системные осложнения, включая менингит, кардит или артрит. Почти все случаи лаймской болезни вызываются одним из трех геновидов - Borrelia afzelii, Borrelia garinii и Borrelia burgdorferi sensu stricto (s.s.). В Европе были обнаружены все три вида, инфицирующие людей. Однако в Северной Америке найден только один вид - Borrelia burgdorferi sensu stricto. Borrelia burgdorferi представляет собой вид грамотрицательных бактерий класса спирохет рода Borrelia. Лечение лаймской болезни антибиотиками обычно является эффективным, но у некоторых пациентов развивается хроническая инвалидизирующая форма болезни, затрагивающая суставы или нервную систему, существенно не улучшающаяся даже после терапии парентеральными антибиотиками, что указывает на потребность в вакцине для популяций с высокой степенью риска.
Внешний поверхностный белок A (OspA) представляет собой 31-кДа антиген, экспрессируемый видом Borrelia burgdorferi s.l., присутствующим в средней кишке иксодовых клещей. Была продемонстрирована эффективность OspA для профилактики лаймской болезни в Северной Америке (Steere et al., N. Engl. J. Med. 339: 209-15,1998; Sigal et al., N. Engl. J. Med. 339:216-22, 1998; erratum in: N. Engl. J. Med. 339:571, 1998). Амино-конец полностью процессированного OspA представляет собой цистеиновый остаток, который посттрансляционно модифицируется тремя жирными ацильными цепями, закрепляющими белок на внешней поверхности бактериальной мембраны (Bouchon et al., Anal. Biochem. 246: 52-61, 1997). Сообщается, что липидирование OspA стабилизирует молекулу (Luft, личное сообщение) и является существенным для защиты в отсутствие сильного адъюванта (Erdile et al., Infect. Immun. 61: 81-90, 1993). Растворимая рекомбинантная форма белка, не имеющая амино-концевого липидного мембраносвязывающего фрагмента, была со-кристаллизована с фрагментом Fab агглютинирующего мышиного моноклонального антитела для определения структуры OspA, который, как было продемонстрировано, содержит 21 антипараллельную β-нить с последующей одной α-спиралью (Li et al., Proc. Natl. Acad. Sci. U.S.A. 94:3584-9, 1997).
Моновалентная вакцина на основе OspA (LYMErix®) для профилактики лаймской болезни выпущена в продажу в США. Однако в Европе гетерогенность последовательностей OspA у трех геновидов препятствует широкой защите вакциной на основе OspA от одного штамма (Gern et al., Vaccine 15:1551-7, 1997). В европейских изолятах были определены семь основных серотипов OspA (обозначенных как серотипы 1-7, Wilske et al., J. Clin. Microbiol. 31:340-50, 1993). Серотипы OspA коррелируют с видами; серотип 1 соответствует B. burgdorferi s.s., серотип 2 соответствует B. afzelii и серотипы 3-7 соответствуют B. garinii.
Защитный иммунитет, приобретенный в результате иммунизации с помощью OspA, является исключительным, поскольку взаимодействие между иммунным ответом хозяина и патогеном происходит не в хозяине, а в средней кишке клеща-переносчика. В случае лаймской болезни, клещ выступает в роли переносчика или носителя при передаче лаймской болезни от животных людям. OspA-специфическое антитело, приобретенное во время кормления инфицированного клеща, препятствует переносу B. burgdorferi s.l. иммунизированному млекопитающему-хозяину (de Silva et al., J. Exp. Med. 183: 271-5, 1996). Защита является антитело-медиируемой и преимущественно обеспечивается бактерицидным антителом, хотя антитело, блокирующее прикрепление спирохеты к рецептору выстилки кишечного эпителия клеща, также может быть эффективным (Pal et al., J. Immunol. 166: 7398-403, 2001).
Рациональная разработка эффективных вакцин OspA требует идентификации защитных эпитопов, таких как определяемых защитным моноклональным антителом LA-2 (Golde et al., Infect. Immun. 65: 882-9, 1997). Анализ способами рентгеновской кристаллографии и ЯМР был использован для идентификации иммунологически важных гипервариабельных доменов OspA и локализации эпитопа LA-2 путем картирования на аминокислотах 203-257 (Ding et al., J. Mol. Biol. 302: 1153-64, 2000; Luft et al. J Infect Dis. 185 (Suppl. 1): S46-51, 2002).
В данной области техники существует потребность в разработке вакцины OspA, обеспечивающей широкую защиту против различных видов Borrelia, встречающихся в США, Европе и других регионах. Приведенное далее описание содержит характеристики такой вакцины.
Сущность изобретения
Изобретение направлено на удовлетворение одной или более потребностей в данной области техники, касающихся профилактики и лечения лаймской болезни или лайм-боррелиоза.
Изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 1, 3 и 5. В некоторых аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, состоящую из нуклеотидной последовательности, выбранной из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 1, 3 и 5. В других аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из: (а) нуклеотидной последовательности с по меньшей мере 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99 процентами идентичности последовательности с молекулой нуклеиновой кислоты, содержащей нуклеотидную последовательность, приведенную в SEQ ID NO: 1, SEQ ID NO: 3 или SEQ ID NO: 5; и (б) нуклеотидной последовательности, комплементарной к (а). В дополнительных аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из: (а) нуклеотидной последовательности, кодирующей полипептид с по меньшей мере 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99 процентами идентичности последовательности с полипептидом, содержащим аминокислотную последовательность, приведенную в SEQ ID NO: 2, SEQ ID NO: 4 или SEQ ID NO: 6; и (б) нуклеотидной последовательности, комплементарной к (а). В других аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из: (а) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 2, SEQ ID NO: 4 или SEQ ID NO: 6, причем полипептид содержит замещение от одной до 25 консервативных аминокислот; (б) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 2, SEQ ID NO: 4 или SEQ ID NO: 6, причем полипептид содержит инсерцию от одной до 25 консервативных аминокислот; (в) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 2, SEQ ID NO: 4 или SEQ ID NO: 6, причем полипептид содержит внутреннюю делецию от одной до 25 консервативных аминокислот; (г) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 2, SEQ ID NO: 4 или SEQ ID NO: 6, причем полипептид содержит C- и/или N-терминальное усечение от одной до 25 аминокислот; (д) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 2, SEQ ID NO: 4 или SEQ ID NO: 6, причем полипептид содержит модификацию от одной до 25 аминокислот, выбранную из аминокислотных замещений, аминокислотных инсерций, аминокислотных делеций, C-терминального усечения или N-терминального усечения; и (е) нуклеотидной последовательности, комплементарной к любой из (а)-(д).
Изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 7, 9 и 11. В некоторых аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, состоящую из нуклеотидной последовательности, выбранной из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 7, 9 и 11. В дополнительных аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из: (а) нуклеотидной последовательности с по меньшей мере 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99 процентами идентичности последовательности с молекулой нуклеиновой кислоты, содержащей нуклеотидную последовательность, приведенную в SEQ ID NO: 7, SEQ ID NO: 9 или SEQ ID NO: 11; и (б) нуклеотидной последовательности, комплементарной к (а). В дополнительных аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из: (а) нуклеотидной последовательности, кодирующей полипептид с по меньшей мере 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99 процентами идентичности последовательности с полипептидом, содержащим аминокислотную последовательность, приведенную в SEQ ID NO: 8, SEQ ID NO: 10 или SEQ ID NO: 12; и (б) нуклеотидной последовательности, комплементарной к (а). В других аспектах, изобретение включает изолированную молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, выбранную из группы, состоящей из: (а) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 8, SEQ ID NO: 10 или SEQ ID NO: 12, причем полипептид содержит замещение от одной до 25 консервативных аминокислот; (б) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 8, SEQ ID NO: 10 или SEQ ID NO: 12, причем полипептид содержит инсерцию от одной до 25 консервативных аминокислот; (в) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 8, SEQ ID NO: 10 или SEQ ID NO: 12, причем полипептид содержит внутреннюю делецию от одной до 25 консервативных аминокислот; (г) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 8, SEQ ID NO: 10 или SEQ ID NO: 12, причем полипептид содержит C- и/или N-терминальное усечение от одной до 25 аминокислот; (д) нуклеотидной последовательности, кодирующей полипептид, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 8, SEQ ID NO: 10 или SEQ ID NO: 12, причем полипептид содержит модификацию от одной до 25 аминокислот, выбранную из аминокислотных замещений, аминокислотных инсерций, аминокислотных делеций, C-терминального усечения или N-терминального усечения; и (е) нуклеотидной последовательности, комплементарной к любой из (а)-(д).
Изобретение включает векторы, клетки-хозяева и способы получения полипептидов путем культивации клеток-хозяев, описанных тут. В некоторых аспектах, изобретение включает вектор, содержащий любые молекулы нуклеиновой кислоты, описанные тут. В других аспектах, изобретение включает клетку-хозяина, которая содержит такие векторы. В некоторых аспектах, клетка-хозяин представляет собой эукариотическую клетку. В других аспектах, клетка-хозяин представляет собой прокариотическую клетку. В различных аспектах, способ получения полипептида включает культивацию клеток-хозяев, описанных тут, в условиях, пригодных для экспрессии полипептида и, необязательно, выделение полипептида из культуры. В различных аспектах, изобретение включает композиции, содержащие любые из таких химерных молекул нуклеиновой кислоты или любые векторы, содержащие такие молекулы нуклеиновой кислоты и фармацевтически приемлемый носитель или носители.
Изобретение включает композиции, содержащие любые молекулы нуклеиновой кислоты, описанные тут, или любые векторы, описанные тут, и фармацевтически приемлемый носитель. В некоторых аспектах, изобретение включает композиции, содержащие по меньшей мере две молекулы нуклеиновой кислоты, описанные тут, и фармацевтически приемлемый носитель, причем молекулы нуклеиновой кислоты имеют разные нуклеотидные последовательности. В конкретных аспектах, изобретение включает композиции, содержащие комбинацию нуклеотидных последовательностей, приведенных в SEQ ID NOS: 1, 3 и 5.
Изобретение включает изолированный полипептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 2, 4 и 6. В некоторых аспектах, изобретение включает изолированный полипептид, состоящий из аминокислотной последовательности, выбранной из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 2, 4 и 6. В дополнительных аспектах, изобретение включает изолированный полипептид, содержащий аминокислотную последовательность, состоящую из по меньшей мере 200 аминокислотных остатков, с по меньшей мере 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99 процентами идентичности последовательности с полипептидом, содержащим аминокислотную последовательность, приведенную в SEQ ID NO:2, SEQ ID NO:4 или SEQ ID NO: 6. В дополнительных аспектах, изобретение включает изолированный полипептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 8, 10 и 12. В других аспектах, изобретение включает изолированный полипептид, состоящий из аминокислотной последовательности, выбранной из группы, состоящей из последовательностей, приведенных в SEQ ID NOS: 8, 10 и 12. В некоторых аспектах, изобретение включает изолированный полипептид, содержащий аминокислотную последовательность, состоящую из по меньшей мере 200 аминокислотных остатков, с по меньшей мере 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99 процентами идентичности последовательности с полипептидом, содержащим аминокислотную последовательность, приведенную в SEQ ID NO: 8, SEQ ID NO: 10 или SEQ ID NO: 12.
Изобретение включает композиции, содержащие любые из полипептидов, описанных тут, и фармацевтически приемлемый носитель. В некоторых аспектах, изобретение включает композиции, содержащие по меньшей мере два полипептида, описанных тут и фармацевтически приемлемый носитель, причем полипептиды имеют разные аминокислотные последовательности. В конкретных аспектах, изобретение включает композиции, содержащие комбинацию полипептидов, содержащих аминокислотные последовательности, приведенные в SEQ ID NOS: 2, 4 и 6.
Изобретение включает иммуногенные композиции. В некоторых аспектах, иммуногенная композиция по изобретению содержит любую из описанных тут композиций и фармацевтически приемлемый носитель. В различных аспектах, иммуногенная композиция обладает способностью индуцировать продуцирование антитела, которое специфически связывается с внешним поверхностным белком A (OspA). В определенных аспектах, иммуногенная композиция обладает способностью индуцировать продуцирование антитела, которое специфически связывается с Borrelia. В конкретных аспектах, иммуногенная композиция обладает способностью индуцировать продуцирование антитела, нейтрализующего Borrelia. В определенных аспектах, Borrelia представляет собой Borrelia burgdorferi sensu lato. В конкретных аспектах, Borrelia представляет собой Borrelia afzelii, Borrelia garinii или Borrelia burgdorferi sensu stricto. В дополнительных аспектах, Borrelia представляет собой Borrelia japonica, Borrelia andersonii, Borrelia bissettii, Borrelia sinica, Borrelia turdi, Borrelia tanukii, Borrelia valaisiana, Borrelia lusitaniae, Borrelia spielmanii, Borrelia miyamotoi или Borrelia lonestar. В некоторых аспектах, антитело продуцируется животным. В дополнительных аспектах, животное представляет собой млекопитающее. В других аспектах, млекопитающее является человеком.
Изобретение включает композиции вакцины. В некоторых аспектах, композиция вакцины по изобретению содержит любую иммуногенную композицию, описанную тут, и фармацевтически приемлемый носитель. В различных аспектах, изобретение включает комбинированную вакцину. В определенных аспектах, комбинированная вакцина по изобретению содержит любую композицию вакцины, описанную тут, в сочетании с по меньшей мере второй композицией вакцины. В некоторых аспектах, вторая композиция вакцины защищает от переносимой клещами болезни. В различных аспектах, переносимая клещами болезнь представляет собой пятнистую лихорадку Скалистых гор, бабезиоз, возвратную лихорадку, колорадскую клещевую лихорадку, моноцитарный эрлихиоз человека (HME), гранулоцитарный эрлихиоз человека (HGE), клещевую сыпную лихорадку STARI (Southern Tick-Associated Rash Illness), туляремию, клещевой паралич, энцефалит Повассан, ку-лихорадку, конго-крымскую геморрагическую лихорадку, цитауксзооноз (cytauxzoonosis), марсельскую лихорадку или клещевой энцефалит. В других аспектах, вторая композиция вакцины представляет собой вакцину, выбранную из группы, состоящей из: вакцины клещевого энцефалита, вакцины японского энцефалита и вакцины пятнистой лихорадки Скалистых гор. В различных аспектах, вторая композиция вакцины имеет сезонный график иммунизации, совместимый с иммунизацией против инфекции Borrelia или лаймской болезни.
Изобретение включает способы индуцирования иммунологического ответа у субъекта. В различных аспектах, такие способы включают стадию введения субъекту любой из иммуногенных композиций или композиций вакцины, описанных тут, в количестве, эффективно индуцирующем иммунологический ответ. В определенных аспектах, иммунологический ответ включает продуцирование анти-OspA антитела. Изобретение включает антитела или их фрагменты, специфически связывающиеся с любыми из описанных тут полипептидов.
Изобретение включает способы профилактики или лечения инфекции Borrelia или лаймской болезни у субъекта. В различных аспектах, такие способы включают стадию введения субъекту любой из композиций вакцины, описанных тут, или любой из комбинированных вакцин, описанных тут, в количестве, обеспечивающем эффективную профилактику или лечение инфекции Borrelia или лаймской болезни. В других аспектах, такие способы включают стадию введения субъекту любых описанных тут антител в количестве, обеспечивающем эффективную профилактику или лечение инфекции Borrelia или лаймской болезни. В определенных аспектах, такие способы включают стадию введения субъекту антитела или его фрагмента, полученного путем иммунизации млекопитающего композицией вакцины по любому из пп. 28-34, в количестве, обеспечивающем эффективную профилактику или лечение инфекции Borrelia или лаймской болезни. В некоторых аспектах, антитело или его фрагмент представляет собой гипериммунную сыворотку, гипериммунную плазму или их очищенную иммуноглобулиновую фракцию.
Изобретение включает способы пассивной профилактики инфекции Borrelia или лаймской болезни у субъекта, включающие стадию введения субъекту анти-OspA антитела или его фрагмента, полученного путем иммунизации млекопитающего любой из композиций вакцины, описанных тут, в количестве, обеспечивающем эффективную профилактику инфекции Borrelia или лаймской болезни, где антитело или его фрагмент представляют собой очищенный препарат иммуноглобулина или препарат иммуноглобулинового фрагмента.
Изобретение включает способы профилактики инфекции Borrelia или лаймской болезни у субъекта, включающие стадию введения субъекту анти-OspA моноклонального антитела или его фрагмента, вырабатываемого после иммунизации субъекта любой из композиций вакцины, описанных тут, в количестве, обеспечивающем эффективную профилактику инфекции Borrelia или лаймской болезни. В некоторых аспектах, моноклональное антитело или его фрагмент являются гуманизированными. В конкретном аспекте, моноклональное антитело представляет собой F237/BK2.
Изобретение включает использование композиций по изобретению для изготовления лекарственных препаратов. Настоящее изобретение также предусматривает другие родственные аспекты.
Изложенная выше сущность изобретения не предназначена для описания всех аспектов изобретения, и дополнительные аспекты описаны в других разделах, таких как приведенное далее детальное описание. Весь документ должен рассматриваться как единое раскрытие изобретения и следует понимать, что предусматриваются все комбинации признаков, описанных тут, даже если комбинация признаков не встречается вместе в одном и том же предложении, или абзаце, или разделе данного документа. Другие признаки и преимущества изобретения будут понятны из приведенного далее детального описания. Следует понимать, однако, что детальное описание и конкретные примеры, указывающие конкретные варианты воплощения изобретения, приводятся только с целью иллюстрации, потому что различные изменения и модификации сущности и объема изобретения будут понятны квалифицированным специалистам в данной области техники из данного детального описания.
Краткое описание чертежей
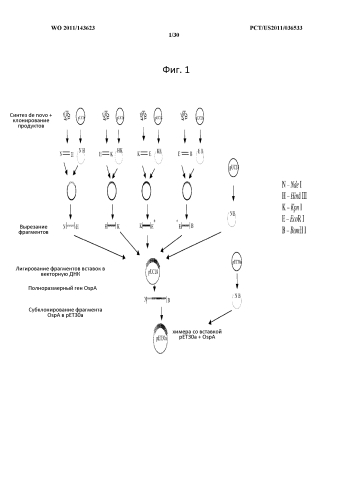
Фигура 1 представляет собой общую схему получения липидированных химерных конструктов OspA.
Фигура 2 представляет собой аминокислотную последовательность lipB sOspA 1/2251 (SEQ ID NO: 2).
Фигура 3 изображает нуклеотидную (SEQ ID NO: 1) и расшифрованные аминокислотные последовательности (SEQ ID NO: 2) lipB sOspA 1/2251.
Фигура 4 представляет собой аминокислотную последовательность lipB sOspA 6/4 (SEQ ID NO: 4).
Фигура 5 изображает нуклеотидную (SEQ ID NO: 3) и расшифрованные аминокислотные последовательности (SEQ ID NO: 4) lipB sOspA 6/4.
Фигура 6 представляет собой аминокислотную последовательность lipB sOspA 5/3 (SEQ ID NO: 6).
Фигура 7 изображает нуклеотидную (SEQ ID NO: 5) и расшифрованные аминокислотные последовательности (SEQ ID NO: 6) lipB sOspA 5/3.
Фигура 8 изображает оптимизацию использования кодонов для высокого уровня экспрессии.
Фигура 9 изображает различия между последовательностями липидированных и нелипидированных конструктов.
Фигура 10 представляет собой описание системы экспрессии T7.
Фигура 11 представляет собой результаты анализа способом ДСН-ПААГ, показывающие экспрессию новых рекомбинантных белков OspA индуцированными и неиндуцированными культурами.
Фигура 12 представляет собой карту плазмиды pUC18.
Фигура 13 представляет собой карту плазмиды pET30a.
Фигура 14 изображает стратегию создания фрагмента Kpn I - Bam HI lipB sOspA 5/3.
Фигура 15 изображает выравнивание с указанием аминокислотной замены (SEQ ID NO: 39) в lipB sOspA 1/2251 и праймерные последовательности PCR (SEQ ID NOS: 21 и 41), используемые для введения замены (lipB OspA 1/2 mod (SEQ ID NO: 38); консенсусная последовательность (SEQ ID NO: 40)).
Фигура 16 изображает выравнивание OspA-последовательности Blip OspA BPBP/A1 с модифицированной молекулой lipB sOspA 1/2251. Верхняя нить представляет собой исходную последовательность (SEQ ID NO: 42), и нижняя нить представляет собой оптимизированную последовательность (SEQ ID NO: 43). Примечание: три основания (CAT) в начале последовательности не показаны; они образуют часть сайта Nde I CATATG.
Фигура 17 изображает выравнивание OspA-последовательности Blip OspA KT с модифицированной молекулой lipB sOspA 6/4. Верхняя нить представляет собой исходную последовательность (SEQ ID NO: 44) и нижняя нить представляет собой оптимизированную последовательность (SEQ ID NO: 45). Примечание: Одно основание (C) в начале последовательности не показано; оно входит в состав сайта Nde I CATATG.
Фигура 18 изображает выравнивание OspA-последовательности Blip OspA 5/3 с модифицированной молекулой lipB sOspA 5/3. Верхняя нить представляет собой исходную последовательность (SEQ ID NO: 46) и нижняя нить представляет собой оптимизированную последовательность (SEQ ID NO: 47).
Фигура 19 изображает распределение функциональных анти-OspA ответов по результатам проведения анализов на поверхностное связывание антител и ингибирование роста у защищенных и инфицированных животных, иммунизированных 3 нг OspA 1/2 перед контрольным заражением штаммом B. burgdorferi s.s. B31. p-Значения Манна-Уитни продемонстрировали высокозначимые различия по содержанию функциональных антител между защищенными и инфицированными животными.
Фигура 20 изображает распределение функциональных анти-OspA ответов по результатам проведения анализов на поверхностное связывание антител и ингибирование роста у защищенных и инфицированных животных, иммунизированных 3 нг OspA 1/2 перед контрольным заражением природными клещами. p-Значения Манна-Уитни продемонстрировали высокозначимые различия по содержанию функциональных антител между защищенными и инфицированными животными.
Фигура 21 изображает поверхностное связывание (средние интенсивности флуоресценции (MFI)) и ингибирование роста (титры GI-50) в пуле мышиной сыворотки после иммунизации тремя дозами 3-компонентной вакцины химерного OspA. Эффективное поверхностное связывание и ингибирование роста наблюдались для всех шести штаммах Borrelia, экспрессирующих типы OspA, гомологичные типам OspA в вакцине (типы 1-6).
Фигура 22 изображает титры средней интенсивности флуоресценции (MFI), которые были получены с использованием сывороток дня 42 индивидуальных мышей, иммунизированных комбинациями вакцин rOspA путем проведения анализа на поверхностное связывание (SBA). Результаты показали, что все три компонента rOspA (1/2, 6/4 и 5/3) являются необходимыми в мультивалентной вакцине для индуцирования высоких титров поверхностного связывания IgG-антител против всех 6 штаммов у C3H-мышей. Двухкомпонентные вакцины не покрывают полностью 2 отсутствующие штамма.
Фигура 23 изображает ингибирование роста Borreliae с использованием сыворотки дня 42 индивидуальных мышей (в группах по 10), иммунизированных комбинациями вакцин rOspA. Только мультивалентная вакцина (вакцина, содержащая все три штамма) давала >50% ингибирования роста у >90% животных (n=10). Черные столбики (со сплошной заливкой) указывают штаммы, гомологичные использованной вакцине.
Фигура 24 изображает покрытие (coverage) Borreliae, экспрессирующих внутритиповые варианты OspA. Поверхностное связывание было классифицировано на сильное (усиление флуоресценции >10-кратного) или более слабое (2-10-кратное усиление флуоресценции).
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение предусматривает химерные молекулы OspA, пригодные для использования в качестве антигенов, которые могут быть введены как иммуногенная композиция или композиция вакцины при лаймской болезни или инфекции Borrelia. Перед детальным пояснением каких-либо вариантов воплощения изобретения укажем, что изобретение не должно рассматриваться как ограниченное в его применении деталями конструкции и конфигурацией компонентов, указанных в приведенном ниже описании или проиллюстрированных на фигурах и в примерах. Используемые тут заголовки разделов приводятся только в организационных целях и не должны пониматься как ограничивающие описываемый предмет. Все упоминаемые в данной заявке первоисточники явным образом включены сюда в качестве ссылок.
Изобретение охватывает другие варианты воплощения и практикуется или осуществляется различными способами. Также, следует понимать, что фразеология и терминология, используемые тут, предназначены для описания и не должны рассматриваться как ограничивающие. Термины "включающий", "содержащий" или "имеющий" и их варианты следует понимать как охватывающие перечисленные далее позиции и их эквиваленты, а также дополнительные позиции.
Варианты воплощения изобретения проиллюстрированы на примерах конструирования и синтеза трех химерных кодирующих последовательностей OspA, которые кодируют три различные липидированные молекулы OspA, обладающие некоторыми общими признаками. Каждая химерная кодирующая последовательность представляет два серотипа OspA, и химерные кодирующие последовательности были сконструированы таким образом, чтобы они кодировали стабильные химерные молекулы OspA, являющиеся безопасными и сильно иммуногенными, и обеспечивающие защиту субъекта против инфекции B. burgdorferi sensu lato (s.l.).
В одном аспекте, химерные молекулы OspA содержат проксимальный участок от одного серотипа OspA, вместе с дистальным участком от другого серотипа OspA, сохраняя при этом защитные свойства обоих родительских полипептидов. Химерные молекулы нуклеиновой кислоты OspA экспрессировали в Escherichia coli (E. coli) для получения антигенов, которые могли быть введены в комбинированную вакцину для обеспечения защиты против всех шести распространенных серотипов (серотипы 1-6), ассоциированных с лаймской болезнью или инфекцией Borrelia в Европе и против единственного серотипа OspA, ассоциированного с лаймской болезнью или инфекцией Borrelia в Северной Америке. Поскольку вакцина, содержащая серотипы 1-6, обеспечивает защиту против B. afzelii, B. garinii и B. burgdorferi, вакцина предназначена для глобального применения.
Изобретение также включает приготовление второго набора химерных кодирующих последовательностей OspA которые, в одном аспекте, являются производными от первого набора из трех генов, путем удаления последовательностей нуклеиновых кислот, кодирующих лидерную последовательность, необходимую для продуцирования липидированной молекулы OspA. Два набора конструктов (дающих липидированные и нелипидированные полипептиды) были необходимы для оценки простоты их продуцирования в ферментере (биомасса, стабильность, выход продуктов и т.д.), для определения того, насколько легко может осуществляться очистка разных типов антигена и для сравнения их биологических характеристик (профиль безопасности и эффективность защиты).
Изобретение включает иммуногенные композиции, содержащие химерные молекулы OspA по изобретению. Изобретение аналогично включает вакцины и наборы вакцин, содержащих такие молекулы OspA, способы получения иммуногенных композиций и вакцин и использование иммуногенных композиций и вакцин в медицинской терапии и профилактике человека и животных. Изобретение дополнительно включает способы иммунизации против лаймской болезни или инфекции Borrelia с использованием композиций OspA, описанных тут, и использование композиций OspA в производстве лекарственных средств для профилактики лаймской болезни или инфекция Borrelia.
Определения
Если не указано иное, то все технические и научные термины, используемые тут, имеют значения, общеизвестные рядовым специалистам в области техники, к которой принадлежит данное изобретение. Следующие источники содержат общие определения многих терминов, используемых в данном изобретении: Singleton, et al., DICTIONARY OF MICROBIOLOGY AND MOLECULAR BIOLOGY (2d ed. 1994); THE CAMBRIDGE DICTIONARY OF SCIENCE AND TECHNOLOGY (Walker ed., 1988); THE GLOSSARY OF GENETICS, 5TH ED., R. Rieger, et al. (eds.), Springer Verlag (1991); и Hale и Marham, THE HARPER COLLINS DICTIONARY OF BIOLOGY (1991).
В тексте используются следующие аббревиатуры:
| AA | аминокислота |
| Amp | ампициллин |
| п.о. (bp) | пар оснований |
| B. afzelii | Borrelia afzelii |
| B. burdorferi | Borrelia burgdorferi |
| B. garinii | Borrelia garinii |
| ДНК (DNA) | дезоксирибонуклеиновая кислота |
| dNTPs | дезоксинуклеотидтрифосфат |
| E. coli | Escherichia coli |
| содержание GC | процент последовательности, содержащей основания гуанин и цитозин |
| hLFA-1 | ассоциированный с функцией лейкоцитов человеческий антиген-1 |
| ВЭЖХ (HPLC) | высокоэффективная жидкостная хроматография |
| IP | интеллектуальная собственность |
| IPTG | изопропил-бета-D-тиогалактопиранозид |
| Kan | канамицин |
| кДа (kDa) | килодальтон |
| LB | среда Луриа |
| Lip B | лидерная последовательность внешнего поверхностного белка B |
| Mab | моноклональное антитело |
| OD | оптическая плотность |
| OspA | внешний поверхностный белок A |
| OspB | внешний поверхностный белок B |
| ПЦР (PCR) | полимеразная цепная реакция |
| РНК (RNA) | рибонуклеиновая кислота |
| s.l. | sensu lato |
| s.s. | sensu stricto |
| ДСН (SDS) | додецилсульфат натрия |
| SMK | питательная среда для E. coli (среда с кетоглутаратом-сорбитом) |
| тРНК (tRNA) | транспортная рибонуклеиновая кислота |
| WCB | рабочий банк клеток |
Отметим, что, в используемом в данном описании и приложенной формуле изобретения значении, формы единственного числа (в английском тексте - с артиклями “a”, “an” и “the”) включают ссылки на множественное число, если из контекста явным образом не следует иное.
В используемом тут значении, следующие термины имеют указанные для них значения, если не будет указано иное.
Термин “ген” относится к ДНК-последовательности, кодирующей последовательность аминокислот, которая содержит все или часть одного или более полипептидов, белков или ферментов, и может включать или не включать интроны и регуляторные ДНК-последовательности, такие как промоторные или энхансерные последовательности, 5'-нетранслируемую область или 3'-нетранслируемую область, которые влияют, например, на условия, в которых ген экспрессируется. В данном описании, ген OspA является бактериальным и потому не содержит интронов. Термин “кодирующая последовательность” относится к ДНК-последовательности, которая кодирует последовательность аминокислот, но не содержит интронов или регуляторных последовательностей. Аналогично, в данном описании кодирующая последовательность OspA не содержит регуляторных последовательностей.
“Нуклеиновая кислота”, или “последовательность нуклеиновой кислоты”, или “молекула нуклеиновой кислоты” относится к дезоксирибонуклеотидам или рибонуклеотидам и их полимерам в одно- или двухцепочечной форме. Термин охватывает нуклеиновые кислоты, которые содержат известные нуклеотидные аналоги или модифицированные остатки в основной цепи или связи, являются синтетическими, природными и неприродными, обладают способностью к связыванию, близкой к эталонной нуклеиновой кислоте, и подвергаются метаболизму аналогично эталонным нуклеотидам. Примеры таких аналогов включают, без ограничений, фосфоротиоаты, фосфорамидаты, метилфосфонаты, хиральные метилфосфонаты, 2-O-метилрибонуклеотиды, пептидо-нуклеиновые кислоты (PNAs). Термины охватывают молекулы, состоящие из любых известных аналогов оснований ДНК и РНК, таких как, без ограничений, 4-ацетилцитозин, 8-гидрокси-N6-метиладенин, азиридинилцитозин, псевдоизоцитозин, 5-(карбоксигидроксилметил)урацил, 5-фторурацил, 5-бромурацил, 5-карбоксиметиламинометил-2-тиоурацил, 5-карбоксиметиламинометилурацил, дигидроурацил, инозин, N6-изопентениладенин, 1-метиладенин, 1-метилпсевдоурацил, 1-метилгуанин, 1-метилинозин, 2,2-диметилгуанин, 2-метиладенин, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-метиладенин, 7-метилгуанин, 5-метиламинометилурацил, 5-метоксиаминометил-2-тиоурацил, бета-D-маннозилквеозин, 5'-метоксикарбонилметилурацил, 5-метоксиурацил, 2-метилтио-N6-изопентениладенин, урацил-5-оксиуксусной кислоты сложный метиловый эфир, урацил-5-оксиуксусная кислота, оксибутоксозин, псевдоурацил, квеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, N-урацил-5-оксиуксусной кислоты сложный метиловый эфир, урацил-5-оксиуксусная кислота, псевдоурацил, квеозин, 2-тиоцитозин и 2,6-диаминопурин.
Если не указано иное, конкретная последовательность нуклеиновой кислоты также охватывает по умолчанию ее консервативно модифицированные варианты (напр., замещения вырожденного кодона) и комплементарные последовательности, а также явным образом указанную последовательность. Конкретнее, замещения вырожденного кодона, в некоторых аспектах, получают путем генерирования последовательностей, в которых третье положение одного или более выбранных (или всех) кодонов замещено остатками смешанных оснований и/или дезоксиинозина (Batzer et al., Nucleic Acid Res. 19:5081 (1991); Ohtsuka et al., J. Biol. Chem. 260:2605-2608 (1985); Rossolini et al., Mol. Cell. Probes 8:91-98 (1994)). Термин нуклеиновая кислота используется взаимозаменяемо с геном, кДНК, мРНК, олигонуклеотидом и полинуклеотидом.
Термины “полипептид”, “пептид” и “белок” используются в данном описании взаимозаменяемо по отношению к полимеру, состоящему из аминокислотных остатков, соединенных пептидными связями. Термины относятся к аминокислотным полимерам, в которых один или несколько аминокислотных остатков представляют собой искусственный химический миметик соответствующей природной аминокислоты, а также к природным аминокислотным полимерам и неприродным аминокислотным полимерам. Термин “белок” типично относится к крупным полипептидам. Термин “пептид” типично относится к коротким полипептидам. Синтетические полипептиды могут быть синтезированы, например, с помощью автоматического полипептидного синтезатора.
Термин “молекула OspA” или “химерная молекула OspA” относится, в одном аспекте, к “нуклеиновой кислоте OspA”, содержащей нуклеотидную последовательность SEQ ID NO: 1 (lipB sOspA 1/2251), SEQ ID NO: 3 (lipB sOspA 6/4), SEQ ID NO: 5 (lipB sOspA 5/3), SEQ ID NO: 7 (sOspA 1/2251), SEQ ID NO: