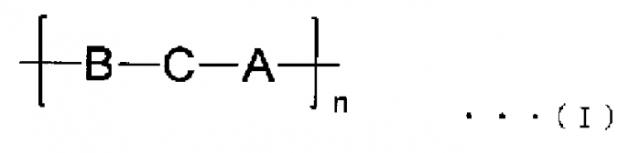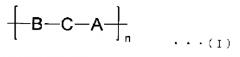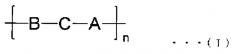Биоразрушаемая частица, вещество для васкулярной эмболизации и способ получения биоразрушаемых частиц
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к эндоваскулярной хирургии, и раскрывает биоразрушаемую частицу для эмболизации и способ получения стерилизованной биоразрушаемой частицы. Биоразрушаемая частица включает блоксополимер, получаемый путем сополимеризации биоразрушаемого сополимера, образованного из гидроксикарбоновых кислот a1 и a2, гомополимеры которых имеют температуру стеклования не менее 40°C не более -40°C соответственно, водорастворимого полимера, включающего аминогруппу, гидроксильную или карбоксильную группу у каждого из обоих концов указанного водорастворимого полимера, и поливалентного соединения, включающего дикарбоновую кислоту, ее галогенангидрид, кислотные ангидриды или сложный эфир. Способ включает стадию сополимеризации биоразрушаемого сополимера, водорастворимого полимера и поливалентного соединения для получения блоксополимера, стадии грануляции, нанесения покрытия и радиационного облучения вышеуказанной биоразрушаемой частицы. Группа изобретений позволяет получать биоразрушаемые частицы для васкулярной эмболизации, которые менее склонны к коагуляции, имеют улучшенную гибкость, форма которых восстанавливается после прохождения через катетер. 3 н. и 6 з.п ф-лы, 7 пр., 2 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к биоразрушаемой частице, веществу для васкулярной эмболизации и способу получения биоразрушаемой частицы.
Предпосылки создания изобретения
В целях гемостаза в разрезе пораженной зоны, блокирования подачи питательного вещества к опухоли, поддерживания концентрации противоракового лекарственного средства в опухоли, и т.п., сополимер поли(молочная кислота/гликолевая кислота) (патентный документ 1), блоксополимер на основе полиэтиленгликоля и полимолочной кислоты (патентные документы 2-5) или мультиблочный сополимер, получаемый путем сополимеризации молочной кислоты, полиэтиленгликоля, многоосновной карбоновой кислоты и т.п. (патентный документ 6) используют в качестве полимерных частиц для эмболизации кровеносных сосудов и т.п.
Такие полимерные частицы для эмболизации кровеносных сосудов и т.п. используют в форме сферических частиц для того, чтобы непроницаемо и надежно подвергать эмболизации кровеносные сосуды и т.п. Однако, так как частицы доставляются на место-мишень, как, например, кровеносный сосуд, через микрокатетер, или т.п., частицам присущи проблемы, как например недостаточная гибкость самих частиц, проявление агрегации, вызывающей закупоривание катетера, и необратимая деформация полимерных частиц до их достижения места-мишени.
Для того чтобы решить эти проблемы, были сделаны попытки предотвращения их агрегации, например, путем нанесения покрытия на поверхность полимерных частиц с помощью полиэтиленгликоля, и, следовательно, увеличения их способности проходить через катетер (патентный документ 7), путем смешения множества типов полимеров для контролирования гибкости полимерных частиц (патентный документ 8) или путем получения химически сшитых полимерных частиц (патентный документ 9).
Документы уровня техники
[Патентные документы]
[Патентный документ 1] заявка на патент Японии JP 5-969 A
[Патентный документ 2] заявка на патент Японии JP 5-17245 B
[Патентный документ 3] заявка на патент Японии JP 2004-167229 A
[Патентный документ 4] заявка на патент Японии JP 2005-312623 А
[Патентный документ 5] заявка на патент Японии JP 2007-291323 A
[Патентный документ 6] публикация заявки на патент США под номером 2009/0117033
[Патентный документ 7] заявка на патент Японии JP 2007-145826 А
[Патентный документ 8] заявка на патент Японии JP 2007-146146 А
[Патентный документ 9] заявка на патент Японии JP 2005-314535 А
Краткое изложение сущности изобретения
Проблемы, решаемые посредством изобретения
Однако, хотя увеличение способности прохождения через катетер и улучшение за счет контролирования гибкости полимерных частиц можно наблюдать в улучшенных способах, как, например, нанесение покрытия на поверхность полимерных частиц (патентный документ 7), смешение множества типов полимеров (патентный документ 8) и использование химически сшитых полимерных частиц (патентный документ 9), можно наблюдать недостаточное улучшение с точки зрения проблемы необратимой деформации полимерных частиц и, следовательно, необходимо дальнейшее улучшение для достижения эффекта хорошей эмболизации в случае кровеносных сосудов и т.п. То есть, необходимо усовершенствование вещества для эмболизции кровеносных сосудов и т.п., где усилена способность полимерных частиц восстанавливать свою первоначальную форму после прохождения через катетер (в дальнейшем упоминают как «способность восстановления формы частицы»).
Принимая это во внимание, настоящее изобретение направлено на получение биоразрушаемого вещества для васкулярной эмболизации, которое менее склонно к коагуляции и имеет улучшенную гибкость, и форма частицы которого восстанавливается после ее прохождения через катетер, или т.п.
Способы решения проблем
То есть, настоящее изобретение относится к биоразрушаемой частице, веществу для васкулярной эмболизации и способам получения ее, описываемым ниже в пп.(1)-(9).
(1) Биоразрушаемая частица, включающая блоксополимер, получаемый путем сополимеризации: биоразрушаемого сополимера, имеющего структуру, состоящую из, по меньшей мере, гидроксикарбоновой кислоты а1 и гидроксикарбоновой кислоты а2; водорастворимого полимера, включающего функциональную группу, выбираемую из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы, у каждого из обоих концов; и поливалентного соединения, включающего 2 или более функциональных групп, каждая, выбираемая из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы; где гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а1 имеет температуру стеклования не менее чем 40°С, гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а2 имеет температуру стеклования не более чем -40°С, и массовая пропорция структуры, состоящей из гидроксикарбоновой кислоты а2, в биоразрушаемом сополимере составляет от 30% масс. до 90% масс.
(2) Биоразрушаемая частица по п.(1), где блоксополимер представляет собой мультиблочный сополимер, включающий повторяющееся звено нижеприводимой общей формулы (I):
[Химическая формула I]
где А означает блок, образованный биоразрушаемым сополимером или сополимером, получаемым путем ковалентного связывания 2 или более биоразрушаемых сополимеров; В означает блок, образованный водорастворимым полимером; С означает одинарную связь или структуру, образованную поливалентным соединением; и n означает целое число 1 или более.
(3) Биоразрушаемая частица по п.(1) или (2), где сжимающая на 40% нагрузка в насыщенном водой состоянии составляет не более чем 500 мН, и, когда степень сжатия в насыщенном водой состоянии составляет 10%, степень восстановления сжатия составляет не менее чем 40%.
(4) Биоразрушаемая частица по любому одному из пп.(1)-(3), где средневесовая молекулярная масса блоксополимера составляет от 3000 до 300000.
(5) Биоразрушаемая частица по любому одному из пп.(1)-(4), где средневесовая молекулярная масса водорастворимого полимера составляет от 200 до 50000.
(6) Биоразрушаемая частица по любому одному из пп.(1)-(5), где гидроксикарбоновая кислота а1 представляет собой молочную кислоту.
(7) Биоразрушаемая частица по любому одному из пп.(1)-(6), где гидроксикарбоновая кислота а2 представляет собой 6-гидроксикапроновую кислоту.
(8) Вещество для васкулярной эмболизации, образованное из биоразрушаемых частиц по любому из пп.(1)-(7).
(9) Способ получения стерилизованной биоразрушаемой частицы, включающий:
стадию сополимеризации:
биоразрушаемого сополимера, имеющего структуру, образованную из, по меньшей мере, гидроксикарбоновой кислоты а1 и гидроксикарбоновой кислоты а2, где гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а1 имеет температуру стеклования не менее чем 40°С, гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а2 имеет температуру стеклования не более чем -40°С, и массовая пропорция структуры, образованной гидроксикарбоновой кислотой а2, в биоразрушаемом сополимере составляет 30-90% масс.;
водорастворимого полимера, включающего функциональную группу, выбираемую из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы, у каждого из обоих концов; и
поливалентного соединения, включающего 2 или более функциональных групп, каждая, выбираемая из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы,
для получения блоксополимера;
стадию грануляции блоксополимера для получения биоразрушаемой частицы; и
стадию радиационного облучения биоразрушаемой частицы с помощью излучения для получения стерилизованной биоразрушаемой частицы.
Эффект изобретения
Биоразрушаемые частицы согласно настоящему изобретению могут быть подходящим образом использованы в качестве вещества для васкулярной эмболизации, так как агрегация частиц происходит менее вероятно и частицы могут быть легко доставлены на место-мишень, как например кровеносный сосуд, не вызывая закупоривания внутренней стороны катетера или т.п. Далее, так как биоразрушаемые частицы согласно настоящему изобретению обладают повышенной способностью восстановления формы частицы после прохождения через катетер или т.п., место-мишень может быть эффективно подвергнуто эмболизации, используя минимально необходимое количество частиц.
Наилучший вариант осуществления изобретения
Термины, используемые в настоящем описании, представляют собой нижеприводимые термины, если не указано ничего другого.
Баоразрушаемая частица согласно настоящему изобретению включает блоксополимер, получаемый путем сополимеризации: биоразрушаемого сополимера, имеющего структуру, образованную, по меньшей мере, гидроксикарбоновой кислотой а1 и гидроксикарбоновой кислотой а2; водорастворимого полимера, включающего функциональную группу, выбираемую из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы, у каждого из обоих концов; и поливалентного соединения, включающего 2 или более функциональных групп, каждая, выбираемая из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы; где гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а1 имеет температуру стеклования не менее чем 40°С, гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а2, имеет температуру стеклования не более чем -40°С, и массовая пропорция структуры, образованной гидроксикарбоновой кислотой а2, в биоразрушаемом сополимере составляет 30-90% масс.
Термин «биоразрушаемость» означает свойство частицы, образованной из конкретного блоксополимера или биоразрушаемого сополимера, разрушаться, растворяться, абсорбироваться или метаболизироваться в живом организме, или свойство частицы или сополимера выводиться из организма наружу.
Термин «гидроксикарбоновая кислота» включает галоидангидриды гидроксикарбоновых кислот, ангидриды гидроксикарбоновых кислот, эфиры гидроксикарбоновых кислот и циклические соединения, как, например, циклические димеры гидроксикарбоновых кислот. Далее, с точки зрения гидроксикарбоновой кислоты, имеющей оптические изомеры, как например яблочная кислота или винная кислота, гид-роксикарбоновая кислота включает все из своих D-изомеров и L-изомеров и их смеси. Далее, гидроксикарбоновая кислота включает сополимеры, получаемые путем сополимеризации этих гидроксикарбоновых кислот. Примеры гидроксикарбоновой кислоты включают гликолевую кислоту, молочную кислоту, глицериновую кислоту, гидроксимасляную кислоту, яблочную кислоту, винную кислоту, гидроксивалериановую кислоту, 3-гидроксигексановую кислоту и 6-гидроксикапроновую кислоту. Примеры циклического соединения, образованного из гидроксикарбоновой кислоты, включают гликолид, который представляет собой циклический димер гликолевой кислоты, лактид, который представляет собой циклический димер молочной кислоты, и ε-капролактон, который соответствует 6-гидроксикапроновой кислоте. Примеры сополимера, получаемого путем сополимеризации гидроксикарбоновых кислот, включают сополимеры молочной кислоты и гликолевой кислоты и сополимеры 6-гидроксикапроновой кислоты и гликолевой кислоты. Среди них примеры «гидроксикарбоновой кислоты а1», гомополимер которой, получаемый путем гомополимеризации, имеет температуру стеклования не менее чем 40°С, включают молочную кислоту, сополимеры молочной кислоты и гликолевой кислоты, сополимеры молочной кислоты и терефталевой кислоты и сополимеры молочной кислоты и изофталевой кислоты; и примеры «гидроксикарбоновой кислоты а2», гомополимер которой, получаемый путем гомополимеризации, имеет температуру стеклования не более чем -40°С, включают 6-гидроксикапроновую кислоту, сополимеры 6-гидроксикапроновой кислоты и гликолевой кислоты и сополимеры 6-гидроксикапроновой кислоты и полибутиленсукцината (сополимер 1,4-бутандиола и янтарной кислоты). В частности, гидроксикарбоновая кислота а1 предпочтительно представляет собой молочную кислоту, а гидроксикарбоновая кислота а2 предпочтительно представляет собой 6-гидроксикапроновую кислоту. Термин «гомополимер» означает полимер, получаемый путем полимеризации одного типа мономеров как, например, полимолочная кислота, которую получают путем полимеризации одной молочной кислоты, однако, термин «гомополимер, получаемый путем гомополимеризации», согласно настоящему изобретению, также включает полимеры, получаемые путем полимеризации одного типа сополимеров, как например сополимеры молочной кислоты и гликолевой кислоты.
Хотя макромолекулярное соединение с высокой температурой стеклования имеет низкую мобильность полимерной молекулярной цепи вследствие ее массивности, высокой жесткости и низкой подвижности, гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а1 имеет температуру стеклования, предпочтительно, не менее чем 50°С, более предпочтительно, не менее чем 55°С. Гомополимер, получаемый путем гомополимеризации гидроксикарбоновой кислоты а2, имеет температуру стеклования, предпочтительно, не более чем -50°С, более предпочтительно, не более чем -55°С.
Термин «биоразрушаемый сополимер» означает сополимер, обладающий биоразрушаемостью. Термин «сополимер», как используется в данном контексте, означает макромолекулярное соединение, получаемое путем сополимеризации 2 или более типов мономеров, то есть, сополимеризованный продукт, имеющий структуру, образованную из 2 или более типов мономеров. Биоразрушаемому сополимеру согласно настоящему изобретению необходимо иметь структуру, образованную из, по крайней мере, гидроксикарбоновой кислоты а1 и гидроксикарбоновой кислоты а2, то есть, включать гидроксикарбоновую кислоту а1 и гидроксикарбоновую кислоту а2 в качестве исходных мономеров, однако, биоразрушаемый сополимер может иметь структуру, образованную из мономеров (в дальнейшем упоминают как «мономер а3»), других, чем гидроксикарбоновая кислота а1 или гидроксикарбоновая кислота а2. Примеры соединения, которое соответствует мономеру а3, включают диолы, как например гликолевая кислота или гликолид, этиленгликоль, пропиленгликоль, триметиленгликоль, диэтиленгликоль и 1,4-бутандиол; дикарбоновые кислоты, как например щавелевая кислота, малоновая кислота, янтарная кислота, глутаровая кислота, адипиновая кислота, пимелиновая кислота, субериновая кислота, азелаиновая кислота, себациновая кислота, яблочная кислота, винная кислота и додекандиовая кислота; и их галогенангидриды, ангидриды и сложные эфиры. Предпочтительным в качестве мономеров является гликолевая кислота или гликолид или полибутиленсукцинат.
Каждая из гидроксикарбоновой кислоты а1 и гидроксикарбоновой кислоты а2 может быть смесью из 2 или более типов гидроксикарбоновых кислот. Мономер а3 также может представлять собой смесь из 2 или более типов соединений.
Массовая пропорция структуры, образованной гидроксикарбоновой кислотой а2, в биоразрушаемом сополимере должна составлять 30-90% масс. и, для достижения соответствующей гибкости полученной биоразрушаемой частицы, массовая пропорция составляет, предпочтительно, 50-85% масс., более предпочтительно, 70-80% масс.
В случаях, где мономер а3 представляет собой гликолевую кислоту или гликолид, массовая пропорция структуры, образованной мономером а3, в биоразрушаемом сополимере составляет, предпочтительно, не менее чем 5% масс., предпочтительно, не менее чем 10% масс., для дальнейшего повышения биоразрушаемости. С другой стороны, массовая пропорция составляет, предпочтительно, не более чем 35% масс., более предпочтительно, не более чем 30% масс., для избежания снижения растворимости в органическом растворителе.
В случаях, где средневесовая молекулярная масса биоразрушаемого сополимера является очень незначительной, получаемая биоразрушаемая частица желирует и прилипает к внутренней стороне катетера. С другой стороны, в случаях, где средневесовая молекулярная масса является очень большой, биоразрушаемость получаемой биоразрушаемой частицы является низкой. Следовательно, средневесовая молекулярная масса биоразрушаемого сополимера составляет, предпочтительно, от 200 до 100000, более предпочтительно, от 1000 до 80000. Средневесовая молекулярная масса биоразрушаемого сополимера может быть измерена посредством гельпроникающей хроматографии (в дальнейшем упоминают как «GPC-метод» при следующих условиях:
[Условия измерения]
Аппаратура (колонка): TSK gel GMHHR-M (выпускается фирмой Toso Corporation; внутренний диаметр 7,8 мм; длина 30 см; две колонки расположены линейно)
Элюент: хлороформ
Температура колонки: 35°С
Объемная скорость потока: 1,0 мл/мин.
Метод детектирования: показатель преломления
Калибровочная кривая: получаемая при использовании стандартных образцов полистирола
Примеры «водорастворимого полимера, включающего функциональную группу, выбираемую из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы, у каждого из обоих концов» включают полиалкиленгликоли, как например полиэтиленгликоль (в дальнейшем упоминают как «ПЭГ») и полипропиленгликоль и их производные; и сополимеры алкиленгликоля и избыточного количества дикарбоновой кислоты. Водорастворимые полимеры, имеющие гидроксильную группу у обоих концов, являются предпочтительными, и, вследствие своей высокой биосовместимости и биоразрушаемости, более предпочтительным является ПЭГ. Карбоксильная группа может быть превращена в галогенангидридную структуру, сложноэфирную структуру или ангидридную структуру.
В случаях, где средневесовая молекулярная масса водорастворимого полимера является очень незначительной, гидрофильность получаемой биоразрушаемой частицы является низкой и, следовательно, не может быть достигнута равномерная биоразрушаемость. С другой стороны, в случаях, где средневесовая молекулярная масса является очень большой, экскрекция водорастворимого полимера в виде продукта разложения получаемой биоразрушаемой частицы из организма является затруднительной. Следовательно, средневесовая молекулярная масса водорастворимого полимера составляет, предпочтительно, от 200 до 50000, более предпочтительно, от 1000 до 40000. Средневесовая молекулярная масса водорастворимого полимера может быть измерена посредством GPC-метода.
Примеры «поливалентного соединения, включающего 2 или более функциональных групп, каждая, выбираемая из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы» включают дикарбоновые кислоты, как например щавелевая кислота, малоновая кислота, янтарная кислота, глутаровая кислота, адипиновая кислота, пимелиновая кислота, субериновая кислота, азелаиновая кислота, себациновая кислота, яблочная кислота, винная кислота и додекандиовая кислота; лимонная кислота; и мультиразветвленные полимеры, как например гиперразветвленные полимеры и дендримеры, которые имеют 2 или более функциональных групп, каждая, выбираемая из группы, состоящей из гидроксильной группы, аминогруппы и карбоксильной группы, у концов ответвлений; и их галогенангидриды, ангидриды и сложные эфиры. То есть, карбоксильная группа может быть превращена в галогенангидридную структуру, сложноэфирную структуру или ангидридную структуру.
Термин «блоксополимер» означает сополимер, имеющий молекулярную структуру, где 2 или более типов полимеров с различными свойствами связаны вместе через ковалентную(ные) связь(связи) с образованием длинной цепи, и термин «блок» означает каждый из «2 или более типов полимеров с разными свойствами», образующих блоксополимер. Блоксополимер согласно настоящему изобретению получают путем сополимеризации биоразрушаемого сополимера, водорастворимого полимера и поливалентного соединения, как описано выше, и предпочтительно представляет собой мультиблоксополимер, имеющий повторяющееся звено, представленное ниже общей формулой (I):
[Химическая формула 2]
где А означает блок, образованный из биоразрушаемого сополимера или сополимера, получаемого путем ковалентного связывания 2 или более биоразрушаемых сополимеров; В означает блок, состоящий из водорастворимого полимера; С означает одинарную связь или структуру, состоящую из поливалентного соединения; и n означает целое число 1 или более.
Ковалентная связь может быть образована между концевой гидроксильной группой или аминогруппой водорастворимого полимера и карбоксильной группой поливалентного соединения. Далее, ковалентная связь может быть образована между терминальной карбоксильной группой водорастворимого полимера и гидроксильной группой или аминогруппой поливалентного соединения. Карбоксильная группа каждого из них может быть превращена в галогенангидридную структуру, сложноэфирную структуру или ангидридную структуру.
Величина Х, которую рассчитывают в соответствии с нижеприводимым уравнением 1 из: значения Nb, которое представляет собой число молей водорастворимого полимера; значения m, которое представляет собой число гидроксильных групп, аминогрупп и карбоксильных групп в поливалентном соединении; и значения Nc, которое представляет собой число молей поливалентного соединения; составляет, предпочтительно, от 0,8 до 1,2, более предпочтительно, от 0,9 до 1,1.
Х=(2×Nb)/(m×Nc)…Уравнение 1
В этом уравнении, Nb и Nc рассчитывают в соответствии с нижеприводимыми уравнением 2 и уравнением 3, соответственно.
Nb=Wb/Mwb…Уравнение 2
Wb: масса (г) водорастворимого полимера, используемого в реакции сополимеризации
Mwb: средневесовая молекулярная масса (г/моль) водорастворимого полимера, используемого в реакции сополимеризации
Nc=Wc/Mwc…Уравнение 3
Wc: масса (г) поливалентного соединения, используемого в реакции сополимеризации
Mwc: молекулярная масса (г/моль) поливалентного соединения, используемого в реакции сополимеризации
В случаях, где средневесовая молекулярная масса блоксополимера является очень незначительной, получаемая биоразрушаемая частица желирует и прилипает к внутренней стороне катетера. С другой стороны, в случае, где средневесовая молекулярная масса является очень большой, биоразрушаемость получаемой биоразрушаемой частицы является низкой. Следовательно, средневесовая молекулярная масса блоксополимера составляет, предпочтительно, от 3000 до 300000, более предпочтительно, от 4000 до 200000. Средневесовая молекулярная масса блоксополимера может быть измерена посредством GPC-метода.
Для достижения соответствующей растворимости в воде или в органическом растворителе, массовое соотношение блока А к блоку В в мультиблоксополимере составляет, предпочтительно, от 100% масс. до 600% масс., более предпочтительно, от 150% масс. до 550% масс., еще более предпочтительно, от 200% масс. до 500% масс.
Массовая пропорция конкретной структуры в биоразрушаемом сополимере, массовое соотношение блока А к блоку В в мультиблоксополимере и т.п. могут быть рассчитаны на основании результата измерения посредством спектроскопии протонного ядерного магнитного резонанса (в дальнейшем упоминают как «1Н-ЯМР») при следующих условиях. Например, в случаях, где гидроксикарбоновой кислотой а1 является молочная кислота, характерным является атом водорода в α-положении, который имеется в метиновой группе (величина химического сдвига примерно 5,2 м.д.). В случаях, где гидроксикарбоновой кислотой а2 является 6-гидроксикапроновая кислота, характерным является атом водорода α-положении, который имеется в метиленовой группе (величина химического сдвига примерно 2,3 м.д.). В случаях, где мономер а3 представляет собой гликолевую кислоту, характерным является атом водорода в α-положении, который имеется в метиленовой группе (величина химического сдвига примерно 4,8 м.д.). Далее, в случаях, где водорастворимым полимером является ПЭГ, характерными являются 4 атома водорода в этиленовой группе (величина химического сдвига примерно 3,5 м.д.). Базируясь на интегрированной величине сигнала, который появляется при химическом сдвиге для каждого из этих характерных атомов водорода, может быть рассчитана массовая пропорция каждого.
[Условия измерения]
Аппаратура: JNM-EX270 (выпускается фирмой JEOL, 270 МГц)
Растворитель: дейтерированный хлороформ (содержащий 0,05% об. тетраметилсилана в качестве внутреннего стандарта)
Температура измерения: 20°С
В случае биоразрушаемой частицы согласно настоящему изобретению, сжимающая на 40% нагрузка в насыщенном водой состоянии составляет не более чем 500 мН, и, когда степень сжатия в насыщенном водой состоянии составляет 10%, степень восстановления сжатия составляет не менее чем 40%.
Термин «насыщенное водой состояние» означает состояние, где, когда примерно 20 мг биоразрушаемых частиц погружено в 10 мл забуференного фосфатом соляного раствора при температуре 37°С (в то время, как пробирка в качестве контейнера вращается при использовании ротатора со скоростью 0,5 поворотов в секунду для перемешивания содержимого пробирки), содержание воды в биоразрушаемой частице является постоянным. Термин «постоянное содержание воды», как используется в данном контексте, означает состояние, где, когда массу биоразрушаемых частиц, погруженных в забуференный фосфатом соляной раствор при температуре 37°С, измеряют каждую минуту, степень ее изменения со временем составляет не более чем 10%. Степень изменения со временем представляет собой величину Rw (%), которая может быть рассчитана в соответствии с нижеприводимым уравнением 4.
Rw={W(t)-W(t-1)}/W(t)×100…Уравнение 4
W(t): масса (г) биоразрушаемой частицы после погружения в воду на t минут
W(t-1): масса (г) биоразрушаемой частицы после погружения в воду на (t-1) минут
Выражение «сжимающая на 40% нагрузка» представляет собой показатель, представляющий гибкость биоразрушаемой частицы, и означает нагрузку, необходимую для сжатия одной биоразрушаемой частицы на 40% диаметра исходной частицы. В случаях, где сжимающая на 40% нагрузка является очень незначительной, форма биоразрушаемой частицы не может сохраняться, тогда как в случаях, где сжимающая на 40% нагрузка является очень большой, стойкость во время прохождения через катетер или т.п. является высокой, так что, сжимающая на 40% нагрузка биоразрушаемой частицы согласно настоящему изобретению в насыщенном водой состоянии составляет, предпочтительно, 5-500 мН, более предпочтительно, от 10 мН до 450 мН.
Сжимающая на 40% нагрузка биоразрушаемой частицы согласно настоящему изобретению может быть измерена, используя испытательный прибор на микросжатие при следующих условиях. Более конкретно, нагрузку прикладывают к частице до установленного затем тест-усилия в целях определения нагрузки, необходимой для сжатия частицы на 40% диаметра исходной частицы.
[Условия измерения]
Название теста: тест на сжатие
Аппаратура: МСТ-510 (выпускается фирмой Shimadzu Corporation)
Установленное тест-усилие: 4903 мН
Скорость нагружения: 207 мН/с
Время удерживания нагрузки: 0 с
Показатель верхней опрессовки: плоскость, 500 мкм (диаметр).
Выражение «степень восстановления сжатия» означает способность биоразрушаемой частицы восстанавливаться после прохождения через катетер, имеющий небольшой внутренний диаметр, или т.п., и становиться свободной от сжатия, принимающей первоначальную форму, которая сохранялась до сжатия. То есть, степень восстановления сжатия означает показатель, представляющий собой способность восстановления формы частицы. В случаях, где степень восстановления сжатия очень незначительная, биоразрушаемая частица проходит место-мишень кровеносного сосуда, который должен быть эмболизован, и «стекает» в нисходящем направлении. Следовательно, степень восстановления сжатия биоразрушаемой частицы согласно настоящему изобретению при степени сжатия 10% в насыщенном водой состоянии составляет, предпочтительно, не менее чем 40%, более предпочтительно, не менее чем 50%.
Степень восстановления сжатия биоразрушаемой частицы согласно настоящему изобретению при степени сжатия 10% в насыщенном водой состоянии также измеряют, используя тестер микросжатия при следующих условиях, и соответствует величине Rr (%), рассчитываемой в соответствии с уравнениями 5-7, приводимыми ниже. Более конкретно, нагрузку прикладывают к каждой частице до установленного тест-усилия, получаемого в тесте на сжатие, при степени сжатия 10% (то есть, максимальное тест-усилие), и нагрузку затем удаляют до минимального тест-усилия.
[Условия измерения]
Название теста: тест нагрузка/удаление нагрузки
Аппаратура: МСТ-510 (выпускается фирмой Shimadzu Corporation)
Установленное тест-усилие: тест-усилие, получаемое в тесте на сжатие, когда степень сжатия каждой частицы составляет 10%
Скорость нагружения: 4,5 мН/с
Время удерживания нагрузки: 2 с
Показатель верхней опрессовки: диаметр плоскости, 500 мкм (диаметр)
L1=L1b-L1a …Уравнение 5
L1a: изменение диаметра частицы (мкм) во время нагрузки минимального тест-усилия
L1b: изменение диаметра частицы (мкм) во время нагрузки максимального тест-усилия
L2=L2b-L1a …Уравнение 6
L2b: изменение диаметра частицы (мкм) во время нагрузки максимального тест-усилия, затем путем удаления нагрузки до минимального тест-усилия
Rr={(L1-L2)/L1}×100…Уравнение 7
Термин «степень сжатия» означает соотношение диаметра частицы после сжатия биоразрушаемой частицы к ее исходному диаметру, и соответствует величине Cr (%), рассчитываемой в соответствии с уравнением 8, приводимым ниже.
Cr=(L1/d)×100…Уравнение 8
d: средний диаметр (мкм) биоразрушаемой частицы
Принимая во внимание диаметр кровеносного сосуда в случае основного места-мишени эмболизации, средний диаметр биоразрушаемой частицы согласно настоящему изобретению составляет, предпочтительно, 5-2000 мкм, более предпочтительно, 10-1500 мкм. Диаметр лекарственной биоразрушаемой частицы согласно настоящему изобретению может быть измерен посредством метода светорассеяния.
Вещество для васкулярной эмболизации согласно настоящему изобретению состоит из биоразрушаемой частицы согласно настоящему изобретению.
В случаях, где биоразрушаемую частицу согласно настоящему изобретению используют в качестве вещества для васкулярной эмболизации, биоразрушаемая частица может быть использована такой, какая есть, или может быть использована в виде дисперсии в контрастной или дисперсионной среде. Примеры контрастной среды, согласно данному контексту, включают водорастворимые контрастные среды, как, например, инъекционный раствор иопамидола, инъекционный раствор иогексола и инъекционный раствор иоксагликолевой кислоты; и масляные контрастные среды, как, например, иодированное маковое масло. Предпочтительны водорастворимые контрастные среды. Примеры дисперсионной среды включают водные инъекционные растворы и растительные масла, как, например, кунжутное масло и кукурузное масло, содержащие диспергатор, такой как полиоксисорбитановый эфир жирной кислоты, консервант, такой как метилпарабен, или изотонический агент, такой как хлорид натрия. Вещество для васкулярной эмболизации также может содержать антисептик, стабилизатор, солюбилизатор, наполнитель и/или эффективный компонент, такой как противоопухолевый агент.
Способ получения стерилизованной биоразрушаемой частицы согласно настоящему изобретению включает: стадию сополимеризации биоразрушаемого сополимера, водорастворимого полимера и поливалентного соединения для получения блоксополимера; стадию грануляции блоксополимера для получения биоразрушаемой частицы; и стадию радиационного облучения биоразрушаемой частицы с помощью излучения для получения стерилизованной биоразрушаемой частицы.
«Стадия сополимеризации» представляет собой стадию получения блоксополимера путем сополимеризации биоразрушаемого сополимера, водорастворимого полимера и поливалентного соединения. Для контролирования массовой пропорции и т.п. каждой конкретной структуры в биоразрушаемом сополимере, соответственно, предпочтительным является предварительное получение биоразрушаемого сополимера и затем сополимеризация полученного биоразрушаемого сополимера с водорастворимым полимером и поливалентным соединением. Альтернативно, смесь из: гидроксикарбоновой кислоты а1 и гидроксикарбоновой кислоты а2 (и, при необходимости, мономера 3); и водорастворимого полимера и поливалентного соединения; может быть немедленно подвергнута сополимеризации. Альтернативно, только гидроксикарбоновая кислота а1 и гидроксикарбоновая кислота а2 могут быть предварительно сополимеризованы, затем добавляют мономер а3, когда осуществляют сополимеризацию с водорастворимым полимером и поливалентным соединением.
В случаях, где гидроксикарбоновая кислота а1, гидроксикарбоновая кислота а2 и мономер а3 представляют собой молочную кислоту, 6-гидроксикапроновую кислоту и гликолевую кислоту или т.п., соответственно, реакция сополимеризации на стадии сополимеризации предпочтительно является поликонденсацией. С другой стороны, в случаях, где гидроксикарбоновая кислота а1, гидроксикарбоновая кислота а2 и мономер а3 представляют собой циклические соединения, например, лактид, ε-капролактон и гликолид, соответственно, предпочтительной является полимеризация с раскрытием цикла.
В случаях, где биоразрушаемый сополимер получают предварительно, растворитель для реакции представляет собой хороший растворитель для гидроксикарбоновой кислоты а1 и гидроксикарбоновой кислоты а2 (и, когда необходимо, мономера а3). Примеры хорошего растворителя включают дихлорметан, хлороформ и тетрагидрофуран, и смешанные растворители на их основе. Температуру реакции устанавливают такой, чтобы хороший растворитель находился в состоянии кипения с обратным холодильником. Давление реакции может быть пониженным давлением, однако, для простоты операции, предпочтительным является нормальное давление. Время реакции составляет, предпочтительно, 2-24 часа, более предпочтительно, 4-20 часов, для подходящим образом контролирования молекулярной массы получаемого биоразрушаемого сополимера.
С другой стороны, в случаях, где гидроксикарбоновая кислота а1, гидроксикарбоновая кислота а2 и мономер а3 представляют собой циклические соединения, например, лактид, ε-капролактон и гликолид, соответственно, то есть, в случаях, где реакция сополимеризации представляет собой полимеризацию с раскрытием цикла, предпочтительно не использовать растворитель для реакции и устанавливать температуру реакции 100-180°С, более предпочтительно, 110-160°С, для повышения реакционной способности.
В случаях, где биоразрушаемый сополимер получают предварительно, общая концентрация гидроксикарбоновой кислоты а1 и гидроксикарбоновой кислоты а2 (и, когда необходимо, мономера а3) составляет, предпочтительно, 10-100% масс., более предпочтительно, 50-100% масс., хотя общая концентрация изменяется в зависимости от типа гидроксикарбоновых кислот и т.п. С точки зрения концентрации катализатора в растворителе для реакции, если концентрация является очень высокой, удаление катализатора после реакции является затруднительным, тогда как, если концентрация является очень низкой, реакция едва протекает, так что концентрация катализатора составляе