Извлечение жидких элементов путем электролиза оксидов
Иллюстрации
Показать всеИзобретение относится к электролитическому извлечению элемента из соответствующего исходного оксида. Исходное соединение растворяют в расплаве оксида в контакте с катодом и анодом в электролитической ячейке. В процессе электролиза извлекаемый элемент осаждается на жидком катоде и сплавляется с ним. На аноде, содержащем слой твердого оксида поверх металлической анодной подложки, находящемся в контакте с расплавом оксида, выделяется кислород. Для осуществления способа имеется устройство для электролитического извлечения упомянутого элемента из исходного оксида. Техническим результатом является извлечение элементов без использования углерода при получении элементов высокой чистоты. 2 н. и 28 з.п. ф-лы, 4 ил.
Реферат
Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США №61/375935, поданной 23 августа 2010 года Antoine Allanore et al. на способ и устройство для электролиза расплавленных оксидов, содержащих аноды на основе металлического сплава, а также предварительной заявки на патент США №61/489565, поданной 24 мая 2011 года Antoine Allanore et al, на способ и устройство для электролиза расплавленных оксидов, содержащих аноды на основе металлического сплава, содержание которых включено в настоящую заявку во всей полноте посредством ссылки.
Уровень техники
Область техники
Настоящее изобретение относится к извлечению тугоплавких элементов из оксидных руд. В частности, в настоящем изобретении предложены электролитические способы с применением металлических анодов для электролитического извлечения элементов из расплавов оксидов.
Уровень техники
Традиционные способы плавки в случае большинства металлов приводят к выбросу парниковых газов. Например, традиционно применяемый способ получения железа в доменной печи сопряжен со значительным количеством промышленных выбросов, связанных с процессами получения кокса и восстановления железной руды. Процессы горения также вносят вклад в выброс углерода за счет дополнительных стадий процесса, таких как подготовка руды. Производство стали из передельного чугуна также связано с потреблением энергии, например, в электродуговых печах, которая может обеспечиваться за счет сжигания ископаемого топлива. Как полагают, на долю производства железа и стали приходится несколько процентов мирового объема выбросов парниковых газов.
В связи с уменьшением разрешенных объемов выбросов парниковых газов особенно важное значение приобретает поиск альтернативных способов осуществления основных операций процесса плавки металлов. Соответственно, существует потребность в способах извлечения металлов, которые характеризуются пониженным расходом углерода и углеродных видов топлив.
Параллельно растет заинтересованность в способах получения металлов, содержащих растворенный углерод в концентрациях, труднодостижимых при помощи традиционных способов при приемлемой стоимости. Следовательно, особенную ценность имеет технология извлечения без применения углерода, способная обеспечивать получение металлов исключительной чистоты.
Краткое описание изобретения
В рамках способа извлечения целевого элемента из оксидного сырья, содержащего целевой элемент, предложен жидкий электролит, содержащий по меньшей мере 75% масс. оксида. Оксидное сырье растворяют в жидком электролите. Анод, содержащий металлическую анодную подложку, приводят в контакт с электролитом. Катод размещают в контакте с электролитом напротив анода. Растворенное оксидное сырье подвергают электролизу, при этом электроны переносятся от кислородсодержащих предшественников в электролите в металлическую подложку через оксидный слой подложки с образованием газообразного кислорода. Частицы, входящие в состав электролита, содержащего целевой элемент, восстанавливаются с образованием целевого элемента на катоде.
В другом варианте реализации способа извлечения целевого элемента из оксидного сырья, содержащего целевой элемент, предложен жидкий электролит, в котором растворено оксидное сырье. Анод в контакте с электролитом на границе раздела содержит металлическую анодную подложку. По меньшей мере 50% масс. подложки составляет по меньшей мере один элемент, являющийся более реакционноспособным по отношению к кислороду по сравнению с целевым элементом при рабочей температуре границы раздела. Жидкий катод находится в контакте с электролитом напротив анода. Растворенное оксидное сырье подвергают электролизу, при этом электроны перемещаются от кислородсодержащих предшественников в электролите в металлическую подложку через оксидный слой подложки с образованием газообразного кислорода. Частицы, входящие в состав электролита, содержащего целевой элемент, восстанавливаются с образованием целевого элемента на катоде.
В другом варианте реализации способа извлечения железа из исходного оксида предложен жидкий электролит с по меньшей мере 75% масс. оксида, в котором растворено оксидное сырье. Анод в контакте с электролитом на границе раздела содержит металлическую анодную подложку. По меньшей мере 50% масс. подложки составляет хром и по меньшей мере 1% масс. составляет железо. Жидкий катод находится в контакте с электролитом напротив анода. Растворенное оксидное сырье подвергают электролизу, при этом электроны перемещаются от кислородсодержащих предшественников в электролите в металлическую подложку с образованием газообразного кислорода. Частицы в электролите, содержащем целевой элемент, восстанавливаются с образованием целевого элемента на катоде.
Устройство содержит жидкий электролит с по меньшей мере 75% масс. оксида, в том числе кислородсодержащие предшественники и частицы, содержащие целевой элемент, в зависимости от оксидного сырья, растворенного в электролите. Жидкий катод находится в контакте с электролитом. Анод находится в контакте с электролитом напротив катода. Анод содержит металлическую анодную подложку и слой твердого оксида, контактирующий с электролитом на границе раздела. Устройство при подсоединении анода и катода к источнику питания выполнено с возможностью электролиза растворенного оксидного сырья, переноса электронов от кислородсодержащих предшественников через слой твердого оксида с образованием газообразного кислорода и восстановления частиц, содержащих целевой элемент, с образованием целевого элемента на катоде.
В другом варианте реализации устройство содержит жидкий электролит с по меньшей мере 75% масс. оксида, который включает кислородсодержащие предшественники и частицы, содержащие железо, в зависимости от оксидного сырья, растворенного в электролите. Жидкий катод находится в контакте с электролитом. Анод контактирует с электролитом напротив катода. Анод содержит металлическую анодную подложку, которая содержит по меньшей мере 50% масс. хрома и по меньшей мере 1% масс. железа. Устройство при подсоединении анода и катода к источнику питания выполнено с возможностью электролиза растворенного соединения оксидного сырья, переноса электронов от кислородсодержащих предшественников с образованием газообразного кислорода и восстановления частиц, содержащих железо, с образованием железа на катоде.
Краткое описание чертежей
Предшествующее описание станет более понятным из последующего подробного описания настоящего изобретения, при рассмотрении совместно с прилагаемыми чертежами, в которых одинаковые номера позиций указывают на идентичные или функционально схожие элементы:
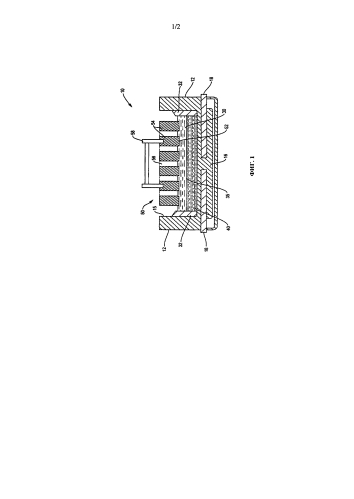
ФИГ.1 представляет собой вертикальное сечение, показывающее электрохимическое устройство, предназначенное для извлечения целевого элемента из соединения оксидного сырья согласно настоящему изобретению.
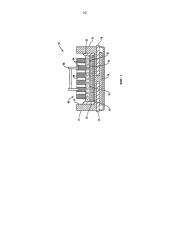
ФИГ.2 представляет собой схему, показывающую электрохимическое устройство из ФИГ.1, включенное в цепь с источником питания согласно настоящему изобретению.
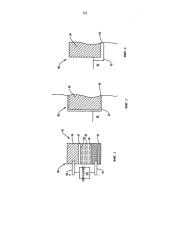
ФИГ.3 представляет собой вертикальное сечение, показывающее фрагмент анода, на подложке которого при предварительном электролизе в электрохимическом устройстве согласно настоящему изобретению формируется оксидный слой; и
ФИГ.4 представляет собой вертикальное сечение, показывающее фрагмент анода, который получали предварительно до помещения в электрохимическое устройство согласно настоящему изобретению.
Следует иметь в виду, что указанные фигуры не обязательно изображены в масштабе.
Подробное описание иллюстративного варианта реализации
Электролиз расплавленных оксидов (molten oxide electrolysis, "МОЕ") включает в себя прямой электролиз исходного оксида с целью извлечения из него целевого элемента. МОЕ обеспечивает получение целевого металла с образованием газообразного кислорода и без выделения, или с выделением восстановленного, углекислого газа или других нежелательных летучих соединений. Поскольку целевой металл восстанавливают непосредственно из оксидов, подготовительная обработка исходных соединений является намного более чистой и простой, чем в случае обычных способов извлечения для большинства металлов. МОЕ обладает потенциалом для производства металла исключительной чистоты, особенно в отношении так называемых элементов внедрения, а именно углерода и азота. Поскольку МОЕ обеспечивает получение целевого элемента из жидкой формы, можно избежать трудностей, связанных с дендритными отложениями. Кроме того, МОЕ является энергоэффективным для извлечения элемента в его жидком состоянии, поскольку необратимые изменения, неотъемлемо сопровождающие прохождение электрического тока через компоненты электролитической ячейки, также служат для поддержания компонентов ячейки при требуемых высоких температурах.
Целевой элемент может иметь высокую температуру плавления, например более 1200°C или 1400°C. Примеры включают марганец (Tm=1246°C), кремний (Tm=1414°C), никель (Tm=1455°C), кобальт (Tm=1495°C), железо (Tm=1538°C), титан (Tm=1670°C), цирконий (Tm=1855°C), хром (Tm=1907°C).
Вероятные подходящие исходные оксиды содержат желаемый целевой элемент и кислород. Например, возможные подходящие исходные оксиды для извлечения титана включают, но не ограничиваются ими, монооксид титана (TiO), полуторную окись титана (Ti2O3), диоксид титана (TiO2). Никель можно извлекать из оксида никеля, например NiO. Железо можно извлекать из оксида железа, например оксида железа (Fe2O3) или закиси-окиси железа (Fe3O4). Хром можно извлекать из оксида хрома (Cr2O3). Марганец можно извлекать из оксида марганца, например MnO, Mn3O4, Mn2O3, MnO3 или Mn2O7. Фаза смешанного оксида, например хромит (FeCr2O4) и ильменит (FeTiO3), в качестве исходного соединения позволяет из одного соединения получать осадок, состоящий из двух элементов.
Согласно ФИГ.1 и ФИГ.2 в иллюстративном варианте реализации электрометаллургическая ячейка, пригодная для извлечения целевого элемента из соединения оксидного сырья, включает жидкий электролит 30, катод 40 и анод 50. Электролит 30 и катод 40 содержатся в оболочке ячейки или в корпусе 12.
Катод 40 является, например, жидкостью, содержащей целевой элемент. Внутри корпуса 12, например, расположена электронно-проводящая подложка катода 16, на которой находится катод 40. Подложка катода 16 является, например, веществом, устойчивым к воздействию катода 40. В некоторых вариантах реализации подложка катода 40 может быть молибденовой. Стержни катодных металлических токоприемников 18, заделанные в подложку катода 16, обеспечивают соединение катода 40 с внешним источником питания 60 и служат в качестве отрицательного полюса во время работы ячейки 10.
Электролит 30 контактирует с катодом 40 на границе раздела электролит-электрод 35. Электролит 30 является жидкостью, способной растворять оксидное сырье, содержащее целевой элемент. Например, электролит 30 представляет собой расплавленную оксидную смесь или расплав оксида. Устройство 10, например, работает в условиях, которые приводят к образованию периферического замерзшего слоя электролита 32 между расплавом оксида 30 и внутренними стенками 15 корпуса 12. Замерзший слой электролита 32 защищает внутренние стенки 15 от химического воздействия расплава оксида 30.
Анод 50 погружен в электролит 30 напротив катода 40. Анод 50 может являться единым и непрерывным. В качестве иллюстрации, каналы 56, проходящие через анод 50, разработаны в качестве соответствующих путей между верхней поверхностью электролита 30 и внешней стороной ячейки 10. Электронно-проводящая металлическая анодная подложка 54, например, содержит на себе слой твердого оксида 61, предназначенный для ограничения расхода подложки 54 до приемлемого уровня во время работы ячейки 10. Анод 50 контактирует с электролитом 30 на границе раздела 52 с ним. Электронно-проводящие металлические стержни анода 58, встроенные в анод 50, выполнены с возможностью обеспечения соединения анода 50 с внешним источником питания 60 и служат в качестве положительного полюса во время работы ячейки 10.
Эквивалентно, множество по существу идентичных анодных блоков представляют собой анод 50. Проводящая металлической анодная подложка 54 каждого из блоков, например, содержит на себе слой твердого оксида 61. Анодные блоки находятся в электрической связи с общим анодным приемником 58, имеют общий электрический потенциал и расположены с промежутками друг между другом, образующими каналы 56.
Соответствующие составы электролита 30, анода 50 и катода 40, корпуса 12 и других элементов ячейки 10 выбирают с учетом взаимной совместимости и обеспечения требуемых рабочих параметров и срока службы ячейки 10.
Жидкий катод 40 может являться по существу идентичным по составу желаемому целевому элементу. Альтернативно, жидкий катод 40 дополнительно содержит элементы, отличные от получаемого целевого элемента. Основной и остаточный расплавленные металлы, изготавливаемые из металла более благородного, чем целевой металл, могут служить в качестве катода 40, например катод из расплава меди 40, на который осаждается никель, или катод из расплава железа 40, на который осаждается хром. Указанный случай можно совмещать с прямым получением сплава желаемого состава при добавлении, посредством восстановления частиц в электролите 30, как описано ниже, одного или более элементов для сплавления с компонентами, которые уже содержатся в катоде 40. Катод 40 с составом, с которым производимый целевой элемент легко сплавляется, составляет среду пониженной активности целевого элемента по сравнению с моноэлементной жидкостью. В указанном случае напряжение, необходимое для превращения исходного оксида в целевой элемент при помощи МОЕ в ячейке 10, соответственно снижается. Многоэлементный катод также может обеспечить возможность работы МОЕ ячейки 10 при температуре ниже, чем температура плавления целевого элемента, при производстве жидкого продукта. Как вариант, катод 40 может являться твердым веществом.
Электролит 30 в ячейке 10, как правило, представляет собой растворитель, одно или более вспомогательных соединений и другие, необязательные, ингредиенты, растворенные в нем. Электролит 30 растворяет оксидное сырье, обеспечивая наличие кислородсодержащих анионных частиц и катионных предшественников для производства целевого элемента.
Согласно настоящему описанию касательно электролита 30 термин расплав оксида обозначает жидкость, получаемую путем плавления одного или более твердых оксидов, с содержанием по меньшей мере 25% масс., 50% масс., 75% масс., 85% масс. или более электролита 30. В качестве иллюстрации, состав электролита удовлетворяет нескольким критериям. Состав расплава оксида 30 для извлечения целевого тугоплавкого элемента выбирают согласно его способности растворять соединение сырья, содержащее целевой элемент, а также другим химическим и физическим свойствам, известным специалистам в данной области техники. Электролит 30, в качестве иллюстрации, имеет температуру плавления ниже, чем температура плавления целевого элемента (или сплава, составляющего катод 40), и тем самым обеспечивает применимость MOE ячейки 10 с адекватной текучестью электролита. Электролит 30, обладающий плотностью намного ниже, чем плотность целевого элемента при применяемом профиле температуры в MOE ячейке 10, позволяет осуществлять гравитационное отделение электролита 30 от целевого элемента, осажденного на катоде 40.
Электрическая проводимость электролита 30 является, например, достаточно низкой, чтобы при практических значениях межэлектродного пространства и плотности потока количество теплоты Джоуля являлось достаточным для поддержания желаемых высоких рабочих температур в МОЕ ячейке 10. В качестве иллюстрации электрическая проводимость электролита может составлять от 0,5 до 1,0 или 2,0 См/см. Для сравнительно небольшого расстояния анод-катод проводимость электролита может составлять менее 0,5 См/см. Относительно низкий электронный вклад в электрическую проводимость жидкого электролита, т.е. примерно меньше чем 10% от общей электронной проводимости, позволяет получать элемент при помощи MOE при приемлемо высокой фарадеевской эффективности. Низкое давление паров компонентов электролита при температурах внутри ячейки 10 и высокие потенциалы разложения компонентов электролита по сравнению с потенциалом разложения исходного соединения ограничивают потерю вещества из электролита 30 и изменение его состава в течение срока службы MOE ячейки 10.
Расплав оксида электролита 30 может содержать, например, кремнезем, глинозем, оксид магния и оксид кальция. Жидкости, содержащие оксид кальция (СаО), могут являться, в силу своего положения в электрохимическом ряду, подходящими расплавами оксидов. Например, жидкости на основе двойной системы оксид магния-оксид кальция (MgO-CaO) с добавками диоксида кремния (SiO2), оксида алюминия (Al2O3) или других оксидов может обеспечивать подходящие расплавы оксидов для извлечения относительно инертных тугоплавких элементов, таких как никель, железо или хром. Электролит 30 может содержать оксид, содержащий один или более из бериллия, стронция, бария, тория, урана, гафния, циркония и редкоземельный металл. Согласно настоящему описанию редкоземельные металлы представляют собой пятнадцать лантаноидов, а также скандий и иттрий. Указанные компоненты электролита также могут содержаться в аноде 50 для обеспечения преимущества в процессе электролиза в ячейке 10, как описано ниже со ссылкой на ФИГ.4.
Иллюстративный анод 50 служит главным образом в качестве акцептора электронов своей поверхностью на границе раздела 52, которая, в качестве иллюстрации, представляет собой поверхность, способную выдерживать выделение кислорода при приемлемом напряжении. Соответственно, фрагмент анода 50, контактирующий с электролитом 30 в ячейке 10, является по существу инертным, является стабильным в агрессивной среде и при высоких температурах. Таким образом, анод 50 может нуждаться в меньшей частоте замены по сравнению с обычным расходом анода. Относительно стабильный контур на границе раздела 52, предусмотренный составом на границе раздела 52, может обеспечить меньшее расстояние между катодом 40 и анодом 50. Данное расположение требует более низкого напряжения для управления электролизом и, следовательно, обеспечивает более низкую стоимость на единицу производимого целевого элемента по сравнению с расположением с большим расстоянием.
Металлические свойства подложки 54 наделяют анод 50 преимуществами по отношению к стоимости и простоты производства в больших сложных формах по сравнению с высокотемпературными веществами, такими как графит, композитные материалы или керамика. Следовательно, иллюстративный анод 50 может работать при значительно более низкой температуре, чем катод 40, например, благодаря охлаждению, индуцированному выделением газа на границе раздела 52.
Металлическая анодная подложка 54 содержит непрерывную металлическую фазу. Металлическая фаза может состоять главным образом из основного металлического элемента. Согласно настоящему описанию слово элемент в отношении анода 50 имеет обычное химическое значение, обозначающее элемент периодической таблицы. Вероятные подходящие элементы для основного металлического элемента подложки анода 54 в ячейке 10 включают, например, Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Y, Zr, Nb, Mo, Hf, Ta, W, один из благородных металлов или целевой элемент, получаемый в ячейке 10. Основной металлический элемент анодной подложки 54 может быть более реакционноспособным по отношению к кислороду, чем целевой элемент при рабочей температуре границы раздела 52. Другими словами, энергия Гиббса образования оксида для преобладающего металлического элемента может быть большей величины, чем для желаемого целевого элемента, или оксид преобладающего металлического элемента является более стабильным, чем оксид целевого элемента. Альтернативно, преобладающий металлический элемент может являться целевым элементом. Несколько из целевых элементов, вероятно подходящих элементов, перечисленные выше, и/или элементов, имеющих стабильные оксиды, могут вместе составлять больше чем 50% анодной подложки 54. Металлическая фаза может быть номинально моноэлементной, т.е. состоять из преобладающего элемента, за исключением малых содержаний неопределенных примесей, например порядка 0,01% масс., 0,1% масс. или 1% масс.
Альтернативно, металлическая фаза подложки 54 может представлять собой сплав, содержащий преобладающий металлический элемент и дополнительный миноритарный элемент или множество таких миноритарных элементов. Преобладающий металлический элемент может содержаться в подложке 54 в концентрации 50% масс., 60% масс., 70% масс., 80% масс., 90% масс. или больше. Один или несколько металлических элементов в подложке 54 могут присутствовать в суммарных концентрациях по меньшей мере 1% масс., 5% масс., 10% масс., 15% масс., 25% масс., 35% масс. или 45% масс. от общего содержания металлов в сплаве. Отдельные миноритарные элементы могут содержаться в количестве по меньшей мере 0,1% масс., 1% масс., 5% масс., 10% масс., 15% масс. или 25% масс. от общего содержания металлов в сплаве.
Состав сплава в подложке 54 может постепенно меняться с концентрацией преобладающего металлического элемента, возрастающей или убывающей при удалении от границы раздела. В одном варианте реализации подложка 54 постоянного или переменного состава представляет собой, по существу, весь анод 50 за исключением слоя оксида 61, нанесенного на подложку 54. В альтернативном варианте реализации анод 50 содержит непрерывную оболочку анод-сплав, которая является подложкой 54, нанесенную на ядро из металла с более низкой стоимостью по сравнению со сплавом на подложке 54 и совместимого с ним, например, по температуре плавления и свойствам теплового расширения. Переход между подложкой и ядром может являться резким или достигаться за счет постепенного изменения состава.
Миноритарный элементный компонент, составляющий меньше чем 50% масс. от массы анодной подложки54, в качестве иллюстрации, относится к одному из следующих классов; тугоплавкие элементы, перечисленные выше в качестве возможного целевого элемента; элемент, для которого энергия Гиббса образования оксида составляет меньшую величину, чем для желаемого целевого элемента при рабочей температуре границы раздела 52 в ячейке 10, и который объединяется с преобладающим металлическим элементом с образованием сплава с приемлемо высокой температурой плавления; бериллий, стронций, барий, торий, уран, гафний, цирконий или редкоземельный металл; или другой элемент, имеющий высокую температуру плавления и образующий оксид, устойчивый к окислению, при рабочих условиях в ячейке 10.
Не ограничиваясь какой-либо теорией, в настоящем изобретении полагают, что компонентный элемент в анодной подложке 54 может образовывать стабильные связи с кислородом при рабочих условиях в ячейке 10, при этом компонент является частью слоя твердого оксида 61 на границе раздела 52. Таким образом, любая реакция в ячейке 10 с участием компонента анодной подложки 54, например с ингредиентом расплава оксида 30 или любых частиц, образуемых на границе раздела 52, может являться самоограничивающейся. Оксид в слое твердого оксида 61 на границе раздела 52 может являться более стабильным, чем исходный оксид, подвергающегося электролизу с образованием целевого элемента. Таким образом, слой твердого оксида 61 на границе раздела 52 может защищать подложку 54 от чрезмерного расхода в процессе электролиза исходного соединения в ячейке 10. Элементы, образующиеся в электролите 30, также могут фиксироваться в твердом оксиде на границе раздела 52.
В одном подходе преобладающий металлический элемент в подложке 54 является тем же элементом, что и целевой элемент. В данном случае слой твердого оксида 61 может включать области, имеющие состав, аналогичный составу оксидного сырья, из которого извлекают целевой элемент. Таким образом, дополнительный электролиз оксида в слое твердого оксида 61 может приводить к приращению целевого элемента на катоде 40 без введения нежелательных загрязняющих компонентов. Тем не менее, ячейка 10 может работать для поддержания среды, насыщенной кислородом, на границе раздела 52, тем самым поддерживая слой твердого оксида 61 и, следовательно, ограничивая расход анода 50. Например, электролит 30 может являться насыщенным относительно соединения целевого элемента оксидного сырья. Такое насыщение можно поддерживать путем обеспечения достаточного количества соединения оксидного сырья, контактирующего с расплавом 30, до начала работы ячейки. Или насыщение в расплаве 30 также можно создавать в течение переходного стартового периода, в течение которого анод высвобождает вещество в расплав 30. Альтернативное локальное насыщение расплава 30 относительно кислорода устанавливается при образовании газообразного кислорода на границе раздела 52 в процессе электролиза.
В некоторых вариантах реализации анод 50 содержит хром в качестве преобладающего металлического элемента. Распространенность и относительно низкая стоимость хрома отвечает требованиям его применения в промышленных масштабах процесса извлечения металла, такого как MOE. Физические свойства хрома облегчают изготовление и обработку анода при высоких температурах. В одном варианте реализации анод на основе хрома 50 дополнительно содержит по меньшей мере один другой переходный или тугоплавкий металл, например тантал и/или ванадий. Такой анод на основе хрома 50 является подходящим для применения в ячейке 10 при температурах вплоть до 1500°C и выше. В другом варианте реализации анод на основе тугоплавкого металла дополнительно содержит железо. Железо может содержаться в количестве, большем чем 5% масс., 10% масс., 15% масс., 20% масс., 25% масс. или 30% масс.
В типовой последовательности осуществления процесса производства выбранного целевого элемента из исходного оксида в ячейке 10, анод 50 сначала удаляют из электролита 30, в результате чего цепь, которая включает источник питания 60 и ячейку 10, остается незамкнутой. Оксидное соединение вводят в электролит 30, соединение растворяется в электролите 30, в результате чего оно присутствует в электролите в форме соответствующих ионов, содержащих целевой элемент и кислород. Источник питания 60 работает в незамкнутой цепи, как если бы желаемый ток проходил через катод 40 и анод 50. Таким образом, анод 50 является анодно поляризованным. Анод 50 в поляризованном состоянии опускают в электролит 30 для образования границы раздела 52, тем самым замыкая цепь, которая включает источник 60 и ячейку 10, позволяя току протекать через ячейку 10 и инициируя электролиз в ячейке 10.
Во время работы источника питания 60 кислородсодержащие предшественники в электролите 30 перемещаются к границе раздела 52, в качестве иллюстрации, на поверхностях анода 50, обращенных к катоду 40, и поверхностях, выстилающих каналы 56. Электроны удаляются из кислородсодержащих предшественников, перемещаются через слой оксида 61 к границе раздела 52 и через металлическую подложку 54 анода 50 через анодные стержни 58. Тем самым, частицы в электролите 30 анодно окисляются на границе раздела 52 с образованием газообразного кислорода. Газ состоит в основном из кислорода и тем самым образуется на границе раздела 52, проходит через каналы 56 и выходит из ячейки 10. В процессе электролиза анод 50 может поддерживать плотность тока, усредненную по границе раздела 52 с электролитом 30, примерно или больше чем, например, 0,05 А/см2, 0,5 А/см2, 1 А/см2, 5 А/см2 или 10 А/см2.
Одновременно источник питания 60 доставляет электроны через стержни приемников 18, подложку катода 16 и катод 40. На границе раздела электролит-электрод 35 электроны перемещаются к частицам в электролите 40, содержащем целевой элемент;
Таким образом, частицы восстанавливаются с образованием целевого элемента в виде жидкости. Получаемое вещество образуется на катоде 40 и в дальнейшем функционирует как часть катода 40. Целевой металл может составлять примерно 80% масс., 90% масс., 95% масс., 99% масс. или более от количества вещества, получаемого на катоде при помощи восстановления.
Ячейка 10 может быть изначально выполнена так, чтобы содержать по меньшей мере один элемент в катоде 40, не являющийся целевым элементом. Таким образом, результат электролиза в ячейке 10 может обеспечивать наличие целевого элемента в жидком сплаве, который составляет катод 40, в силу того, что в ячейке 10 продолжается электролиз. Целевой элемент можно периодически удалять с катода 40, например, при помощи выпуска ячейки 10. Ячейку 10 можно применять для получения целевого элемента непрерывно путем постоянного добавления соединения оксидного сырья. Как вариант, более одного целевого элемента может образовываться на жидком катоде 40 в процессе работы ячейки 10 в результате одновременного или последовательного электролиза частиц, образующихся в соответствующих индивидуальных исходных оксидах или отдельных смешанных оксидах, растворенных в электролите 30.
Вне связи с какой-либо теорией, полагают, что один или несколько механизмов отвечают за состав слоя твердого оксида 61. Оксид можно получать на металлической анодной подложке 54 из металлических элементов, образующихся в металлической анодной подложке 54, до того как анод 50 помещают в ячейку 10. В одном варианте реализации анод 50 обрабатывают в окислительной атмосфере при высокой температуре для образования оксида на металлической анодной подложке 54. На ФИГ.3 изображен фрагмент анода 50, помещенный в электролит 30 после предварительного образования слоя оксида 65 на аноде 50 вне ячейки 10 (ФИГ.1). Способы получения слоя оксида на металлической подложке известны специалистам в данной области техники.
Оксид также можно образовывать на аноде 50 после его размещения в контакте с расплавом оксида 30 в ячейке 10. В этом случае кислород из электролита 30 окисляет компоненты анодной подложки 54 и становится частью анода 50. На ФИГ.4 изображен фрагмент анода 50 после образования слоя оксида 63 in situ в результате работы внешнего источника питания 60 (ФИГ.2), подсоединенного через стержни приемников 18 и анодные стрежни 58. Согласно ФИГ.2 и ФИГ.4 в полученном in situ слое оксида 63 также могут присутствовать и другие элементные компоненты электролита 30. Полученный in situ слой оксида 63 может первоначально быть образован в процессе электролиза в ячейке 10, который не приводит к получению целевого элемента на катоде 40. Кроме того, полученный in situ слой оксида 63 может первоначально быть образован на ранних стадиях электролиза растворенного соединения оксидного сырья с образованием целевого металла. Начальный расход относительно небольшой части анодной подложки 54 на границе раздела 52, в качестве иллюстрации, защищает анод 50 от чрезмерного расхода в ходе длительного непрерывного электролитического производства целевого металла, как описано выше. Слой оксида 63 может содержать области шпинели. Электронно-проводящая шпинель на границе раздела 52 может поддерживать желаемую скорость производства металла, облегчая перенос электронов от границы раздела 52 на металлическую подложку 54. Редкоземельные элементы, перемещающиеся от электролита 30 и встраивающиеся в слой твердого оксида 61 в концентрациях примерно, например, от 0,1% масс. до 1% масс., могут повышать стабильность слоя оксида 61. Редкоземельные элементы могут дополнительно встраиваться в металлическую подложку 54, тем самым повышая стабильность границы раздела между металлической подложкой 54 и слоем оксида 61.
Согласно ФИГ.2, ФИГ.3 и ФИГ.4 слой твердого оксида 61 может содержать ассоциации металл-кислород, образуемые в процессе предварительного электролиза, описанного для слоя 65, в процессе in situ, описанном для слоя оксида 63 или в результате их обоих. В одном варианте реализации слой твердого оксида 61 является слоистым, подложка 54, содержащая предварительно образованный слой оксида, покрыта слоем оксида, получаемым in situ на границе раздела 52 с электролитом 30. При другом подходе, слой твердого оксида 61 на границе раздела 52 с электролитом 30 может содержать соответствующие области предварительно образованного слоя оксида и слоя оксида, получаемого in situ. Например, шпинель может осаждаться в процессе электролиза в местах проникания шлака через слой предварительно образованного оксида основного элемента.
В качестве примера конкретного применения МОЕ, извлечение железа может давать полезную информацию, касающуюся преимуществ и особенностей, связанных с иллюстративным устройством и способом. В одном варианте реализации МОЕ, применяемый при производстве железа и/или стали, протекает следующим образом,
2Fe2O3(s)→4Fe3++6O2-→4Fe(I)+3/2O2(g),
тем самым обеспечивая резкое сокращение выбросов парниковых газов по сравнению с традиционными способами производства железа и стали. Снижения количества углекислого газа при помощи MOE можно достигать даже тогда, когда электролиз, используемый при производстве железа в ячейке 10, осуществляют за счет электроэнергии, получаемой при сжигании ископаемого топлива, например в случае природного газа.
MOE позволяет растворять в расплавленной смеси оксидов 30 ряд железных руд различных сортов, размеров частиц и морфологии. Мелкие и ультрамелкие частицы материала оксидного сырья можно вводить непосредственно в МОЕ ячейку. Таким образом, MOE может работать без расхода энергии и других затрат на стадиях гранулирования или спекания блоков, обычно применяемых перед извлечением железа. По существу, MOE подход превращает оксид железа в жидкий металл за одну стадию. Ожидается, что по существу любую фазу оксида железа, в том числе магнетит и гематит, можно вводить в шлак и в конечном счете растворять в расплаве оксида.
Более того, химическая селективность электролиза может гарантировать отсутствие фосфора или других элементов из пустой породы в железе, осажденном на катоде 40. Металл, получаемый на катоде 40, может содержать высокий процент железа, например 90% масс., 95% масс., 99% масс., 99,9% масс. или больше. Нежелательные элементы стабилизируются в ионной форме в электролите вследствие их более отрицательных потенциалов разложения, поэтому становится возможным производство железа или стали желаемой чистоты из низкосортных железных руд. Избирательность МОЕ и фактическое отсутствие углерода среди компонентов иллюстративной электролитической ячейки 10, в частности анода 50, позволяет железу на катоде 40 служить основой для сплавов высокой чистоты или составов с низким содержанием углерода, таких как нержавеющие стали.
Жидкий электролит смешанного оксида 30 или шлак, применяемые в МОЕ устройстве, например в ячейке 10, для извлечения железа, могут обладать жидкостными свойствами текучести и плотности, желаемым для шлаков, обычно применяемым в контексте извлечения железа. Для электролитического извлечения чистого железа при помощи МОЕ электролит 30, в качестве иллюстрации, характеризуется температурой плавления между 1350°C и 1450°C, при более низких температурах плавления, допустимых при производстве сплава на катоде 40, как описано выше. Жидкости в системе CaO-MgO-Al2O3-SiO2 с добавками, например, оксида иттрия, оксида циркония или оксида тория могут быть подходящими электролитами для извлечения железа.
Другой критерий отбора состава электролита относится к смешанной валентности железа. Для шлака в равновесии с атмосферным давлением и составом октаэдрически координированные катионы железа в расплаве оксида приводят к образованию полярона железа, который может способствовать переносу электронов через шлак 30. Железо (II) принимает октаэдрическую координацию, в то время как железо (III) предполагает распределение между обеими тетраэдрической и октаэдрической координационными геометриями. Вероятно, что высокоосновные шлаки имеют тенденцию стабилизировать тетраэдрически координированное железо (III) и снижать концентрацию железа (II) и октаэдрически координированного железа (III), тем самым ограничивая электронную проводимость в шлаке. Кроме того, основные