Способ получения раствора и раствор для лечения, профилактики заболеваний и повреждений роговицы
Иллюстрации
Показать всеГруппа изобретений относится к области медицины, а именно к офтальмологии и офтальмохирургии, и предназначена для получения раствора для лечения и профилактики заболеваний и повреждений роговицы. Для получения раствора стерильный хондроитинсульфат и гидроксиэтилцеллюлозу растворяют в сбалансированном солевом растворе, доведенном до кипения. Перемешивают, отстаивают и стерилизуют в автоклаве при 120°C. Одновременно с гидроксиэтилцеллюлозой добавляют гидроксипропилметилцеллюлозу, причем предварительно их стерилизуют термоударом при 120-280°C в течение 3-30 мин. При этом раствор перемешивают в течение 1 ч и отстаивают в течение 12 ч. Полученный раствор содержит, г/100,0 мл: хондроитинсульфат - 0,02-4,0; гидроксиэтилцеллюлоза - 0,15-1,0; гидроксипропилметилцеллюлоза - 0,15-1,0; сбалансированный солевой раствор - до 100,0. Использование группы изобретений позволяет повысить когезивность, репаративные, протективные, противоотечные и противовоспалительные свойства получаемого раствора. 2 н.п. ф-лы, 2 табл., 3 пр.
Реферат
Изобретение относится к области офтальмологии и офтальмохирургии, а более конкретно к медицинской промышленности, и касается получения раствора для лечения и профилактики заболеваний роговой оболочки глаза, для лечения любых повреждений тканей глаза с явлениями воспаления и отека, который также может быть использован в качестве протектора тканей глаза.
Известен способ получения раствора и раствор для защиты роговицы от повреждений, описанный в патенте RU 2336862 от 27.02.2006. Известный способ включает растворение гидроксиэтилцеллюлозы и хондроитинсульфата, перемешивание и стерилизацию.
Недостатком указанного способа является то, что в раствор к хондроитинсульфату добавляют вязкий компонент - гидроксиэтилцеллюлозу, что значительно затрудняет приготовление раствора и равномерное растворение и распределение всех компонентов по всему объему раствора. Это приводит к увеличению времени приготовления раствора.
Известеный раствор для защиты роговицы от повреждений содержит водорастворимые производные целлюлозы, гликозаминогликаны и солевой раствор.
Однако из-за отсутствия в нем ингредиентов, обеспечивающих необходимую вязкость, способствующих нормальному метаболизму клеток роговицы и протективным свойствам, он не обладает пролонгированными противовоспалительными и противоотечными свойствами.
Техническим результатом является сокращение времени приготовления раствора.
Еще одним техническим результатом, достигаемым при использовании изобретения, в части раствора для лечения, профилактики заболеваний роговицы, является повышение когезивности получаемого раствора за счет добавления смеси стерильных гидроксиэтилцеллюлозы и гидроксипропилметилцеллюлозы.
Техническим результатом, в части раствора для лечения и профилактики заболеваний и повреждений роговицы, является также повышение репаративных, протективных, противоотечных и противовоспалительных свойств за счет введения в композицию компонентов, активно влияющих на пролиферацию клеток и их метаболизм.
Технический результат согласно изобретению достигается в части способа тем, что в способе получения раствора, включающем растворение в сбалансированном солевом растворе, доведенном до кипения, стерильного хондроитинсульфата и гидроксиэтилцеллюлозы, перемешивание, отстаивание и стерилизацию в автоклаве при 120°C, одновременно с гидроксиэтилцеллюлозой добавляют гидроксипропилметилцеллюлозу, причем предварительно их стерилизуют термоударом при 120-280°C в течение 3-30 минут, перемешивание осуществляют в течение 1 часа, отстаивание раствора - в течение 12 часов.
Технический результат достигается также тем, что раствор для лечения, профилактики заболеваний и повреждений роговицы характеризуется тем, что получен по п.1 и содержит хондроитинсульфат, гидроксипропилметилцеллюлозу, гидроксиэтилцеллюлозу и сбалансированный солевой раствор при следующем соотношении компонентов, г/100,0 мл:
| Хондроитинсульфат | 0,02-4,0 |
| Гидроксиэтилцеллюлоза | 0,15-1,0 |
| Гидроксипропилметилцеллюлоза | 0,15-1,0 |
| Сбалансированный солевой раствор | до 100,0 |
Использование в качестве растворителя сбалансированного солевого раствора обусловлено несколькими обстоятельствами. Прежде всего, он содержит все минеральные компоненты, необходимые для поддержания изотоничности и осмолярности при добавлении других веществ, при нагревании без изменения pH получаемого раствора, а также обладает большой буферной емкостью, что особенно важно для метаболизма клеток тканей глаза и при хранении раствора. Так, для создания условий осмолярности, равной осмолярности плазмы крови или ультрафильтрата плазмы крови - камерной влаги (300 м/осмоль), требуются солевые растворы, строго соблюдающие эти параметры.
В изобретении используют коммерческий сбалансированный солевой раствор фирмы Алкон (BSS Canada. РОСС RU 0001 11 ИМ 02) с осмолярностью 306 м/осмоль, что не исключает применения других растворов с аналогичными свойствами и характеристиками, в том числе 0,9% раствор очищенной поваренной соли.
Сбалансированный солевой раствор согласно изобретению нагревают до кипения, что необходимо для полного растворения стерильного хондроитинсульфата и снижения пирогенности раствора.
Полученный раствор обладает дисперсивностью, отвечающей за равномерное и быстрое распределение по поверхности глаза с одновременным сохранением когезивных свойств, обеспечивающих объемность получаемой защитной пленки.
Согласно изобретению в качестве основного вещества для получения раствора для лечения и профилактики заболеваний роговицы, отличающего его от прототипа, является гидроксипропилметилцеллюлоза. Это вещество является сложным производным целлюлозы. Введение в раствор стерилизованной предлагаемым способом гидроксипропилметилцеллюлозы позволяет существенно поменять реологию раствора, положительно влияющую на его лечебное действие, что было доказано нами экспериментально.
При наружном применении, в виде инстилляций слабовязкого раствора, он способен оказывать протекторное действие на поверхность глаза, однако его действие краткосрочно. При введении в полость глаза в виде более вязкого раствора он обладает способностью защищать эндотелий роговицы от повреждающего воздействия удаляемых хрусталиковых масс при удалении катарактально измененного хрусталика. Однако из-за высокой дисперсивности блокирует защищаемую поверхность и способен вызвать кратковременное повышение внутриглазного давления. Введение гидроксипропилметилцеллюлозы в составе предлагаемого раствора позволило нивелировать этот отрицательный эффект и одновременно увеличить время удержания раствора на поверхности глаза.
Известно, что хондроитинсульфат способен положительно влиять на репарацию тканей глаза, в частности роговой оболочки, не оказывая ингибирующего действия на пролиферацию эпителиальных клеток роговицы и синтез ими коллагенов десцеметовой мембраны, что важно для предотвращения прорастания эпителия в строму поврежденной роговицы.
Хондроитинсульфат является сложным полисахаридом и входит в состав протеогликанов различных тканей глаза - роговицы, склеры, конъюнктивы, трабекулярной сети и шлеммова канала.
Основным гликозаминогликаном многих тканей глаза является хондроитинсульфат, а роговицы - кератансульфат. Биосинтез протеогликанов в тканях глаза, в частности роговицы, осуществляется главным образом активированными фибробластами стромы роговицы, эпителием и в незначительной степени эндотелием. Его лечебное действие дозозависимое и зависит от времени экспозиции этого вещества на поверхность роговицы. Введение в раствор гидроксипропилметилцеллюлозы позволило значительно увеличить время экспозиции всего раствора и хондроитинсульфата, в частности, на поверхность глаза.
Хондроитинсульфат согласно изобретению стерилизуют термоударом при 120-280°C в вакуумной или сухожаровой печи, что позволяет депирогенизировать хондроитинсульфат, являющийся биопрепаратом (органическое вещество, получаемое из биологического сырья), изначально контаминированным микробной флорой. При этом выбранный режим позволяет разрушить эндотоксины, присутствующие даже в стерильном хондроитинсульфате, представляющие собой оболочки бактериальных тел, без разрушения полимерной цепи хондроитинсульфата. Хондроитинсульфат вводят в кипящий сбалансированный раствор в стерильном виде, что также не снижает его активности, но значительно улучшает качество целевого продукта, который часто контаминирован микробной флорой и поэтому требует предварительной стерилизации. Применение термоудара дополнительно приводит к высушиванию поверхности частиц порошкообразного хондроитинсульфата, поэтому при введении в раствор его частицы в первый момент контакта с водным раствором не слипаются и не образуют комков, за счет чего уменьшается время растворения хондроитинсульфата в 2 раза.
Хондроитинсульфат, примененный в изобретении, является коммерческой субстанцией из хряща трахей быка (хондроитин-4-сульфат А) ("Сигма", США (Cat. №С 3884 К)), что не исключает возможности применения изомера хондроитин-6-сульфата (С) из плавников акульего хряща, при этом это может быть и хондроитинсульфат из других источников, если он по количественному и качественному составу будет соответствовать характеристикам описываемой субстанции.
После полного растворения стерильного хондроитинсульфата в горячий раствор добавляют стерильные гидроксипропилметилцеллюлозу и гидроксиэтилцеллюлозу - водорастворимые производные целлюлозы. Указанные продукты имеют разную растворимость в зависимости от температуры раствора. Гидроксиэтилцеллюлоза при повышении температуры раствора увеличивает свою растворимость, а гидроксипропилметилцеллюлоза при температуре выше 40°C теряет растворимость в воде, переходя из гелеобразного состояния в золь. Частицы золя более быстро и равномерно распределяются в массе раствора. При последующем остывании раствора частицы гидроксипропилметилцеллюлозы также более равномерно и быстро растворяются в массе раствора. Этот эффект позволяет быстро получать максимально гомогенную коллоидную систему, в которой в сети из линейных молекул гидроксипропилметилцеллюлозы равномерно распределяются более глобулярные молекулы гидроксиэтилцеллюлозы и хондроитинсульфата. Такая коллоидная система позволяет при применении раствора в лечебных целях замедлить испарение воды, что увеличивает время существования защитной пленки раствора на глазу. Это увеличивает экспозицию хондроитинсульфата на ткани глаза. В части способа приготовления это позволяет сократить время приготовления раствора.
Положительное действие хондроитинсульфата имеет дозозависимый эффект и зависит от времени экспозиции этого вещества на ткани глаза. Чем дольше экспозиция, тем выше положительное протективное и регенераторное действие хондроитинсульфата.
В изобретении применена коммерческая гидроксиэтилцеллюлоза фармацевтическая фирмы «Геркулес» (Натросол 250 Pharm, Бельгия), что, однако, не исключает использования водорастворимых производных целлюлозы других производителей, обладающих аналогичными характеристиками и свойствами.
Гидроксипропилметилцеллюлоза и гидроксиэтилцеллюлоза вводятся в раствор с целью придания ему протективных вязкоэластических свойств. Сочетание этих двух водорастворимых производных целлюлозы позволяет уменьшить испаряемость полученного раствора и уменьшить его способность к выведению с поверхности глаза. Это обеспечивается тем, что сочетание дисперсивного вискоэластика, каковым является гидроксипропилметилцеллюлоза, и более когезивного вискоэластика - гидроксиэтилцеллюлозы увеличивает время высыхания раствора и усилие вязкого сдвига, оно становится значительно сильнее, чем у указанных водорастворимых производных порознь. Это в сочетании с хондроитинсульфатом создает синэргический эффект, который невозможен без сочетания всех компонентов и последовательностей способа приготовления раствора. Смесь водорастворимых производных целлюлозы стерилизуется термоударом от 1 до 30 минут при температуре 120-280°C. Этот режим не вызывает термодеструкцию полимерных цепей гидроксиэтилцеллюлозы и гидроксипропилметилцеллюлозы с одновременной надежной стерилизацией и депирогенизацией за счет термического распада микробных тел и эндотоксинов, образующихся при разрушении мемран бактерий. Кроме того, стерилизация термоударом позволяет более полно высушить водорастворимые производные целлюлозы. Дополнительное высушивание поверхности частиц порошкообразных производных целлюлозы приводит к тому, что при растворении в воде или солевых растворах эти частицы, попадая в раствор, не слипаются с образованием комков, что при последующем растворении значительно сокращает время приготовления раствора и улучшает их реологические свойства за счет лучшей дисперсии в начале процесса растворения. Прогрев смеси порошка гидроксиэтилцеллюлозы и гидроксипропилметилцеллюлозы менее одной минуты не дает требуемого высыхания поверхности частиц и надежной депирогенизации даже при температуре выше 280°C, прогрев более 30 минут приводит к деструкции компонентов смеси даже при температуре ниже 120°C. Температура выше 280°C также приводит к деструкции компонентов смеси производных целлюлозы, а температура ниже 120°C не обеспечивает их надежной депирогенизации. Перемешивание раствора ведут в течение 1 часа, так как это время, достаточное для распределения водорастворимых производных целлюлозы по всему объему раствора. Это время установлено нами экспериментально, оно в два раза меньше, чем время, требуемое для перемешивания раствора по прототипу.
После перемешивания раствор отстаивают в течение 12 часов. Данное время отстаивания необходимо для окончательного распределения всех компонентов по объему раствора и приобретения им окончательной вязкости. Это время также в два раза меньше, чем время, требуемое для отстаивания раствора по прототипу. Это время установлено нами экспериментально. В сумме реализация предлагаемого изобретения сокращает общее время приготовления раствора в два раза.
После отстаивания раствор разливают по флаконам и стерилизуют.
Краткая технология получения фармацевтической композиции
Порошкообразный хондроитинсульфат стерилизуют термоударом в сухожаровом или вакуумном шкафу при температуре 120-280°C в течение 1-30 минут. 50,0 мл сбалансированного солевого раствора нагревают до кипения и добавляют в него стерильный порошок субстанции 0,002 г хондроитин-6-4-сульфата, порошкообразные гидроксипропилметилцеллюлозу и гидроксиэтилцеллюлозу, стерилизуют в вакуумном или сухожаровом шкафу при температуре 120-280°C 1-30 минут, перемешивают и добавляют в равном количестве по 0,15 г в кипящий раствор, перемешивают в течение 1 часа и доводят объем сбалансированного солевого раствора до 100,0 мл, отстаивают раствор в течение 12 часов, разливают во флаконы и стерилизуют автоклавированием в течение 10 минут при 120°С.
Раствор согласно изобретению содержит хондроитинсульфат от 0,02 до 4,0 г, что является оптимальным для проявления противовоспалительного, репаративного и противоотечного эффекта, а также для надежного протективного эффекта на эпителиальные и эндотелиальные клетки роговицы и другие ткани глаза.
Концентрация хондроитинсульфата менее 0,02 г не оказывает выраженного стимулирующего эффекта на процесс репарации эпителия и стромы роговицы, а концентрация более 4,0 г может вызывать аллергическую реакцию.
В качестве вещества, придающего раствору вязкость и пролонгирующие свойства, в растворе применено два водорастворимых производных целлюлозы: гидроксиэтилцеллюлоза в концентрации от 0,15 до 1,0 г на 100 мл и гидроксипропилметилцеллюлоза в концентрации от 0,15 до 1,0 г на 100 мл. Таким образом, чтобы содержание указанных производных целлюлозы на 100 мл было не менее 0,3 г и не более 2,0 г.
Концентрация ниже 0,3 г на 100 мл не придает раствору вязкости, а при концентрации выше 2,0 г на 100 мл возникают трудности распределения основного вещества и других компонентов по всему объему раствора.
Применение смеси двух водорастворимых производных позволяет уменьшить скорость высыхания раствора, что подтверждается данными таблицы 1.
В качестве растворителя и стабилизатора компонентов раствора согласно изобретению в композиции использован сбалансированный солевой раствор, который был разработан фирмой Алкон специально для тканей глаза и в настоящее время является общепринятым для применения в офтальмологии и офтальмохирургии. Допускается использование 0,9% раствора очищенной поваренной соли.
Приготовление раствора контролируется на каждой стадии его получения и включает основные методики оценки его характеристик, принятые для Гос. Фармакопеи XI издания.
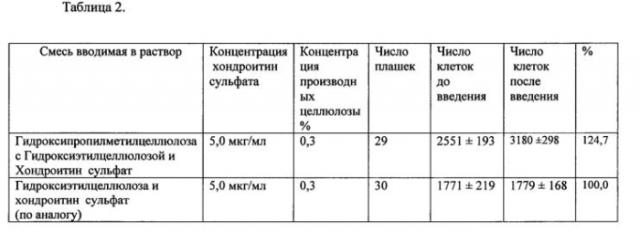
Стимулирующий эффект на синтез клетками эпителия и кератоцитов стромы роговой оболочки проводили на первичной культуре клеток, для чего в культуру клеток с обедненной средой вводили раствор с концентрацией хондроитинсульфата 200 мкг/мл и с помощью радиоактивной метки отмечали ее включение через 24 часа после инкубации. Результаты этих исследований изложены в таблице 2.
Противовоспалительный и репарационный эффект предлагаемого раствора изучали на экспериментальных животных - кроликах породы Шиншилла, которым под местной анестезией 0,5% раствора дикаина наносили радиальные разрезы на 2/3 толщины роговицы и проводили инстилляции раствора в каждый оперированный глаз, контрольным животным закапывали физиологический раствор хлорида натрия.
На сроки 7, 14 и 21 день после операции животных выводили из эксперимента внутрисердечным введением высокой дозы тиопентала натрия, роговицы секторально вырезали и готовили гистологические срезы для световой микроскопии.
Гистоморфологические исследования проводили на микроскопе Opton Германия.
Изучение гистологических препаратов показало, что в опытных глазах процесс репарации протекал более гладко, без явлений отека и воспаления роговицы и окружающих тканей.
Противоотечный эффект раствора определяли путем помещения свежевыкроенных роговиц кроликов в полученный по Примеру 3 раствор на 2 часа, контрольным раствором служил раствор, полученный по прототипу. Смесь 1:1 гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы - увеличение толщины роговицы было на 30% меньше, чем сравнивая с раствором по прототипу. Подсчет эндотелиальных клеток выявил отсутствие потери клеток в опытных препаратах по сравнению с контролем.
Это свидетельствует о том, что предлагаемый раствор обладает протективным и противоотечным действием.
При использовании раствора для лечения и профилактики заболеваний и повреждений роговицы согласно изобретению ускоряются процессы заживления тканей, чем обеспечивается сокращение сроков лечения и реабилитации пациентов. Входящие в раствор компоненты обеспечивают патогенетически направленную терапию заболеваний и повреждений роговицы. Для лучшего понимания сущности изобретение поясняется примерами конкретного исполнения.
Пример 1
Смесь из 0,15 г гидроксипропилметилцеллюлозы и 0,15 гидроксиэтилцеллюлозы прокаливают 30 мин при 120°C. 50,0 мл сбалансированного солевого раствора нагревают до кипения и добавляют в него стерильный порошок 0,002 г хондроитинсульфата ("Сигма", США, Кат. №С 4384 К), перемешивают и добавляют прокаленную смесь гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы. Полученный вязкий раствор перемешивают в течение 1 часа, добавляют солевой сбалансированный раствор до 100,0 мл, отстаивают раствор в течение 12 часов, разливают во флаконы и стерилизуют в течение 10 минут при 120°C. Получен раствор при следующем соотношении компонентов, г/100,0 мл: хондроитинсульфата - 0,005 ("Сигма", США, Кат. №С 4384 К), гидроксиэтилцеллюлозы (Натросол 250 Pharm, "Геркулес", Голландия) - 0,15, гидроксипропилметилцеллюлозы (Wolff Cellulosics) -0,15, сбалансированного солевого раствора (BSS Alcon, Canada. РОСС RU 0001 11 ИМ 02) - до 100,0.
Раствор согласно изобретению применяется в качестве лечебно-профилактического средства при лечении заболеваний и повреждений роговицы с явлениями воспаления и отека, а также в качестве профилактического средства при "синдроме сухого глаза". Восстановление скорости разрыва слезной пленки происходит на 1 сутки применения по сравнению с 3 сутками при применении раствора по прототипу.
Пример 2
Смесь из 0,5 г гидроксипропилметилцеллюлозы и 0,5 гидроксиэтилцеллюлозы прокаливают 20 мин при 180°C. 50,0 мл сбалансированного солевого раствора нагревают до кипения и добавляют в него стерильный порошок 0,1 г хондроитинсульфата ("Сигма", США, Кат. №С 4384 К), перемешивают и добавляют прокаленную смесь гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы. Полученный вязкий раствор перемешивают в течение 1 часа, добавляют солевой сбалансированный раствор до 100,0 мл, отстаивают раствор в течение 12 часов, разливают во флаконы и стерилизуют в течение 10 минут при 120°C.
Получен раствор при следующем соотношении компонентов, г/100,0 мл: хондроитинсульфата ("Сигма" США, Кат. №С 4384 К) - 0,1, гидроксиэтилцеллюлозы (Натросол 250 Pharm, "Геркулес", Голландия) - 0,5, гидроксипропилметилцеллюлозы - 0,5 (Wolff Cellulosics), сбалансированного солевого раствора (BSS Alcon, Canada. РОСС RU 0001 11 ИМ 02) - до 100,0.
Раствор применяется в качестве лечебно-профилактического средства при лечении заболеваний роговицы, при хирургических вмешательствах (удаление катаракты) и лазерных операциях на роговице, конъюнктиве и склере, а также при любых заболеваниях и повреждениях роговицы и окружающих тканей глаза с явлениями воспаления и отека. Устранение синдрома красного глаза происходит на 2 сутки после начала применения раствора по сравнению с 4 сутками при применении раствора по прототипу.
Пример 3
Смесь из 1,0 г гидроксипропилметилцеллюлозы и 1,0 гидроксиэтилцеллюлозы прокаливают 1 мин при 280°C. 50,0 мл сбалансированного солевого раствора нагревают до кипения и добавляют в нее стерильный порошок 4,0 г хондроитинсульфата ("Сигма", США, Кат. №С 4384 К), перемешивают и добавляют прокаленную смесь гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы в соотношении 1:1, перемешивают в течение 1 часа, добавляют солевой сбалансированный раствор (BSS Alcon, Canada. РОСС RU 0001 11 ИМ 02), отстаивают раствор в течение 12 часов, разливают во флаконы и стерилизуют в течение 10 минут при 120°C. Получен раствор при следующем соотношении компонентов, г/100,0 мл: хондроитинсульфата ("Сигма", США, Кат. №С 4384 К) - 4,0, гидроксиэтилцеллюлозы (Натросол 250 Pharm, "Геркулес", Голландия) - 1,0, гидроксипропилметилцеллюлозы - 1,0 (Wolff Cellulosics), сбалансированного солевого раствора (BSS Alcon, Canada. РОСС RU 0001 11 ИМ 02) - до 100,0.
Раствор применяется в качестве лечебно-профилактического и протективного средства при хирургических и лазерных операциях на роговице, при экстракции катаракты, требующих защиты эндотелия роговой оболочки глаза и тканей передней камеры, при операциях на конъюнктиве и склере, а также при любых повреждениях роговицы и окружающих тканей глаза, а также в качестве средства для предупреждения явлений воспаления и отека. Потеря эндотелиальных клеток при применении раствора на 30% меньше, чем при применении раствора по прототипу.
1. Способ получения раствора для лечения, профилактики заболеваний и повреждений роговицы, включающий растворение в сбалансированном солевом растворе, доведенном до кипения, стерильного хондроитинсульфата и гидроксиэтилцеллюлозы, перемешивание, отстаивание и стерилизацию в автоклаве при 120°С, отличающийся тем, что одновременно с гидроксиэтилцеллюлозой добавляют гидроксипропилметилцеллюлозу, причем предварительно их стерилизуют термоударом при 120-280°С в течение 3-30 мин, перемешивание осуществляют в течение 1 ч, отстаивание раствора - в течение 12 ч.
2. Раствор для лечения, профилактики заболеваний и повреждений роговицы, характеризующийся тем, что получен по п. 1 и содержит хондроитинсульфат, гидроксипропилметилцеллюлозу, гидроксиэтилцеллюлозу и сбалансированный солевой раствор при следующем соотношении компонентов, г/100,0 мл:
| Хондроитинсульфат | 0,02-4,0 |
| Гидроксиэтилцеллюлоза | 0,15-1,0 |
| Гидроксипропилметилцеллюлоза | 0,15-1,0 |
| Сбалансированный солевой раствор | до 100,0 |