Средство, обладающее нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности и медицине и представляет собой средство, обладающее нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения, характеризующееся тем, что оно включает 4-амино-3-фенилбутановую кислоту, L-аргинин гидрохлорид, при этом мольное соотношение 4-амино-3-фенилбутановой кислоты и указанного L-аргинина гидрохлорида составляет 1:2. Изобретение обеспечивает расширение арсенала малотоксичных средств, обладающих нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения. 5 табл.
Реферат
Изобретение относится к фармацевтической промышленности и медицине и касается средств, содержащих производные гамма-аминомасляной кислоты (ГАМК), обладающих нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения.
Гамма-аминомасляная кислота (ГАМК) является важнейшим тормозным нейромедиатором центральной нервной системы млекопитающих, восстанавливает процессы метаболизма в головном мозге. Она повышает продуктивность мышления, улучшает память и используется, в основном, для лечения сосудистых заболеваний головного мозга [1. Машковский М.Д. Лекарственные средства. М.: «Новая волна». 2012; 2. Раевский К.С Нейрофармакологические и нейрохимические аспекты / К.С.Раевский, В.П. Георгиев // Медиаторные аминокислоты 1986. М.: «Медицина».- 165 с.; 3. Ковалев Г.В. Ноотропные средства. Волгоград. Нижне-Волжское книжное издательство. 1990. 368 с.]. Известно средство, обладающее антиишемической, гипотензивной, противоаритмической и ноотропной активностью, включающее производное ГАМК 4-амино-3-фенилбутановую кислоту и глутаминовую или никотиновую кислоты (RU №2216322). Полученное средство имеет меньшую токсичность, чем ее компоненты, оказывают более выраженное антиангинальное и противоаритмическое действие, снижают артериальное давление (RU №2216322). Нейропротекторное действие композиции в условиях ишемического нарушения мозгового кровообращения не описано. Известно также, что соли 4-амино-3-фенилбутановой кислоты обладают церебропротекторной активностью в условиях алкогольного и электроконвульсивного повреждения мозга (RU №2393855). Однако вышеперечисленные средства не нашли применения в терапии недостаточности мозгового кровообращения.
L-Аргинин - условно-незаменимая альфа-аминокислота, является природным L-изомером аминокислоты аргинина, необходимой для синтеза ряда белков и оксида азота (NO) - регулятора многих физиологических и патологических процессов [1. Львова О.А. и др. К вопросу о роли оксида азота в норме и при патологии нервной системы // Electronic scientific magazine "System integration in public health services". - 2011. - C. 20; 2. Andrew P.J., Mayer B. Enzymatic function of nitric oxide synthases // Cardiovascular research. - 1999. - T. 43. - №. 3. - C. 521-531]. L-Аргинин, как субстрат синтеза оксида азота, улучшает эндотелиальную функцию сосудов при сердечно-сосудистой недостаточности, сахарном диабете и гиперхолестеринемии [1. Бувалъцев В.И. Международ, мед. журнал. 2001 // Т. - Т. 3. - С. 9-14; 2. Марков X.М. Молекулярные механизмы дисфункции сосудистого эндотелия // Кардиология. - 2005. - Т. 45. - №. 12. - С. 62-72].
L-Аргинин входит в состав композиций, обладающих эндотелиопротективным, вазодилатирующим и ангиопротекторным эффектом (RU 2464019). Известно также, что L-аргинин разрешен в виде биологически активной добавки (Вазотон) при лечении сахарного диабета второго типа, физических и умственных перегрузках, атеросклерозе и др. [http://www.rlsnet.ru/baa_tn_id_31639.htm].
Нейропротекторное действие L-аргинина в условиях ишемического нарушения мозгового кровообращения неизвестно.
Проблема профилактики и лечения заболеваний, связанных с нарушениями мозгового кровообращения в результате травм головного и спинного мозга, с увеличением психических нагрузок, со значительным распространением психических расстройств у взрослых и детей, остается одной из актуальных задач современной медицины. В этой связи особый интерес представляют препараты, обладающие нейропротекторным действием к внешним факторам, повреждающим процессы деятельности мозга, а также способные улучшать качество его высших функций (мышление, память, внимание) [Мирзоян Р.С. Нейропротекторные и цереброваскулярные эффекты ГАМК-миметиков // Экспериментальная и клиническая фармакология. - 2003. - Т. 66. - №. 2. - С. 53-56]. На современном этапе известно значительное число представителей лекарственных препаратов разных классов, обладающих нейропротекторным действием. Однако несмотря на широкий спектр лекарственных средств, применяющихся для профилактики и лечения нарушений мозгового кровообращения, эффективность их остается низкой [Путилина М. В. Особенности комбинированной нейропротекторной терапии острых нарушений мозгового кровообращения // РМЖ. - 2009. - Т. 17. - №. 4. - С. 261-6].
В настоящее время в качестве нейропротекторного средства широкое распространение в практической медицине получил препарат пирацетам. Он является представителем группы ноотропных препаратов. Оказывает положительное влияние на обменные процессы и кровообращение мозга. Пирацетам применяют при разных заболеваниях центральной нервной системы, особенно связанных с сосудистыми нарушениями и патологией обменных процессов головного мозга, в том числе у людей пожилого и старческого возраста. Однако по многим общим фармакологическим тестам он имеет невысокую эффективность. Кроме того, пирацетам вызывает ряд существенных побочных эффектов: повышенную раздражительность, депрессию, нарушение сна, диспепсические расстройства, обострение коронарной недостаточности у больных пожилого возраста [Машковский М.Д. Лекарственные средства. М.: «Новая волна». 2012].
Поэтому поиск и разработка новых высокоэффективных средств с широким спектром нейропротекторного действия, безопасных при длительном применении, позволяющих осуществлять фармакологическую коррекцию совокупности симптомов ишемического нарушения мозгового кровообращения и избежать необходимость одновременного назначения нескольких лекарств, по-прежнему остается одной из актуальных задач современной фармакологии и терапии ишемических нарушений мозгового кровообращения.
Задача изобретения - получить высокоэффективное и малотоксичное производное ГАМК, обладающее нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения и расширить ассортимент подобных средств.
Поставленная задача реализуется предлагаемым комбинированным средством, включающим 4-амино-3-фенилбутановую кислоту и L-аргинин гидрохлорид. Причем соотношение 4-амино-3-фенилбутановая кислота: L-аргинин гидрохлорид как 1:2 (АФБАГ). При этом получают средство, обладающее комплексом нейропротекторных свойств в условиях ишемического нарушения мозгового кровообращения, превышающих таковые или отсутствующие у исходного вещества и ряда известных лекарственных средств целевого назначения.
Лекарственное средство содержит эффективную дозу композиции 4-амино-3-фенилбутановой кислоты с L-аргинином гидрохлоридом и фармакологически приемлемые носители и целевые добавки.
Технический результат предлагаемого изобретения заключается в том, что предлагаемое средство малотоксично и способно оказывать нейропротекторное действие в условиях ишемического нарушения мозгового кровообращения.
Изобретение иллюстрируется следующими примерами:
Пример
В шаровую мельницу загружают 12.5 г (0.07 моль) 4-амино-3-фенилбутановой кислоты и 29.4 (1.4 моль) L-аргинина гидрохлорида. Смесь тщательно перемешивают в течение 0,5-1 часа, затем выгружают полученный продукт. Выход количественный.
Полученное таким образом комбинированное средство было изучено в опытах на животных.
Далее приводятся примеры, иллюстрирующие специфическую активность композиции 4-амино-3-фенилбутановой кислоты (АФК) с L-аргинином гидрохлоридом (АГХ).
Для изучения нейропротекторного действия композиции АФБАГ в условиях ишемического нарушения мозгового кровообращения использовали модель острого нарушения мозгового кровотока (ОНМК), вызванного одномоментной билатеральной окклюзией общих сонных артерий [Руководство по проведению доклинических исследований лекарственных средств. Часть первая / под ред. А.Н. Миронова. - М.: Гриф и К, 2012. - 944 с.]. Животным под эфирным наркозом была осуществлена одномоментная двусторонняя перевязка общих сонных артерий (ОСА) с регистрацией количества выживших животных через 6, 12, 24, 48 и 72 часа после операции.
Для выявления нейропротекторного действия композиции АФБАГ использовали тесты, позволяющие оценить неврологический статус животных в постишемический период: неврологический дефицит, спонтанное двигательное, и ориетировочно-исследовательское поведение, мнестическая функция [Руководство по проведению доклинических исследований лекарственных средств. Часть первая / под ред. А.Н. Миронова. - М.: Гриф и К, 2012. - 944 с].
Обработка полученных данных проводилась с использованием статистических методов оценки результатов исследования, которые позволяют оценить степень фармакологической эффективности.
В работе были использованы белые беспородные крысы-самцы линии Вистар, рандомизированные по возрасту (четыре месяца) и массе (220-240 г), содержавшиеся в условиях лабораторного вивария, на стандартном пищевом рационе, при свободном доступе к воде и естественном световом режиме. Приводимые в таблицах значения показателей представляют собой среднестатистическую оценку результатов измерения параметров с учетом принятых уровней достоверности (р<0,05).
Острая токсичность (LD50 мг/кг) композиции 4-амино-3-фенилбутановой кислоты с L-аргинином гидрохлоридом (АФБАГ) оценивалась по выживаемости белых мышей через 24 часа после внутрибрюшного введения средства и составляет>2000 мг/кг, что позволяет классифицировать исследуемое вещество как малотоксичное. Для сравнения, острая токсичность пирацетама составляет 12000 мг/кг [Оганисян А.Ш. и др. Производные конденсированных тиенопиримидинов. Синтез и нейротропные свойства новых производных пирано [4′, 3′: 4, 5] тиено [3, 2-е] триазоло [3, 4-b] пиримидинов //Химико-фармацевтический журнал. - 2003. - Т. 37. - №. 1. - С. 15-16].
Экспериментальное изучение эффективности заявляемой композиции АФБАГ в условиях ишемического нарушения мозгового кровообращения проводили в сравнении с каждым препаратом, входящим в состав композиции [4-амино-3-фенилбутановой кислотой (АФК), L-аргинином гидрохлоридом (L-АГХ)] и с препаратом сравнения пирацетамом.
Для проведения эксперимента были сформированы следующие группы животных: контрольная группа 1 - ложнооперированные животные, которым после подведения лигатуры под сосуды, общие сонные артерии не перевязывались - позитивный контроль; контрольная группа 2 - животные с одномоментной окклюзией сонных артерий, получавшие дистиллированную воду - негативный контроль; опытная группа 3 - животные с ишемией, получавшие композицию АФБАГ; опытная группа 4 - животные с ишемией, получавшие 4-амино-3-фенилбутановую кислоту (АФК); опытная группа 5 - крысы с ишемией, получавшие L -аргинин гидрохлорид (АГХ); опытная группа 6 - крысы с ишемией, получавшие препарат сравнения пирацетам.
Исследуемую композицию - АФБАГ в дозе 50 мг/кг, 4-амино-3-фенилбутановую кислоту (14,8 мг/кг), L-аргинин гидрохлорид (35,2 мг/кг), препарат сравнения пирацетам в дозе 800 мг/кг и воду вводили per os через 2 часа после начала операции и далее один раз в сутки на протяжении трех дней.
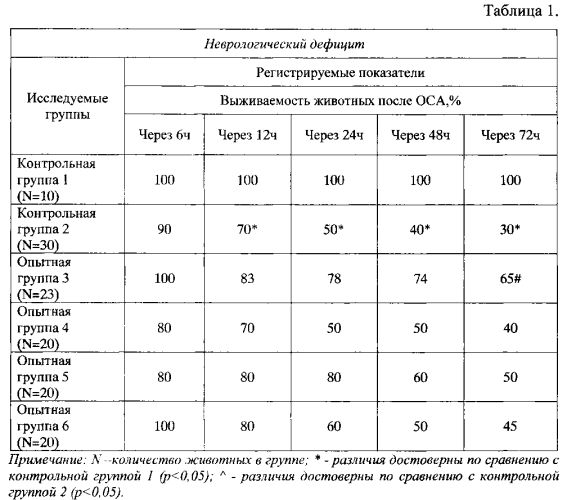
Неврологический дефицит в условиях ишемического нарушения мозгового кровообращения (табл. 1, 2)
Количество выживших животных и неврологический дефицит регистрировали через 6, 12, 24, 48 и 72 часа после операции перевязки артерий. Неврологический дефицит оценивали в баллах по шкале McGrow в модификации Ганнушкиной И.В. Спонтанное двигательное и ориетировочно-исследовательское поведение определяли в тесте «Открытое поле» (ОП).
Результаты эксперимента показали, что при перевязке общих сонных артерий у животных к 72-му часу наблюдений после операции показатель летальности был достоверно ниже у крыс опытной группы 3 по сравнению с животными контрольной группы 2 (табл. 1).
Таким образом, композиция АФБАГ обладает нейропротекторным действием в условиях ишемии мозга и по активности превосходит таковое у компонентов композиции АФК и L-АГХ и препарата сравнения пирацетама (табл. 1).
После окклюзии у групп испытуемых животных наблюдался неврологический дефицит в виде тремора, вялости одно- и двухсторонних полуптозов и птозов, манежных движений, парезов и параличей конечностей. При этом на протяжении всего периода наблюдения балл неврологического дефицита был наивысшим (от 9.5±0.1 до 8.4±0.2 балла) у животных контрольной группы 2 (табл. 2). У крыс опытной группы 3, получавших композицию АФБАГ до окклюзии, степень неврологического дефицита была значительно меньше (от 7.4±0.2 до 5.8±0.7), чем у животных контрольной группы 2. Пирацетам незначительно уменьшал проявления неврологического дефицита (от 7.8±0.2 до 7.2±0.7). При этом сравнительный анализ баллов неврологического дефицита у групп испытуемых животных показал, что его проявления у крыс опытной группы 3, получавших композицию АФБАГ, были существенно ниже, чем в контрольной группе 2 (табл. 2).
Спонтанное двигательное и ориетировочно-исследовательское поведение в условиях ишемического нарушения мозгового кровообращения (табл. 3)
Двигательное поведение животных в условиях ишемии головного мозга изучали в тесте «Открытое поле» (ОП) [Руководство по проведению доклинических исследований лекарственных средств. Часть первая / под ред. А.Н. Миронова. - М.: Гриф и К, 2012. - 944 с.]. Методика открытого поля используется для изучения влияния вещества на показатели спонтанного индивидуального поведения животных (двигательную, ориентировочно-исследовательскую активность и эмоциональный статус).
Эксперимент проводился в стандартном круглом манеже диаметром 97 см и высотой 42 см. Крысу помещали в центр камеры хвостом к экспериментатору и наблюдали за ее поведением в течение 3 минут. В тесте регистрировали: число пересеченных секторов на периферии, число пересеченных ярко-освещенных секторов, количество вертикальных стоек, количество заглядываний в отверстия. Количество пересеченных секторов характеризует спонтанную двигательную активность животных, сумма стоек и заглядываний в отверстия - суммарную ориентировочно-исследовательскую активность.
Результаты эксперимента в тесте «ОП» показали, что у животных опытной группы 3, получающих композицию АФБАГ, через 72 часа после операции статистически значимо повышалось количество пересеченных секторов (двигательная активность), число стоек и заглядываний в отверстия (ориентировочно-исследовательская активность), что указывает на наличие у заявляемой композиции значительного нейропротекторного действия (табл. 3). У животных опытной группы 6, получавших препарат пирацетам, показатели двигательной активности несколько меньше, чем у крыс, получавших композицию АФБАГ (табл. 3).
Таким образом, результаты эксперимента показали, что введение экспериментальным животным заявляемой композиции АФБАГ в условиях недостаточности мозгового кровообращения существенно повышает выживаемость животных и снижает выраженность их неврологического дефицита. Это показывает, что композиция АФБАГ обладает выраженным нейропротекторным действием, при этом компоненты ее состава (АФК и L-АГХ) значительно уступают по активности композиции АФБАГ (табл. 3).
Антиамнестическое действие композиции в условиях ишемического нарушения мозгового кровообращения (табл. 4, 5)
Оценку мнестической функции животных проводили в стандартных психоневрологических тестах: «Условная реакция пассивного избегания» (УРПИ), «Тест экстраполяционного избавления» (ТЭИ) [Руководство по проведению доклинических исследований лекарственных средств. Часть первая/под ред. А.Н. Миронова. - М.: Гриф и К, 2012. - 944 с.].
Тест «Условнаяреакция пассивного избегания» (табл. 4)
Методика теста УРПИ позволяет оценить влияние веществ на формирование, сохранение и воспроизведение памятного следа в норме и в условиях его нарушения.
Обучение животных проводилось в установке, состоящей из двух смежных отсеков, один из которых размером 60×40×40 см открыт сверху и ярко освещен (1340 Лм). Другая камера с электрифицированным полом меньшего размера (15×15×15 см), затемненная, закрытая со всех сторон, и имеет отверстие (8×8 см) для сообщения с большим отсеком. Эксперимент выполнялся в два этапа: выработка у животных условного рефлекса пассивного избегания и воспроизведение памятного следа в динамике через 24 и 72 часа.
Во время обучения тестируемое животное помещали на середину площадки освещенного отсека, хвостом к отверстию в темный отсек. В течение трех минут за животным велось визуальное наблюдение. После каждого захода в темный отсек животному наносили электроболевое раздражение (40 В, 3 импульса по 1 сек, с интервалом 0,5 сек), животных, не заходящих в темную камеру за это время, из опыта исключали. На этапе обучения животных регистрировали следующие показатели: время от момента помещения животного в середину площадки до первого захода в темный отсек (латентный период первого захода) и количество заходов в него.
Эксперимент воспроизведения памятного следа выполнялся следующим образом: обученное животное помещали на середину площадки освещенного отсека, хвостом к отверстию в темный отсек и в течение трех минут вели визуальное наблюдение за животным. После каждого захода в темный отсек животному не наносили электроболевую стимуляцию. На этом этапе регистрировали следующие показатели: латентный период первого захода, количество заходов в него и общее время нахождения животного в темном отсеке. В эксперименте сравнивали латентный период первого захода животных в темный отсек и количество заходов в него в тесте воспроизведения памятного следа с аналогичными показателями при обучении. Увеличение латентного периода и уменьшение числа заходов указывают на обученность животного и сохранность в памяти информации об аверсивности темного отсека. [Буреш Я. и др. Методики и основные эксперименты по изучению мозга и поведения. - Высш. шк., 1991]. Общее время нахождения в темном отсеке, регистрируемое при воспроизведениях навыка, также отражает сохранность памятного следа у животного - чем меньше времени животное проводит в темном отсеке, тем лучше оно помнит о нанесенном ему здесь электроболевом раздражении.
Введение композиции АФБАГ у животных опытной группы 3 с экспериментальной ишемией головного мозга на этапе воспроизведения навыка избегания через 72 часа после операции наблюдалось увеличение латентного периода захода животных в темный отсек, уменьшение количества заходов в него и времени пребывания в нем по отношению к контрольной группе 2 (табл. 4). Такое положительное влияние композиции КАФАГ на обучаемость и память животных, замедление угасания памятного следа в динамике свидетельствует о наличии нейропротекторного действия у заявляемой композиции.
«Тест экстраполяционного избавления» (табл. 5)
Методика теста ТЭИ позволяет оценить индивидуальные различия когнитивного стиля решения задачи (поиска пути активного избавления из аверсивной среды).
Обучение животных проводилось в цилиндрической емкости диаметром 35 см, заполненной водой с температурой 16-18°C. Емкость содержала пластиковый цилиндрический колпак, диаметром 9 см и высотой 23 см, края которого погружались в воду на 2.5 см. Эксперимент выполнялся в два этапа: выработка у животных условного рефлекса избавления и проверка сохранности навыка экстраполяционного избавления в динамике через 24 и 72 часа.
Во время обучения тестируемое животное помещали в емкость под колпак. В течение трех минут за ним велось визуальное наблюдение. Животные подныривали под края колпака и избавлялись, таким образом, от аверсивной водной среды. Не решившие задачу животные из опыта исключались. На этапе обучения животных регистрировали следующие показатели: время от момента погружения животного в воду до начала активного плавания (латентный период двигательной активности), время иммобилизации (животное пассивно плавает в воде со слегка поднятой головой, все четыре конечности неподвижны), количество прыжков в колпаке (активные попытки выпрыгнуть из воды) и время от момента погружения животного в воду до подныривания под края колпака (латентный период подныривания)
Эксперимент воспроизведения навыка экстраполяционного избавления у животных выполняли следующим образом: обученное животное помещали в аквариум под колпак. В течение трех минут за ним велось визуальное наблюдение. При оценке когнитивных функций регистрировали наиболее значимые показатели: латентный период двигательной активности (характеристика скорости ориентировочных реакций); латентный период подныривания (показатель способности к экстраполяции, чем меньше значение показателя, тем выше скорость решения экстраполяционной задачи). В эксперименте сравнивали показатели, определяющие степень обученности животного и состояние памяти: латентный период подныривания животного при обучении и воспроизведении навыка экстраполяционного избавления (чем значительнее он уменьшается при воспроизведении навыка, тем больше обученность животного и сохраннее памятный след).
При введении композиции АФБАГ животным опытной группы 3 с экспериментальной ишемией головного мозга на этапах воспроизведения навыка через 72 часа отмечалось статистически значимое уменьшение времени решения экстраполяционной задачи (табл. 5). При этом компоненты композиции АФК и L-АГХ и препарат сравнения пирацетам значительно уступали композиции АФБАГ по активности. Такое положительное влияние композиции АФБАГ на когнитивные функции у животных свидетельствует, что она обладает выраженным нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения.
Таким образом, результаты экспериментов показали, что композиция 4-амино-3-фенилбутановой кислоты с L-аргинином (АФБАГ) обладает нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения. При этом нейропротекторное действие ее более выражено, чем у ее компонентов 4-амино-3-фенилбутановой кислоты, L-аргинина гидрохлорида и препарата сравнения пирацетама. Введение композиции АФБАГ существенно увеличивает выживаемость крыс и снижает выраженность неврологических нарушений и когнитивного дефицита у животных, перенесших острое нарушение мозгового кровообращения. Она в значительной степени способна уменьшать последствия тяжелой гипоксии, связанной с нарушением мозгового кровообращения.
Приведенные данные фармакологической активности композиции АФБАГ делают весьма перспективной разработку на ее основе малотоксичного и эффективного нейропротекторного средства для профилактики и лечения нарушений мозгового кровообращения различного генеза.
Средство, обладающее нейропротекторным действием в условиях ишемического нарушения мозгового кровообращения, характеризующееся тем, что оно включает 4-амино-3-фенилбутановую кислоту, L-аргинин гидрохлорид, при этом мольное соотношение 4-амино-3-фенилбутановой кислоты и указанного L-аргинина гидрохлорида составляет 1:2.