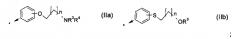Производные 4-гидрокси-1,2,3,4-тетрагидронафталин-1-ил-мочевины и их применение в лечении, среди прочего, заболеваний дыхательного тракта
Иллюстрации
Показать всеИзобретение относится к индивидуальным соединениям, содержащим 4-гидрокси-1,2,3,4-тетрагидронафталин-1-ил-мочевину, и их фармацевтически приемлемым солям. Соединения изобретения обладают свойствами ингибитора активности МАР-киназы р38. Изобретение также относится к фармацевтической композиции, к способу ингибирования активности МАР-киназы р38 и к применению соединений в изготовлении лекарственного средства. Технический результат: получены новые соединения, обладающие свойствами ингибитора активности МАР-киназы р38, которые могут применяться в качестве противовоспалительных агентов в лечении заболеваний дыхательного тракта. 4 н. и 5 з.п. ф-лы, 3 табл., 34 пр.
Реферат
Это изобретение относится к соединениям и композициям, которые являются ингибиторами МАРК р38, полезными в качестве противовоспалительных агентов в лечении, среди прочего, заболеваний дыхательного тракта.
Предшествующий уровень техники
Митоген-активируемые протеинкиназы (МАРК) составляют семейство пролин-направляемых серин/треонинкиназ, которые активируют свои субстраты посредством двойного фосфорилирования. Существуют четыре известные человеческие изоформы МАР-киназы p38: p38α, p38β, p38γ и p38δ. Р38-киназы, которые также известны как белки, связывающие противовоспалительные лекарственные средства, подавляющие цитокины (CSBP), стресс-активируемые протеинкиназы (SAPK) и RK, обуславливают фосфорилирование (Stein et ai, Ann. Rep. Med Chem., 1996, 31, 289-298) и активацию факторов транскрипции (таких как ATF-2, MAX, CHOP и C/ERPb), а также других киназ (таких как МАРКАР-К2/3 или МК2/3), а сами активируются посредством физического и химического стресса (например ультрафиолетом (UV), осмотическим стрессом), провоспалительными цитокинами и бактериальными липополисахаридами (LPS) (Herlaar Ε. & Brown Ζ., Molecular Medicine Today, 1999, 5, 439-447). Было показано, что продукты фосфорилирования р38 опосредуют выработку воспалительных цитокинов, включая фактор некроза опухоли альфа (TNF-α) и интерлейкин-1 (IL-1) и циклооксигеназу-2 (СОХ-2). Также известно, что IL-1 и TNF-α стимулируют выработку других провоспалительных цитокинов, таких как IL-6 и IL-8.
IL-1 и TNF-α являются биологическими веществами, продуцируемыми различными клетками, такими как моноциты или макрофаги. Было показано, что IL-1 опосредует различные виды биологических активностей, которые, как полагали, являются важными при иммунорегуляции и других физиологических состояниях, таких как воспаление (например, Dinarello et al., Rev. Infect. Disease, 1984, 6, 51). Избыточное или неконтролируемое продуцирование TNF (в частности TNF-α) вовлечено в опосредование или обострение ряда заболеваний, и полагают, что TNF может вызывать или вносить вклад в воспалительные эффекты в целом. IL-8 является хемотаксическим фактором, продуцируемым некоторыми видами клеток, включая мононуклеарные клетки, фибробласты, эндотелиальные клетки и кератиноциты. Его выработку эндотелиальными клетками индуцирует IL-1, TNF или липополисахарид (LPS). IL-8 стимулирует ряд функций in vitro. Было показано, что он обладает свойствами хемоаттрактанта для нейтрофилов, Т-лимфоцитов и базофилов. Увеличение продуцирования IL-8 также обуславливает хемотаксис нейтрофилов к месту воспаления in vivo.
Предполагают, что ингибирование передачи сигнала через р38, которая помимо IL-1, TNF и IL-8, описанных выше, также необходима для синтеза и/или действия некоторых дополнительных провоспалительных белков (например IL-6, GM-CSF (гранулоцитарно-макрофагальный колониестимулирующий фактор), СОХ-2, коллагеназы и стромелизина), является высокоэффективным механизмом регулирования избыточной и деструктивной активации иммунной системы. Это предположение подтверждается сильнодействующими и разнообразными механизмами противовоспалительной активности, описанными для ингибиторов р38-киназы (Badger et al., J. Pharm. Exp.Thera., 1996, 279, 1453-1461; Griswold et al, Pharmacol. Comm., 1996, 7, 323-229). В частности, ингибиторы р38-киназы описаны в качестве сильнодействующих агентов для лечения ревматоидного артрита. Помимо связей между активацией р38 и хроническим воспалением и артритом, имеются также данные, дающие основание предполагать роль р38 в патогенезе заболеваний дыхательных путей, в частности хронической обструктивной болезни легких (COPD) и астмы. Стрессовые стимулы (включая табачный дым, инфекции или продукты окисления) могут вызывать воспаление в легких. Ингибиторы р38, как было показано, ингибируют LPS и индуцированные овальбумином TNF-α, IL-1β, IL-6, IL-4, IL-5 и IL-13 в дыхательных путях (Haddad et al, Br. J. Pharmacol., 2001, 132 (8), 1715-1724; Underwood etal, Am. J. Physiol. Lung Cell. Mol. 2000, 279, 895-902; Duan et al., 2005 Am. J. Respir. Crit. Care Med., 171, 571-578; Escort ef al Br. J. Pharmacol., 2000, 131, 173-176; Underwood et al., J. Pharmacol. Exp. Ther. 2000, 293, 281-288). Кроме того, они значительно ингибируют нейтрофилию и высвобождение матриксной металлопротеиназы-9 (ММР-9) в животных моделях, подвергнутых воздействию LPS, озона или сигаретного дыма. Имеется также значительное количество данных доклинических исследований, подчеркивающих потенциальные преимущества ингибирования р38-киназы, что может быть существенным в легких (Lee et al., Immunopharmacology, 2000, 47, 185-200). Таким образом, терапевтическое ингибирование активации р38 может быть важным в регуляции воспаления дыхательных путей.
Роль пути р38МАРК при различных заболеваниях рассмотрена P. Chopra et al. (Expert Opinion on Investigational Drugs, 2008, 17(10), 1411-1425). Полагают, что соединения по настоящему изобретению могут быть использованы для лечения заболеваний, опосредованных р38, таких как астма, хронический или острый бронхостеноз, бронхит, острое повреждение легких и бронхоэктаз, легочная артериальная гипертензия, туберкулез, рак легких, воспаление вообще (например воспалительное заболевание кишечника), артрит, нейровоспаление, боль, лихорадка, фиброзирующие заболевания, легочные расстройства и заболевания (например гипероксическое альвеолярное повреждение), сердечно-сосудистые заболевания, постишемическое реперфузионное повреждение и застойная сердечная недостаточность, кардиомиопатия, инсульт, ишемия, реперфузионное повреждение, реперфузионное повреждение почек, отек головного мозга, нейротравма и травма головного мозга, нейродегенеративные расстройства, расстройства центральной нервной системы, заболевание печени и нефрит, желудочно-кишечные заболевания, язвенные болезни, болезнь Крона, глазные заболевания, офтальмологические заболевания, глаукома, острое повреждение тканей глаза и глазные травмы, диабет, диабетическая нефропатия, кожные заболевания, миалгии вследствие инфекции, гриппа, эндотоксический шок, синдром токсического шока, аутоиммунное заболевание, отторжение трансплантата, заболевания, сопровождающиеся резорбцией костной ткани, рассеянный склероз, псориаз, экзема, расстройства женской репродуктивной системы, патологические (но незлокачественные) состояния, такие как гемангиомы, ангиофиброма носоглотки и аваскулярный некроз кости, доброкачественные и злокачественные опухоли/неоплазия, включая рак, лейкоз, лимфому, системную красную волчанку (SLE), ангиогенез, включая неоплазию, кровотечение, свертывание, лучевое поражение и/или метастаз. Продолжительное высвобождение активного TNF может вызывать кахексию и анорексию, и TNF может представлять опасность для жизни. TNF также вовлечен в инфекционные заболевания. Они включают, например, малярию, микобактериальную инфекцию и менингит. Они также включают, среди прочего, вирусные инфекции, такие как HIV (вирус иммунодефицита человека), вирус гриппа и вирус герпеса, включая вирус простого герпеса 1 типа (HSV-1), вирус простого герпеса 2 типа (HSV-2), цитомегаловирус (CMV), вирус ветряной оспы (VZV), вирус Эпштейна-Барр, вирус герпеса человека 6 типа (HHV-6), вирус герпеса человека 7 типа (HHV-7), вирус герпеса человека 8 типа (HHV-8), ложное бешенство и ринотрахеит.
Известные ингибиторы р38-киназы рассмотрены G.J. Hanson (Expert Opinions on Therapeutic Patents, 1997, 7, 729-733), J Hynes et al. (Current Topics in Medicinal Chemistry, 2005, 5, 967-985), C. Dominguez et al (Expert Opinions on Therapeutics Patents, 2005, 15, 801-816) и L.H. Pettus & R.P. Wurtz (Current Topics in Medicinal Chemistry, 2008, 8, 1452-1467). Ингибиторы р38-киназы, содержащие триазолопиридиновый мотив, известны в данной области техники, например, из WO 07/091152, WO 04/072072, WO 06/018727.
Краткое описание изобретения
Соединения по настоящему изобретению являются ингибиторами митоген-активируемой протеинкиназы р38 ("р38 МАРК", "р38-киназа" или "р38"), включая р38α-киназу, и являются ингибиторами продуцирования цитокинов и хемокинов, включая продуцирование TNF-α и IL-8. Они имеют ряд терапевтических применений при лечении воспалительных заболеваний, в частности аллергических и неаллергических заболеваний дыхательных путей, более конкретно обструктивных или воспалительных заболеваний дыхательных путей, таких как хроническая обструктивная болезнь легких ("COPD") и астма. Поэтому они особенно подходят для доставки в легкие посредством ингаляции через нос или рот.
Краткое изложение сущности изобретения
Находящаяся на одновременном рассмотрении международная заявка на патент авторов настоящего изобретения № PCT/GB 2011/051076 касается, среди прочего, соединений формулы (I), которые являются ингибиторами р38 МАРК, полезными в качестве противовоспалительных агентов в лечении, среди прочего, заболеваний респираторного тракта:
где:
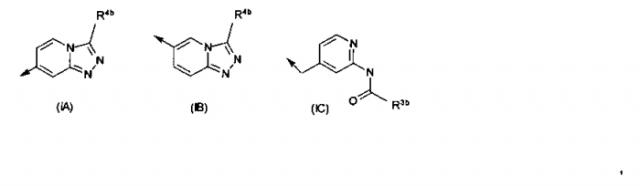
R1 представляет собой радикал формулы (IA), или (IB), или (IC):
где
R4b представляет собой C1-С6алкил, С3-С6циклоалкил, возможно замещенный фенил, возможно замещенный 5- или 6-членный моноциклический гетероарил или радикал формулы (IIa) или (IIb)
где n равно 1 или 2; и R3 и R4 независимо представляют собой Η или C1-С6алкил, либо R3 и R4, взятые вместе с азотом, к которому они присоединены, образуют 6-членное гетероциклическое кольцо, возможно содержащее дополнительный гетероатом, выбранный из N и О;
R3b представляет собой возможно замещенный С1-С6алкил; -NH2; моно- или ди-(С1-С6)алкиламино; моно- или ди-(С1-С3)алкил-Х-(С1-С3)алкиламино, где X представляет собой О, S или NH; N-морфолино; N-пиперидинил, N-пиперазинил или N-(С1-С3)алкилпиперазин-1-ил;
Υ представляет собой -О- или -S(O)p-, где p равно 0, 1 или 2;
А представляет собой возможно замещенный циклоалкиленовый радикал, имеющий 5, 6 или 7 кольцевых атомов, конденсированный с фенильным кольцом;
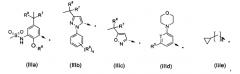
R2 представляет собой радикал формулы (IIIa), (IIIb), (IIIc), (IIId) или (IIIe):
где
q равно 0, 1, 2 или 3;
Τ представляет собой -Ν= или -СН=;
R5 представляет собой Η или F;
R7 представляет собой -СН3; -С2Н5; -СН2ОН, -CH2SCH3; -SCH3 или -SC2H5;
R8 представляет собой -СН3 или -С2Н5; и
R6 в каждом случае независимо представляет собой Н, C1-С6алкил, гидрокси или галоген;
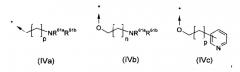
или один R6 представляет собой радикал формулы (IVa), (IVb) или (IVc)
тогда как любой другой R6 независимо представляет собой Н, С1-С6алкил, гидроксил или галоген;
где в формулах (IVa), (IVb) и (IVc) n и p являются такими, как определено выше;
и где в R6
R61a и R61b представляют собой Н, алкил, либо R61a и R61b могут быть объединены вместе с азотом, к которому они присоединены, с образованием 4-7-членного гетероциклического кольца, возможно содержащего дополнительный гетероатом, выбранный из N и О, такого как пиперидиновое, пиперазиновое или морфолиновое кольцо.
Настоящее изобретение относится к соединениям, которые являются ингибиторами р38 МАРК, попадающими в объем формулы (I) из заявки № PCT/GB 2011/051076, но конкретно в ней не раскрытыми.
Описание изобретения
Согласно настоящему изобретению предложено соединение выбранное из группы, состоящей из:
1-(5-трет-бутил-2-фенил-2Н-пиразол-3-ил)-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-циклопропил-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-[3-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илсульфанил)-индан-1-ил]-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-[4-{3-[3-(2-морфолин-4-ил-этокси)-фенил]-[1,2,4]триазоло[4,3-а]пиридин-6-илокси}-1,2,3,4-тетрагидро-нафталин-1-ил)-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-7-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-{5-трет-бутил-2-[3-(2-морфолин-4-ил-этокси)-фенил]-2Η-пиразол-3-ил}-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-{4-(3-(2-гидрокси-фенил)-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил}-мочевины;
1-(5-трет-бутил-изоксазол-3-ил)-3-[3-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-индан-1-ил]-мочевины;
N-(4-{4-[3-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-уреидо]-1,2,3,4-тетрагидро-нафталин-1-илоксиметил}-пиридин-2-ил)-2-метокси-ацетамида;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-{4-[3-(2-гидрокси-этилсульфанил)-фенил]-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетра гидро-нафталин-1-ил-мочевины;
1-{5-трет-бутил-2-[3-(2-диметиламино-этокси)-фенил]-2Н-пиразол-3-ил}-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-[5-трет-бутил-2-(4-гидрокси-фенил)-2Н-пиразол-3-ил]-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-112,314-тетрагидро-нафталин-1-ил]-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-[4-(3-трет-бутил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-(5-трет-бутил-изоксазол-3-ил)-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-(5-трет-бутил-2-л-толил-2Н-пиразол-3-ил)-3-[4-(3-циклопентил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-[5-трет-бутил-2-(3-морфолин-4-илметил-фенил)-2Н-пиразол-3-ил]-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-a]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил-3-{4-(3-(2,6-дихлор-фенил [1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил}-мочевины;
1-(5-трет-бутил-2-л-толил-2Н-пиразол-3-ил)-3-[4-(3-циклопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил}-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-[4-(3-пиридин-2-ил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил}-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил-3-{4-(3-(2-хлор-фенил)-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил}-мочевины;
1-{4-[3-(2-бензилокси-фенил)-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил}-3-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-мочевины;
1-[5-трет-бутил-2-(3-хлор-4-гидрокси-фенил)-2Н-пиразол-3-ил]-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-[4-(3-циклогексил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-[5-трет-бутил-2-(4-хлор-3-гидрокси-фенил)-2Н-пиразол-3-ил]-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
N-(5-трет-бутил-3-{3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-уреидо}-2-метокси-фенил)-метансульфонамида;
1-(3-фтор-5-морфолин-4-ил-фенил)-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-{5-трет-бутил-2-(4-фтор-3-морфолин-4-илметил-фенил)-2Н-пиразол-3-ил}-3-[4-(3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-6-илокси)-1,2,3,4-тетрагидро-нафталин-1-ил]-мочевины;
1-[5-трет-бутил-2-(3-хлор-4-гидрокси-фенил)-2Н-пиразол-3-ил]-3-(4-{3-[2-(2-гидрокси-этилсульфанил)-фенил]-[1,2,4]триазоло[4,3-а]пиридин-6-илокси}-1,2,3,4-тетрагидро-нафталин-1-ил)-мочевины;
1-[5-трет-бутил-2-(3-хлор-4-гидрокси-фенил)-2Н-пиразол-3-ил]-3-(4-{3-[2-(2-гидрокси-этилсульфанил)-фенил]-[1,2,4]триазоло[4,3-а]пиридин-6-илокси}-1,2,3,4-тетрагидро-нафталин-1-ил)-мочевины;
1-(5-трет-бутил-2-п-толил-2Н-пиразол-3-ил)-3-{(4-[3-(2-пирролидин-1-ил-пиридин-4-ил)-[1,2,4]триазоло[4,3-а]пиридин-6-илокси]-1,2,3,4-тетрагидро-нафталин-1-ил}-мочевины;
и его фармацевтически приемлемые соли.
В частности, в настоящем изобретении предложено соединение, выбранное из группы, состоящей из соединений, перечисленных в Таблице ниже, или его фармацевтически приемлемая соль:
Другой аспект изобретения включает фармацевтические композиции, содержащие соединение по изобретению вместе с одним или более фармацевтически приемлемыми носителями и/или эксципиентами. Особенно предпочтительными являются композиции, изготовленные с возможностью ингалирования для легочного введения.
В другом аспекте изобретение включает применение соединения по изобретению для лечения заболеваний или состояний, при которых полезно ингибирование активности МАР-киназы р38. Предпочтительным применением является лечение обструктивных или воспалительных заболеваний дыхательных путей. Потенциально подлежат лечению соединениями по настоящему изобретению все формы обструктивных или воспалительных заболеваний дыхательных путей, в частности обструктивное или воспалительное заболевание дыхательных путей, которое выбрано из группы, состоящей из хронической эозинофильной пневмонии, астмы, COPD, COPD, которая включает хронический бронхит, легочную эмфизему или одышку, ассоциированную или не ассоциированную с COPD, COPD, которая характеризуется необратимой прогрессирующей обструкцией дыхательных путей, респираторного дистресс-синдрома легких (ARDS), обострения гиперреактивности дыхательных путей после терапии другими лекарственными средствами и заболевания дыхательных путей, которое ассоциировано с легочной гипертензией, хронических воспалительных заболеваний, включая муковисцидоз, бронхоэктаз и фиброз легких (идиопатический). Ожидается, что эффективность будет выше, когда ингибиторы р38 киназы вводят либо локально в легкое (например, посредством ингаляции и интраназальной доставки) или системным образом (например, пероральная, внутривенная и подкожная доставка).
Соединения по изобретению могут существовать в одной или более чем одной геометрической, оптической, энантиомерной, диастереомерной и таутомерной форме, включая, без ограничения ими, цис- и транс-формы, Е- и Z-формы, R-, S- и мезо-формы, кето- и енольные формы. Если не оговорено особо, ссылка на конкретное соединение включает все такие изомерные формы, в том числе их рацемические и другие смеси. Когда это целесообразно, такие изомеры могут быть выделены из их смесей путем использования или адаптации известных способов (например хроматографических методик и методик перекристаллизации). Когда это целесообразно, такие изомеры могут быть получены путем использования или адаптации известных способов (например ассиметрического синтеза).
Использованный здесь термин "соль" включает соли присоединения оснований, соли присоединения кислот и соли аммония. Соединения по изобретению, которые являются кислотными, могут образовывать соли, включая фармацевтически приемлемые соли, с основаниями, такими как гидроксиды щелочных металлов, например гидроксиды натрия и калия; гидроксиды щелочноземельных металлов, например гидроксиды кальция, бария и магния; с органическими основаниями, например N-метил-D-глюкамином, холином, трис(гидроксиметил)аминометаном, L-аргинином, L-лизином, N-этилпиперидином, дибензиламином и им подобными. Те соединения по изобретению, которые являются основными, могут образовывать соли, включая фармацевтически приемлемые соли, с неорганическими кислотами, например с галогенводородными кислотами, такими как соляная или бромистоводородная кислоты, серной кислотой, азотной кислотой или фосфорной кислотой и им подобными, и с органическими кислотами, например с уксусной, трифторуксусной, винной, янтарной, фумаровой, малеиновой, яблочной, салициловой, лимонной, метансульфоновой, пара-толуолсульфоновой, бензойной, бензолсульфоновой, глутаминовой, молочной и миндальной кислотами и им подобными. Те соединения по изобретению, которые имеют основной азот, могут также образовывать четвертичные аммониевые соли с фармацевтически приемлемым противоионом, таким как аммоний, хлорид, бромид, ацетат, формиат, пара-толуол сульфонат, сукцинат, гемисукцинат, нафталин-бис-сульфонат, метансульфонат, трифторацетат, ксинафоат и им подобные. Для обзора солей см. Handbook of Pharmaceutical Salts: Properties. Selection, and Use by Stahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002).
Полагают, что соединения по изобретению могут быть получены в форме гидратов и сольватов. Любая ссылка здесь, включая формулу изобретения, на "соединения, к которым относится изобретение", или "соединения по изобретению", или "настоящие соединения" и тому подобное включает ссылку на гидраты солей и сольваты таких соединений. Термин "сольват" использован здесь для описания молекулярного комплекса, содержащего соединение по изобретению и стехиометрическое количество одной или более чем одной молекулы фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" используют, когда указанный растворитель представляет собой воду.
Отдельные соединения по изобретению могут существовать в нескольких полиморфных формах и могут быть получены в различных кристаллических формах.
Соединения также могут быть введены в форме пролекарств. Таким образом, некоторые производные соединений, которые могут быть активны сами по себе или могут сами иметь небольшую активность или не иметь фармакологической активности вообще, могут при введении в организм или нанесении на тело превращаться в соединения по изобретению, имеющие требуемую активность, посредством, например, гидролитического расщепления. Такие производные называют "пролекарствами". Дополнительную информацию по применению пролекарств можно найти в Prodrugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T. Higuchi and V.J. Stella) и Bioreversible Carriers in Drug Design. Pergamon Press, 1987 (ed. Ε.B. Roche, American Pharmaceutical Association; C.S. Larsen and J. ⌀stergaard, Design and application of prodrugs, In Textbook of Drug Design and Discovery, 3rd Edition, 2002, Taylor and Francis).
Пролекарства в соответствии с изобретением могут, например, быть получены посредством замены соответствующих функциональных групп, присутствующих в соединениях по изобретению, определенными группировками, известными специалистам в данной области как ′про-группировки′, как описано, например, в Design of Prodrugs by Η. Bundgaard (Elsevier, 1985).
Воплощения изобретения
В одном воплощении соединения по изобретению представляют собой соединения формулы (Ia) или его фармацевтически приемлемые соли:
где группа R1 выбрана из группы, состоящей из:
- 3-[3-(2-морфолин-4-ил-этокси)-фенил]-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- (3-изопропил-[1,2,4]триазоло[4,3-а]пиридин-7-ила;
- 3-(2-гидрокси-фенил)-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- {2-[(метоксиацетил)амино]пиридин-4-ил}метила;
- 3-[3-(2-гидрокси-этилсульфанил)-фенил]-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-трет-бутил-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-циклопентил-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-(2,6-дихлор-фенил)-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-циклопропил-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-пиридин-2-ил-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-(2-хлор-фенил)-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-(2-бензилокси-фенил)-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-циклогексил-[1,2,4]триазоло[4,3-а]пиридин-6-ила;
- 3-(2-пирролидин-1-ил-пиридин-4-ил)-[1,2,4]триазоло[4,3-а]пиридин-6-ила.
В одном воплощении предложены соединения формулы (Ia1), которые представляют собой соединения формулы (Ia), как они определены выше, где углеродный стереогенный центр, обозначенный цифрой (1), имеет абсолютную конфигурацию, представленную ниже:
В предпочтительном воплощении предложены соединения формулы (Ia2), которые представляют собой соединения формулы (Ia), как они определены выше, где углеродные стереогенные центры, обозначенные цифрами (1) и (2), имеют абсолютную конфигурацию, представленную ниже:
В другом воплощении соединения по изобретению представляют собой соединения формулы (Ib) или их фармацевтически приемлемые соли:
где группа R2 выбрана из группы, состоящей из:
- 5-трет-бутил-2-фенил-2Н-пиразол-3-ила;
- циклопропила;
- 5-трет-бутил-2-[3-(2-морфолин-4-ил-этокси)-фенил]-2Н-пиразол-3-ила;
- 5-трет-бутил-2-[3-(2-диметиламино-этокси)-фенил]-2Н-пиразол-3-ила;
- 5-трет-бутил-2-(3-хлор-4-гидрокси-фенил)-2Н-пиразол-3-ила;
- 5-трет-бутил-2-(4-хлор-3-гидроксифенил)-2Н-пиразол-3-ила;
- 5-трет)-бутил-2-(4-гидрокси-фенил)-2Н-пиразол-3-ила;
- 5-трет-бутил-изоксазол-3-ила;
- 5-трет-бутил-2-(3-морфолин-4-илметил-фенил)-2Н-пиразол-3-ила;
- 5-трет-бутил-3-метансульфониламино-2-метокси-фенила;
- 3-фтор-5-морфолин-4-ил-фенила;
- 5-трет-бутил-2-(4-фтор-3-морфолин-4-илметил-фенил)-2Н-пиразол-3-ила.
В одном воплощении предложены соединения формулы (Ib2), которые представляют собой соединения формулы (Ib), как они определены выше, где углеродный стереогенный центр, обозначенный цифрой (1), имеет абсолютную конфигурацию, представленную ниже:
В предпочтительном воплощении предложены соединения формулы (Ib2), которые представляют собой соединения формулы (Ib), как они определены выше, где углеродные стереогенные центры, обозначенные цифрами (1) и (2), имеют абсолютную конфигурацию, представленную ниже:
В другом воплощении предложены соединения формулы (Ib), которые представляют собой соединения формулы (Ib3), как они определены выше, где углеродные стереогенные центры, обозначенные цифрами (1) и (2), имеют абсолютную конфигурацию, представленную ниже:
Применение
Как упомянуто выше, соединения по изобретению являются ингибиторами р38МАРК и поэтому могут быть использованы для лечения заболеваний или состояний, при которых полезно ингибирование фермента р38. Такие заболевания и состояния известны из литературы, и некоторые были упомянуты выше. Однако соединения в общем применяют в качестве противовоспалительных агентов, в частности для использования в лечении респираторного заболевания. В частности, соединения могут быть использованы в лечении хронической обструктивной болезни легких (COPD), хронического бронхита, фиброза легких, пневмонии, острого респираторного дистресс-синдрома (ARDS), эмфиземы легких или эмфиземы, вызванной курением, эндогенной (неаллергической) астмы и экзогенной (аллергической) астмы, легкой астмы, умеренной астмы, тяжелой астмы, стероид-резистентной астмы, нейтрофильной астмы, бронхиальной астмы, астмы, вызванной физическоой нагрузкой, профессиональной астмы и астмы, вызванной бактериальной инфекцией, муковисцидоза, легочного фиброза и бронхоэктаза.
В настоящем изобретении предложено применение соединений по изобретению для предупреждения и/или лечения любого заболевания или состояния, при котором полезно ингибирование фермента р38.
В дополнительном аспекте настоящего изобретения предложено применение соединений по изобретению для изготовления лекарственного средства для предупреждения и/или лечения любого заболевания или состояния, при котором полезно ингибирование фермента р38.
Кроме того, в настоящем изобретении предложен способ предупреждения и/или лечения любого заболевания или состояния, при котором полезно ингибирование фермента р38, включающий введение нуждающемуся в таком лечении пациенту терапевтически эффективного количества соединения по изобретению.
Композиции
Как упомянуто выше, соединения, к которым относится изобретение, являются ингибиторами р38-киназы и полезны в лечении некоторых заболеваний, например воспалительных заболеваний дыхательного тракта. Примеры таких заболеваний названы выше и включают астму, ринит, аллергический синдром дыхательных путей, бронхит и хроническую обструктивную болезнь легких.
Следует понимать, что конкретная доза для любого конкретного пациента будет зависеть от множества факторов, включая активность конкретного используемого соединения, возраста, массы тела, общего состояния здоровья, пола, питания, времени введения, пути введения, скорости выведения, комбинации лекарственных средств и тяжести конкретного заболевания, подвергаемого лечению. Оптимальные дозы и частота дозирования будут определены клиническим испытанием, как требуется в области фармацевтики. В целом, диапазон суточной дозы для перорального введения будет находиться в пределах от примерно 0,001 мг до примерно 100 мг на кг массы тела человека, часто от 0,01 мг до примерно 50 мг на кг, например от 0,1 до 10 мг на кг, в виде однократной или в виде разделенных доз. В целом, диапазон суточной дозы для ингаляционного введения будет находиться в пределах от примерно 0,1 мкг до примерно 1 мг на кг массы тела человека, предпочтительно от 0,1 мкг до 50 мкг на кг, в виде однократной или в виде разделенных доз. С другой стороны, в некоторых случаях может быть необходимо использование дозировок вне этих пределов. Для задачи данного изобретения ингаляционное введение является предпочтительным.
Соединения, к которым относится изобретение, могут быть получены для введения посредством любого пути в соответствии с их фармакокинетическими свойствами. Перорально вводимые композиции могут находиться в форме таблеток, капсул, порошков, гранул, лепешек, жидких или гелеобразных препаратов, таких как пероральные, местные или стерильные парентеральные растворы или суспензии. Таблетки и капсулы для перорального введения могут находиться в виде стандартной лекарственной формы и могут содержать традиционные эксципиенты, такие как связующие агенты, например сироп, аравийская камедь, желатин, сорбит, трагакант или поливинилпирролидон; наполнители, например лактозу, сахар, кукурузный крахмал, фосфат кальция, сорбит или глицин; смазывающее вещество для таблетирования, например стеарат магния, тальк, полиэтиленгликоль или диоксид кремния; разрыхлители, например картофельный крахмал, или приемлемые увлажняющие агенты, такие как лаурилсульфат натрия. Таблетки могут быть покрыты оболочкой согласно способам, хорошо известным в обычной фармацевтической практике. Пероральные жидкие препараты могут находиться в форме, например, водных или масляных суспензий, растворов, эмульсий, сиропов или эликсиров, или могут быть представлены в виде сухого продукта для разведения водой или другим подходящим носителем перед применением. Такие жидкие препараты могут содержать традиционные вспомогательные вещества, такие как суспендирующие агенты, например сорбит, сироп, метилцеллюлоза, крахмальная патока, желатин, гидрированные пищевые жиры; эмульгирующие агенты, например лецитин, сорбитанмоноолеат или аравийская камедь; неводные носители (которые могут включать пищевые масла), например миндальное масло, фракционированное кокосовое масло, сложные эфиры жирных кислот и, например, глицерина, пропиленгликоля или этилового спирта; консерванты, например метил- или пропил-пара-гидроксибензоат или сорбиновая кислота, и при необходимости традиционные ароматизаторы или красители.
Для местного применения на кожу лекарственное средство может быть приготовлено в виде крема, лосьона или мази. Композиции в виде крема или мази, которые могут быть использованы для лекарственного средства, являются традиционными композициями, хорошо известными в данной области техники, например, такими как описано в стандартных пособиях по фармацевтике, таких как Британская Фармакопея.
Активный ингредиент также можно вводить парентерально в стерильной среде. В зависимости от применяемого носителя и концентрации лекарственное средство может быть либо суспендировано, либо растворено в носителе. Предпочтительно в носителе могут быть растворены адъюванты, такие как анестетик местного действия, консервант и буферные агенты.
Однако для лечения воспалительного заболевания дыхательного тракта соединения по изобретению могут также быть приготовлены в виде препарата для ингаляции, например в виде назального спрея или ингаляторов сухого порошка или аэрозольных ингаляторов. Для доставки посредством ингаляции активное соединение предпочтительно находится в форме микрочастиц. Они могут быть приготовлены различными методами, включая сушку распылением, лиофильную сушку и микронизацию. Получение аэрозоля может быть осуществлено с использованием, например, струйных аэрозольных ингаляторов под давлением или ультразвуковых аэрозольных ингаляторов, предпочтительно при использовании дозированных аэрозолей на основе пропеллента или введения микронизированных активных соединений без пропеллента, например из капсул для ингаляции или других систем доставки "сухого порошка".
В качестве примера, композиция по изобретению может быть приготовлена в виде суспензии для доставки с помощью небулайзера или в виде аэрозоля в жидком пропелленте, например для использования в дозирующем ингаляторе под давлением (PMDI). Пропелленты, подходящие для использования в PMDI, известны специалисту в данной области техники и включают CFC-12 (хлорфторуглерод), HFA-134a (гидрофторалкан), HFA-227, HCFC-22 (CCl2F2) (гидрофторхлоруглерод) и HFA-152 (CH4F2 и изобутан).
В предпочтительном воплощении изобретения композиция по изобретению находится в форме сухого порошка для доставки при использованиии ингалятора сухого порошка (DPI). Известно много типов DPI.
Микрочастицы для доставки посредством введения могут быть приготовлены в виде препарата с эксципиентами, которые способствуют доставке и высвобождению. Например, в препарате сухого порошка микрочастицы могут быть приготовлены вместе с крупными частицами носителя, которые способствуют переносу из DPI в легкое. Подходящие частицы носителей известны и включают частицы лактозы; они могут иметь масс-медианный аэродинамический диаметр более чем 90 мкм.
Примером препарата на основе аэрозоля является следующий:
| Соединение по изобретению | 24 мг/баллончик |
| Лецитин, NF, жидкий, конц. | 1,2 мг/баллончик |
| Трихлорфторметан, NF | 4,025 г/баллончик |
| Дихлордифторметан, NF | 12,15 г/баллончик. |
Активные соединения можно дозировать, как описано, в зависимости от используемой системы ингалятора. Помимо активных соединений лекарственные формы могут дополнительно содержать эксципиенты, такие как, например, пропелленты (например Фриген в случае дозированных аэрозолей), поверхностно-активные вещества, эмульгаторы, стабилизаторы, консерванты, ароматизаторы, наполнители (например лактозу в случае порошковых ингаляторов) или, при необходимости, дополнительные активные соединения.
Для целей ингаляции доступно большое количество систем, с помощью которых могут быть получены и введены аэрозоли с оптимальным размером частиц при использовании ингаляционного метода, который подходит для пациента. Помимо использования переходников (спейсеры, расширители) и грушевидных контейнеров (например Nebulator®, Volumatic®) и автоматических устройств, распыляющих спрей (Autohaler®), для дозированных аэрозолей, в частности в случае порошковых ингаляторов, в наличии имеется ряд технических решений (например Diskhaler®, Rotadisk®, Turbohaler® или ингаляторы, например, как описано в ЕР-А-0505321). Кроме того, соединения по изобретению можно доставлять в многокамерных устройствах, тем самым делая возможной доставку комбинаций агентов.
Комбинации
Другие соединения можно объединять с соединениями, к которым относится изобретение, для предупреждения и лечения воспалительных заболеваний, в частности респираторных заболеваний. Таким образом, настоящее изобретение также относится к фармацевтическим композициям, содержащим терапевтически эффективное количество соединения по изобретению и одного или более чем одного другого терапевтического агента. Подходящие терапевтические агенты для комбинированной терапии с соединениями по изобретению включают, без ограничения ими: (1) кортикостероиды, такие как пропионат флутиказона, фуроат флутиказона, фуроат мометазона, дипропионат беклометазона, циклесонид, будесонид, GSK 685698, GSK 870086, QAE 397, QMF 149, ТРИ 020; (2) агонисты β2-адренорецепторов, такие как сальбутамол, альбутерол, тербуталин, фенотерол, и агонисты β2-адренорецепторов длительного действия, такие как салметерол, индакатерол, формотерол (включая фумарат формотерола), арформотерол, кармотерол, GSK 642444, GSK 159797, GSK 159802, GSK 597501, GSK 678007, AZD3199; (3) комбинированные продукты кортикостероид/р2-агонист длительного действия, такие как салметерол/пропионат флутиказона (адваир/серетид), формотеро