Биоразрушаемый материал и способ получения биоразрушаемого материала
Иллюстрации
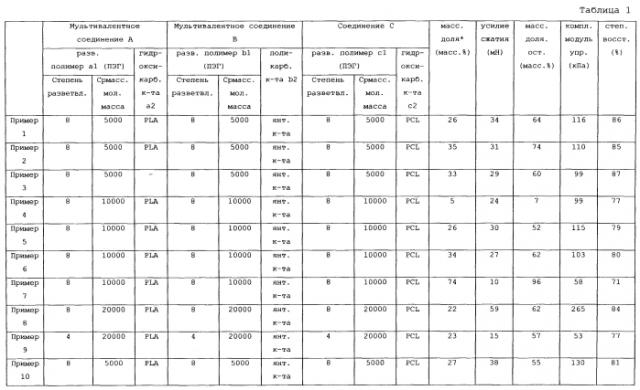
Показать всеИзобретение направлено на разработку биоразрушаемого материала с улучшенной способностью к разрушению в биологической среде, повышенной способностью к восстановлению формы после деформации материала и улучшенной эластичностью. Биоразрушаемый материал, который представляет собой сшитый поперечными химическими связями продукт мультивалентного соединения A, включающего 3 или более функциональные группы X, например гидроксильные группы, мультивалентного соединения B, включающего 3 или более функциональные группы Y, например карбоксильные группы, а также соединения C, имеющего структуру производного гидроксикарбоновой кислоты, гомополимер которой, полученный при гомополимеризации, имеет температуру стеклования -40°C или ниже. Также изобретение относится к материалам для эмболизации сосудов, перевязки ран, к материалу, предупреждающему недержание мочи, антиадгезионному материалу, которые состоят из указанного биоразрушаемого материала. 7 н. и 6 з.п. ф-лы, 1 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к биоразрушаемому материалу и способу получения биоразрушаемого материала.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
В целях остановки кровотечения после разреза пораженной зоны, блокирования поступления питательных веществ к опухоли, поддержания концентрации противоракового препарата в опухоли и подобных целей, в качестве полимерных частиц для эмболизации кровеносных сосудов и т.п. применялись сополимер поли(молочная кислота/гликолевая кислота) (патентный документ 1), блок-сополимер полиэтиленгликоля и полимолочной кислоты и т.д. (патентные документы 2-5) или мультиблок сополимер, полученный сополимеризацией молочной кислоты, полиэтиленгликоля, поликарбоновой кислоты и т.п. (патентный документ 6) и т.д.
Применение подобных полимерных частиц для эмболизации кровеносных сосудов и аналогичных целей было связано с такими проблемами, как невозможность добиться быстрого биоразрушения после выполнения целевых функций. Кроме того, поскольку эти полимерные частицы, которые применяются в форме сферических частиц с тем, чтобы плотно и надежно эмболизировать кровеносные сосуды и т.п., доставляются к целевому участку в кровеносном сосуде и т.п. через микрокатетер, имеющий небольшой диаметр, возникает такая проблема, как забивание катетера из-за недостаточной эластичности полимерных частиц или агрегации между ними, или же необратимая деформация частиц перед тем, как они достигнут целевого участка.
Для решения этих проблем предпринимались попытки регулировать эластичность полимерных частиц путем разработки частиц, сформированных из смеси полимеров нескольких типов (патентный документ 7) или путем разработки полимерных частиц, сшитых поперечными химическими связями (патентный документ 8). Кроме того, сообщалось о попытках покрытия поверхности полимерных частиц полиэтиленгликолем, чтобы предупредить агрегацию полимерных частиц и, тем самым, улучшить их способность проходить через катетер (патентный документ 9).
Кроме того, для предотвращения адгезии (образования спаек) между поврежденным участком поверхности органа, который появляется из-за хирургического вмешательства, и окружающими тканями, в качестве биоразрушаемого материала, например, антиадгезионного материала, перевязочного материала, гемостатического материала или материала, предупреждающего недержание мочи, применяется образующийся in situ гель, состоящий из такого сополимера, как, например, поли(этиленгликоль/полимолочная кислота) и полигликолевая кислота и т.п. (патентный документ 10); или гель, состоящий из декстрана и поли N-изопропилакриламида (патентный документ 11); или двухкомпонентный гель, состоящий из полиэтиленгликоля и т.п. и поликарбокси полисахарида (патентный документ 12); гель, состоящий из 2 типов полиэтиленгликолей и т.п. (патентный документ 13); или поперечно-сшитый ионный гель, например, карбоксиметилхитозан (патентный документ 14).
Сополимер поли(этиленгликоль/пропиленгликоль) (патентный документ 15), сополимер поли(молочная кислота/диоксанон) (патентный документ 16), сополимер поли(этиленгликоль/ модифицированная аминокислота/немодифицированная аминокислота) (патентный документ 17), сополимер поли(молочная кислота/депсипептид/этиленгликоль) (патентный документ 18), пористый лист, состоящий из сополимера поли(молочная кислота/этиленгликоль) (патентный документ 19) и т.д. также применялись, в качестве биоразрушаемого материала, например, антиадгезионного материала, перевязочного материала, кровоостанавливающего материала или материала для предупреждения недержания мочи; кроме того, предпринимались попытки регулировать способность материала к разрушению под действием биологической среды и его эластичность.
ССЫЛКИ НА ИСТОЧНИКИ ИЗВЕСТНОГО УРОВНЯ ТЕХНИКИ
Патентные документы
Патентный документ 1: JP 5-969 A
Патентный документ 2: JP 5-17245 B
Патентный документ 3: JP 2004-167229 A
Патентный документ 4: JP 2005-312623 A
Патентный документ 5: JP 2007-291323 A
Патентный документ 6: US 2009/0117033 A
Патентный документ 7: JP 2007-146146 A
Патентный документ 8: JP 4 655505 B
Патентный документ 9: JP 2007-145826 A
Патентный документ 10: JP 3107514 B
Патентный документ 11: JP 2003-252936 A
Патентный документ 12: JP 2003-531682 A
Патентный документ 13: JP 2002-541923 A
Патентный документ 14: JP 7-90041 B
Патентный документ 15: WO 96/21056
Патентный документ 16: JP 3483753 B
Патентный документ 17: JP 4735260 B
Патентный документ 18: JP 4734772 B
Патентный документ 19: JP 2008-36134 A
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Проблемы, которые предполагалось решить настоящим изобретением
Хотя усовершенствованные методики, такие как смешивание полимеров нескольких типов (патентный документ 7), применение химически сшитых полимерных частиц (патентный документ 8) и покрытие поверхности полимерных частиц (патентный документ 9), были способны улучшить регулирование эластичности полимерных частиц или их способности проходить через катетер, не удалось добиться существенного улучшения в отношении проблемы необратимой деформации полимерных частиц. Для достижения достаточного эффекта эмболизации кровеносных сосудов и т.п. необходимы дополнительные усовершенствования. Конкретно, имелась необходимость разработки материала для эмболизации кровеносных сосудов и т.п., например, полимерных частиц с высокой способностью восстанавливать свою исходную форму после прохождения через катетер (далее по тексту именуемой «степень восстановления формы частиц»).
Далее, хотя были достигнуты определенные успехи в улучшении биоразрушаемости или эластичности материалов, например, антиадгезионных материалов, перевязочных материалов, кровоостанавливающих материалов или материалов для предотвращения недержания мочи, биоразрушаемые материалы, состоящие, например, из двухкомпонентных гелей сталкиваются с той проблемой, что их физические свойства могут меняться в зависимости от факторов окружающей среды (например, температуры, влажности или pH) или соотношения компонентов смеси на целевом участке. Кроме того, поскольку поверхность органа или ткани, поврежденная при хирургическом вмешательстве, испытывает постоянное растяжение и сжатие, нанесенный на них биоразрушаемый материал может подвергаться необратимой деформации. В отношении этой проблемы, не удалось добиться существенного улучшения традиционных биоразрушаемых материалов, и существует потребность в разработке материала, например, антиадгезионного материала, перевязочного материала, кровоостанавливающего материала или материала для предотвращения недержания мочи, имеющего стабильные физические свойства и высокую степень восстановления формы.
Соответственно, цель настоящего изобретения заключалась в разработке биоразрушаемого материала с улучшенной степенью восстановления формы после деформации материала и улучшенной эластичностью.
Средства для решения указанных проблем
Настоящее изобретение конкретно относится к биоразрушаемому материалу и способу его получения, которые описаны ниже в пп. 1-15.
1. Биоразрушаемый материал, который представляет собой сшитый поперечными химическими связями продукт: мультивалентного соединения A, включающего 3 или более функциональные группы X, выбранные из группы, состоящей из гидроксильной группы, тиольной группы и аминогруппы; мультивалентного соединения B, включающего 3 или более функциональные группы Y, выбранные из группы, состоящей из карбоксильной группы, изоцианатной группы и тиоизоцианатной группы; а также соединения C, имеющего структуру, образованную из гидроксикарбоновой кислоты, гомополимер которой, полученный при гомополимеризации, имеет температуру стеклования -40°C или ниже.
2. Биоразрушаемый материал по п. 1, где массовая доля структуры, образовавшейся из соединения C, составляет от 18 до 70 мас.%.
3. Биоразрушаемый материал по пп. 1 или 2, где мультивалентное соединение A представляет собой одно из следующих соединений a)-e):
a) гомополимер или сополимер мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из полиэтиленгликоля, полипропиленгликоля, поливинилового спирта, полигидроксиэтилакрилата, полигидроксиэтилэтилметакрилата, карбоксиметилцеллюлозы, гидроксиметилцеллюлозы и гидроксиэтилцеллюлозы;
b) сополимер мономера водорастворимого полимера и мономера(ов) гидрофобного полимера(ов), выбранного из группы, состоящей из винилацетата и винилкапролактама;
c) сополимер мономера водорастворимого полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которых, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше;
d) разветвленный полимер, образованный связыванием всех гидроксильных групп полиола с гомополимером или сополимером мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из полиэтиленгликоля и полипропиленгликоля;
e) сополимер разветвленного полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше.
4. Биоразрушаемый материал по любому из пп. 1-3, где мультивалентное соединение B представляет собой одно из следующих соединений f)-i):
f) соединение, образованное при связывании гидроксильной группы(групп) гомополимера или сополимера мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из полиэтиленгликоля, полипропиленгликоля, поливинилового спирта, полигидроксиэтилакрилата, полигидроксиэтилметакрилата, карбоксиметилцеллюлозы, гидроксиметилцеллюлозы и гидроксиэтилцеллюлозы с поликарбоновой кислотой(ами);
g) соединение, образованное при связывании гидроксильной группы(групп) сополимера мономера водорастворимого полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше, с поликарбоновой кислотой(ами);
h) соединение, образованное при связывании гидроксильной группы(групп) разветвленного полимера, образованного при связывании всех гидроксильных групп полиола с гомополимером или сополимером мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из полиэтиленгликоля и полипропиленгликоля, с поликарбоновой кислотой(ами);
i) соединение, образованное связыванием гидроксильной группы(групп) сополимера разветвленного полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше, с поликарбоновой кислотой(ами).
5. Биоразрушаемый материал по любому из пп. 1-4, где соединение C представляет собой сополимер мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из полиэтиленгликоля, полипропиленгликоля, поливинилового спирта, полигидроксиэтилакрилата, полигидроксиэтилметакрилата, карбоксиметилцеллюлозы, гидроксиметилцеллюлозы и гидроксиэтилцеллюлозы, и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, полученный при гомополимеризации, имеет/имеют температуру стеклования -40°C или ниже.
6. Биоразрушаемый материал по любому из пп. 1-5, где соединение C представляет собой 6-гидроксикапроновую кислоту (6-гидроксигексановую кислоту).
7. Биоразрушаемый материал по любому из пп. 3-6, где разветвленный полимер имеет степень разветвления от 3 до 16.
8. Биоразрушаемый материал по любому из пп. 3-7, где полиол выбран из группы, состоящей из глицерина, полиглицерина и пентаэритрита.
9. Биоразрушаемый материал по любому из пп. 3-8, где гидроксикарбоновая кислота(кислоты), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше, выбрана(ы) из группы, состоящей из гликолевой кислоты, молочной кислоты, глицериновой кислоты, гидроксимасляной кислоты, яблочной кислоты, винной кислоты, гидроксивалериановой кислоты и 3-гидроксигексановой кислоты.
10. Биоразрушаемый материал по любому из пп. 4-9, где поликарбоновая кислота(кислоты) выбрана/выбраны из группы, состоящей из щавелевой кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, адипиновой кислоты, пимелиновой кислоты, пробковой кислоты, азелаиновой кислоты, себациновой кислоты, яблочной кислоты, винной кислоты и фумаровой кислоты.
11. Материал для эмболизации сосудов, состоящий из биоразрушаемого материала по любому из пп. 1-10.
12. Антиадгезионный материал, состоящий из биоразрушаемого материала по любому из пп. 1-10.
13. Материал для перевязки ран, состоящий из биоразрушаемого материала по любому из пп. 1-10.
14. Кровоостанавливающий материал, состоящий из биоразрушаемого материала по любому из пп. 1-10.
15. Материал, предупреждающий недержание мочи, состоящий из биоразрушаемого материала по любому из пп. 1-10.
16. Способ получения биоразрушаемого материала, где указанный способ включает стадию поперечного сшивания, в которой мультивалентное соединение A, включающее 3 или более функциональные группы X, выбранные из группы, состоящей из гидроксильной группы, тиольной группы и аминогруппы, мультивалентное соединение B, включающее 3 или более функциональные группы Y, выбранные из группы, состоящей из карбоксильной группы, изоцианатной группы и тиоизоцианатной группы, а также соединение C, имеющее структуру, образованную из гидроксикарбоновой кислоты, гомополимер которого, полученный при гомополимеризации, имеет температуру стеклования -40°C или ниже, растворяют в растворителе, который позволяет проводить химическую реакцию поперечного сшивания, с получением биоразрушаемого материала.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
Биоразрушаемый материал по настоящему изобретению имеет улучшенную биоразрушаемость и улучшенную степень восстановления формы после деформации материала, и может успешно применяться в качестве материала для эмболизации сосудов, который, например, можно легко доставить к целевому участку кровеносного сосуда или другого органа без забивания катетера, и который претерпевает быстрое разрушение в биологической среде и рассасывается после эффективной эмболизации целевого участка. Далее, поскольку биоразрушаемый материал по настоящему изобретению имеет улучшенную прочность на разрыв и прочность при сдвиге, и способен восстанавливать свою форму после деформации от растягивающего или сдвигающего усилия, его можно успешно применять в качестве такого материала, как антиадгезионный материал, перевязочный материал, кровоостанавливающий материал или материал, предупреждающий недержание мочи, например, наклеивая на орган или окружающую ткань, которая постоянно претерпевает растяжение и сжатие.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Используемые в заявке термины соответствуют данным ниже определениям, если не указано иное.
Биоразрушаемый материал по настоящему изобретению характеризуется тем, что он является сшитым поперечными химическими связями продуктом, состоящим из: мультивалентного соединения A, включающего 3 или более функциональные группы X, выбранные из группы, состоящей из гидроксильной группы, тиольной группы и аминогруппы; мультивалентного соединения B, включающего 3 или более функциональные группы Y, выбранные из группы, состоящей из карбоксильной группы, изоцианатной группы и тиоизоцианатной группы; а также соединения C, имеющего структуру, образованную из гидроксикарбоновой кислоты, гомополимер которой, полученный при гомополимеризации, имеет температуру стеклования -40°C или ниже.
Термин «биоразрушаемый» относится к способности биоразрушаемого материала разрушаться, растворяться, поглощаться или подвергаться метаболизму в живом организме, или выводиться из организма за его пределы. Примеры реакций разрушения материала включают гидролиз и разрушение под действием ферментов. Предпочтительным путем является гидролиз, т.к. он не зависит от ферментов.
Термин «сшитый поперечными химическими связями» относится к связыванию мультивалентного соединения A, мультивалентного соединения B и соединения C с использованием реагента, способствующего образованию поперечных связей (кросс-линкера). Примеры связей включают сложноэфирные связи, тиоэфирные связи, амидные связи и т.п. Предпочтительными являются сложноэфирные связи, поскольку они обеспечивают повышенную способность материала к биоразрушению. Кросс-линкер предпочтительно представляет собой реагент, осуществляющий дегидратацию-конденсацию. Наличие «сшивания поперечными химическими связями» можно подтвердить отсутствием изменения внешнего вида биоразрушаемого материала после погружения материала в воду на 1 час при температуре 25°C.
Массовая доля структуры, образовавшейся из упомянутого соединения C, в биоразрушаемом материале по настоящему изобретению предпочтительно составляет от 18 до 70 мас.%. Для улучшения эластичности и биоразрушаемости полученного биоразрушаемого материала, эта массовая доля, более предпочтительно, составляет от 20 до 65 мас.%.
Примеры «мультивалентного соединения A» включают:
i) гомополимер или сополимер, состоящий из мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из полиэтиленгликоля (далее по тексту именуемого «ПЭГ»), полипропиленгликоля (далее по тексту именуемого «ППГ»), поливинилового спирта (далее по тексту именуемого «PVA»), полигидроксиэтилакрилата, полигидроксиэтилэтилметакрилата, карбоксиметилцеллюлозы, гидроксиметил целлюлозы и гидроксиэтилцеллюлозы;
ii) сополимер мономера водорастворимого полимера и мономера(ов) гидрофобного полимера(ов), выбранного из группы, состоящей из винилацетата и винилкалролактама;
iii) сополимер мономера водорастворимого полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше;
iv) разветвленный полимер, образующийся при связывании всех гидроксильных групп полиола с гомополимером или сополимером мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из ПЭГ и ППГ; и
v) сополимер разветвленного полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше.
Мультивалентное соединение A содержит 3 или более функциональные группы X, выбранные из группы, состоящей из гидроксильной группы, тиольной группы и аминогруппы. Производные мультивалентного соединения A, например, галогенангидриды, сложные эфиры, ангидриды и гидрохлориды, также включены в число мультивалентных соединений А.
Для достижения устойчивого химического сшивания мультивалентного соединения A с мультивалентным соединением В и соединением С, и для улучшения биосовместимости полученного биоразрушаемого материала «водорастворимый полимер» предпочтительно является полиалкиленгликолем, например, ПЭГ или ППГ; полигидроксиалкил(мет)акрилатом, например, PVA, полигидроксиэтилметакрилатом или полигидроксиэтилакрилатом; или производным целлюлозы, например, карбоксиметилцеллюлозой, гидроксиметилцеллюлозой или гидроксиэтилцеллюлозой; более предпочтительно, полиалкиленгликолем.
Для увеличения плотности химического сшивания получаемого биоразрушаемого материала, мультивалентное соединение A предпочтительно является разветвленным соединением, например, разветвленным полимером (разветвленным полимером a1), образованным при связывании всех гидроксильных групп полиола с гомополимером или сополимером, состоящим из мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей ПЭГ и ППГ, более предпочтительно, сополимера разветвленного полимера и гидроксикарбоновой кислоты(кислот) (гидроксикарбоновой кислоты a2), еще более предпочтительно, блок-сополимера, в котором гидроксикарбоновая кислота(кислоты) связана/связаны с концом(ами) разветвленного полимера. Полиол предпочтительно является глицерином, полиглицерином или моносахаридом, например, пентаэритритом.
Примеры «мультивалентного соединения B» включают:
i) соединение, образованное при связывании гидроксильной группы(групп) гомополимера или сополимера мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из ПЭГ, ППГ, PVA, полигидроксиэтилакрилата, полигидроксиэтилметакрилата, карбоксиметилцеллюлозы, гидроксиметилцеллюлозы и гидроксиэтилцеллюлозы с поликарбоновой кислотой(ами);
ii) соединение, образованное при связывании гидроксильной группы(групп) сополимера мономера водорастворимого полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше, с поликарбоновой кислотой(ами);
iii) соединение, образованное при связывании гидроксильной группы(групп) разветвленного полимера, образованного при связывании всех гидроксильных групп полиола с гомополимером или сополимером мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из ПЭГ и ППГ, с поликарбоновой кислотой(ами); и
vi) соединение, образованное при связывании гидроксильной группы(групп) сополимера разветвленного полимера и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше, с поликарбоновой кислотой(ами).
Мультивалентное соединение B содержит 3 или более функциональные группы Y, выбранные из группы, состоящей из карбоксильной группы, изоцианатной группы и тиоизоцианатной группы. Производные мультивалентного соединения B, такие как галогенангидриды, сложные эфиры и ангидриды кислот также входят в число мультивалентных соединений В.
В качестве поликарбоновой кислоты, которая является одним из компонентов мультивалентного соединения B, предпочтительными с точки зрения доступности являются дикарбоновые кислоты, такие как щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, глутаровая кислота, адипиновая кислота, пимелиновая кислота, пробковая кислота, азелаиновая кислота, себациновая кислота, яблочная кислота, винная кислота или додекандиовая кислота; или лимонная кислота. Более предпочтительной является янтарная кислота, которая присутствует в живом организме и является весьма безопасной.
Мультивалентное соединение B предпочтительно является разветвленным соединением, например, соединением, образовавшимся при связывании гидроксильной группы(групп) разветвленного полимера (разветвленного полимера b1), образованного при связывании всех гидроксильных групп полиола с гомополимером или сополимером мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из ПЭГ и ППГ, с поликарбоновой кислотой(ами) (поликарбоновой кислотой b2). Полиол предпочтительно представляет собой глицерин, полиглицерин или моносахарид, например, пентаэритрит.
«Гидроксикарбоновая кислота», которая является одним из компонентов мультивалентного соединения A, мультивалентного соединения B, а также соединения C, включает циклические соединения, например, циклические димеры гидроксикарбоновых кислот. Производные гидроксикарбоновых кислот, такие как галогенангидриды, сложные эфиры и ангидриды кислот также включены в число гидроксикарбоновых кислот. Что касается гидроксикарбоновых кислот, имеющих оптические изомеры, например, яблочной кислоты и винной кислоты, термин «гидроксикарбоновая кислота» включает все их D-изомеры, L-изомеры, а также их смеси. Далее, гидроксикарбоновые кислоты включают сополимеры, образованные в результате сополимеризации этих гидроксикарбоновых кислот. Примеры гидроксикарбоновых кислот включают гликолевую кислоту, молочную кислоту, глицериновую кислоту, гидроксимасляную кислоту, яблочную кислоту, винную кислоту, гидроксивалериановую кислоту, 3-гидроксигексановую кислоту и 6-гидроксикапроновую кислоту. Примеры циклических соединений, состоящих из гидроксикарбоновых кислот, включают гликолид, который является циклическим димером гликолевой кислоты, лактид, который является циклическим димером молочной кислоты и s-капролактон, который соответствует 6-гидроксикапроновой кислоте. Примеры сополимеров, образующихся при сополимеризации гидроксикарбоновых кислот, включают сополимеры молочной кислоты и гликолевой кислоты, сополимеры молочной кислоты и терефталевой кислоты, сополимеры молочной кислоты и изофталевой кислоты, сополимеры 6-гидроксикапроновой кислоты и гликолевой кислоты, а также сополимеры 6-гидроксикапроновой кислоты и полибутилен сукцината (сополимера 1,4-бутандиола и янтарной кислоты). Гидроксикарбоновая кислота, гомополимер которой, образующийся при гомополимеризации, имеет температуру стеклования -39°C или выше, предпочтительно является молочной кислотой.
Примеры «гидроксикарбоновой кислоты, гомополимер которой, образующийся при гомополимеризации, имеет температуру стеклования -40°C или ниже», которая является компонентом «соединения C», включают 6-гидроксикапроновую кислоту, сополимеры 6-гидроксикапроновой кислоты и гликолевой кислоты, а также сополимеры 6-гидроксикапроновой кислоты и полибутилен сукцината (сополимера 1,4-бутандиола и янтарной кислоты). Предпочтительной является 6-гидроксикапроновая кислота. Термин «гомополимер» относится к полимеру, образующемуся при полимеризации одного типа мономера, например, полимолочной кислоте, образующейся при полимеризации чистой молочной кислоты. Однако понятие «гомополимер, образующийся при гомополимеризации» в настоящем изобретении охватывает также полимеры, образовавшиеся при полимеризации сополимеров одного типа, например, сополимера молочной кислоты и гликолевой кислоты.
Для увеличения плотности сшивания поперечными химическими связями соединения C с мультивалентным соединением А и мультивалентным соединением В, гидроксикарбоновая кислота, гомополимер которой, образующийся при гомополимеризации, имеет температуру стеклования -40°C или ниже, предпочтительно является сополимером мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из ПЭГ, ППГ, PVA, полигидроксиэтилакрилата, полигидроксиэтилметакрилата, карбоксиметилцеллюлозы, гидроксиметилцеллюлозы и гидроксиэтилцеллюлозы и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -40°C или ниже; более предпочтительно, сополимером разветвленного полимера, образующегося при связывании всех гидроксильных групп полиола с гомополимером или сополимером мономера(ов) водорастворимого полимера(ов), выбранного из группы, состоящей из ПЭГ и ППГ, и гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -40°C или ниже.
В случаях, когда мультивалентное соединение A, мультивалентное соединение B и соединение C являются разветвленными соединениями, они предпочтительно имеют степень разветвления от 3 до 16, более предпочтительно, от 4 до 12. В то время, как слишком низкая степень разветвления приводит к невозможности увеличить плотность сшивания химическими связями и обеспечить достаточную прочность биоразрушаемого материала, слишком высокая степень разветвления может помешать реакции образования поперечных химических связей из-за пространственных препятствий.
В случаях, когда мультивалентное соединение A, мультивалентное соединение B и соединение C являются сополимерами, они могут быть полимером любого из следующих типов: статистическим сополимером, блок-сополимером или чередующимся сополимером. Однако предпочтительно, они являются блок-сополимерами, поскольку механические и другие свойства получаемого биоразрушаемого материала можно легко регулировать и можно улучшить его эластичность и биоразрушаемость. Термин «сополимер» в данном описании относится к высокомолекулярному соединению, образовавшемуся при сополимеризации двух или нескольких типов мономеров. Термин «блок-сополимер» относится к сополимеру, в котором ковалентно связаны как минимум два или несколько типов полимеров, состоящих из различных повторяющихся звеньев, с образованием молекулярной структуры, напоминающей длинную цепь, где термин «блок» относится к каждому из «как минимум двух или нескольких типов полимеров, состоящих из различных повторяющихся звеньев», составляющих блок-сополимер.
Массовая доля структуры, образовавшейся из гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -39°C или выше в упомянутом выше мультивалентном соединении А предпочтительно составляет от 10 до 300 мас.%. Для достижения достаточной эластичности и биоразрушаемости получаемого биоразрушаемого материала, это массовое соотношение предпочтительно составляет от 30% до 250 мас.%, еще более предпочтительно от 40 до 200 мас.%.
Массовая доля структуры, образовавшейся из гидроксикарбоновой кислоты(кислот), гомополимер(ы) которой, образующийся при гомополимеризации, имеет/имеют температуру стеклования -40°C или ниже в упомянутом выше соединении С предпочтительно составляет от 10 до 300 мас.%. Для достижения достаточной эластичности и биоразрушаемости получаемого биоразрушаемого материала, это массовое соотношение предпочтительно составляет от 30% до 250 мас.%, еще более предпочтительно от 40 до 200 мас.%.
Если среднемассовые молекулярные массы мультивалентного соединения A, мультивалентного соединения B и соединения C будут слишком низкими, скорость биологического разрушения биоразрушаемого материала увеличится слишком сильно, и не удастся получить необходимый эффект эмболизации, например, при эмболизации сосудов. С другой стороны, если среднемассовые молекулярные массы мультивалентного соединения A, мультивалентного соединения B и соединения C будут слишком высокими, понизится способность биоразрушаемого материала к разрушению. Поэтому среднемассовые молекулярные массы упомянутых мультивалентного соединения A, мультивалентного соединения B и соединения C предпочтительно находятся в пределах от 1000 до 50000, более предпочтительно от 3000 до 30000. Среднемассовые молекулярные массы упомянутых мультивалентного соединения A, мультивалентного соединения B и соединения C можно измерить с помощью гель-проникающей хроматографии (далее по тексту именуемой «методика GPC») в следующих условиях:
Условия измерения:
Аппарат (колонка): TSKgel GMHHR-M (производства Tosoh Corporation; внутренний диаметр: 7,8 мм; длина: 30 см; две колонки расположены линейно);
Элюент: хлороформ;
Температура колонки: 35°C;
Скорость потока: 1,0 мл/мин;
Способ детектирования: показатель преломления;
Калибровочная кривая: строили с использованием стандартных образцов полистирола.
Предпочтительно, чтобы величина NB/(NA+NC) имела значение от 1,2 до 4,0, где МВ≥МАС и величина (NA+NC)/NB имела значение от 1,2 до 4,0, где МВ<МАС, более предпочтительно, чтобы значения указанных величин находились в пределах от 1,3 до 3,0, еще более предпочтительно от 1,4 до 2,5, где NA означает число молей функциональных групп X, содержащихся в мультивалентном соединении A; NB означает число молей функциональных групп Y, содержащихся в мультивалентном соединении В; и NC означает число молей функциональных групп соединения C, выбранных из группы, состоящей из гидроксильной группы, тиольной группы, аминогруппы, карбоксильной группы, изоцианатной группы и тиоизоцианатной группы; и где переменные величины определяются указанным ниже образом:
MA: среднемассовая молекулярная масса мультивалентного соединения A;
MB: среднемассовая молекулярная масса мультивалентного соединения B;
MC: среднемассовая молекулярная масса соединения C;
MAC: среднемассовая молекулярная масса смеси мультивалентного соединения A и соединения C.
Согласно знаниям известного уровня техники (JP 2007-145826 A), равенство значений NB и (NA+NC) увеличит до максимума количество сформировавшихся связей, т.е. максимально повысит плотность поперечного сшивания, в результате чего теоретически не останется не вступивших в реакцию функциональных групп. Однако в настоящем изобретении предпочтительно, чтобы одна из величин NB и (NA+NC) превышала другую, находясь в оптимальном диапазоне относительно нее.
Массовые доли и прочие параметры конкретных структур в каждом компоненте из числа мультивалентного соединения A, мультивалентного соединения B и соединения C можно вычислить на основании результатов измерений, полученных с применением методики ядерного магнитного резонанса (далее по тексту именуемой «1H-ЯМР») в указанных ниже условиях. Например, в случае, если гидроксикарбоновая кислота является молочной кислотой, для определения указанных параметров может использоваться каждый атом водорода метиновой группы в α-положении (величина химического сдвига: примерно 5,2 м.д.). В случае, если гидроксикарбоновая кислота представляет собой 6-гидроксикарбоновую кислоту, для определения указанных параметров может использоваться атом водорода метиленовой группы в соположении (величина химического сдвига: примерно 2,3 м.д.). В случае, если гидроксикарбоновая кислота представляет собой гликолевую кислоту, для определения указанных параметров может использоваться атом водорода метиленовой группы в α-положении (величина химического сдвига: примерно 4,8 м.д.). С другой стороны, что касается ПЭГ, для определения указанных параметров могут использоваться 4 атома водорода этиленовых групп (величина химического сдвига: примерно 3,5 м.д.). Каждую массовую долю можно вычислить исходя из интегральных значений сигнала, появляющегося при каждом из указанных характеристических химических сдвигов атомов водорода.
Условия регистрации спектров ЯМР
Спектрометр: JNM-EX270 (производства JEOL Ltd., 270 МГц);
Растворитель: дейтерированный хлороформ (содержащий 0,05 об.% TMS в качестве внутреннего стандарта);
Температура регистрации спектра: 20°C.
В случаях, если биоразрушаемый материал по настоящему изобретению получают в виде ацетонитрил-содержащей пленки, комплексный модуль упругости этого материала предпочтительно составляет от 40 до 400 кПа. Комплексный модуль упругости можно вычислить, исходя из результатов измерений, полученных на устройстве для измерения вязкоупругих свойств (далее по тесту именуемого «реометром») при указанных ниже условиях.
Конкретно, указанные количества мультивалентного соединения A, мультивалентного соединения B и соединения C (все в виде 0,3 г/мл растворов в ацетонитриле), а также катализатор (0,1 г/мл раствор в ацетонитриле) и концентрированный раствор конденсирующего агента быстро смешивали с получением смешанного раствора. Затем 500 мкл смешанного раствора капали на пластину устройства, помещая смешанный раствор между неподвижной и подвижной пластинами устройства, и осуществляли тест на динамическую вязкоупругость в течение 105 с после смешивания.
Условия проведения измерений
Наименование теста: тест на динамическую вязкоупругость;
Прибор (реометр): MCR301 (производства Anton Parr Ltd.);
Неподвижная пластина: CP40-1 (диаметр: 39,958 мм; угол: 1°);
Зазор: 0,081 мм (расстояние между неподвижной пластиной и пластиной устройства, между которыми помещают образец);
Деформация: 0,1% (постоянная);
Угловая скорость: 10 рад/с (постоянная);
Температура измерения: 25°C;
Время измерения: 18000 с.
Термин «ацетонитрил-содержащая пленка» относится к пленке, сформированной поперечным сшиванием химически связями мультивалентного соединения A, мультивалентного соединения B и соединения C, в которой по-прежнему содержится ацетонитрил, причем указанная пленка получена после измерения реометром.
Термин «комплексный модуль упругости» означает величину, отображающую эластичность биоразрушаемого материала и относящуюся к значению модуля Е* (кПа), вычисленному по приведенному ниже уравнению 1, причем эта величина описывает как упругие так и вязкие свойства измеряемого образца, который является вязкоупругим телом.
Конкретно, в случаях, когда биоразрушаемый материал по настоящему изобретению применяется в качестве материала для эмболизации сосудов, слишком низкое значение комплексного модуля