Стабильные и растворимые антитела, ингибирующие vegf
Иллюстрации
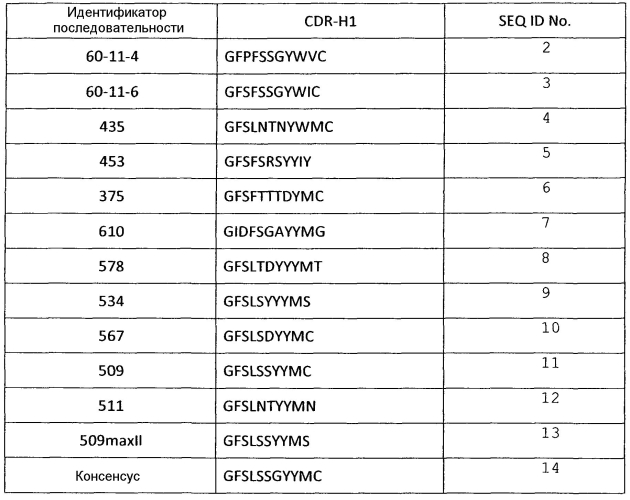
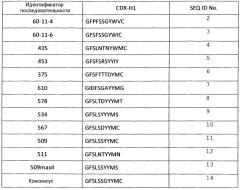
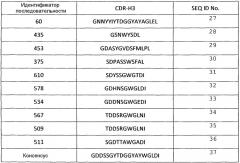
Показать всеИзобретение относится к биохимии. Описано рекомбинантное антитело, его фрагмент, нейтрализующие VEGF человека, содержащие вариабельную область тяжелой цепи (VH), где VH содержит CDRH1, CDRH2 и CDRH3 последовательности SEQ ID NO: 8, SEQ ID NO: 20 и SEQ ID NO: 32 соответственно, и вариабельную область легкой цепи (VL), где VL содержит CDRL1, CDRL2 и CDRL3 последовательности SEQ ID NO: 43, SEQ ID NO: 55 и SEQ ID NO: 66 соответственно и где вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 164 и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 87. Представлены фармацевтические композиции для лечения VEGF-опосредованного заболевания и способы лечения VEGF-опосредованного заболевания. 7 н. и 3 з.п. ф-лы, 15 ил., 12 табл., 7 пр.
Реферат
Релевантная информация
По настоящей заявке испрашивается приоритет US 61/133212, поданной 25 июня 2008 года, US 61/075697, поданной 25 июня 2008 года, US 61/155041, поданной 24 февраля 2009 года и US 61/075692, поданной 25 июня 2008 года.
Содержания любых патентов, заявок на патент и ссылок, цитируемых в этом описании, включены в настоящее описание в качестве ссылки в полном объеме.
Уровень техники
Считается, что ангиогенез участвует в патогенезе различных нарушений, включая солидные опухоли, внутриглазные неоваскулярные синдромы, такие как пролиферативные ретинопатии или возрастная дегенерация желтого пятна (AMD), ревматоидный артрит и псориаз (Folkman et al., J. Biol. Chem. 267: 10931-10934 (1992); Klagsbrun et al., Annu. Rev. Physiol. 53: 217-239 (1991); и Garner A, Vascular diseases. In: Pathobiology of ocular disease. A dynamic approach. Garner A, Klinrworth G K, Eds. 2nd Edition Marcel Dekker, NY, pp 1625-1710 (1994)). При солидных опухолях, ангиогенез и рост новой сосудистой сети обеспечивает выживание опухоли, и между плотностью микрососудов в срезах опухолей и выживанием пациентов в случае рака молочной железы и других раковых опухолей была продемонстрирована четкая корреляция (Weidner et al. N Engl J Med 324: 1-6 (1991); Horak et al. Lancet 340: 1120-1124 (1992); и Macchiarini et al. Lancet 340: 145-146 (1992)).
Эндотелиальный фактор роста сосудов (VEGF) является известным регуляторным фактором ангиогенеза и неоваскуляризации, и было показано, что он является ключевым медиатором неоваскуляризации, связанной с опухолями и внутриглазными нарушениями (Ferrara et al. Endocr. Rev. 18: 4-25 (1997)). мРНК VEGF сверхэкспрессируется во многих опухолях человека, и концентрация VEGF в глазных жидкостях в высокой степени коррелируют с наличием активной пролиферации кровеносных сосудов у пациентов с диабетической ретинопатией и другими связанными с ишемией ретинопатиями (Berkman et al., J Clin Invest 91: 153-159 (1993); Brown et al. Human Pathol. 26: 86-91 (1995); Brown et al. Cancer Res. 53: 4727-4735 (1993); Mattern et al. Brit. J. Cancer. 73: 931-934 (1996); и Dvorak et al. Am J. Pathol. 146: 1029-1039 (1995); Aiello et al. N. Engl. J. Med. 331: 1480-1487 (1994)). Кроме того, недавние исследования показали наличие локализованного VEGF в хороидальных неоваскулярных мембранах у пациентов, пораженных AMD (Lopez et al. Invest. Ophtalmo. Vis. Sci. 37: 855-868 (1996)). Нейтрализующие антитела против VEGF могут быть использованы для подавления роста различных линий опухолевых клеток человека у «голых» мышей, а также ингибирования внутриглазного ангиогенеза на моделях ишемических ретинальных нарушений (Kim et al. Nature 362: 841-844 (1993); Warren et al. J. Clin. Invest 95: 1789-1797 (1995); Borgstrom et al. Cancer Res. 56: 4032-4039 (1996); и Melnyk et al. Cancer Res. 56: 921-924 (1996)) (Adamis et al. Arch. Opthalmol. 114: 66-71 (1996)).
Таким образом, существует потребность в моноклональных антителах против VEGF, которые могут быть использованы для лечения солидных опухолей и различных неоваскулярных внутриглазных заболеваний.
Сущность изобретения
Настоящее изобретение относится к растворимым и стабильным анти-VEGF-иммуносвязывающим агентам, содержащим CDR моноклональных антител кролика. Указанные антитела предназначены для диагностики и/или лечения VEGF-опосредованных нарушений. Также описаны гибридомы, нуклеиновые кислоты, векторы и клетки-хозяева для экспрессии рекомбинантных антител по настоящему изобретению, способы их выделения и использование указанных антител в медицине.
Краткое описание фигур
Фиг. 1 иллюстрирует кинетику связывания выбранных scFv с hVEGF165 с использованием Biacore (hVEGF165). Фиг. 1а показывает данные, полученные для 511max: Ka (1/Ms): 6,59E+05; SE (ka): 1,10E+03; kd (1/s): 4,40E-05; SE (kd): 6,30E-07; KD (M): 6,67E-11. Фиг. 1b показывает данные, полученные для 578max: Ka (1/Ms): 7,00E+05; SE (ka): 1,40E+03; kd (1/s): 3,07E-04; SE (kd): 8,50E-07; KD (M): 4,39E-10.
Фиг. 2 иллюстрирует видоспецифичность, показывая кинетику связывания 578max с VEGF человека, мыши и крысы. Фиг. 2а показывает данные, полученные для VEGF165 человека: Ka (1/Ms): 7,00E+05; SE (ka): 1,40E+03; kd (1/s): 3,07E-04; SE (kd): 8,50E-07; KD (M): 4,39E-10. Фиг. 2b показывает данные, полученные для VEGF164 мыши: Ka (1/Ms): 1,03E+06; SE (ka): 2,30E+03; kd(1/s): 4,40E-04; SE(kd): 9,40E-07; KD(M): 4,29E-10. Фиг. 2c показывает данные, полученные для VEGF164 крысы: Ka (1/Ms): 8,83E+05; SE (ka): 2,50E+03; kd (1/s): 5,28E-04; SE (kd): 1,20E-06; KD (M): 5,98E-10.
Фиг. 3 иллюстрирует кинетику связывания 578max с VEGF-изоформами (hVEGF121 и hVEGF110). Фиг. 3a показывает данные, полученные для VEGF165 человека: Ka (1/Ms): 7,00E+05; SE (ka): 1,4E+03; kd (1/s): 3,07E-04; SE (kd): 8,50E-07; KD (M): 4,39E-10. Фиг. 3b показывает данные, полученные для VEGF121 человека: Ka (1/Ms): 5,87E+05; SE (ka): 1,20E+03; kd (1/s): 5,58E-04; SE (kd): 9,60E-07; KD (M): 9,50E-11.
Фиг. 4 изображает кинетику связывания 578max, 578minmax и 578wt с hVEGF165. Фиг. 4а показывает данные, полученные для 578max: Ka (1/Ms): 7,00E+05; SE (ka): 1,40E+03; kd (1/s): 3,07E-04; SE (kd): 8,50E-07; KD (M): 4,39E-10. Фиг. 4b показывает данные, полученные для 578minmax: Ka (1/Ms): 8,06E+05; SE (ka): 2,10E+03; kd (1/s): 5,04E-04; SE (kd): 1,10E-06; KD (M): 6,25E-10. Фиг. 4c показывает данные, полученные для 578wt-His: Ka (1/Ms): 8,45E+05; SE (ka): 1,60E+03; kd (1/s): 1,69E-04; SE (kd): 7,60E-07; KD (M): 2,00E-10.
Фиг. 5 иллюстрирует термическую стабильность 578max, 578minmax и 578minmax_DHP (разворачивание, измеренное посредством FT-IR). Фиг. 5а: 578minmax (ESBA903): Tm=71,1°C; Фиг. 5b: 578minmax_DHP (#961): Tm=70,2°C; Фиг. 5c: 578max (#821): Tm=70,4°C.
Фиг. 6 иллюстрирует денатурацию и осаждение производныех 578 после теплового стресса (Фиг. 6а: 50°C, Фиг. 6b: 60°C, Фиг. 6c: 70°C) в течение 30 минут.
Фиг. 7 иллюстрирует растворимость 578max, 578minmax и 578minmax_DHP (определяемую по осаждению сульфатом аммония). Фиг. 7a: 578max (#821). V50 был равен 27,24%. Фиг. 7b: 578minmax (ESBA903). V50 был равен 28,13. Фиг. 7c: 578minmax_DHP (#961). V50 был равен 32,36%.
Фиг. 8 иллюстрирует конкурентный ELISA VEGFR2 относительно HUVEC-анализа в качестве способов для измерения эффективности. Фиг. 8a: Сравнение Lucentis и 511max (#802) в конкурентном ELISA VEGFR2. R2 Lucentis: 0,9417; R2 ESBA802: 0,9700. EC50 Lucentis: 7,137 нМ; EC50 #802: 0,8221 нМ. Фиг. 8b: Сравнение Lucentis и 578max (#821) в конкурентном ELISA VEGFR2. Фиг. 8c: Сравнение Lucentis, 511maxC-his и 534max в HUVEC-анализе. R2 Lucentis 0,9399; R2 EP511maxC-his: 0,9313, R2 EP534max: 0,7391. EC50 Lucentis: 0,08825 нМ, EC50 511maxC-his: 0,7646 нМ, EC50 534max: 63,49 нМ. Фиг. 8d: Сравнение Lucentis, 578min и 578max в HUVEC-анализе. R2 Lucentis: 0,9419, R2 EP578min: 0,8886, R2 EP578max: 0,9274. EC50 Lucentis: 0,1529 нМ, EC50 578min: 1,528 нМ, EC50 578max: 0,1031 нМ.
Фиг. 9 иллюстрирует действия 578minmax на пролиферацию HUVEC, индуцируемую hVEGF165. Параметры этого анализа были следующими: 0,08 нМ (3 нг/мл); инкубирование с VEGF и тест-изделием: 96 часов. EC50 была равна 0,08959 нМ для Lucentis и 0,05516 нМ для 578minmax, в то время как R2 был равен 0,9066 для Lucentis и 0,9622 для 578minmax.
Фиг. 10 иллюстрирует действия 578minmax на пролиферации HUVEC, индуцируемые VEGF164 мыши и VEGF164 крысы. Параметры этого анализа были следующими: концентрация VEGF164 мыши: 0,08 нМ (3 нг/мл); концентрация VEGF164 крысы: 0,3 нМ (11,3 нг/мл). Обе концентрации выбирали при EC90 для VEGF-индуцированной пролиферации HUVEC; инкубирование с VEGF и тест-изделием: 96 часов. Фиг. 10a иллюстрирует данные, полученные для VEGF мыши. EC50 была равна 0,1196 нМ для V1253 и 0,06309 нМ для 578minmax, в то время как R2 был равен 0,02744 для Lucentis, 0,9348 для V1253 и 0,9767 для EP578minmax. Lucentis не ингибировал пролиферацию HUVEC, индуцированную VEGF мыши. Фиг. 10b иллюстрирует данные, полученные для VEGF крысы. EC50 была равна 1,597 нМ для V1253 и 0,06974 нМ для 578minmax, в то время как R2 был равен 0,7664 для V1253 и 0,6635 для 578minmax.
Фиг. 11 иллюстрирует исследования эффективности с использованием анализа Miles в голых морских свинках (часть I). Голым морским свинкам вводили внутривенно краситель альмаровый синий. Спустя один час после инъекции красителя премикс 2 hVEGF (2,61 нМ) и Lucentis, ESBA903 или #802 соответственно инъецировали в кожу животного 3. Спустя один час после инъекции этих растворов животных 3 эвтаназировали и шкурки собирали, очищали и фотографировали цифровым способом с использованием падающего света и рассеянного света. Площадь красителя Evans Blue, который просачивался в места инъекции, оценивали с использованием изображения J и строили график зависимости площади удерживания от дозы.
Фиг. 12 иллюстрирует исследования эффективности с использованием анализа Miles в голых морских свинках (часть II). Фиг. 12a показывает результаты, полученные для #803 (511max). EC50 была равна 5,990 нМ и имела статистический разброс между 2,060 и 17,41 нМ, тогда как R2 был равен 0,5800. Фиг. 12b показывает результаты, полученные для ESBA903 (578minmax). EC50 был равен 3,989 и имел статистический разброс между 1,456 и 10,93 нМ, тогда как R2 был равен 0,3920. Фиг. 12c показывает зону просачивания красителя для Lucentis. EC50 для Lucentis не могла быть рассчитана вследствие плохой подгонки кривой.
Фиг. 13 иллюстрирует исследования эффективности с использованием модифицированного анализа Miles в крысах (предварительно смешанные hVEGF165 и 578minmax (ESBA903)). Фиг. 13а иллюстрирует понижающую проницаемость эффективность Авастина на VEGF-индуцированном ретинальном васкулярном просачивании в крысах - доза-ответ. Авастин ингибирует hVEGF-индуцируемую ретинальную васкулярную проницаемость. Предварительное смешивание перед инъекцией. Приблизительно эквимолярные, 3-кратный или 10-кратный избыток. *p<0,05 (VEGF vs. BSA), **p<0,05 (Авастин-обработанные vs. VEGF). Фиг. 13b показывает понижающую проницаемость эффективность ESBA903 после VEGF-индуцируемого ретинального васкулярного просачивания в крысах. Доза-ответ (предварительно смешанные, ivt). Полное ингибирование hVEGF-индуцируемой ретинальной васкулярной проницаемости ESBA903. Предварительное смешивание перед инъекцией. Приблизительно эквимолярные, 3-кратный или 10-кратный избыток. *p<0,05 (VEGF s. BSA), **p<0,05 (ESBA903-обработанные vs. VEGF).
Фиг. 14 иллюстрирует исследования эффективности с использованием модифицированного анализа Miles в крысах (местное введение 578minmax (ESBA903)). Понижающую проницаемость AL-51287 (ESBA903) после VEGF-индуцированного ретинального васкулярного просачивания в крысах испытывали после местного введения. За пять дней перед обработкой, 4 капли/день с 10 нг/мл готовой формы ESBA903. *p<0,05 (VEGF vs. BSA), **p<0,05 (VEGF vs. AL-51287), ***p=0,060 (AL-51287 vs. AL-52667), ****(VEGF vs. AL-39324); p<0,05 (AL-39324 vs. носителя-ссылочного контроля). AL-51287: ESBA903; AL-52657: местный носитель-ссылочный контроль; AL-39324: ингибитор-малая молекула RTK.
Фиг. 15 иллюстрирует определение CDR1 VH, используемое в настоящем описании.
Подробное описание
Изобретение относится к растворимым и стабильным анти-VEGF-связывающим агентам, содержащим CDR из моноклональных антител кролика. Указанные иммуносвязывающие агенты предназначены для диагностики и/или лечения VEGF-опосредованных нарушений. Также описаны гибридомы, нуклеиновые кислоты, векторы и клетки-хозяева для экспрессии рекомбинантных антител по настоящему изобретению, способы их выделения и использование указанных антител в медицине.
Определения
Для облегчения понимания настоящего изобретения некоторые термины будут определены следующим образом. Дополнительные определения представлены во всем подробном описании.
Термин "VEGF" относится к состоящему из 165 аминокислот эндотелиальному фактору роста сосудов и соответствующим состоящим из 121 аминокислоты, 189 аминокислот и 206 аминокислот эндотелиальным факторам роста сосудов, описанным Leung et al., Science 246: 1306 (1989) и Houck et al., Mol. Endocrin. 5: 1806 (1991), а также к природным аллельным и процессированным формам этих факторов роста.
Термин "VEGF-рецептор" или "VEGFr" относится к клеточному рецептору VEGF, обычно рецептору клеточной поверхности, обнаруживаемому на эндотелиальных клетках сосудов, а также его вариантам, которые сохраняют способность связываться с hVEGF. Одним из примеров VEGF-рецептора является fms-подобная тирозинкиназа (flt), трансмембранный рецептор в семействе тирозинкиназ. DeVries et al., Science 255: 989 (1992); Shibuya et al., Oncogene 5: 519 (1990). Рецептор flt содержит внеклеточный домен, трансмембранный домен и внутриклеточный домен с тирозинкиназной активностью. Внеклеточный домен участвует в связывании с VEGF, тогда как внутриклеточный домен участвует в трансдукции сигнала. Другим примером VEGF-рецептора является рецептор flk-1 (также называемый KDR). Matthews et al., Proc. Nat. Acad. Sci. 88: 9026 (1991); Terman et al., Oncogene 6: 1677 (1991); Terman et al., Biochem. Biophys. Res. Commun. 187: 1579 (1992). Связывание VEGF с рецептором flt приводит к образованию по меньшей мере двух высокомолекулярных комплексов со средней молекулярной массой 205000 и 300000 Дальтон. Считается, что комплекс 300000 Дальтон является димером, содержащим две молекулы рецептора, связанные с единственной молекулой VEGF.
Термин "кролик” относится в контексте настоящей заявки к животному, принадлежащему семейству заячьих.
Термин "антитело" является в контексте настоящей заявки синонимом для "иммуноглобулина". Антитела по настоящему изобретению могут быть полноразмерными иммуноглобулинами или их фрагментами, содержащими по меньшей мере один вариабельный домен иммуноглобулина, такими как отдельные вариабельные домены, Fv (Skerra A. and Pluckthun, A. (1988) Science 240: 1038-41), scFv (Bird, R.E. et al (1988) Science 242: 423-26; Huston, J.S. et al., (1988) Proc. Natl. Acad. Sci. USA 85: 5879-83), Fab, F(ab′)2 или другие фрагменты, хорошо известные специалисту в данной области.
Термин "CDR" относится к одному из шести гипервариабельных районов в вариабельных доменах антитела, которые в основном способствуют связыванию антитела с антигеном. Одно из наиболее часто используемых определений для этих шести CDR представлено в статье Kabat E.A. et al., (1991) Sequences of proteins of immunological interest. NIH Publication 91-3242). В контексте настоящей заявки определение CDR Кабата относятся только к CDR1, CDR2 и CDR3 вариабельного домена легкой цепи (CDR L1, CDR L2, CDR L3 или L1, L2, L3), а также к CDR2 и CDR3 вариабельного домена тяжелой цепи (CDR H2, CDR H3 или H2, H3). Однако CDR1 тяжелой цепи (CDR H1 или H1) определяется в данном случае следующими остатками (согласно нумерации Кабата): он начинается с положения 26 и заканчивается перед положением 36. Он является в основном слиянием CDR H1, по-разному определяемым Кабатом и Хотиа (см. также Фиг. 15 для иллюстрации).
Термин "каркас антитела", или иногда только "каркас", относится в данном случае к части вариабельного домена, либо VL, либо VH, которая служит в качестве каркаса для антигенсвязывающих петель (CDR) вариабельного домена. В сущности, он является вариабельным доменом без CDR.
Термин "одноцепочечное антитело", "одноцепочечный Fv" или "scFv" относится к молекуле, содержащей вариабельный домен тяжелой цепи антитела (или район; VH) и вариабельный домен легкой цепи (или район; VL), связанные линкером. Такие молекулы scFv могут иметь общие структуры: NH2-VL-линкер-VH-COOH или NH2-VH-линкер-VL-COOH.
В контексте настоящей заявки "идентичность" обозначает совпадение последовательности двух полипептидов, молекул или двух нуклеиновых кислоты. Если какое-либо положение в обеих из этих двух сравниваемых последовательностей занято одним и тем же основанием или мономерной аминокислотной субъединицей (например, если какое-либо положение в каждой из двух молекул ДНК занято аденином или какое-либо положение в каждом из двух полипептидов занято лизином), то соответствующие молекулы являются идентичными в этом положении. "Процентная идентичность" двух последовательностей является функцией числа совпадающих положений, являющихся общими для этих двух последовательностей, деленного на число сравниваемых положений х 100. Например, если совпадают 6 из 10 положений в двух последовательностях, то эти последовательности имеют 60% идентичность. В качестве примера, DNA-последовательности CTGACT и CAGGTT имеют 50% идентичность (совпадают 3 из 6 общих положений). Обычно сравнение делается при сопоставлении двух последовательностей для получения максимальной идентичности. Такое сопоставление может быть обеспечено с использованием, например, способа Needleman et al., (1970) J. Mol. Biol. 48:443-453, осуществляемого предпочтительно компьютерными программами, такими как программа Align (DNAstar, Inc.). Процентная идентичность двух аминокислотных последовательностей может быть также определена с использованием алгоритма E. Meyers and W. Miller {Comput. Appl. Biosci., 4: 1 1-17 (1988)), который включен в программу ALIGN (версию 2.0), с использованием таблицы PAM120 взвешенных остатков, штрафа за удлинение 12 и штрафа за пропуск 4. Кроме того, процентная идентичность между двумя аминокислотными последовательностями может быть определена с использованием алгоритма Needleman и Wunsch (J. Mol. Biol. 48: 444-453 (1970)), который был включен в программу GAP в пакете программ GCG.software (доступном в www.gcg.com), с использованием либо матрицы Blossum 62, либо матрицы PAM250 и величины пропуска 16, 14, 12, 10, 8, 6 или 4 и величины удлинения 1, 2, 3, 4, 5 или 6.
"Сходными" последовательностями являются последовательности, которые при сравнении имеют идентичные и сходные аминокислотные остатки, где сходные остатки являются консервативными заменами соответствующих аминокислотных остатков при выравнивании ссылочной последовательности. В этом отношении "консервативная замена" остатка в эталонной последовательности является заменой остатком, который является физически или функционально сходным с соответствующим ссылочным остатком, например, который имеет сходные размер, форму, электрический заряд, химические свойства, в том числе способность образовывать ковалентные или водородные связи, или т.п. Таким образом, “модифицированная консервативной заменой” последовательность является последовательностью, которая отличается от эталонной последовательности или последовательности дикого типа тем, что присутствуют одна или несколько консервативных замен. “Процентное сходство” двух последовательностей является функцией числа положений, которые содержат совпадающие остатки или консервативные замены, общие у этих двух последовательностей, разделенного на число сравниваемых положений, х 100. Например, если 6 из 10 положений в двух последовательностях совпадают и 2 из 10 положений содержат консервативные замены, то эти две последовательности имеют 80% положительное сходство.
В контексте настоящей заявки термин "модификации консервативными последовательностями" обозначает аминокислотные модификации, которые не оказывают отрицательного влияния на свойства связывания или не изменяют свойства связывания антитела, содержащего эту аминокислотную последовательность. Такие модификации с консервативными заменами включают нуклеотидные и аминокислотные замены, добавления и делеции. Например, модификации могут быть введены стандартными способами, известными в данной области, такими как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены включают в себя замены, в которых аминокислотный остаток заменен аминокислотным остатком, имеющим сходную боковую цепь. Семейства аминокислотных остатков, имеющих сходные боковые цепи, были определены в данной области. Эти семейства включают в себя аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислотными боковыми цепями (например, аспарагиновую кислоту, глутаминовую кислоту), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, прогнозируемый не являющийся незаменимым аминокислотный остаток в антителе против VEGF человека, предпочтительно заменяют другим аминокислотным остатком того же самого семейства боковых цепей. Способы идентификации нуклеотидных и аминокислотных консервативных замен, которые не влияют на связывание с антигеном, хорошо известны в данной области (см., например, Brummell et al., Biochem. 32: 1180-1187 (1993); Kobayashi et al., Protein Eng. 12(10): 879-884 (1999) и Burks et al., Proc. Natl. Acad. Sci. USA 94: 412-417 (1997)).
"Аминокислотной консенсусной последовательностью" называют в контексте настоящей заявки аминокислотную последовательность, которая может быть получена с использованием матрицы из по меньшей мере двух и предпочтительно более выравненных аминокислотных последовательностей и допускает пропуски в этом сопоставлении, так чтобы можно было определить наиболее частый аминокислотный остаток в каждом положении. Консенсусной последовательностью является последовательность, которая содержит аминокислоты, которые наиболее часто присутствуют в каждом положении. В случае, когда две или более аминокислоты представлены одинаково в одном положении, эта консенсусная последовательность включает в себя обе или все эти аминокислоты.
Аминокислотную последовательность белка можно анализировать на различных уровнях. Например, консервативность или вариабельность может проявляться на уровне единственного остатка, на уровне множественных остатков, множественных остатков с пропусками и тому подобное. Остатки могут проявлять консервативность идентичного остатка или могут быть консервативными на уровне класса. Примеры классов аминокислот включают полярные, но не заряженные R-группы (серин, треонин, аспарагин и глутамин); положительно заряженные R-группы (лизин, аргинин и гистидин); отрицательно заряженные R-группы (глутаминовая кислота и аспарагиновая кислота); гидрофобные R-группы (аланин, изолейцин, лейцин, метионин, фенилаланин, триптофан, валин и тирозин) и особые аминокислоты (цистеин, глицин и пролин). Специалисту в данной области известны другие классы, и они могут быть определены с использованием структурных определений или других данных для оценки заменяемости. В этом смысле заменяемой аминокислотой может быть названа любая аминокислота, которая может быть заменена и может сохранять функциональную консервативность в этом положении.
Однако следует учитывать, что аминокислоты в одном и том же классе могут применяться по своим биофизическим свойствам. Например, понятно, что некоторые гидрофобные R-группы (например, аланин, серин или треонин) являются более гидрофильными (т.е. имеют более высокую гидрофильность или более низкую гидрофобность), чем другие гидрофобные R-группы (например, валин или лейцин). Относительная гидрофильность или гидрофобность может быть определена общепринятыми в данной области способами (см., например, Rose et al., Science, 229: 834-838 (1985) и Cornette et al., J. Mol Biol, 195: 659-685 (1987)).
В контексте настоящей заявки при сравнении одной аминокислотной последовательности (например, первой последовательности VH или VL) с одной или несколькими дополнительными аминокислотными последовательностями (например, одной или несколькими VH или VL в базе данных) положение аминокислоты в одной последовательности (например, первой последовательности VH или VL) может сравниваться с “соответствующим положением” в одной или нескольких дополнительных аминокислотных последовательностях. В контексте настоящей заявки "соответствующее положение" представляет эквивалентное положение в последовательности(ях), сравниваемых при оптимальном сопоставлении этих последовательностей, т.е. при сравнении этих последовательностей с достижением максимальной процентной идентичности или высочайшего процентного сходства.
В контексте настоящей заявки термин "база данных антител" относится к коллекции двух или более аминокислотных последовательностей антител ("множеству" последовательностей) и обычно относится к коллекции десятков, сотен или даже тысяч аминокислотных последовательностей. База данных последовательностей может хранить аминокислотные последовательности, например коллекции VH-районов антител, VL-районов антител или обоих или может хранить коллекцию scFv-последовательностей, содержащих VH- и VL-районы. Предпочтительно эта база данных хранит в доступной для поиска фиксированной среде, например в компьютере в доступной для поиска компьютерной программе. В одном из вариантов осуществления база данных антител является базой данных, содержащей последовательности антител эмбрионального типа или состоящей из последовательностей антител эмбрионального типа. В другом варианте осуществления база данных антител является базой данных, содержащей зрелые (т.е. экспрессируемые) последовательности антител или состоящей из зрелых (т.е. экспрессируемых) последовательностей антител (например, базой данных Кабата зрелых последовательностей антител, например базой данных KBD). Еще в одном из вариантов осуществления эта база данных содержит функционально выбранные последовательности или состоит из функционально выбранных последовательностей (например, последовательностей, выбранных на основе QC-анализа).
Термин "иммуносвязывающий агент" относится к молекуле, которая содержит весь антигенсвязывающий сайт или часть антигенсвязывающего сайта антитела, например весь вариабельный домен тяжелой цепи и/или легкой цепи или часть вариабельного домена тяжелой цепи и/или легкой цепи, так что этот иммуносвязывающий агент связывает антиген-мишень. Не ограничивающие примеры иммуносвязывающих агентов включают полноразмерные молекулы иммуноглобулинов и одноцепочечные scFv, а также фрагменты антител, включающие, но не ограничивающиеся ими, (i) Fab-фрагмент, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CHI; (ii) F(ab′)2-фрагмент, бивалентный фрагмент, содержащий два Fab-фрагмента, связанные дисульфидным мостиком в шарнирной области; (iii) Fab′-фрагмент, который по существу является Fab с частью шарнирного района (см. Fundamental Immunology (Paul ed., 3.sup.rd ed. 1993); (iv) Fd-фрагмент, состоящий из доменов VH и CH1; (v) Fv-фрагмент, состоящий из доменов VL и VH единственного плеча антитела, (vi) однодоменное антитело, такое как Dab-фрагмент (Ward et al., (1989) Nature 341: 544-546), который состоит из домена VH или VL, верблюда (см. Hamers-Casterman, et al., Nature 363: 446-448 (1993) и Dumoulin, et al., Protein Science 11: 500-515 (2002)) или антитело акулы (например, нанотела Ig-NAR акулы, Nanobodies®); и (vii) нанотело, район тяжелой цепи, содержащий вариабельный домен и два константных домена.
В контексте настоящей заявки термин "функциональное свойство" является свойством полипептида (например, иммуносвязывающего агента), в отношении которого является желательным и/или выгодным для специалиста в данной области улучшение (например, относительно общепринятого полипептида), например, для улучшения свойств приготовления или терапевтической эффективности этого полипептида. В одном из вариантов осуществления этим функциональным свойством является стабильность (например, термостабильность). В другом варианте осуществления этим функциональным свойством является растворимость (например, при клеточных условиях). Еще в одном из вариантов осуществления этим функциональным свойством является отсутствие агрегации. Еще в одном из вариантов осуществления этим функциональным свойством является экспрессия белка (например, в прокариотической клетке). Еще в одном из вариантов осуществления этим функциональным свойством является эффективность рефолдинга после солюбилизации тельца включения в соответствующем процессе очистки. В некоторых вариантах осуществления антигенсвязывающая активность не является функциональным свойством, которое желательно улучшить.
Термин "эпитоп" или "антигенная детерминанта" относится к сайту на антигене (например, на VEGF), с которым специфически связывается иммуноглобулин или антитело. Эпитоп обычно включает по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 последовательных или непоследовательных аминокислот в уникальной пространственной конформации. См., например, Epitope Mapping Protocols in Methods in Molecular Biology, Vol. 66, G.E. Morris, Ed. (1996).
Термины "специфическое связывание", "селективное связывание", "селективно связывается" и "специфически связывается" относятся к связыванию антитела с эпитопом на предварительно определенном антигене. Обычно, это антитело связывается с аффинностью (KD), приблизительно меньшей чем 10-7M, например меньшей чем приблизительно 10-8M, 10-9M или 10-10M или даже более низкой.
Термин "KD" или "Kd" относится к константе диссоциации в равновесном состоянии конкретного взаимодействия антитело-антиген. Обычно антитела по настоящему изобретению связываются с VEGF с константой диссоциации равновесного состояния (KD), меньшей чем приблизительно 10-7M, например меньшей чем приблизительно 10-8M, 10-9M или 10-10M, или даже более низкой, например, определенной технологией резонанса поверхностных плазмонов (SPR) в приборе BIACORE.
Термины "нейтрализует VEGF", "ингибирует VEGF" и "блокирует VEGF" используются взаимозаменяемо для обозначения способности антитела по настоящему изобретению препятствовать взаимодействию антитела по настоящему изобретению с одним или несколькими VEGF-рецепторами, такими как VEGFR-1 и/или VEGFR-2, и, например, запуску трансдукции сигнала.
"Рекомбинантный иммуносвязывающий агент" относится в контексте настоящей заявки к иммуносвязывающему агенту, продуцируемому экспрессией из рекомбинантной ДНК.
"Химерный" иммуносвязывающий агент в контексте настоящей заявки имеет часть тяжелой цепи и/или легкой цепи, идентичную соответствующей последовательности или гомологичную соответствующим последовательностям антитела, полученных из конкретного вида или принадлежащих к конкретному классу или подклассу антител, тогда как остальная часть цепи (цепей) является идентичной с соответствующими последовательностями или гомологичной соответствующим последовательностям в антителах, полученных из другого вида или принадлежащих другому классу или подклассу антител, а также фрагменты таких антител. Используемое в данном случае гуманизированное антитело является субпопуляцией химерных антител.
"Гуманизированные антитела" обозначают в контексте настоящей заявки иммуносвязывающие агенты, которые были синтезированы с использованием технологии рекомбинантных ДНК для исключения иммунной реакции на чужеродные антигены. Гуманизация является хорошо известным способом уменьшения иммуногенности моноклональных антител, полученных из ксеногенных источников. Она включает выбор акцепторного каркаса, предпочтительно акцепторного каркаса человека, степени CDR из донорского иммуносвязывающего агента, подлежащей встраиванию в этот акцепторный каркас и замены остатков из донорского каркаса в акцепторный каркас. Общий способ трансплантации CDR в акцепторные каркасы человека был описан Winter в патенте США 5225539, содержание которого включено в настоящее описание в качестве ссылки в полном объеме. В US 6407213, содержание которого включено в настоящее описание в качестве ссылки в полном объеме, раскрыт ряд аминокислотных положений этого каркаса, где замена из донорского иммуносвязывающего агента является предпочтительной.
Термин "молекулы нуклеиновой кислоты" относится к молекулам ДНК и молекулам РНК. Молекула нуклеиновой кислоты может быть одноцепочечной или двухцепочечной, но предпочтительно она является двухцепочечной ДНК. Нуклеиновая кислота является "функционально связанной", если она находится в функциональной взаимосвязи с другой последовательностью нуклеиновой кислоты. Например, промотор или энхансер функционально связан с кодирующей последовательностью, если он влияет на транскрипцию этой последовательности.
Термин "вектор" относится к молекуле нуклеиновой кислоты, способной транспортировать другую нуклеиновую кислоту, с которой она связана. Одним типом вектора является "плазмида", которая является кольцевой двухцепочечной ДНК-петлей, в которую могут быть лигированы дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, в котором дополнительные сегменты ДНК могут быть лигированы в вирусный геном. Некоторые векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, имеющие бактериальную точку начала репликации и эписомальные векторы млекопитающих). Другие векторы (например, неэписомные векторы млекопитающих) могут быть введены в геном клетки-хозяина и посредством этого реплицируются вместе с геномом хозяина.
Термин "клетка-хозяин" относится к клетке, в которую был введен экспрессирующий вектор. Клетки-хозяева могут включать в себя бактериальные, микробные клетки, клетки растений или клетки животных. Бактерии, которые восприимчивы к трансформации, включают в себя члены семейства Enterobacteriaceae, такие как штаммы Escherichia coli или Salmonella; Bacillaceae, такие как Bacillus subtilis; Pneumococcus; Streptococcus и Haemophilus influenzae. Подходящие микроорганизмы включают в себя Saccharomyces cerevisiae и Pichia pastoris. Подходящие линии клеток-хозяев животных включают в себя CHO (линии яичника китайского хомячка) и клетки NS0.
Термины "лечить", "лечение" или "терапия" относятся к терапевтическим или профилактическим мерам, описанным в настоящем описании. Способы "терапии" предусматривают введение больному антитела по настоящему изобретению, например больному с VEGF-опосредованным нарушением, или больному, который в конечном счете может приобрести такое нарушение, для профилактики, лечения, задержки, уменьшения тяжести или ослабления одного или нескольких симптомов этого нарушения или рецидива нарушения или для продления выживания индивида за пределы выживания, которые ожидались в отсутствие такого лечения.
Термин "VEGF-опосредованное нарушение" относится к любому нарушению, возникновению, прогрессированию или хроническим симптомам или состояниям заболевания, которое требует участия VEGF. Примеры VEGF-опосредованных нарушений включают, но не ограничиваются ими, возрастную дегенерацию желтого пятна, неоваскулярную глаукому, диабетическую ретинопатию, ретинопатию недоношенных, ретролентальную фиброплазию, карциномы молочной железы, карциномы легких, желудочные карциномы, эзофагеальные карциномы, колоректальные карциномы, карциномы печени, карциномы яичника, комы, арренобластомы, карциномы шейки матки, эндометриальную карциному, эндометриальную гиперплазию, эндометриоз, фибросаркомы, хориокарциному, рак головы и шеи, назофарингеальную карциному, карциномы гортани, гепатобластому, саркому Капоши, меланому, кожные карциномы, гемангиомы, кавернозную гемангиому, гемангиобластому, карциномы поджелудочной железы, ретинобластому, астроцитому, глиобластому, Шванному, олигодендроглиому, медуллобластому, нейробластомы, рабдомиосаркому, остеогенную саркому, лейомиосаркомы, карциномы мочеполовых путей, карциномы щитовидной железы, опухоль Вильмса, почечно-клеточную карциному, рак предстательной железы, аномальную пролиферацию сосудов, ассоциированную с факоматозом, эдему (например, ассоциированную с опухолями головного мозга), синдром Мейжа, ревматоидный артрит, псориаз и атеросклероз.
Термин "эффективная доза" или "эффективная дозировка" относится к количеству, достаточному для достижения или по меньшей мере для частичного достижения желаемого эффекта. Термин "терапевтически эффективная доза" определяется как количество, достаточное для излечения или по меньшей мере задержки этого заболевания и его осложнений в пациенте, уже страдающем от этого заболевания. Количества, эффективные для этого применения, будут зависеть от тяжести подлежащего лечению нарушения и общего состояния собственной иммунной системы пациента.
Термин "индивид" относится к любому человеку или животному (не человеку). Например, способы и композиции по настоящему изобретению могут быть использованы для лечения индивида с VEGF-опосредованным нарушением.
Термин "Min-трансплантат" или "min" относится в контексте настоящей заявки к гуманизированному вариабельному домену, который был получен трансплантацией кроличьих CDR из кроличьего вариабельного домена в природный акцепторный каркас человека (FW 1.4, SEQ ID NO: 172). В этих каркасных районах не проводят никаких изменений. Сам каркас предварительно выбран с точки зрения желаемых функциональных свойств (растворимости и стабильности).
Термин "Max-трансплантат" или "max" относится в контексте настоящей заявки к гуманизированному вариабельному домену, который был получен трансплантацией кроличьих CDRs из кроличьего вариабельного домена в "модифицированный консервативными кроличьими остатками” акцепторный каркас человека "RabTor" (rFW1.4, SEQ ID NO: 173), или в его производное, называемое rFW1.4 (v2) (SEQ ID NO: 174). Этот каркас "RabTor" получали включением консервативных кроличьих остатков (или же остатков, которые являются довольно вариабельными в других видах) в положениях каркаса, обычно участвующих в структуре и стабильности вариабельного домена кролика, с целью генерирования универсально применимого каркаса, который принимает фактически любой набор кроличьих CDR без необходимости трансплантации остатков донорского каркаса, других, чем остатки в положениях, которые являются различными в их предполагаемой последовательности-предшественнике, например, которые были изменены во время соматической гипермутации и, следовательно, возможно, влияют на связывание антигена. Определено, что эта предполагаемая последовательность-предшественник является самой близкой копией зародышевой линии кролика, и в случае, когда эта самая близкая копия зародышевой линии не может быть установлена, консенсусом кроличьей подгруппы или конс