Производные n-ациламинокислот для лечения таких патологий кожи, как целлюлит
Иллюстрации
Показать всеИзобретение относится к применению соединений
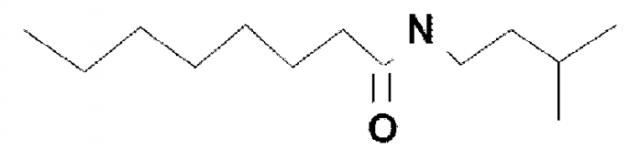
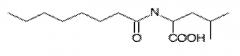
(N-изопентилоктанамид), (4-метил-2-(октаноиламино)пентановая кислота), или их фармацевтически приемлемых солей для получения композиции для лечения кожи млекопитающих для снижения количества подкожного жира или предотвращения накопления подкожного жира. Изобретение обеспечивает соединения с липолитической и антиадипогенной активностью, приемлемые для профилактики и лечения целлюлита. 4 н. и 8 з.п. ф-лы, 4 пр., 7 ил., 2 табл.
Реферат
По данной заявке испрашивается приоритет по предварительной заявке США №61/361179, поданной 2 июля 2010 года, которая включена в настоящее описание посредством ссылки во всей своей полноте.
Область техники, к которой относится изобретение
Изобретение относится к низкомолекулярным соединениям с биологической и терапевтической активностью. В частности, изобретение относится к низкомолекулярным соединениям с липолитической и антиадипогенной активностью. Двумя примерами таких молекул являются 4-метил-2-(октаноиламино)пентановая кислота и N-изопентилоктанамид. Изобретение дополнительно относится к способам профилактики или лечения таких патологий кожи, как целлюлит, с использованием низкомолекулярных соединений с липолитической и антиадипоцитогенной активностью.
Предпосылки создания изобретения
Целлюлит может появляться в результате накопления деградировавшей жировой ткани в коже. Один или несколько факторов, способствующих данному нарушению, включают недостаточное артериальное или венозное кровообращение, гормональные нарушения и проблемы с лимфообращением. Предпосылкой, лежащей в основе появления целлюлита, является повышенное накопление жира в адипоцитах кожи. Становясь существенно нагруженными жиром (липиды в форме триглицеридов), адипоциты увеличиваются в объеме и становятся гипертрофированными, иногда до высокой степени. Компрессия кровяных и лимфатических сосудов жировыми массами, возникшая в результате гипертрофии, вызывает недостаточность оттока жидкости и застой токсинов в коже. Отек и разрушение соединительной ткани, возникающие в результате данных условий, приводят к неравномерно испещренному внешнему виду, который характеризует целлюлит.
Одним из достижений производства продуктов по уходу за кожей является разработка малых (менее чем 500 ММ) молекул, способных проникать через кожу, которые могут стимулировать разрушение жировых отложений при целлюлите и других патологиях кожи. Было показано, что октановая кислота, свободная жирная кислота, которую также обозначают как октаноат или каприловая кислота, участвует в организме в процессах самомодуляции метаболизма липидов в адипоцитах (2000, Guo et al., Biochem. J. 349:463-471; 2002, Han et al., J. Nutr. 132:904-910; 2004, Lei et al., Obesity Res. 12:599-610; 2006, Guo et al., Nutr. Metab. (Lond.) 3:30; опубликованная патентная заявка США No. 2005/0019372), и, таким образом, является кандидатом для создания лекарственного средства для лечения целлюлита. Октановую кислоту естественным образом обнаруживают в молоке и некоторых жирах растительного происхождения (например, кокосовом и пальмовом маслах) и широко используют в качестве пищевой добавки для широкого спектра назначений, включая противогрибковую активность. Кроме своей липолитической активности, октановая кислота также поглощается адипоцитами и вместе с глицерином и другими жирными кислотами используется для синтеза триглицеридов (фиг.1).
Другие соединения, помимо октановой кислоты, о которых известно, что они способны регулировать метаболизм липидов в адипоцитах, преимущественно накапливаются из лекарственных средств для системного введения, разработанных для различных патологий сердца и дыхания. Такие средства включают изопротеренол (бета-адренергический агонист), аминофиллин (ингибитор фосфодиэстеразы) и теофиллин (ингибитор фосфодиэстеразы, по структуре сходный с кофеином). Данные молекулы вводят с помощью инъекции как часть схемы лечения при мезотерапии или используют местно для уменьшения жировых отложений при таких патологиях, как целлюлит. Улучшения доступности данных молекул для применения в производстве продуктов по уходу за кожей потребует получения соединений, которые (i) относятся к безрецептурным лекарственным средствам, (ii) природного происхождения, (iii) обладают свойствами хорошего проникновения через кожу и (iv) обладают повышенной липолитической активностью по сравнению с липолитической активностью других доступных в настоящий момент молекул.
Сущность изобретения
Вариант осуществления настоящего изобретения можно отнести к способу лечения кожи млекопитающих, включающему введение композиции на кожу млекопитающего. Композиция может содержать фармацевтически приемлемый носитель и фармацевтически эффективное количество соединения или его фармацевтически приемлемой соли. В свою очередь, соединение может быть представлено формулой R1-C(O)-NH-R2, где R1 содержит цепь, включающую 5-35 атомов углерода, фрагмент формулы R1-C(O) представляет собой ацильную группу жирных кислот, и R2 содержит органическую группу.
В определенных вариантах осуществления настоящего изобретения фрагмент NH-R2 формулы R1-C(O)-NH-R2 может содержать аминокислоту. В этом случае, группа R2 содержит альфа-углерод, карбоксильную группу и боковую группу в виде аминокислоты; группа NH соединена с альфа-углеродным атомом аминокислоты. В других вариантах осуществления настоящего изобретения фрагмент NH-R2 формулы R1-C(O)-NH-R2 может содержать аналог аминокислоты, в этом случае аналог отличается от аминокислоты отсутствием карбоксильной группы, присоединенной к альфа-углероду аминокислоты. В этом случае, группа R2 содержит альфа-углеродный атом и боковую группу в виде аминокислоты; группа NH присоединена к альфа-углеродному атому аналога аминокислоты. Боковая группа в виде аминокислоты или аналога аминокислоты может быть гидрофобной. Аминокислотами в данных вариантах осуществления (либо свободная аминокислота, или указанный выше аналог) могут быть лейцин, изолейцин, валин или аланин.
В определенных вариантах осуществления указанного выше способа применяют соединения, содержащие или состоящие из формулы:
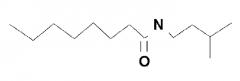
N-изопентилоктанамид
Для осуществления других конкретных вариантов осуществления указанного выше способа применяют соединение, содержащее или состоящее из формулы:
4-метил-2-(октаноиламино)пентановая кислота
В варианте осуществления с 4-метил-2-(октаноиламино)пентановой кислотой, очевидно, что группа R2 представляет собой лейцин, тогда как группа R2 в варианте осуществления с N-изопентилоктанамидом представляет собой лейцин без карбоксильной группы. Варианты осуществления дополнительно включают фармацевтически приемлемые соли указанных соединений.
В определенных вариантах осуществления настоящего изобретения цепь группы R1 из формулы R1-C(O)-NH-R2 может содержать 7-21 атомов углерода. В этих и других вариантах осуществления, где длина цепи R1 составляет 7 атомов углерода, ацильная группа жирных кислот R1-C(O)- может представлять собой октаноильную группу. Эти и другие варианты осуществления изобретения могут содержать группу R2, которая содержит 2-15 атомов углерода; так, группа R2 может необязательно состоять из атомов углерода и водорода. Однако в других вариантах осуществления изобретения R2 может содержать 5-9 атомов углерода, и группа R1 может содержать 5-13 атомов углерода. Ацильная группа жирных кислот в одном или нескольких вариантах осуществления изобретения может быть насыщенной или ненасыщенной.
Композиция для применения в определенных вариантах осуществления указанного выше способа может быть в форме аэрозоля, эмульсии, жидкости, лосьона, крема, пасты, мази, порошка или пены. В дополнение к содержанию соединения формулы R1-C(O)-NH-R2, композиция может дополнительно содержать карнитин, ресвератрол, изопротеренол, аминофилин, теофиллин, кофеин или любое другое соединение, способствующее липолизу, или соединение, ингибирующее липогенез.
В определенных вариантах осуществления указанного выше способа соединение можно наносить на кожу поверх подкожного слоя, где распределение жира является патологическим по сравнению с его нормальным распределением под кожей. В других вариантах осуществления соединение можно наносить на кожу поверх подкожного слоя, который вызывает склонность к распределению жира, являющемуся патологическим по сравнению с его нормальным распределением под кожей. Конкретные варианты осуществления настоящего изобретения включают применение соединения для кожи с целлюлитом или для кожи, склонной к развитию целлюлита.
Варианты осуществления изобретения также относятся к способу увеличения продукции глицерина клетками, включающему контакт указанной клетки с соединением формулы R1-C(O)-NH-R2, где R1 содержит цепь с 5-35 атомами углерода, фрагмент формулы R1-C(O) представляет собой разветвленную ацильную группу, и R2 содержит органическую группу. В определенных вариантах осуществления клетка, являющаяся мишенью в данном способе, представляет собой адипоцит или адипоцит, запасаемый подкожной жировкой тканью. С помощью конкретных вариантов осуществления соединения способствуют метаболизированию клеткой молекул триглицеридов, запасаемых в клетке, до глицерина и жирных кислот.
Варианты осуществления настоящего изобретения также относятся к способу уменьшения адипогенеза, который подразумевает контакт указанной клетки с соединением формулы R1-C(O)-NH-R2, где R1 содержит цепь с 5-35 атомами углерода, фрагмент формулы R1-C(O) представляет собой разветвленную ацильную группу, и R2 содержит органическую группу. В определенных вариантах осуществления клетка, являющаяся мишенью в данном способе, представляет собой адипоцит или предшественник адипоцита, или адипоцит или предшественник адипоцита, запасаемые подкожной жировкой тканью. С помощью конкретных вариантов осуществления соединение способствует снижению запасания клеткой липидов (например, адипоцитом или предшественником адипоцита). Уменьшение запасания липидов может вызывать снижение содержания липидов в цитоплазме.
Краткое описание фигур
На фиг.1 представлены метаболические процессы липогенеза и липолиза. Изображенные жирные кислоты представляют собой молекулы гексановой кислоты.
На фиг.2 представлены химические формулы для (A) 4-метил-2-(октаноиламино)пентановой кислоты и (B) N-изопентилоктанамида. Для каждого из соединений дополнительно указаны структурная и основная молекулярная формулы, а также молекулярная масса (ММ).
На фиг.3 представлены конкретные пути передачи сигнала в адипоцитах, лежащие в основе (A) липогенеза и (B) липолиза. LDL, липопротеины низкой плотности; VLDL, липопротеины очень низкой плотности; TG, триглицериды; FFA, свободные жирные кислоты; HSL, гормоночувствительная липаза; AQP7, аквапорин-7.
На фиг.4 представлена относительная продукция свободных жирных кислот в адипоцитах 3T3-L1, которые в течение ночи подвергали инкубированию с 100 мкг/мл карнитина, ресвератрола, изопротеренола, аминофиллина, теофиллина, кофеина, 4-метил-2-(октаноиламино)пентановой кислоты (HB2031) или N-изопентилоктанамид (HB2032). Для контрольного образца использовали забуференный фосфатном солевой раствор (PBS).
На фиг.5 представлена относительная продукция свободных жирных кислот в адипоцитах 3T3-L1, которые в течение ночи подвергали инкубированию с 100 мкг/мл изопротеренола, 4-метил-2-(октаноиламино)пентановой кислоты (HB2031) или N-изопентилоктанамида (HB2032). Для контрольного образца использовали PBS.
На фиг.6 представлена антиадипогенная активность N-изопентилоктанамида (HB2032). A) предшественники адипоцитов 3T3-L1 выращивали в полной среде без добавления соединений, вызывающих адипогенез. B) стимулировали полную дифференцировку предшественников адипоцитов 3T3-L1 до адипоцитов после девяти суток стимулирования с помощью индукторов адипогенеза. C) Клетки обрабатывали 100 мкг/мл HB2032 в присутствии индукторов адипогенеза в течение девяти суток. D) Клетки обрабатывали 150 мкг/мл HB2032 в присутствии индукторов адипогенеза в течение девяти суток. E) Клетки обрабатывали 200 мкг/мл HB2032 в присутствии индукторов адипогенеза в течение девяти суток. Клетки окрашивали масляным красным на содержание липидов. Представленные изображения получены с помощью стереомикроскопа.
На фиг.7 представлены эффекты 100 мкг/мл 4-метил-2-(октаноиламино)пентановой кислоты (HB2031) и N-изопентилоктанамида (HB2032) на жизнеспособность кожи с использованием модели кожи EpiDerm™ (MatTek, MA) в сочетании с модифицированным анализом MTT, после инкубационных периодов в 2, 5 и 18 часов. В качестве контроля использовали обработку глицерином.
Подробное описание изобретения
Настоящее изобретение обеспечивает соединения, жирные амиды, в частности, для модулирования адипоцитов с помощью стимуляции процессов липолиза. Примерами таких соединений являются 4-метил-2-(октаноиламино)пентановая кислота (фиг.2A) и N-изопентилоктанамид (фиг.2B), молекулярная масса каждого из которых составляет менее чем 300 ММ, и которые вызывают более выраженный распад триглицеридов в адипоцитах, по сравнению с доступными в настоящее время молекулами, такими как изопротеренол, аминофиллин и теофиллин. Описываемые в настоящем описании соединения не являются токсичными по отношению к клеткам кожи. Свойства данных соединений, наряду с их липидизацией, которая влияет на их способность проникать через кожу, делают эти соединения особенно пригодными для профилактики и лечения негативных эффектов аномального отложения жира в коже (например, целлюлита и стрий). Такое положительное воздействие на кожу по настоящему изобретению также связано с увеличением уровня глицерина в коже, которое улучшает состояние кожи.
Примером соединения по настоящему изобретению является 4-метил-2-(октаноиламино)пентановая кислота. Данное соединение альтернативно обозначают как, например, 4-метил-2-(каприлоиламино)валериановую кислоту, 4-метил-2-(октаноиламино)валериановую кислоту или 4-метил-2-(каприлоиламино)валериановую кислоту. Номенклатура для данной молекулы основана на присутствии октаноиламиногруппы в положении 2 атома углерода (в положении 1 находится атом углерода карбоксильной группы) пентановой кислоты и метильной группы в положении 4 атома углерода пентановой кислоты. Соединения, содержащие или состоящие из 4-метил-2-(октаноиламино)пентановой кислоты, можно использовать по настоящему изобретению.
Другим примером соединения по настоящему изобретению является N-изопентилоктанамид. Данное соединение альтернативно обозначают, например, как N-изоамилооктанамид, N-изопентилкаприламид или N-изоамилкаприламид. Соединения, содержащие или состоящие из N-изопентилоктанамида, можно использовать по настоящему изобретению.
Примеры соединений, которые можно использовать по настоящему изобретению, имеют или представлены химической формулой
R1-CO-NH-R2.
Соединения 4-метил-2-(октаноиламино)пентановая кислота и N-изопентилоктанамид соответствуют данной формуле.
В данной области хорошо известно, что компонент R1-CO- формулы R1-CO-NH-R2 можно получать, например, из жирной кислоты. Специалистам в данной области понятно, что R1-CO- можно получать из жирной кислоты (ЖК), R1 может содержать гидрокарбоновую цепь (например, алкан, алкен, алкин или различные вариации цепей ЖК, как описано в настоящем описании), и -CO- можно получать из карбоксильной группы, конденсированной с фрагментом -NH-R2. Компонент R1-CO- в данном случае может содержать или состоять из ацильной группы жирных кислот. R1 может быть представлен в виде алифатической группы, содержащей только углерод и водород, или может дополнительно содержать другие атомы, такие как, например, кислород и азот. Примеры насыщенных жирных кислот (т.е., где R1 представляет собой алкан), которые можно использовать для обеспечения компонента R1-CO- соединений по изобретению, имеют общую формулу CH3(CH2)nCOOH и перечислены в таблице 1.
| Таблица 1Насыщенные жирные кислоты | ||
| Систематическое название | Тривиальное название | Сокращенное обозначение |
| бутановая кислота | масляная кислота | 4:0 |
| пентановая кислота | валериановая кислота | 5:0 |
| гексановая кислота | капроновая кислота | 6:0 |
| октановая кислота | каприловая кислота | 8:0 |
| нонановая кислота | пеларгоновая кислота | 9:0 |
| декановая кислота | каприловая кислота | 10:0 |
| додекановая кислота | лауриновая кислота | 12:0 |
| тетрадекановая кислота | миристиновая кислота | 14:0 |
| гексадекановая кислота | пальмитиновая кислота | 16:0 |
| гептадекановая кислота | маргариновая (стеариновая) кислота | 17:0 |
| октадекановая кислота | стеариновая кислота | 18:0 |
| эйкозановая кислота | арахиновая кислота | 20:0 |
| докозановая кислота | бегеновая кислота | 22:0 |
| тетракозановая кислота | лигноцериновая кислота | 24:0 |
| церотиновая кислота | церотиновая кислота | 26:0 |
| гептакозановая кислота | карбоцериновая кислота | 27:0 |
| октакозановая кислота | монтановая кислота | 28:0 |
| триаконтановая кислота | мелиссиновая кислота | 30:0 |
| дотриаконтановая кислота | лацериновая кислота | 32:0 |
| тритриаконтановая кислота | псилластеариловая кислота | 33:0 |
| тетратриаконтановая кислота | геддовая кислота | 34:0 |
| пентатриаконтановая кислота | церопластическая кислота | 35:0 |
Длина углеводородной цепи жирной кислоты или ацильной группы жирных кислот (т.е. R1-CO-) (важно, что атом углерода карбоксильной группы считается одним из углеродов в цепи) равна или превышает 4 атома углерода. В примерах жирных кислот/ацильных групп жирных кислот, пригодных для обеспечения и/или описания изобретения, длина цепи составляет 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или 40 атомов углерода. Таким образом, отсюда следует, что длина цепи R1 может составлять 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38 или 39 атомов углерода. В определенных вариантах осуществления длина цепи ацильной группы жирных кислот составляет 6-36, 8-16, 8-18, 8-20, 8-22 или 8-24 атомов углерода; таким образом, длина R1 для данных вариантов осуществления составляет 5-35, 7-15, 7-17, 7-19, 7-21 или 7-23 атомов углерода, соответственно. Другие жирные кислоты/ацильные группы жирных кислот, полезные согласно изобретению, обладают длинами цепей, с четным или нечетным числом атомов углерода. Жирные кислоты или ацильные группы жирных кислот с короткой, средней или длинной цепями можно использовать для получения вариантов осуществления настоящего изобретения. Жирные кислоты со средней длиной цепи, как правило, имеют от 8 (или 6) до 10 (или 12) атомов углерода, тогда как жирные кислоты с длинной цепью, как правило, имеют от 14 (или 12) и более атомов углерода. Незаменимые жирные кислоты и жирные кислоты, не являющиеся незаменимыми, также являются частью изобретения, а также жирные кислоты, полученные естественным образом или искусственно синтезированные.
Специалистам в данной области известно, что соответствующая ацильная группа жирных кислот для любой жирной кислоты; например, ацильная группа жирных кислот для жирной кислоты CH3(CH2)6COOH (октановая кислота) представляет собой CH3(CH2)6CO- (октаноильная группа) (R1=7). Таким образом, раскрытие в настоящем описании, относящееся к жирным кислотам, также относится к соответствующим ацильным группам жирных кислот. Примерами ацильных групп жирных кислот являются бутаноил, пентаноил, гексаноил, гептаноил, октаноил, наноил, деканоил, додеканоил, татрадеканоил, гексадеканоил, гептадеканоил, октадеканоил, эйкозаноил, докозаноил, татракозаноил, гексакозаноил, гептакозаноил, октакозаноил и триаконтаноил.
Жирные кислоты, полезные для применения по изобретению, могут включать насыщенные жирные кислоты (т.е. алкановая цепь без двойных связей между атомами углеродов цепи и с максимальным количеством атомов водорода) и ненасыщенные жирные кислоты (т.е. алекеновая или алкиновая цепь, по меньшей мере, с одной двойной и/или тройной связью между атомами углеродов цепи, соответственно). Примерами ненасыщенных жирных кислот являются мононенасыщенные (MUFA), если в цепи присутствует только одна двойная связь, полиеноевые (или полиненасыщенные жирные кислоты, PUFA), если в цепи присутствуют две или более двойных связей (например, с заместителем в виде метилена, полиметилена, сопряженных диенов, алленовых кислот, кумуленовых кислот), и ацетиленовые, если в цепи содержится тройная связь. Другие примеры ненасыщенных жирных кислот представляют собой омега-3 (n-3), омега-6 (n-6) и омега-9 (n-9) жирные кислоты. Примеры ненасыщенных жирных кислот (т.е. R1 представляет собой алкен или алкин), которые можно использовать для обеспечения компонента R1-CO- соединений по изобретению перечислены в таблице 2.
| Таблица 2Ненасыщенные жирные кислоты | ||
| Систематическое название | Тривиальное название | Сокращенное обозначение |
| 9-цис-тетрадеценовая кислота | миристоленовая кислота | 14:1 (n-5) |
| 9-цис-гексадеценовая кислота | пальмитолеиновая кислота | 16:1 (n-7) |
| 6-цис-гексадеценовая кислота | сапиеновая кислота | 16:1 (n-10) |
| цис-7,10,13-гексадецетриеновая кислота | 16:3 (n-3) | |
| 9-цис-октадециленовая кислота | олеиновая кислота | 18:1 (n-9) |
| цис-9,12-октадекадиеновая кислота | линолевая кислота | 18:2 (n-6) |
| цис-9,11-октадекадиеновая кислота | сопряженная линолевая кислота | 18:2 (n-6) |
| цис-9,12,15 октадекадиеновая кислота | α-линоленовая кислота (ALA) | 18:3 (n-3) |
| цис-6,9,12-октадекадиеновая кислота | γ-линоленовая кислота (GLA) | 18:3 (n-6) |
| цис-6,9,12,15-октадекадиеновая кислота | стеаридоновая кислота (SDA) | 18:4 (n-3) |
| цис-11,14,17-эйкозатетраеновая кислота | эйкозатетраеновая кислота (ETE) | 20:3 (n-3) |
| цис-8,11,14-эйкозатетраеновая кислота | дигомо-7-линоленовая кислота (DGLA) | 20:3 (n-6) |
| цис-5,8,11,14-эйкозатетраеновая кислота | арахидоновая кислота | 20:4 (n-6) |
| цис-8,11,14,17-эйкозатетраеновая кислота | эйкозатетраеновая кислота (ETA) | 20:4 (n-3) |
| цис-5,8,11,14,17-эйкозатетраеновая кислота | эйкозапентаеновая кислота (EPA) | 20:5 (n-3) |
| (Z)-докоз-13-еноевая кислота | эруковая кислота | 22:1 (n-9) |
| цис-7,10,13,16,19-докозапентаеновая кислота | докозапентаеновая кислота (DPA), | 22:5 (n-3) |
| цис-4,7,10,13,16,19-докозагексаеновая кислота | докозагексаеновая кислота (DHA) | 22:6 (n-3) |
| цис-9,12,15,18,21-докозагексаеновая кислота | тетракозапентаеновая кислота | 24:5 (n-3) |
| цис-6,9,12,15,18,21-тетракозеновая кислота | тетракозагексаеновая кислота (низиновая кислота) | 24:6 (n-3) |
Другие менее распространенные типы жирных кислот можно использовать для получения соединений по изобретению, включая кислоты с другими типами групп в углеводородной цепи вместо метила. Примерами групп в составе цепи кроме метильной являются простой эфир, карбоксильная группа, кетон, сложный эфир и альдегидная группы. Другие примеры менее распространенных жирных кислот представляют собой кислоты с цепями, содержащими разветвленные группы, помимо водорода. Примерами альтернативных жирных кислот, которые можно использовать по изобретению, являются гидроксижирные кислоты, дикарбоновые кислоты, карбонаты жирных кислот, дивиниловые эфиры жирных кислот, серосодержащие жирные кислоты, амиды жирных кислот, метокси и ацетокси-жирные кислоты, кето-жирные кислоты, альдегидные жирные кислоты, галогенированные жирные кислоты (например, F, Cl, Br), нитрированные жирные кислоты, жирные кислоты с разветвленными цепями, жирные кислоты с моно- или полиразветвленными цепями, разветвленные метокси жирные кислоты, разветвленные гидрокси жирные кислоты (например, миколовая кислота), жирные кислоты, содержащие циклические структуры, циклопропановые кислоты, циклобутановые кислоты (например, ladderanes), циклопентиловые кислоты, фурановые кислоты, циклогексиловые и гексениловые кислоты, фениловые и бензойные алкановые кислоты, эпоксикислоты, циклические жирные пероксиды и липоевая кислота.
Наряду с тем, что соединения по настоящему изобретению можно получать с использованием жирных кислот, описываемых в настоящем описании, другие структуры для получения соединений совершенно очевидны специалистам в данной области. Таким образом, в случае, если настоящее изобретение описывает компонент R1-CO- формулы R1-CO-NH-R2 в терминах жирных кислот и продукции из них, данное изобретение, по существу, не ограничивает синтезируемые из жирных кислот соединения. Тогда как другие способы синтеза, используемые для получения соединений по изобретению, также пригодны и доступны для описания компонента R1-CO- в отношении свойств его жирной кислоты или ацильной группы жирных кислот.
В данной области хорошо известно, что компонент R1-CO-NH- формулы R1-CO-NH-R2 можно получать из или описывать, например, в качестве амида жирной кислоты (называемый также алкиламидом). Амид жирной кислоты можно получать путем конденсации жирной кислоты, как описано в настоящем описании, с амином (например, с аммиаком, первичным амином, вторичным амином). Примеры амидов жирных кислот, которые можно использовать для обеспечения компонента R1-CO-NH- формулы R1-CO-NH-R2 являются, таким образом, очевидными, учитывая описанные примеры жирных кислот. Неограничивающий список амидов жирных кислот включает пентанамид (валериановый амид), гексанамид (капроновый амид), октанамид (каприловый амид), нонанамид (пеларгоновый амид), деканамид (каприновый амид), додеканамид (лауриновый амид), тетрадеканамид (миристиновый амид), пальмитиновый амид, арахидоновый амид, бегеновый амид, стеариновый амид, олеиновый амид, эруковый амид и ретиноламид.
Аминокислоты и их производные можно использовать для получения фрагмента -NH-R2 формулы R1-CO-NH-R2 соединения по изобретению. Примерами аминокислот, которые можно использовать как в L-, так и в D-формах, являются, аланин, аргинин, аспарагин, аспарагиновая кислота, цистеин, глутамин, глутаминовая кислота, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин и валин. Другими примерами аминокислот являются норлейцин, норвалин, альфа-аминооктаноат, бета-метилфенилаланин, альфа-аминофенилацетат, орнитин, таурин, карнитин, γ-аминомасляная кислота (GABA), L-DOPA (L-3,4-дигидроксифенилаланин), гидроксипролин, селенометионин и селеноцистеин. Аминокислоты с центральным атомом углерода (альфа-углерод, Cα), присоединенным к аминогруппе, карбоксильной группе и боковой группе (R). Общая структурная формула свободной аминокислоты приведена ниже:
Специалистам в данной области понятно, что аминогруппа, присоединенная к альфа-углероду аминокислоты, может быть использована для обеспечения фрагмента -NH формулы R1-CO-NH-R2, в этом случае, R2 будет содержать или состоять из альфа-углерода, боковой группы и карбоксильной группы аминокислоты. Примером соединения формулы R1-CO-NH-R2 с его фрагментом -NH-R2, полученным из аминокислоты, может являться 4-метил-2-(октаноиламино)пентановая кислота
В данном примере фрагмент -NH-R2 может быть получен из лейцина. Альтернативно, специалистам в данной области также понятно, что аминогруппу, в том состоянии, в котором она находится в боковых группах конкретной аминокислоты (например, аргинин, аспарагин, глутамин, лизин, гистидин, пролин, триптофан), можно использовать для обеспечения фрагмента -NH формулы R1-CO-NH-R2, где R2 содержит или состоит из альфа-углерода, карбоксильной группы, аминогруппы и остальных боковых групп аминокислоты.
Производные аминокислоты включают производные соли и производные без аминогруппы или карбоксильной группы, присоединенные к альфа-углероду. Другими примерами являются аминокислоты с модифицированной боковой группой, такой как этерифицированная или амидированная группа. Примером соединения формулы R1-CO-NH-R2 с ее фрагментом -NH-R2, полученным из аналога аминокислоты, может являться N-изопентилоктанамид
В данном примере фрагмент -NH-R2 может быть получен из лейцина без карбоксильной (COOH) группы, которая, иными словами, присоединена к альфа-углероду.
Боковая группа аминокислоты или производного аминокислоты, откуда фрагмент -NH-R2 формулы R1-CO-NH-R2 может быть получен или, иными словами, с ними схож, могут быть заряжены положительно, заряжены отрицательно, полярными, полярными незаряженными, неполярными, гидрофобными, кислыми, основными, алифатическими или нейтральными.
В данной области хорошо известно, как можно получать соединения по настоящему изобретению. Например, способы синтеза могут включать конденсацию или присоединение жирной кислоты (например, кислоты, описываемой в настоящем описании) к аминокислоте или соединению, связанному с аминокислотой. В публикации патентной заявки США № 2008/0200704, включенной в настоящее описание посредством ссылки во всей своей полноте, описан пример органического синтеза такого типа. Специалистам в данной области также очевидны описываемые ниже способы (примеры), касающиеся синтеза 4-метил-2-(октаноиламино)пентановой кислоты и N-изопентилоктанамида, которые можно применять для получения других соединений для осуществления изобретения.
Следует считать очевидным, что в случае, если настоящее изобретение относится к фрагментам формулы, полученным из аминокислоты или любой другой части или группы, то данное раскрытие относится к обоим продуктам, которые были произведены с использованием указанной аминокислоты, группы или фрагмента, а также к продуктам, полученным из других компонентов. В последних примерах, полезно сослаться на конечный продукт в отношении его групп, на основании из сходства или соответствия конкретным химическим группам, таким как аминокислоты.
Фрагмент -NH-R2 формулы R1-CO-NH-R2 можно считать кэпом, кэпирующей группой или блокирующей группой в отношении ацильной группы жирных кислот R1-CO-. В этом случае, фрагмент -NH-R2 предотвращает взаимодействие ацильной группы жирных кислот со спиртовой группой (R-OH) с образованием сложного эфира. Так как ацильная группа связана с амидом, его карбоксильный углерод не подвергнут или менее подвергнут нуклеофильной атаке электрофила, такого как спирт.
Примеры соединений, которые можно использовать по настоящему изобретению частично или полностью липофильны (гидрофобны) с молекулярной массой до 200, 250, 300, приблизительно 350, 400, 450, 500, 550 или 600. Как правило, липофильность соединений, по большей части, обеспечивается группой R1. Данные соединения по изобретению, которые являются частично липофильными, могут быть поляризованы таким образом, что группа R1 обладает гидрофобными свойствами, и группа R2, необязательно в сочетании с промежуточным кором -CO-NH-, приобретает некоторые свойства гидрофильности. Соединения по настоящему изобретению и/или их R1 или R2 компоненты могут быть липофильными или гидрофобными приблизительно на 100%, 95%, 90%, 85%, 80%, 75%, 70%, 65%, 60%, 55%, 50%, 45%, 40%, 35% или 30%.
Другими примерами согласно настоящему изобретению являются соединения формулы R1-CO-NH-R2, раскрытые в настоящем описании и обладающие одинаковой активностью (например, липолитической активностью) как 4-метил-2-(октаноиламино)пентановая кислота или N-изопентилоктанамид, или активность любого из данных соединений составляет, по меньшей мере, приблизительно 10%, 20%, 30%, 40%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 90%, 95%, 96%, 97%, 98% или 99%.
Все из вариантов осуществления соединений по изобретению могут быть в "изолированном" состоянии. Например, под "изолированным" соединением понимают состояние полного или частичного очищения. В некоторых случаях, изолированное соединение будет являться частью более крупной композиции, буферной системы или смеси реактивов. В остальных случаях, изолированное соединение может быть очищено до гомогенности. Композиция может содержать соединение на уровне, по меньшей мере, приблизительно 50, 80, 90 или 95% (на основании молярности или массы) от всех других видов, которые также присутствуют в ней. Смеси описанных соединений можно использовать для осуществления способов по изобретению.
Дополнительные варианты осуществления настоящего изобретения направлены на способы применения соединений, описываемых в настоящем описании, например, в составах или в качестве терапевтических средств. Способы могут включать применение отдельных соединений или сложных соединений в комбинации (т.е. смесей). Таким образом, конкретные варианты осуществления изобретения используют в качестве лекарственных средств, содержащих соединения, описываемые в настоящем описании, и способы производства данных лекарственных средств.
В конкретных примерах композицию по изобретению можно наносить на устройства, помещаемые поверх кожи или под кожей. Данные устройства включают трансдермальные лоскуты, имплантаты и инъекции (например, мезотерапия), которые способствуют высвобождению субстанций таким образом, чтобы они контактировали с кожей или волосяным фолликулом с помощью пассивных или активных механизмов высвобождения. Субстанции можно применять, например, местно на эпидермис через равные промежутки времени, такие как один или два раза в день, с подходящим носителем и в эффективной концентрации. Одна или несколько инъекций в кожу представляет другой путь введения пептидов по изобретению в кожу или любую другую ткань.
Композиции, используемые для доставки соединений в способах, описываемых в настоящем описании, могут быть в форме аэрозоля, эмульсии, раствора, лосьона, крема, пасты, мази, порошка, пены или другом фармацевтически приемлемом составе. Кроме того, соединения могут быть доставлены с использованием менее распространенных составов, таких как деионизированная/дистиллированная вода, PBS или в растворе стандартного медицинского физиологического раствора.
Как правило, фармацевтически приемлемый состав будет включать любой носитель, пригодный для применения на коже человека или на слизистых поверхностях. Подобные фармацевтически приемлемые носители включают этанол, диметилсульфоксид, глицерин, диоксид кремния, оксид алюминия, крахмал, и эквивалентные носители и растворители. Необязательно, состав может быть с косметическими средствами и/или содержать другие соединения, такие как ретиноиды или другие пептиды, которые могут действовать в качестве адъювантов для терапевтического действия пептидов по настоящему изобретению. Антибиотики также можно добавлять в состав с целью предотвращения инфекции, тем самым, позволяя протекать максимально-интенсивному процессу заживления. Терапевтические и/или косметические пептиды можно использовать в сочетании с соединениями настоящего изобретения. Концентрация соединения(й) в настоящей композиции может составлять приблизительно от 0,1 мкг/мл до приблизительно 50 мкг/мл или приблизительно от 0,1 мкг/мл до приблизительно 100 мкг/мл; однако, конечная концентрация для применения может варьировать за пределы этих диапазонов, в зависимости от природы ткани-мишени, биоактивности пептидов настоящего изобретения и использования любых адъювантов или способов достижения лучшей абсорбции композиции. Подобные показатели хорошо известны специалистам в данной области. Например, концентрация соединения(ий) для применения на практике по настоящему изобретению может составлять приблизительно 0,1, 1, 2, 5, 10, 15, 20, 25, 50, 75, 100, 200, 500 или 1000 мкг/мл.
Введение соединений по изобретению и связанных с ними композиций может быть осуществлено в отношении людей и животных, включая всех млекопитающих (например, свиней, коров, лошадей, овец, коз, мышей, крыс, кошек, собак, хорьков, приматов). Применение также м