Способ получения этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата
Иллюстрации
Показать всеПредлагаемое изобретение относится к химии производных изоксазолов, в частности к способу получения этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата, который представляет интерес в качестве полупродуктов в синтезе биологически активных веществ. Способ получения 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата осуществляют конденсацией солянокислого гидроксиламина с предварительно полученным производным ацетоуксусного эфира в спиртовой среде с последующим выделением полученного продукта. В качестве производного ацетоуксусного эфира используют предварительно полученный ацилированием натриевого енолята ацетоуксусного эфира хлорангидридом 3-феноксибензойной кислоты этил 3-оксо-2-(3-феноксибензоил)бутаноат, конденсацию ведут в среде этилового спирта при температуре 80°С в течение 2 часов, а продукт выделяют фильтрацией. Технический результат - получение этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата в мякгих условиях с хорошим выходом и высокой степенью чистоты. 1 пр.
Реферат
Предлагаемое изобретение относится к химии производных изоксазолов, в частности к способу получения этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата, который является новым по структуре 3-феноксифенилсодержащим соединением и может представлять интерес в качестве полупродуктов в синтезе биологически активных веществ.
Известен способ получения производных изоксазола конденсацией β-дикетонов с гидрохлоридом гидроксиламина в пиридине. В результате были получены 3-замещенные-5-(2-гидроксифенил)изоксазолы с выходами 76-81%. [Vijey Aanandhi Muthukumar, Sujatha Ramasamy, Sharmila Alladi, Journal of Pharmacy Research 2011, 4(12), 4654-4657].
Недостатком данного метода являются сложности с выделением продукта, а именно: продукт кристаллизуется в течение суток, после чего требует дополнительной очистки на хроматографической колонке.
Данным методом невозможно получить вещества заявляемой структурной формулы.
Известен способ получения 4-(адамантил)-3,5-дизамещенного изоксазолов взаимодействием α-(1-адамантил)-β-дикарбонильных соединений, предварительно полученных реакцией комплекса β-дикарбонильных соединений с ионами Co (II) и 1-бром адамантаном, с гидрохлоридом гидроксиламина в присутствии эквимолярного количества гидроокиси натрия в водно-спиртовой среде в течение 2 часов [A. Gonzalez, J. Marquet, M. Moreno-Manas. Tetrahedron, 42, 4253 (1986)].
Однако данный способ из-за использования гидроокиси натрия в водно-спиртовой среде невозможно применить для синтеза этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата, так как возможен гидролиз сложноэфирной группы.
Наиболее близким является способ получения метил 5-(2-метилфенил)изоксазол-4-карбоксилата через ряд последовательных реакций на основе 2-метилацетофенона, в результате чего был получен сначала метил (2Z)-3-(диметиламино)-2-(2-метилбензоил)акрилат, который далее взаимодействует с гидрохлоридом гидроксиламина в метаноле в течение 18 часов [Пат. RU 2480467, МПК C07D 413/06, А61К 31/454, А61Р 27/06. Опубл. 27.04.2013].
Недостатками данного метода являются длительное время синтеза, использование метанола в качестве растворителя.
Задачей предлагаемого изобретения является разработка технологичного способа синтеза этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата.
Техническим результатом является расширение ассортимента химических соединений, в частности получение нового этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата с хорошим выходом и высокой степенью чистоты.
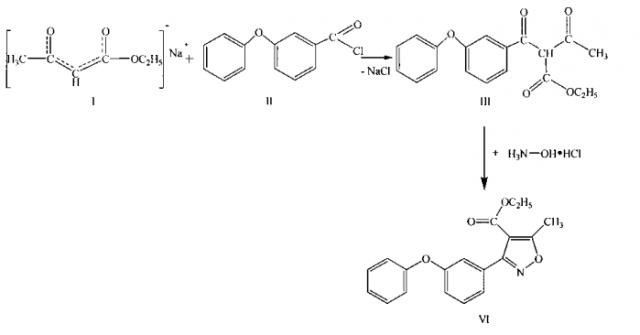
Поставленный технический результат достигается в способе получения 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата конденсацией солянокислого гидроксиламина с предварительно полученным производным ацетоуксусного эфира в спиртовой среде с последующим выделением полученного продукта, при этом в качестве производного ацетоуксусного эфира используют предварительно полученный ацилированием натриевого енолята ацетоуксусного эфира хлорангидридом 3-феноксибензойной кислоты этил 3-оксо-2-(3-феноксибензоил)бутаноат, конденсацию ведут в среде этилового спирта при температуре 80°C в течение 2 часов, а продукт выделяют фильтрацией.
Сущностью способа является конденсация этил 3-оксо-2-(3-феноксибензоил)бутаноата (III), предварительно полученного ацилированием натриевого енолята ацетоуксусного эфира хлорангидридом 3-феноксибензойной кислоты, с гидроксиламином в среде этилового спирта без выделения этил 3-оксо-2-(3-феноксибензоил)бутаноата.
Реакцию хлорангидрида 3-феноксибензойной кислоты с ацетоуксусным эфиром и с металлическим натрием проводят при температуре -10 до 25°C при существенном отсутствии воды, а именно в абсолютном диэтиловом эфире. В результате взаимодействия натриевого енолята ацетоуксусного эфира с хлорангидридом 3-феноксибензойной кислоты образуется этил 3-оксо-2-(3-феноксибензоил)бутаноат, который является обнаруживаемым в реакционном растворе и при необходимости может быть выделен. Для дальнейшего процесса выделение этил 3-оксо-2-(3-феноксибензоил)бутаноата не требуется. Перед последующим взаимодействием реакционную смесь фильтруют при сниженном давлении, в результате чего удаляют из нее хлорид натрия и диэтиловый эфир.
После этого проводят конденсацию солянокислого гидроксиламина с полученным этил 3-оксо-2-(3-феноксибензоил)бутаноатом в спиртовом растворе бинуклеофила (солянокислый гидроксиламин). Реакцию ведут при температуре 80°C в течение 2 часов. После этого выпавший в осадок продукт выделяют фильтрованием, а его очистку осуществляют перекристаллизацией из ацетона.
Несмотря на возможность взаимодействия бинуклеофила с тремя карбонильными атомами углерода (1-3), обнаружено, что конденсация этил 3-оксо-2-(3-феноксибензоил)бутаноата с фенилгидразином протекает по 1 и 2 атомам углерода.
Пример 1. Этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилат.
В круглодонную трехгорлую колбу, оборудованную капельной воронкой, механической мешалкой, обратным холодильником с хлоркальциевой трубкой, помещали 100 мл абсолютного эфира и 0,6 г (26 ммоль) натрия. Колбу помещали в баню со льдом и по каплям при перемешивании приливали 3,5 г (27 ммоль) ацетоуксусного эфира, после чего интенсивно перемешивали в течение 2 часов. К полученному натриевому еноляту ацетоуксусного эфира (I) при перемешивании прибавляли по каплям раствор 5,8 г (25 ммоль) хлорангидрида 3-феноксибензойной кислоты (II) в 50 мл абсолютного эфира. Смесь перемешивали в течение 3 часов. Перед последующим взаимодействием реакционную смесь фильтровали при сниженном давлении на фильтре Шотта, в результате чего удаляли из нее хлорид натрия и диэтиловый эфир.
Во вторую четырехгорлую колбу на 100 мл, снабженную эффективной механической мешалкой и обратным холодильником, помещали 1,75 г (25 ммоль) солянокислого гидроксиламина, 25 мл этилового спирта и полученный ранее этил 3-оксо-2-(3-феноксибензоил)бутаноат (III). Реакционную массу при постоянном перемешивании нагревали до 80°C и выдерживали при этой температуре в течение двух часов для более полного взаимодействия. При этом реакционная масса приобретает бурый цвет. По окончании реакции реакционную массу охлаждали до комнатной температуры, продукт отфильтровывали, промывали 95%-ным этиловым спиртом. Для дополнительной очистки этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилат перекристаллизовывают из дихлорэтана. Продукт - белые игольчатые кристаллы. Выход - 6,5 г (20 ммоль, 81%). Т.пл. 115-117°C.
Спектр ЯМР 1Η, δ, м.д.: 7,10-7,51 м (9Н, C6H5OC6H4); 4,18 т (H, -CH2-O), 2,48 т (H, -CH3), 1,32 с (Н, -CH3).
Хроматомасс-спектр, m/z (I, %): 323 (100) [M]+, чистота 98%.
Таким образом, предлагаемое техническое решение позволяет получить и выделить этил 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилат простым и удобным в исполнении способом в мягких условиях с хорошим выходом и высокой степенью чистоты.
Способ получения 5-метил-3-(3-феноксифенил)изоксазол-4-карбоксилата конденсацией солянокислого гидроксиламина с предварительно полученным производным ацетоуксусного эфира в спиртовой среде с последующим выделением полученного продукта, отличающийся тем, что в качестве производного ацетоуксусного эфира используют предварительно полученный ацилированием натриевого енолята ацетоуксусного эфира хлорангидридом 3-феноксибензойной кислоты этил 3-оксо-2-(3-феноксибензоил)бутаноат, конденсацию ведут в среде этилового спирта при температуре 80°С в течение 2 часов, а продукт выделяют фильтрацией.