Эндопротезы, имеющие покрытие активным соединением
Иллюстрации
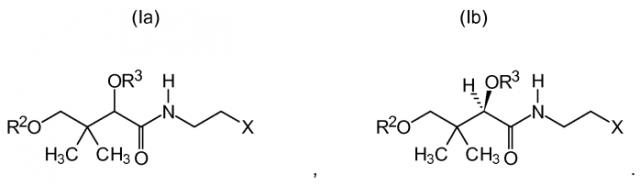
Показать всеГруппа изобретений относится к медицине, конкретно к эндопротезу с лекарственным покрытием, которое содержит или состоит по меньшей мере из одного антибиотика и по меньшей мере из одного соединения общей формулы:
а также их солей. Покрытие эндопротезов обеспечивает отсутствие осложнений в ходе лечения и длительное применение. 2 н. и 6 з.п. ф-лы, 6 ил., 12 табл., 49 пр.
Реферат
Настоящее изобретение относится к эндопротезам, имеющим покрытие активным агентом, которое содержит или состоит из по меньшей мере одного антибиотика и по меньшей мере одного дополнительного соединения, соответствующего одной из указанных ниже общих формул
Эндопротезы представляют собой имплантаты, которые находятся в организме постоянно или в течение длительного периода и заменяют поврежденную часть тела полностью или частично. Требования к таким заменяющим или вспомогательным элементам очень высокие, и, в зависимости от условий зоны имплантации, они значительно различаются. Существуют отличия между медицинскими, функциональными, пластиковыми эндопротезами, а также зубными имплантатами. К имплантатам относятся водители сердечного ритма, стенты и сосудистые трансплантаты, имплантаты для глубокой стимуляции мозга, так называемые водители ритма мозговой активности, используемые, например, при болезни Паркинсона, искусственные сердца и портальные катетеры, ортопедические имплантаты, например, для замены суставов, или материалы, применяемые для хирургического лечения переломов костей, офтальмологические имплантаты, такие как хрусталик глаза, имплантаты сетчатки, стекловидного тела, роговицы, зубные имплантаты, материалы для реконструкции черепа, костного замещения, протезы полового члена, сфинктерные протезы, кохлеарные имплантаты, а также съемные средства для функциональной поддержки, используемые в течение ограниченного периода, такие как катетеры, например, мочевые катетеры, сердечные катетеры, дыхательные трубки, венозные катетеры, канюли, а также имплантаты, которые применяют только в качестве депо активных веществ.
Производимые из биосовместимых материалов эндопротезы могут значительно различаться по материалу и внешнему виду, в зависимости от локализации применения, и могут состоять, например, из металла, металлических сплавов, пластмасс или полимеров, таких как PEAK (полиарилэфиркетоны), PEEK (полиэфирэфиркетон), PEK (полиэфиркетон), PEEEK, PEEKEK и PEKK, из керамических материалов, а также из их комбинаций. В зависимости от композиции материала, локализации применения эндопротезов и ревизии эндопротезов, с учетом частоты их хирургического применения, они могут быть биоустойчивыми, биоразлагаемыми, биоинертными или биологически активными и иметь шероховатую или гладкую, микропористую или макропористую, гидрофильную или гидрофобную поверхность с нанесенным покрытием или предварительно обработанную любым другим способом. Для покрытия имеет значение форма элемента, на который наносится покрытие, а также материал этого элемента, поскольку разные способы покрытия могут быть обусловлены геометрическими параметрами. В изобретении приведены такие способы, как покрытие погружением, напылением, накапыванием (нанесением пипеткой), электропрядением и т.д., а также комбинации из возможных способов, с помощью которых можно достичь оптимального подхода для высокого качества покрытия, и, таким образом, положительного влияния на терапевтическую эффективность и успешное применение покрытия.
Оптимально эффективное покрытие поверхности эндопротеза должно увеличивать запланированный ресурс работы эндопротеза или, по меньшей мере, увеличивать необходимое время пребывания в организме, и такое покрытие должно предотвращать ревизию протеза, которая может быть необходимой, несмотря на оптимальную подгонку протеза и отсутствие осложнений при его введении. С помощью покрытия должна осуществляться адаптация имплантата к окружающим тканям, покрытие должно способствовать процессу заживления без осложнений, содействовать принятию инородного тела в организме и предотвращать или уменьшать потенциальные посторонние факторы, которые могут препятствовать и предотвращать процесс заживления.
Например, ортопедические имплантаты, такие как протезы, используемые в костной системе, например, протез тазобедренного сустава или протез коленного сустава, должны входить в прочную и немедленную связь с принимающей костью. Эту связь можно улучшать путем нанесения на поверхность биологически активного слоя, например, гидроксиапатита, или слоя других подходящих покрытий с фосфатом кальция, который представляет собой важный минеральный компонент костной ткани. Один из примеров дальнейших разработок в области таких покрытий для костных имплантатов известен под торговым наименованием покрытия Palacos R+G Heraeus, которое состоит из смеси костного цемента высокой вязкости и гентамицина сульфата. Но даже в этом случае всегда существуют проблемы восприятия имплантата костью организма, поэтому это покрытие является эффективным лишь отчасти, так как вымывание активного агента из матрицы происходит без адаптации дозы, и матрица, не содержащая активный агент, становится неадекватной для дальнейшего процесса заживления и использования эндопротеза в течение длительного времени. Таким образом, желаемая цель не достигается, поскольку результаты остаются неудовлетворительными даже при уменьшении частоты ревизий при использовании Palacos R+G.
В других областях применения, например, в имплантатах хрусталика глаза или на поверхности просвета пищеводных стентов, требуется гладкая, гидрофильная, и также предпочтительно кислотоустойчивая поверхность. Оптимизация таких протезов путем нанесения покрытий представляет собой очень широкое поле деятельности; разработки в этой области, которые должны соответствовать типу заболевания, локализации заболевания, заданным условиям и, конечно, состоянию пациента, еще далеки от завершения и постоянно сталкиваются с отдельными трудностями.
Таким образом, можно утверждать, что, несмотря на наличие большого количества вариантов покрытий эндопротезов, применяемые во всех зонах локализации эндопротезы вызывают постоянные проблемы, которые не могут улучшать качество жизни пациентов и приводят к ревизии имплантата. Причины осложнений разнообразны и их примерно можно разделить на две группы:
1. Хирургическая техника, дефектные материалы, конструктивные проблемы общего характера, а также обусловленные встречающимися индивидуальными биологическими различиями и т.д.
2. В целом неблагоприятные явления адаптации различного происхождения, абразивные изменения кости или хряща, воспаление, бактериальное обсеменение, реакции иммунной системы на инородные тела.
Выявлена неэффективность покрытия эндопротезов чистыми антибиотиками без добавок или без матрицы, поскольку, во-первых, антибиотик растворяется за короткое время, а во-вторых, с веществом невозможно изготовить слой, обладающий адгезивностью к эндопротезу, так как покрытие имеет порошкообразный, сухой, крошащийся и рассыпчатый вид. Следовательно, невозможно понять, какое количество антибиотика достигает целевой локализации и может быть эффективным. В этих условиях терапевтический эффект и заключение об эффективности эндопротеза с покрытием ставится под сомнение в связи с отсутствием точности и воспроизводимости минимального высвобождаемого количества. Наличие этих недостатков не может соответствовать разнообразным необходимым условиям в зоне имплантации и ни при каких условиях не может гарантировать адекватный, оптимальный и беспроблемный процесс заживления. Фиг.4а и 4b показывают крошащуюся поверхность эндопротеза, покрытого гентамицина сульфатом путем напыления. Фиг.4а и 4b отчетливо показывают нежесткое, крошащееся, хрупкое покрытие гентамицина сульфатом, при этом гентамицина сульфат непрочно прилипает к поверхности медицинского устройства и, следовательно, покрытие легко отслаивается и является совершенно непригодным для получения медицинского устройства с покрытием, которое отвечает требованиям к медицинской продукции, требованиям к ее хранению, стерилизации и одобрения регулирующих органов.
К сожалению, покрытие эндопротезов, изготовленное из гентамицина сульфата и пальмитиновой кислоты, представляющей собой длинноцепочечную ненасыщенную жирную кислоту (С16:0), показывает неконтролируемое высвобождение гентамицина пальмитата in vitro и высокие начальные показатели вымываемой концентрации без видимой задержки высвобождения. Дополнительно, высвобождается только до 58% гентамицина сульфата, что также вызывает недостаточный терапевтический эффект. При этом гентамицина сульфат образует непрочное и крошащееся покрытие, которое отслаивается уже при стерилизации и упаковке медицинского устройства с покрытием, а с другой стороны, зоны с покрытием способны к такой прочной адгезии с поверхностью имплантата, что высвобождение гентамицина из этих зон практически не происходит, так что в конечном счете получаемый уровень высвобождения гентамицина только слегка превышает 50%. Таким образом, покрытие гентамицина сульфатом не подходит для нанесения и высвобождения антибиотика гентамицина с поверхности медицинского устройства. Кроме того, несмотря на более хорошую адгезию или даже по этой причине, в дополнение к недостаточному высвобождению антибиотика, в особенности антибиотика в пальмитатной матрице на эндопротезе, проблемой также является токсичность пальмитиновой кислоты в виде обнаруженной цитотоксичности пальмитиновой кислоты, и, следовательно, ее непригодность в качестве оптимальной матрицы для антибиотика. Другая проблема заключается в способности пальмитиновой кислоты препятствовать дальнейшему ходу заживления, что особенно заметно в отношении костных имплантатов, так как перемещение, или диффузия и скорость диффузии веществ в окружающую среду отличаются, в особенности по сравнению с имплантатом в содержащей жидкость среде.
Задачей настоящего изобретения является создание покрытых эндопротезов, которые после имплантации не имеют известных недостатков, или эти недостатки в значительной степени уменьшены, и при этом упомянутые эндопротезы отвечают минимально необходимым требованиям, предъявляемым к эндопротезам для гарантии отсутствия осложнений в ходе лечения и беспроблемного длительного применения. Эта задача решается с помощью технических предписаний независимых пунктов формулы настоящего изобретения. Другие предпочтительные варианты осуществления изобретения следуют из зависимых пунктов формулы изобретения, из описания и примеров.
Было обнаружено, что вышеупомянутые недостатки, которые возникают после имплантации эндопротеза, и в частности, имплантата, контактирующего с костной тканью, могут быть предотвращены или могут быть уменьшены путем покрытия эндопротеза активным агентом, содержащим или состоящим по меньшей мере из одного антибиотика и по меньшей мере из одного соединения общей формулы (Ia) и/или (Ib).
и/или
где Х представляет собой -СООН, -COOR1, -CH2OH, -CH2OR1,
R2 и R3 независимо друг от друга представляют собой -COOR4, -COOR5, -COR4, -COR5, -R4, -R5, -Н;
R1, R4 и R5 независимо друг от друга представляют собой следующие соединения: -CH3, -C2H5, -C3H7, -CH(CH3)2, -C4H9, -CH2-CH(CH3)2, -CH(CH3)-C2H5, -C(CH3)3, -C5H11, -CH(CH3)-C3H7, -CH2-CH(CH3)-C2H5, -CH(CH3)-CH(CH3)2, -C(CH3)2-C2H5, -CH2-C(CH3)3, -CH(C2H5)2, -C2H4-CH(CH3)2, -C6H13, -C3H6-CH(CH3)2, -C2H4-CH(CH3)-C2H5, -CH(CH3)-C4H9, -CH2-CH(CH3)-C3H7, -CH(CH3)-CH2-CH(CH3)2, -CH(CH3)-CH(CH3)-C2H5, -CH2-CH(CH3)-CH(CH3)2, -CH2-C(CH3)2-C2H5, -C(CH3)2-C3H7, -C(CH3)2-CH(CH3)2, -CH(CH3)-C(CH3)3, -C7H15, -C3H6-C(CH3)3, -C4H8-CH(CH3)2, -C8H17, -C4H8-C(CH3)3, -C5H10-CH(CH3)2, -C9H19, -C5H10-C(CH3)3, -C6H12-CH(CH3)2, -C10H21, -C6H12-C(CH3)3 и -C7H14-CH(CH3)2, -CH=CH2, -CH2-CH=CH2, -C(CH3)=CH2, -CH=CH-CH3, -C2H4-CH=CH2, -CH2-CH=CH-CH3, -CH=CH-C2H5, -CH2-C(CH3)=CH2, -CH(CH3)-CH=CH, -CH=C(CH3)2, -C(CH3)=CH-CH3, -CH=CH-CH=CH2, -C3H6-CH=CH2, -C2H4-CH=CH-CH3, -CH2-CH=CH-C2H5, -CH=CH-C3H7, -CH2-CH=CH-CH=CH2, -CH=CH-CH=CH-CH3, -CH=CH-CH2-CH=CH2, -C(CH3)=CH-CH=CH2, -CH=C(CH3)-CH=CH2, -CH=CH-C(CH3)=CH2, -C2H4-C(CH3)=CH2, -CH2-CH(CH3)-CH=CH2, -CH(CH3)-CH2-CH=CH2, -CH2-CH=C(CH3)2, -CH2-C(CH3)=CH-CH3, -CH(CH3)-CH=CH-CH3, -CH=CH-CH(CH3)2, -CH=C(CH3)-C2H5, -C(CH3)=CH-C2H5, -C(CH3)=C(CH3)2, -C(CH3)2-CH=CH2, -CH(CH3)-C(CH3)=CH2, -C(CH3)=CH-CH=CH2, -CH=C(CH3)-CH=CH2, -CH=CH-C(CH3)=CH2, -C4H8-CH=CH2, -C3H6-CH=CH-CH3, -C2H4-CH=CH-C2H5, -CH2-CH=CH-C3H7, -CH=CH-C4H9, -C3H6-C(CH3)=CH2, -C2H4-CH(CH3)-CH=CH2, -CH2-CH(CH3)-CH2-CH=CH2, -CH(CH3)-C2H4-CH=CH2, -C2H4-CH=C(CH3)2, -C2H4-C(CH3)=CH-CH3, -CH2-CH(CH3)-CH=CH-CH3, -CH(CH3)-CH2-CH=CH-CH3, -CH2-CH=CH-CH(CH3)2, -CH2-CH=C(CH3)-C2H5, -CH2-C(CH3)=CH-C2H5, -CH(CH3)-CH=CH-C2H5, -CH=CH-CH2-CH(CH3)2, -CH=CH-CH(CH3)-C2H5, -CH=C(CH3)-C3H7, -C(CH3)=CH-C3H7, -CH2-CH(CH3)-C(CH3)=CH2, -CH(CH3)-CH2-C(CH3)=CH2, -CH(CH3)-CH(CH3)-CH=CH2, -CH2-C(CH3)2-CH=CH2, -C(CH3)2-CH2-CH=CH2, -CH2-C(CH3)=C(CH3)2, -CH(CH3)-CH=C(CH3)2, -C(CH3)2-CH=CH-CH3, -CH(CH3)-C(CH3)=CH-CH3, -CH=C(CH3)-CH(CH3)2, -C(CH3)=CH-CH(CH3)2, -C(CH3)=C(CH3)-C2H5, -CH=CH-C(CH3)3, -C(CH3)2-C(CH3)=CH2, -CH(C2H5)-C(CH3)=CH2, -C(CH3)(C2H5)-CH=CH2, -CH(CH3)-C(C2H5)=CH2, -CH2-C(C3H7)=CH2, -CH2-C(C2H5)=CH-CH3, -CH(C2H5)-CH=CH-CH3, -C(C4H9)=CH2, -C(C3H7)=CH-CH3, -C(C2H5)=CH-C2H5, -C(C2H5)=C(CH3)2, -C[C(CH3)3]=CH2, -C[CH(CH3)(C2H5)]=CH2, -C[CH2-CH(CH3)2]=CH2, -C2H4-CH=CH-CH=CH2, -CH2-CH=CH-CH2-CH=CH2, -CH=CH-C2H4-CH=CH2, -CH2-CH=CH-CH=CH-CH3, -CH=CH-CH2-CH=CH-CH3, -CH=CH-CH=CH-C2H5, -CH2-CH=CH-C(CH3)=CH2, -CH2-CH=C(CH3)-CH=CH2, -CH2-C(CH3)=CH-CH=CH2, -CH(CH3)-CH=CH-CH=CH2, -CH=CH-CH2-C(CH3)=CH2, -CH=CH-CH(CH3)-CH=CH2, -CH=C(CH3)-CH2-CH=CH2, -C(CH3)=CH-CH2-CH=CH2, -CH=CH-CH=C(CH3)2, -CH=CH-C(CH3)=CH-CH3, -CH=C(CH3)-CH=CH-CH3, -C(CH3)=CH-CH=CH-CH3, -CH=C(CH3)-C(CH3)=CH2, -C(CH3)=CH-C(CH3)=CH2, -C(CH3)=C(CH3)-CH=CH2, -CH=CH-CH=CH-CH=CH2, -C5H10-CH=CH2, -C4H8-CH=CH-CH3, -C3H6-CH=C(CH3)2, -C6H12-CH=CH2, -C5H10-CH=CH-CH3, -C4H8-CH=C(CH3)2, -C7H12-CH=CH2, -C6H12-CH=CH-CH3, -C5H10-CH=C(CH3)2, -C8H14-CH=CH2, -C7H14-CH=CH-CH3 и -C6H12-CH=C(CH3)2, -C≡CH, -C≡C-CH3, -CH2-C≡CH, -C2H4-C≡CH, -CH2-C≡C-CH3, -C≡C-C2H5, -C3H6-C≡CH, -C2H4-C≡C-CH3, -CH2-C≡C-C2H5, -C≡C-C3H7, -CH(CH3)-C≡CH, -CH2-CH(CH3)-C≡CH, -CH(CH3)-CH2-C≡CH, -CH(CH3)-C≡C-CH3, -C4H8-C≡CH, -C3H6-C≡C-CH3, -C2H4-C≡C-C2H5, -CH2-C≡C-C3H7, -C≡C-C4H9, -C2H4-CH(CH3)-C≡CH, -CH2-CH(CH3)-CH2-C≡CH, -CH(CH3)-C2H4-C≡CH, -CH2-CH(CH3)-C≡C-CH3, -CH(CH3)-CH2-C≡C-CH3, -CH(CH3)-C≡C-C2H5, -CH2-C≡C-CH(CH3)2, -C≡C-CH(CH3)-C2H5, -C≡C-CH2-CH(CH3)2, -C≡C-C(CH3)3, -CH(C2H5)-C≡C-CH3, -C(CH3)2-C≡C-CH3, -CH(C2H5)-CH2-C≡CH, -CH2-CH(C2H5)-C≡CH, -C(CH3)2-CH2-C≡CH, -CH2-C(CH3)2-C≡CH, -CH(CH3)-CH(CH3)-C≡CH, -CH(C3H7)-C≡CH, -C(CH3)(C2H5)-C≡CH, -C≡C-C≡CH, -CH2-C≡C-C≡CH, -C≡C-C≡C-CH3, -CH(C≡CH)2, -C2H4-C≡C-C≡CH, -CH2-C≡C-CH2-C≡CH, -C≡C-C2H4-C≡CH, -CH2-C≡C-C≡C-CH3, -C≡C-CH2-C≡C-CH3, -C≡C-C≡C-C2H5, -C≡C-CH(CH3)-C≡CH, -CH(CH3)-C≡C-C≡CH, -CH(C≡CH)-CH2-C≡CH, -C(C≡CH)2-CH3, -CH2-CH(C≡CH)2, -CH(C≡CH)-C≡C-CH3, -C≡C-C5H11, -C4H8-C≡C-CH3, -C5H10-C≡CH, -C≡C-C6H13, -C5H10-C≡C-CH3, -C6H12-C≡CH, -C≡C-C7H15, -C6H12-C≡C-CH3, -C7H14-C≡CH, -C≡C-C8H17, -C7H14-C≡C-CH3 и -C8H16-C≡CH,
а также солей, гидратов, сольватов, энантиомеров, диастереомеров, рацематов, смесей энантиомеров и смесей диастереомеров вышеупомянутых соединений.
Неожиданно было обнаружено, что покрытие по изобретению, содержащее по меньшей мере один антибиотик и по меньшей мере одно соединение общей формулы (Ia) и/или (Ib), характеризуется предпочтительной кинетикой элюирования. Антибиотик высвобождается из покрытия быстро и полностью. Дополнительно, покрытие характеризуется пониженной хрупкостью и ломкостью и более хорошей адгезией к эндопротезу, и при этом показывает полное высвобождение, таким образом, значительно снижается риск отслойки покрытия при транспортировке, хранении, стерилизации или во время имплантации.
Предпочтительные соединения
Выявлено, что особенно предпочтительными являются покрытия, содержащие или состоящие из по меньшей мере одного антибиотика и по меньшей мере одного соединения, соответствующего одной из следующих общих формул:
в которых значения R1, R2 и R3 соответствуют указанным выше значениям.
Более предпочтительным является покрытие, содержащее или состоящие из антибиотика и декспантенола или пантотеновой кислоты, а также пантоевой кислоты или пантокаина и/или их производных, таких как формиат, ацетат, пропионат, этиловый сложный эфир или этиловый эфир. Особенно предпочтительным является также покрытие, содержащее или, предпочтительно, состоящее из по меньшей мере одного аминогликозидного антибиотика с пантотеновой кислотой или декспантенолом или с их вышеупомянутыми производными.
Пантотеновая кислота ((R)-N-(2,4-дигидрокси-3,3-диметил-1-оксобутил)-β-аланин) представляет собой витамин из группы витаминов В (витамин B5), который поглощается из пищи и играет важную роль в обмене веществ в качестве компонента коэнзима А ацилтрансферазы. Пантотеновую кислоту в основном можно найти в качестве компонента средств по уходу за волосами и средств против угрей. Пантотеновая кислота может быть представлена одной из следующих формул:
Декспантенол (также называемый пантотенолом, пантенолом, D-пантенолом) имеет систематическое название (+)-(R)-2,4-дигидрокси-N-(3-гидроксипропил)-3,3-диметил-бутанамид и следующую структурную формулу
и давно используется в качестве средства против заболеваний кожи и слизистых оболочек и в косметических продуктах, поскольку обладает противозудным, противовоспалительным, ранозаживляющим эффектом, способствует образованию клеток и хорошо всасывается кожей в виде добавки в водно-масляные эмульсии, при этом накапливается в месте нанесения, и благодаря своим гидрофильным свойствам, увеличивает способность кожи удерживать влагу и улучшает эластичность кожи, а также обладает питательными свойствами и содействует регенерации клеток кожи, тем самым способствуя регенерации. Таким образом, к пантенол-содержащим продуктам относятся ранозаживляющие препараты для местного применения, такие как гели для лечения ожогов и ран, мази для лечения ран, глазные и назальные мази, назальные спреи, венозные мази, гели для полости рта, мази для лечения геморроя, препараты против угрей, кремы для ухода за сухой воспаленной кожей. Декспантенол также содержится в пастилках от боли в горле и в растворах для инъекций.
Для организма в целом декспантенол применяется в качестве компонента витаминных препаратов в виде капсул, таблеток и растворов для инъекций. Дексапантенол также используется в чистящих средствах для контактных линз. Декспантенол превращается в организме в пантотеновую кислоту (витамин B5), которая является предпочтительной в качестве компонента покрытия, и в этой связи его также можно применять для покрытия протезов.
Перечень антибиотиков, которые можно использовать в покрытии согласно изобретению, содержит, среди прочего, следующие: пенициллин, пенициллин G и V, амикацин, амоксициллин, ампициллин, бакампициллин, карбенициллин, инданил пивмециллинам, оксациллин, флуклоксациллин, аминопенициллин, аминокумарин, азитромицин, мезлоциллин, пиперациллин, азлоциллин, темоциллин, тикарциллин, амоксициллин, клавулановая кислота, ампициллин, сульбактам, пиперациллин, тазобактам, сульбактам, цефалоспорины, цефазолин, цефамандол, цефотиам, цефуроксим, цефменоксим, цефодизим, цефоперазон, цефотаксим, цефтазидим, цефсулодин, цефтриаксон, цефепим, цефпиром, цефокситин, цефотетан, цефаклор, цефадроксил, цефалексин, цефуроксимаксетил, цефиксим, цефподоксим, цефтибутен, хлоргексидин, имипенем, грамицидин, канамицин, цетромицин, нарбомицин, телитромицин, линкомицин, меропенем, эртапенем, дорипенем, азтреонам, джозамицин, эритромицин, рокситромицин, кларитромицин, спирамицин, полимиксин B, азитромицин, телитромицин, квинопристин, дальфопристин, клиндамицин, тетрациклин, окситетрациклин, доксициклин, миноциклин, триметоприм, тиротрицин, сульфаметоксазол, сульфаметрол, нитрофурантоин, ломефлоксацин, норфлоксацин, ципрофлоксацин, офлоксацин, флероксацин, левофлоксацин, офлоксацин, эноксацин, фосмидомицин, спарфлоксацин, метициллин, тинидазол, моксифлоксацин, ванкомицин, тейкопланин, линезолид, даптомицин, рифампицин, фузидиевая кислота, фосфомицин, трометамол, хлорамфеникол, метронидазол, колистин, мупироцин, бацитрацин, неомицин, нетилмицин, тигециклин, сульфасалазин, сульфадиазин, сульфадоксин, флуконазол, итраконазол, вориконазол, позаконазол, пириметамин, триметоприм, амфотерицин В, 5-флюцитозин, каспофунгин и/или анидулафунгин.
Особенно предпочтительными являются ингибиторы синтеза клеточной стенки, такие как имипенем, меропенем, эртапенем, азтреонам, пенициллин, аминопенициллины, ациламинопенициллины, изоксазолпенициллины, цефалоспорины, султамициллин, фосфомицин, гликопептиды, такие как ванкомицин и тейкопланин, полипептиды, такие как бацитрацин, колистин, грамицидин, полимиксин В, тиротрицин, и ингибиторы синтеза белка на рибосоме, такие как антибиотики из группы аминогликозидов, также называемые аминогликозидными антибиотиками. Группа аминогликозидов, которые являются особенно предпочтительными для покрытия по изобретению, содержит или состоит из следующих: стрептомицин, неомицин, фрамицетин, паромомицин, рибостамицин, канамицин, амикацин, арбекацин, беканамицин, дибекацин, тобрамицин, спектиномицин, гигромицин В, паромомицина сульфат, гентамицин, нетилмицин, сизомицин, изепамицин, вердамицин, астромицин, апрамицин, ансамицины, такие как рифампицин, генетицин. Особенно предпочтительным аминогликозидом является гентамицин (смесь типов), а также все отдельные соединения, принадлежащие к группе гентамицинов, например, гентамицин B (бетамицин) или гентамицин С1. Используемый активный агент с фармацевтической точки зрения состоит из нескольких самостоятельных соединений группы субстанций гентамицинов, которые содержат почти исключительно гентамицины типа С. Если далее в изобретении не указано иное, термин "гентамицин" всегда означает упомянутую смесь типов.
Аминогликозиды относятся к группе олигосахаридных антибиотиков с комбинациями блоков аминосахара и циклогексана. Выведение происходит главным образом через почки, с коротким периодом полувыведения около двух часов.
Дополнительными предпочтительными антибиотиками являются: даптомицин, тигециклин, хлорамфеникол, доксициклин, моноциклин, тетрациклин, окситетрациклин, азитромицин, кларитромицин, эритромицин, рокситромицин, дальфопристин, хинупристин, клиндамицин, линкомицин, телитромицин, нарбомицин, цетомицин и фузидиевая кислота.
Покрытие согласно настоящему изобретению также может содержать комбинации по меньшей мере из двух указанных антибиотиков. Они могут находиться вместе в одном слое покрытия или могут быть расположены в отдельных слоях один над другим, или могут быть нанесены на разные части протеза.
Выбор антибиотика и его концентрация обычно зависит от инфекции, которая наиболее часто возникает в связи с имплантацией покрытого эндопротеза, и также может зависеть от известной непереносимости у пациента, подлежащего лечению.
Используемые антибиотики могут быть органического, полусинтетического и синтетического происхождения.
С помощью лекарственного покрытия согласно изобретению можно значительно уменьшить число возможных после имплантации жалоб, таких как частота ревизий, и, следовательно, раннее удаление эндопротеза, например, протеза тазобедренного сустава. Таким образом, это лекарственное покрытие идеально предотвращает или по меньшей мере минимизирует до приемлемого уровня первичные инфекции, вызванные грамположительными микроорганизмами и грамотрицательными кишечными бактериями и некишечными бактериями, так, что в конечном счете организм может успешно сдерживать немногочисленные оставшиеся микроорганизмы.
Предпочтительно, чтобы покрытие было нанесено равномерно на весь эндопротез. Кроме того, предпочтительно, если на эндопротезе имеется равномерное распределение антибиотика и по меньшей мере одного соединения с формулой (Ia) и/или (Ib).
В целом имеет преимущество полное покрытие эндопротеза активным веществом, то есть наличие покрытия по всей поверхности эндопротеза. Дополнительно, можно делать покрытие эндопротеза с таким эффектом, что покрытие со смесью антибиотиков и соединением формулы (Ia) и/или (Ib) наносится не равномерно, а с использованием градиента, с тем, чтобы на эндопротезе создавался градиент концентрации. Таким образом, антибиотик и соединение формулы (Ia) и/или (Ib) в более высоких концентрациях можно наносить, например, на середину или на определенные зоны эндопротеза, такие как остальные зоны эндопротеза.
Дополнительно, антибиотик и соединение формулы (Ia) и/или (Ib) также можно наносить только на одну сторону или на одну часть эндопротеза в более высоких концентрациях, чем концентрации на остальной поверхности. В этом случае возможны любые варианты.
Термин «покрытие» или «покрытие активным агентом» включает не только покрытие поверхности, но и заполнение или покрытие складок, полостей, пор, микроигл или других заполняемых зон или на поверхности или внутри эндопротеза.
Поверхность может дополнительно иметь гемосовместимый слой в качестве базового покрытия, который наносится путем ковалентной иммобилизации полусинтетических производных гепарина, например, десульфатированного, реацетилированного гепарина, или производных хитозана, например, N-карбоксиметилированного частично N-ацетилированного хитозана.
Эндопротез может быть полностью снабжен таким покрытием. Также возможно частичное покрытие эндопротезов.
Покрытие из по меньшей мере одного антибиотика и одного соединения общей формулы (Ia) или (Ib) можно смешивать с одним или несколькими другими активными агентами, предпочтительно с противовоспалительным, противоопухолевым, антиангиогенным, антипролиферативным или иммуносупрессивным веществом.
Применимые противовоспалительные, противоопухолевые, антиангиогенные, антипролиферативные или иммуносупрессивные агенты включают следующие: сиролимус (рапамицин), эверолимус, пимекролимус, соматостатин, такролимус, рокситромицин, дунаимицин, аскомицин, бафиломицин, эритромицин, мидекамицин, джозамицин, конканамицин, кларитромицин, тролеандомицин, фолимицин, церивастатин, симвастатин, ловастатин, флувастатин, розувастатин, аторвастатин, правастатин, питавастатин, винбластин, винкристин, виндезин, винорелбин, этопозид, тенипозид, нимустин, кармустин, ломустин, циклофосфамид, 4-гидроксициклофосфамид, эстрамустин, мелфалан, бетулиновая кислота, камптотецин, лапахол, β-лапахон, подофиллотоксин, бетулин, тропфосфамид, 2-этилгидразид подофиловой кислоты, ифосфамид, хлорамбуцил, бендамустин, дакарбазин, бусульфан, прокарбазин, треосульфан, тремозоломид, тиотепа, даунорубицин, доксорубицин, акларубицин, эпирубицин, митоксантрон, идарубицин, блеомицин, митомицин, дактиномицин, метотрексат, флударабин, флударабин-5'-дигидрофосфат, мофебутазон, ацеметацин, диклофенак, лоназолак, дапсон, о-карбамоилфеноксиуксусная кислота, лидокаин, кетопрофен, мефенамовая кислота, пироксикам, мелоксикам, хлорохин, пеницилламин, гидроксихлорохин, ауранофин, ауротиомалат натрия, оксацепрол, целекоксиб, β-ситостерин, адеметионин, миртекаин, полидоканол, нонивамид левоментол, бензокаин, аэсцин, кладрибин, меркаптопурин, тиогуанин, цитарабин, фторурацил, гемцитабин, капецитабин, доцетаксел, карбоплатин, цисплатин, оксалиплатин, амсакрин, иринотекан, топотекан, гидроксимочевина, милтефозин, пентостатин, алдеслейкин, третиноин, аспарагиназа, пегаспараза, анастрозол, экземестан, летрозол, форместан, аминоглютетемид, адриамицин, азитромицин, спирамицин, цефарантин, ингибитор пролиферации гладкомышечных клеток (SMC) 2w типа, эпотилоны А и В, митоксантрон, азатиоприн, микофенолата мофетил, антисмысловой c-myc, антисмысловой b-myc селектин (цитокиновый антагонист), ингибитор белка-переносчика эфиров холестерина (СЕТР), кадгерины, ингибиторы цитокинов, ингибитор COX-2, транскрипционный фактор NFkB, ангиопептин, ципрофлоксацин, камптотецин, флуробластин, моноклональные антитела, ингибирующие пролиферацию мышечных клеток, антагонисты bFGF, пробукол, простагландины, фолиевая кислота и ее производные, витамины группы В, производные витамина D, такие как кальципотриол и такальцитол, тимозин D-1, фумаровая кислота и ее производные, такие как диметилфумарат, ингибитор IL-1 бета, колхицин, доноры NO, такие как пентаэритритилтетранитрат и сиднонимин, S-нитрозированные производные, тамоксифен, стауроспорин, бета-эстрадиол, α-эстрадиол, эстрон, эстриол, этинилэстрадиол, фосфестрол, медроксипрогестерон, эстрадиолципионат, эстрадиолбензоат, траниласт, камебакаурин и другие терпеноиды, которые применяют в противораковой терапии, верапамил, ингибиторы тирозинкиназы (тирфостины), циклоспорин А, паклитаксел и его производные (6-α-гидрокси-паклитаксел, баккатин, таксотер и др.), макроциклические олигомеры недоокиси углерода (MCS) синтетического и природного происхождения и их производные, молграмостим (rhuGM-CSF), пегинтерферон альфа-2b, ланограстим (r Hug-CSF), филграстим, макрогол, дакарбазин, базиликсимаб, даклизумаб, эллиптицин, D-24851 (Калбиохем), колцемид, цитохалазин АЕ, Инданоцин, нокадазол, белок S 100, PI-88, меланоцитстимулирующий гормон (α-МСГ), бацитрацин, антагонисты рецепторов витронектина, азеластин, стимулятор гуанидилциклазы, тканевый ингибитор металлопротеиназы типа 1 и типа 2, свободные нуклеиновые кислоты, нуклеиновые кислоты, включенные в вирусные трансмиттеры, фрагменты ДНК и РНК, ингибитор активатора плазминогена типа 1, ингибитор активатора плазминогена типа 2, антисмысловые олигонуклеотиды, ингибиторы фактора роста эндотелия сосудов (VEGF), например, IGF-1. Положительный эффект в послеоперационный период также имеют антикоагулянты, такие как аргатробан, аспирин, абциксимаб, синтетический антитромбин, бивалирудин, кумадин, эноксопарин, гемопарин® (десульфатированный и N-реацетилированный гепарин), тканевой активатор плазминогена, GpIIb/IIIa рецептор оболочки тромбоцитов, ингибитор Ха фактора, активированный протеин С, антитела, гепарин, гирудин, r-гирудин, Phe-Pro-Arg хлорметил кетон (РРАСК), протамин, проурокиназа, стрептокиназа, варфарин, урокиназа, вазодилататоры, такие как дипиридамол, трапидил, нитропруссид, антагонисты фактора роста тромбоцитов (PDGF), такие как триазолопиримидин и Серамин, ингибиторы ангиотензинпревращающего фермента (АПФ), такие как каптоприл, цилазаприл, лизиноприл, эналаприл, лозартан, ингибиторы тиопротеазы, ингибиторы каспаз, ингибиторы апоптоза, регуляторы апоптоза, такие как p65, антисмысловые олигонуклеотиды NF-kB и Bcl-xL и простациклин, вапипрост, α-, β- и γ-интерфероны, антагонисты гистамина, блокаторы серотонина, галофугинон, нифедипин, токоферол, транираст, молсидомин, чайные полифенолы, эпикатехингаллат, эпигаллокатехингаллат, босвеллиевые кислоты и их производные, лефлуномид, анакинра, этанерцепт, сульфасалазин, этопозид, диклоксациллин, тетрациклин, триамцинолон, мутамицин, прокаинамид, ретиноевая кислота, хинидин, дизопиримид, флекаинид, пропафенон, сотолол, амидорон. Другие лекарственные средства представляют собой стероиды (гидрокортизон, бетаметазон, дексаметазон), нестероидные противовоспалительные средства (НПВС), такие как фенопрофен, ибупрофен, индометацин, напроксен, фенилбутазон и другие. Также в этой области применяются противовирусные средства, такие как ацикловир, ганцикловир и зидовудин. Различные противогрибковые агенты применяются в этой области. Их примеры включают клотримазол, флуцитозин, гризеофульвин, кетоконазол, миконазол, нистатин, тербинафин. Противопротозойные агенты, равные по эффективности, представляют собой, например, хлорохин, мефлохин, хинин, кроме того, существуют природные терпеноиды, такие как гиппоцескулин, баррингтогенол-С21-ангелат, 14-дегидроагростистахин, агроскерин, агростистахин, 17-гидроксиагростистахин, оватодиолид, 4,7-оксициклоанизомелиновая кислота, бакхариноид В1, В2, B3 и В7, тубеимозид, бруцеанол А, В и С, бруцеантинозид С, яданзиозид N и Р, изодезоксиэлефантопин, томенфантопин А и В, коронарин А, В, С и D, урсоловая кислота, гиптатовая кислота А, зеорин, изоиридогерманал, майтенфолиол, эффузантин А, эксцизанин А и В, лонгикаурин В, скульпонеатин С, камебаунин, лейкаменин А и В, 13,18-дегидро-6-альфа-сенециоилоксичапаррин, 1,11-диметоксикантин-6-он, 1-гидрокси-11-метоксиксантин-6-он, скополектин, таксамаирин А и В, регенилол, триптолид, а также цимарин, апоцимарин, аристолохиевая кислота, аноптерин, гидроксианоптерин, анемонин, протоанемонин, берберин, челибуринхлорид, циктоксин, синококулин, бомбрестатин А и В, кудраизофлавон А, куркумин, дигидронитидин, нитидинхлорид, 12-бета-гидроксипрегнадиен-4,16-диен-3,20-дион, билобол, гинкгол, гинкголевая кислота, геленалин, индицин, индицин-N-оксид, лазиокарпин, инотодиол, гликозид 1а, подофиллотоксин, джустицидин А и В, ларреатин, маллотерин, маллотохроманол, изобутирилмаллотохроманол, махирозид А, марчантин А, майтанзин, ликоридицин, маргетин, панкратистатин, лириоденин, оксоушинсунин, аристолактам-AII, биспартенолидин, периплокозид А, галакинозид, урсоловая кислота, дезоксипсороспермин, психорубин, рицин А, сангвинарин, метилсорбифолин, сфателиахромен, стизофиллин, мансонин, стреблозид, акагерин, дигидроусамбаренсин, гидроксиусамбарин, стрихнопентамин, стрихнофиллин, усамбарин, усамбарензин, берберин, лириоденин, оксоушинсунин, дафноретин, ларицирезинол, метоксиларицирезинол, сирингарезинол, умбеллиферон, афромозон, ацетилвисмион В, дезацетилвисмион А, висмион А и В, другие природные терпеноиды, такие как гиппоцескулин, 14-дегидроагростистахин, агроскерин, агростистахин, 17-гидроксиагростистахин, оватодиол