Биологически активное соединение, содержащее кодирующий олигонуклеотид, и библиотека соединений
Иллюстрации
Показать всеГруппа изобретений относится к области биохимии. Предложены соединение и варианты библиотеки соединений для идентификации обладающих требуемыми свойствами соединений. Соединение имеет формулу
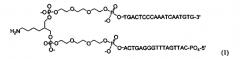
где каждый из n, m и р независимо имеет значение от 1 до 20; X представляет собой функциональный фрагмент, содержащий один или более структурных элементов; Z представляет собой олигонуклеотид, присоединенный по своему 3'-концу к фосфатной группе; Y представляет собой олигонуклеотид, присоединенный по своему 5'-концу к фосфатной группе. Также предложена библиотека для идентификации обладающих требуемыми свойствами соединений, содержащая множество соединений указанной формулы. В другом варианте библиотека содержит по меньшей мере 102 отличающихся указанных соединений, которые содержат функционально связанный с олигонуклеотидом функциональный фрагмент, состоящий из двух или более структурных элементов. 3 н. и 10 з.п. ф-лы, 13 ил., 7 табл., 10 пр.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к области биологической химии, а именно к новому способу синтеза библиотек молекул, содержащих олигонуклеотидную метку. Данные библиотеки могут быть использованы для определения соединений, связывающихся с определенной биологической мишенью.
Уровень техники
Поиск более эффективных способов идентификации соединений, характеризующихся ценными биологическими свойствами, привел к развитию методов скриннинга огромного числа различных соединений, собранных в коллекциях, которые называются комбинаторными библиотеками. Такие библиотеки включают 105 или более различных соединений. Существует множество способов создания комбинаторных библиотек, а также описан комбинаторный синтез пептидов, пептидомиметиков и низкомолекулярных органических молекул.
Две основные проблемы при использовании комбинаторного подхода в создании лекарственных средств заключаются в синтезе библиотек достаточной сложности и в идентификации молекул, обладающих активностью, определенной различными методами анализа. Общеизвестно, что чем выше степень сложности библиотеки, т.е. число различных структур, включенных в библиотеку, тем выше вероятность наличия в библиотеке молекул, обладающих требуемой активностью. Следовательно, методы химического синтеза для создания библиотеки должны обеспечивать получение огромного числа соединений в пределах разумного промежутка времени. Однако с учетом данной "формальной" или общей концентрации, при увеличении числа различных членов в библиотеке снижается концентрация конкретного члена в библиотеке, что осложняет идентификацию активных молекул в библиотеках высокой сложности.
Один из подходов к преодолению таких недостатков заключается в создании кодированных библиотек, и, прежде всего, библиотек, в которых каждое соединение включает амплифицируемую метку. Такие библиотеки включают ДНК-кодированные библиотеки, в которых меченый фрагмент ДНК, идентифицирующий член библиотеки, можно амплифицировать с использованием методов молекулярной биологии, таких как полимеразная цепная реакция. Однако использование таких способов для получения библиотек, включающих огромное множество соединений, еще находится на стадии разработки, и очевидно, что для реализации такого подхода при создании лекарственных средств существует необходимость в развитии усовершенствованных методов создания таких библиотек.
Раскрытие изобретения
В настоящем изобретении предлагается способ синтеза библиотек молекул, которые содержат кодирующую олигонуклеотидную метку. В данном способе используется стратегия "разделения и объединения", которая заключается в том, что раствор, содержащий инициатор, первый структурный элемент, связанный с кодирующим олигонуклеотидом, разделяют на множество фракций ("разделение"). В каждой фракции инициатор взаимодействует со вторым, уникальным, структурным элементом и вторым уникальным олигонуклеотидом, который идентифицирует второй структурный элемент. Эти реакции проводят одновременно или последовательно, и в случае последовательных реакций, каждая реакция предшествует другой реакции. Димерные молекулы, образующиеся в каждой фракции, объединяют ("объединение") и затем снова разделяют на множество фракций. Каждая из таких фракций взаимодействует с третьим уникальным (специфичным для данной фракции) структурным элементом и третьим уникальным олигонуклеотидом, который кодирует структурный элемент. Число специфичных молекул, присутствующих в полученной библиотеке, зависит (1) от числа различных структурных элементов, использованных на каждой стадии синтеза, и (2) от числа стадий разделения и объединения фракций.
В одном варианте воплощения настоящего изобретения предлагается способ синтеза молекулы, содержащей или представляющей собой функциональный фрагмент, эффективно связанный с кодирующим олигонуклеотидом. Такой способ включает следующие стадии: (1) выбор соединения-инициатора, состоящего из функционального фрагмента, содержащего n структурных элементов (где n равно целому числу 1 или более), причем функциональный фрагмент содержит по меньшей мере одну реакционноспособную группу, и эффективно связана с исходным олигонуклеотидом; (2) взаимодействие соединения-инициатора со структурным элементом, содержащим по меньшей мере одну комплементарную реакционноспособную группу, которая является комплементарной в отношении реакционноспособной группы, описанной на стадии (1), в условиях, пригодных для взаимодействия реакционноспособной группы и комплементарной реакционноспособной группы с образованием ковалентной связи; (3) взаимодействие исходного олигонуклеотида с новым олигонуклеотидом, который идентифицирует структурный элемент, описанном на стадии (b) в присутствии фермента, который катализирует лигирование исходного олигонуклеотида и нового олигонуклеотида в условиях, пригодных для лигирования исходного олигонуклеотида и нового олигонуклеотида, с образованием молекулы, содержащей или представляющей собой функциональный фрагмент, включающий n+1 структурных элементов, которые эффективно связаны с кодирующим олигонуклеотидом. Если функциональная группа, описанная на стадии (3) содержит реакционноспособную группу, то стадии 1-3 при необходимости повторяют один или более раз, при этом проводят циклы 1-i (где i равно целому числу 2 или более) с использованием продукта, полученного на стадии (3) цикла s (где s равно целому числу i-1 или менее), выполняющего функции соединения-инициатора в цикле s+1.
В одном варианте воплощения настоящего изобретения предлагается способ синтеза библиотеки соединений, в которой соединения содержат функциональный фрагмент, содержащий 2 или более структурных элементов, эффективно связанных с олигонуклеотидом, который идентифицирует структуру функционального фрагмента. Способ включает следующие стадии: (1) обеспечение раствора, включающего m соединений-инициаторов (где m равно целому числу 1 или более), причем соединения-инициаторы состоят из функционального фрагмента, содержащего n структурных элементов (где n равно целому числу 1 или более), которые эффективно связаны с исходным олигонуклеотидом, идентифицирующим n структурных элементов; (2) разделение раствора, полученного на стадии (2), на r фракций (где r равно целому числу 2 или более); (3) взаимодействие соединений-инициаторов в составе каждой фракции с одним из r структурных элементов с образованием r фракций, содержащих соединения, состоящие из функционального фрагмента, содержащего n+1 структурных элементов, который эффективно связан с исходным олигонуклеотидом; (4) взаимодействие исходного олигонуклеотида в составе каждой фракции с одним из набора r различных новых олигонуклеотидов в присутствии фермента, который катализирует лигирование нового и исходного олигонуклеотидов в условиях, пригодных для ферментативного лигирования нового и исходного олигонуклеотидов, с получением r аликвотных фракций, состоящих из функционального фрагмента, содержащего n+1 структурных элементов, эффективно связанной с удлиненным олигонуклеотидом, который кодирует n+1 структурных элементов. Способ необязательно включает стадию (5) рекомбинирования r фракций, полученных на стадии (4), с получением раствора, содержащего соединения, состоящие из функциональной группы, содержащей n+1 структурных элементов, и эффективно связанной с удлиненным олигонуклеотидом. Стадии (1)-(5) при необходимости повторяют один или более раз, при этом проводят циклы 1-i (где i равно целому числу 2 или более). В цикле s+1 (где s равно целому числу i-1 или менее), раствор, включающий m соединений-инициаторов, описанных на стадии (1), является раствором, описанным на стадии (5) цикла s. Аналогичным образом, соединения-инициаторы, описанные на стадии (1) цикла s+1, являются соединениями-инициаторами, описанными на стадии (5) цикла s.
В предпочтительном варианте, для конденсации структурных элементов на каждой стадии используют стандартные химические реакции. Структурные элементы конденсируют с образованием линейных или разветвленных полимеров или олигомеров, таких как пептиды, пептидомиметики или пептоиды или неолигомерные молекулы, такие как молекулы, включающие структуру-каркас, к которой присоединяют один или более дополнительных химических компонентов. Например, если структурные элементы представляют собой аминокислотные остатки, то их конденсируют с использованием стандартных методов пептидного синтеза, таких как синтез в растворе или твердофазный синтез, с использованием известных пригодных способов введения/удаления защитных групп. Предпочтительным способом для конденсирования структурных элементов является синтез в растворе. В качестве кодирующих олигонуклеотидов используют одноцепочечные или двухцепочечные олигонуклеотиды, предпочтительно двухцепочечные олигонуклеотиды. Кодирующие олигонуклеотиды предпочтительно включают от 4 до 12 оснований или пар оснований на один структурный элемент; кодирующие олигонуклеотиды конденсируют с использованием стандартных методов синтеза олигонуклеотидов в растворе или твердофазного синтеза, но предпочтительно конденсируют с использованием ферментативного синтеза в растворе. Например, олигонуклеотиды конденсируют с использованием топоизомеразы, лигазы или ДНК-полимеразы, если последовательность кодирующих олигонуклеотидов включает инициирующую последовательность для лигирования с одним из таких ферментов. Ферментативная конденсация кодирующих олигонуклеотидов характеризуется следующими преимуществами: (1) высокая точность присоединения по сравнению со стандартной (неферментативной) конденсацией и (2) использование более простого способа введения/удаления защитных групп.
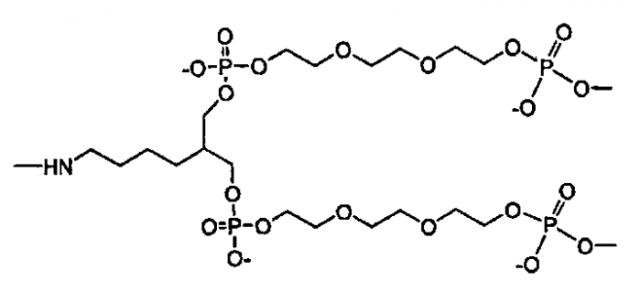
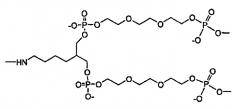
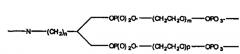
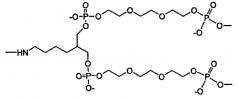
В другом варианте в настоящем изобретении предлагаются соединения формулы I:
где X означает функциональный фрагмент, содержащий один или более структурных элементов; Z означает олигонуклеотид, присоединенный через 3′-концевой участок к B; Y означает олигонуклеотид, который присоединен через 5′-концевой участок к C; A означает функциональную группу, ковалентно связанную с X; B означает функциональную группу, связанную с 3′-концевым участком фрагмента Z; C означает функциональную группу, связанную с 5′-концевым участком фрагмента Y; D, F и E каждый независимо означает бифункциональную связующую группу, а S означает атом или молекулярный каркас. Такие соединения могут быть в синтезированы в том числе с использованием способов по настоящему изобретению.
Настоящее изобретение относится также к библиотеке соединений, содержащей соединения, содержащие функциональный фрагмент, содержащий два или более структурных элементов, и эффективно связанную с олигонуклеотидом, кодирующим структуру функционального фрагмента. Такие библиотеки включают от приблизительно 102 до приблизительно 1012 или более различных членов, например, 102, 103, 104, 105, 106, 107, 108, 109, 1010, 1011, 1012 или более различных членов, т.е. различных молекулярных структур. В одном варианте воплощения настоящего изобретения библиотека соединений содержит соединения, каждое из которых независимо означает соединение формулы I:
где X означает функциональный фрагмент, содержащий один или более структурных элементов; Z означает олигонуклеотид, присоединенный через 3′-концевой участок к B; Y означает олигонуклеотид, присоединенный через 5′-концевой участок C; A означает функциональную группу, ковалентно связанную с X; B означает функциональную группу, связанную с 3′-концевым участком фрагмента Z; C означает функциональную группу, связанную с 5′-концевым участком фрагмента Y; D, F и E каждый независимо означает бифункциональную связующую группу, а S означает атом или молекулярный каркас. Такие библиотеки могут быть синтезированы в том числе с использованием способов по настоящему изобретению.
В другом аспекте настоящего изобретения предлагается способ поиска (идентификации) соединения, которое связывается с биологической мишенью, при этом указанный способ включает следующие стадии: (1) контактирование биологической мишени с библиотекой соединений по настоящему изобретению, включающей соединения, которые содержат функциональный фрагмент, содержащий два или более структурных элемента и эффективно связанный с олигонуклеотидом, кодирующим структуру функционального фрагмента. Данную стадию проводят в условиях, пригодных для связывания по крайней мере одного члена библиотеки соединений с мишенью; (2) удаление членов библиотеки, которые не связаны с мишенью; (3) амплификация кодирующих олигонуклеотидов по меньшей мере одного члена библиотеки соединений, который связывается с мишенью; (4) секвенирование кодирующих олигонуклеотидов, описанных на стадии (3) и использование последовательностей, определенных на стадии (4), для определения структуры функциональных фрагментов членов библиотеки соединений, которые связываются с биологической мишенью.
Настоящее изобретение демонстрирует несколько преимуществ идентификации молекул, обладающих требуемыми свойствами. Например, способы по настоящему изобретению обеспечивают использование ряда химических реакций для конструирования молекул в присутствии олигонуклеотидной метки. Способы по настоящему изобретению позволяют вводить с высокой точностью олигонуклеотидные метки в образующиеся таким образом химические структуры. Более того, указанные способы позволяют проводить синтез библиотек, содержащих множество копий каждого члена, что в свою очередь позволяет проводить множество циклов селекции в отношении биологической мишени и при этом остается достаточное число молекул, которые подвергаются конечному циклу амплификации и секвенирования олигонуклеотидной метки.
Краткое описание чертежей
На фиг. 1 показана схема лигирования двухцепочечных нуклеотидов, причем исходный нуклеотид содержит выступающий участок, комплементарный выступающему участку нового олигонуклеотида. Исходная цепочка изображена в виде свободной, конъюгированной с аминогексильным линкером или конъюгированной с остатком фенилаланина через аминогексильный линкер.
На фиг. 2 показана схема лигирования олигонуклеотидов с использованием фиксирующей цепочки. В данном варианте, фиксирующей цепочкой является 12-членный олигонуклеотид с последовательностями, комплементарными одноцепочечному исходному олигонуклеотиду и одноцепочечному новому олигонуклеотиду.
На фиг. 3 показана схема лигирования исходного и нового олигонуклеотидов, причем исходный олигонуклеотид содержит две ковалентно связанные цепочки, а новый олигонуклеотид является двухцепочечным.
На фиг. 4 показана схема наращивания олигонуклеотидной цепочки с использованием полимеразы. Исходная цепочка изображена в виде свободной, конъюгированной с аминогексильным линкером или конъюгированной с остатком фенилаланина через аминогексильный линкер.
На фиг. 5 показана схема синтетического цикла по одному из вариантов воплощения настоящего изобретения.
На фиг. 6 показана схема многостадийного процесса идентификации с использованием библиотек по настоящему изобретению.
На фиг. 7 показан результат гелевого электрофореза продуктов, полученных в каждом из циклов 1-5, описанных в примере 1, и последующего лигирования замыкающего праймера. Олигонуклеотиды со стандартной молекулярной массой указаны на дорожке 1, и указанные параметры гиперлэддера, для определения количества ДНК, показаны на дорожках 9-12.
На фиг. 8 показана схема конденсации структурных элементов с использованием азид-алкин-циклоприсоединения.
На фиг. 9 и 10 показана конденсация структурных элементов с использованием нуклеофильного ароматического замещения хлорированного триазина.
На фиг. 11 показаны хлорированные гетероароматические структуры, пригодные для синтеза функциональных фрагментов.
На фиг. 12 показана циклизация линейного пептида с использованием реакции азид-алкин-циклоприсоединения.
На фиг. 13A показана хроматограмма библиотеки, полученной, как описано в примере 2, в результате цикла 4.
На фиг. 13B показан масс-спектр библиотеки, полученной, как описано в примере 2, в результате цикла 4.
Осуществление изобретения
Настоящее изобретение относится к способам получения соединений комбинаторных библиотек соединений, к соединениям и библиотекам, которые получают с использованием способов по настоящему изобретению, и к способам использования библиотек для идентификации соединений, обладающих требуемыми свойствами, такими как требуемая биологическая активность. Настоящее изобретение относится также к соединениям, которые идентифицируют с использованием таких способов.
Для получения и анализа комбинаторных химических библиотек используют множество подходов. Примеры включают способы, в которых отдельные члены библиотеки физически отделены друг от друга, например, если синтез отдельного соединения проводят в одном из множества отдельных сосудов. Однако обычно в таких библиотеках анализируют единовременно только одно соединение, или в лучшем случае, несколько соединений, и, следовательно, такой способ не является наиболее эффективным методом скриннинга. Согласно другим способам, соединения синтезируют на твердой фазе. Такие твердые носители включают чипы, в которых специфичные соединения занимают особые участки чипа или мембраны ("адресуемое положение"). Согласно другим способам, соединения синтезируют на гранулах, при этом каждая гранула несет отдельную химическую структуру.
При анализе больших библиотек возникают две проблемы: (1) множество отдельных соединений, которые подвергаются анализу и (2) идентификация соединений, проявляющих активность при данном при данном методе анализа. Согласно одному способу, соединения, проявляющие активность при данном методе анализа, идентифицируют разделением исходной библиотеки на меньшие фракции и подфракции, в каждом случае отбирая фракцию или подфракцию, содержащую активные соединения, и затем снова разделяют на фракции до получения активной подфракции, которая содержит набор соединений, который достаточно мал, чтобы все его компоненты можно было синтезировать каждый в отдельности и получить соединения с требуемой активностью. Такой способ является слишком трудоемким и длительным процессом.
Другой способ обратного анализа комбинаторной библиотеки заключается в использовании библиотек, в которых члены библиотеки содержат индивидуальные метки, т.е. каждая метка, присутствующая в библиотеке, связана с конкретной структурой соединения, присутствующего в библиотеке, таким образом, что идентификация метки определяет структуру меченой молекулы. Один из подходов получения меченых библиотек заключается в использовании олигонуклеотидных меток, как описано, например, в патентах США №5573905, 5708153, 5723598, 6060596, в опубликованных заявках на выдачу патентов PCT WO 93/06121, WO 93/20242, WO 94/13623, WO 00/23458, WO 02/074929 и WO 02/103008, а также в работах Brenner and Lenner (Proc.Natl.Acad.Sci.USA, 89, 5381-5383 (1992); Nielsen and Janda (Methods: A Companion to Methods in Enzymology, 6, 361-371 (1994) и Nielesen, Brenner and Janda (J.Amer.Chem.Soc., 115, 9812-9813 (1993)), каждая из которых полностью включена в настоящее описание в качестве ссылки. Такие метки амплифицируют с использованием, например, полимеразной цепной реакции, для получения большого числа копий меченого фрагмента и идентификации его при секвенировании. Секвенирование меченого фрагмента позволяет идентифицировать структуру связывающей молекулы, которая может быть синтезирована в чистой форме и протестирована. К настоящему времени данные по использованию методологии, описанной в статье Lerner et al., для получения больших библиотек, отсутствуют. В настоящем изобретении предлагается усовершенствование способов получения ДНК-кодированных библиотек, а также первые примеры больших (105 членов и более) библиотек ДНК-кодированных молекул, в которых функциональный фрагмент получают с использованием синтеза в растворе. В настоящем изобретении предлагаются способы простого синтеза комбинаторных библиотек, кодированных олигонуклеотидами, причем указанные способы позволяют с высокой точностью вводить олигонуклеотидную метку в каждый член многочисленного набора молекул.
Способы по настоящему изобретению включают способы синтеза бифункциональных молекул, которые включают первый компонент ("функциональный фрагмент"), которая состоит из структурных элементов, и второй компонент, эффективно связанный с первым компонентом, содержащим олигонуклеотидную метку, которая определяет структуру первого компонента, т.е. олигонуклеотидная метка указывает, какие структурные элементы были использованы при конструировании первого компонента, и в каком порядке они связаны. В основном, информации, содержащейся в олигонуклеотидной метке, оказывается достаточно для определения структурных элементов, использованных для конструирования активного компонента. В определенных вариантах, последовательность олигонуклеотидной метки является достаточной для определения расположения структурных элементов в функциональном фрагменте, например, для пептидных групп достаточно аминокислотной последовательности.
Термин "функциональный фрагмент", использованный в данном контексте, означает химический компонент, содержащий один или более структурных элементов. Предпочтительно, структурные элементы в функциональных фрагментах не означают нуклеиновые кислоты. Функциональным фрагментом является линейный, разветвленный или циклический полимер или олигомер или низкомолекулярная органическая молекула.
Термин "структурный элемент", использованный в данном контексте, означает химическое структурное звено, которое соединено с другими химическими структурными звеньями или присоединено к другим таким звеньям. Если функциональный фрагмент является полимерным или олигомерным, то структурные элементы являются мономерными звеньями полимера или олигомера. Структурные элементы включают также структуру-каркас ("каркасный структурный элемент"), к которому присоединена или может быть присоединена одна или более дополнительных структур ("периферические структурные элементы").
Следует понимать, что термин "структурный элемент", использованный в данном контексте, означает химическое структурное звено, которое входит в состав функционального фрагмента, а также находится в реакционноспособной форме, используемой для синтеза функционального фрагмента. Структурный элемент полностью включен в состав функционального фрагмента, и ни одна из частей структурного элемента не высвобождается при синтезе функционального фрагмента. Например, если в реакциях, идущих с образованием связи, высвобождается небольшая молекула (см. ниже), то в состав функционального фрагмента входит "остаток структурного элемента", т.е. остаток, который образуется в процессе синтеза при высвобождении из структурного элемента атомов, которые присоединяются к высвобожденной молекуле.
В качестве структурных элементов используют любые химические соединения, которые являются комплементарными, т.е. эти структурные элементы способны взаимодействовать друг с другом с образованием структуры, содержащей два или более таких структурных элементов. Обычно, все используемые структурные элементы содержат по крайней мере 2 реакционноспособные группы, хотя некоторые структурные элементы (например, последний структурный элемент олигомерного функционального фрагмента) могут содержать только по одной реакционноспособной группе. Реакционноспособные группы двух различных структурных элементов должны быть комплементарными, т.е. способны взаимодействовать друг с другом с образованием ковалентной связи, необязательно с сопутствующим высвобождением небольшой молекулы, такой как вода, HCl, HF и т.п.
Согласно настоящему изобретению, две реакционноспособных группы являются комплементарными, если они способны взаимодействовать с образованием ковалентной связи. В предпочтительном варианте, реакции с образованием связи протекают быстро в условиях окружающей среды в основном без образования побочных продуктов. Предпочтительно, одна реакционноспособная группа взаимодействует с другой комплементарной реакционноспособной группой только один раз. В одном варианте, комплементарные реакционноспособные группы двух структурных элементов взаимодействуют, например, по механизму нуклеофильного замещения с образованием ковалентной связи. В другом варианте один член пары комплементарных реакционноспособных групп является электрофильной группой, а другой член пары - нуклеофильной группой.
Комплементарные электрофильные и нуклеофильные группы включают любые две группы, которые взаимодействуют по механизму нуклеофильного замещения в пригодных условиях с образованием ковалентной связи. В данной области техники известно множество образующих связь реакций. См., например, March, Advanced Organic Chemistry, 4th ed., New York: John Wiley and Sons (1992), гл. 10-16; Carey and Sundberg, Advanced Organic Chemistry, Part B, Plenum (1990), гл. 1-11; Collman et al., Principles and Applications of Organotransition Metal Chemistry, University Science Books, Mill Valley, Calif. (1987), гл. 13-20, каждая из которых полностью включена в настоящее описание в виде ссылки. Примеры пригодных электрофильных групп включают реакционноспособные карбонильные группы, такие как хлорангидридные группы, сложноэфирные группы, включая карбонилпентафторфенильные эфирные группы и сукцинимидные эфирные группы, кето- и альдегидные группы, реакционноспособные сульфонильные группы, такие как сульфонилхлоридные группы и реакционноспособные фосфонильные группы. Другие электрофильные группы включают концевые эпоксидные группы, изоцианатные группы и галогеналкил группы. Пригодные нуклеофильные группы включают первичные и вторичные аминогруппы, гидроксильные группы и карбоксильные группы.
Пригодные комплементарные реакционноспособные группы перечислены ниже. Специалистам в данной области техники известны другие пары реакционноспособных групп, которые можно использовать в настоящем изобретении, а приведенные ниже примеры не ограничивают объем настоящего изобретения.
В первом варианте комплементарные реакционноспособные группы включают активированные карбоксильные группы, реакционноспособные сульфонильные группы или реакционноспособные фосфонильные группы, или комбинацию указанных выше групп, и первичные или вторичные аминогруппы. В данном варианте комплементарные реакционноспособные группы взаимодействуют в пригодных условиях с образованием амидной, сульфонамидной или фосфонамидатной связи.
Во втором варианте воплощения настоящего изобретения, комплементарные реакционноспособные группы включают эпоксидные группы и первичные или вторичные аминогруппы. Эпоксид-содержащий структурный элемент взаимодействует с аминосодержащим структурным элементом в пригодных условиях с образованием связи углерод-азот, т.е. с образованием β-аминоспирта.
В другом варианте, комплементарные реакционноспособные группы включают азиридиновые группы и первичные или вторичные аминогруппы. В пригодных условиях азиридин-содержащий структурный элемент взаимодействует с аминосодержащим структурным элементом с образованием связи углерод-азот, т.е. с образованием 1,2-диамина. В третьем варианте комплементарные реакционноспособные группы включают изоцианатные группы и первичные или вторичные аминогруппы. Изоцианат-содержащий структурный элемент взаимодействует с амино-содержащим структурным элементом в пригодных условиях с образованием связи углерод-азот, т.е. с образованием остатка мочевины.
В четвертом варианте комплементарные реакционноспособные группы включают изоцианатные группы и гидроксильные группы. Изоцианат-содержащий структурный элемент взаимодействует с гидроксил-содержащим структурным элементом в пригодных условиях с образованием связи углерод-кислород, т.е. с образованием карбаматной группы.
В пятом варианте комплементарные реакционноспособные группы включают амино-группы и карбонил-содержащие группы, такие, как альдегиды или кето-группы. Амины взаимодействуют с такими группами по реакции восстановительного аминирования с образованием новой связи углерод-азот.
В шестом варианте комплементарные реакционноспособные группы включают фосфор-илидные группы и альдегиды или кето-группы. Фосфор-илид-содержащий структурный элемент взаимодействует с альдегид- или кето-содержащим структурным элементом в пригодных условиях с образованием углерод-углеродной двойной связи, т.е. с образованием алкена.
В седьмом варианте комплементарные реакционноспособные группы взаимодействуют по механизму циклоприсоединения с образованием циклической структуры. Один пример таких комплементарных реакционноспособных групп включает алкины и органические азиды, которые в пригодных условиях взаимодействуют с образованием триазольной кольцевой структуры. Пример использования такой реакции для связывания двух структурных элементов показан на фиг. 8. Пригодные условия для проведения таких реакций известны в данной области техники и включают условия, описанные в заявке WO 03/101972, содержание которой полностью включено в настоящее описание в качестве ссылки.
В восьмом варианте комплементарные реакционноспособные группы включают алкилгалогениды и нуклеофилы, такие как аминогруппа, гидроксигруппа или карбоксильная группа. Такие группы взаимодействуют в пригодных условиях с образованием связи углерод-азот (алкилгалогенид + амин) или связи углерод-кислородной (алкилгалогенид + гидроксильная или карбоксильная группа).
В девятом варианте комплементарные реакционноспособные группы включают галогенированную гетероароматическую группу и нуклеофил, и структурные элементы связываются в пригодных условиях по реакции ароматического нуклеофильного замещения. Пригодные галогенированные гетероароматические группы включают хлорированные пиримидины, триазины и пурины, которые взаимодействуют с нуклеофилами, такими как амины, в мягких условиях в водном растворе. Примеры реакции олигонуклеотидов, содержащих трихлортриазиновые группы с аминами показаны на фиг. 9 и 10. Примеры пригодных хлорированных гетероароматических групп показаны на фиг. 11.
Следует понимать, что синтез функционального фрагмента можно проводить с использованием одного конкретного типа реакций конденсации, таких как, без ограничения перечисленным, одна из описанных выше реакций, или с использованием комбинации двух или более реакций конденсации, например, двух или более описанных выше реакций. Например, в одном варианте, структурные элементы соединяют путем сочетания образования амидной связи (комплементарные амино- и карбоксильные группы) и восстановительного аминирования (комплементарные амино- и альдегидные или кетогруппы). Можно использовать любые реакции конденсации при условии, что они совместимы с присутствием олигонуклеотида. Двухцепочечные (дуплексные) олигонуклеотидные метки, использованные в определенных вариантах воплощения настоящего изобретения, являются химически более стабильными по сравнению с одноцепочечными метками, и, следовательно, устойчивы в более широком интервале условий реакции и участвуют в реакциях с образованием связи, что невозможно с использованием одноцепочечных меток.
Структурный элемент кроме реакционноспособной группы или групп, образующих функциональный фрагмент, может включать одну или более функциональных групп. Одну или более из таких дополнительных функциональных групп защищают для предотвращения их вступления в нежелательные реакции. Пригодные защитные группы известны в данной области техники для множества функциональных групп (см. книгу Greene and Wuts, Protective Groups in Organic Synthesys, second edition, New York: John Wiley and Sons (1991), включенную в данный контекст в качестве ссылки). Прежде всего используемые защитные группы включают трет-бутиловые простые и сложные эфиры, ацетали, тритильные эфиры и амины, ацетиловые эфиры, триметилсилиловые эфиры, трихлорэтиловые простые и сложные эфиры и карбаматы.
В одном варианте каждый структурный элемент включает две реакционноспособные группы, которые могут быть одинаковыми или отличаться друг от друга. Например, каждый структурный элемент, добавляемый в цикле s, может включать две одинаковые реакционноспособные группы, но при этом обе группы являются комплементарными с реакционноспособными группами структурных элементов, добавляемых на стадиях s-1 и s+1. В другом варианте, каждый структурный элемент включает две реакционноспособные группы, которые комплементарны друг с другом. Например, библиотеку, содержащую полиамидные молекулы, получают по реакциям между структурными элементами, содержащими две первичные аминогруппы, и структурными элементами, содержащими две активированные карбоксильные группы. В полученных соединениях отсутствуют N- или C-концевые фрагменты, т.к. альтернативные амидные группы имеют противоположное направление. В другом варианте, полиамидную библиотеку получают с использованием структурных элементов, каждый из которых включает аминогруппу и активированную карбоксильную группу. В таком варианте, структурные элементы, добавляемые на стадии n-го цикла, содержат свободную реакционноспособную группу, которая комплементарна с доступной реакционноспособной группой в составе структурного элемента n-1, в то время как, предпочтительно, другая реакционноспособная группа в составе структурного элемента n защищена. Например, если члены библиотеки синтезируют в направлении от C-концевого участка к N-концевому участку, то добавляемые структурные элементы содержат активированную карбоксильную группу и защищенную аминогруппу.
Функциональные фрагменты являются полимерными или олигомерными компонентами, такими как пептиды, пептидомиметики, пептидонуклеиновые кислоты или пептоиды, или они являются низкомолекулярными соединениями, например, молекулами со структурой, включающей центральный каркас, и структурами, расположенными по периферии каркаса. Линейные полимерные или олигомерные библиотеки получают с использованием структурных элементов с двумя реакционноспособными группами, в то время как разветвленные полимерные или олигомерные библиотеки получают с использованием структурных элементов с тремя или более реакционноспособными группами, необязательно в комбинации со структурными элементами, содержащими только две реакционноспособные группы. Такие молекулы можно представить общей формулой X1X2…Xn, где каждый X означает мономерное звено полимера, включающего n мономерных звеньев, где n равно целому числу более 1. В случае олигомерных или полимерных соединений нет необходимости в наличии двух функциональных групп на концевых структурных элементов. Например, в случае полиамидной библиотеки, C-концевой структурный элемент содержит аминогруппу, а присутствие карбоксильной группы необязательно. Аналогичным образом, N-концевой структурный элемент содержит карбоксильную группу, но не содержит аминогруппу.
Разветвленные олигомерные или полимерные соединения синтезируют также при условии, что по крайней мере один структурный элемент включает три функциональные группы, которые взаимодействуют с другими структурными элементами. Библиотека по настоящему изобретению включает линейные молекулы, разветвленные молекулы или их комбинацию.
Библиотеки получают также с использованием, например, каркасных структурных элементов с одной или двумя реакционноспособными группами, в комбинации с другими структурными элементами, содержащими только одну доступную реакционноспособную группу, например, в которых любые другие реакционноспособные группы защищены или нереакционноспособны в отношении других реакционноспособных групп в составе каркасного структурного элемента. В одном варианте, например, полученные молекулы могут быть представлены общей формулой X(Y)n, где X означает каркасный структурный элемент, каждый