Способ получения производных циклопропана
Иллюстрации
Показать всеИзобретение относится к соединению формулы (5): где n представляет собой 0, a R11 представляет собой гидроксил, или его таутомеру, рацемату или стереоизомеру, который является промежуточным соединением для получения производных циклопропана в частности, 2-амино-9-[[1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-пурин-6-она, который обладает противовирусной активностью, а также к способом их получения. 5 н. и 6 з.п. ф-лы.
Реферат
Область техники
Настоящее изобретение относится к получению производных циклопропана и к промежуточным соединениям, полученным в ходе данного способа.
Предшествующий уровень техники
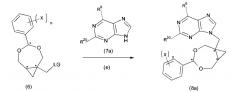
Как известно, производные циклопропана, такие как 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-он, обладают мощной антивирусной активностью.
Первый способ получения 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она описан в патенте EP 0502690. Последовательность реакций, раскрытая в этих документах, включает получение этил-(1S,5S)-2-оксо-3-оксабицикло[3.1.0.]гексан-1-карбоксилата высокой оптической чистоты из R-(-)-эпихлоргидрина и диэтилмалоната. Последующее превращение в (1S,2R)-1,2-бис-(бензоилометил)циклопропилметил-п-толуолсульфонат требует 8 дальнейших стадий, включающих несколько стадий защиты и снятия защиты. (1S,2R)-1,2-бис(бензоилометил)циклопропилметил-п-толуолсульфонат затем сочетают с 2-амино-6-бензилокси-пурином. Наконец, удаление всех защитных гидроксильных групп приводит к целевому продукту. В одной из стадий диметилкетальная функциональная группа применяется в качестве диольной защитной функциональной группы в процессе превращения этильной функциональной группы в гидроксильную. Однако вследствие невысокой стабильности эту защитную группу требуется заменить для дальнейшего превращения гидроксильной группы в уходящую.
При синтезе аналогов 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она, раскрытом в патенте EP 0649840, дополнительно продемонстрировано, что использование более устойчивой дифенилкетальной функциональной группы исключает необходимость замещения диольной защитной группы в процессе синтеза. Однако, установление этой защитной группы требует применения высокотоксичного 2,3-дихлор-5,6-дицианобензохинона (DDQ) и потенциально взрывчатого дифенилдиазометана.
Другой способ получения 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она раскрыт в патенте EP 0675123. Последовательность реакций, описанных в этих документах, подобна вышеприведенному способу. Конкретно, этил-(1S,5R)-2-оксо-3-оксабицикло[3.1.0]гексан-1-карбоксилат высокой оптической частоты получают из R-(-)-эпихлоргидрина и диэтилмалоната. Затем сложноэфирную функциональную группу селективно восстанавливают в гидроксильную, при этом раскрывают и заново замыкают лактоновую группу. Затем гидроксильную группу дополнительно превращают в уходящую группу, и соединение сочетают с 2-амино-6 хлорпурином. Наконец, гидролиз основной группы в гуанин с последующим восстановлением лактонового кольца в диол приводит к образованию целевого продукта.
Формальный синтез 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она, включающий в качестве ключевой стадии внутримолекулярное циклопропанирование D-рибозы действием ненасыщенного диазосоединения, описан Галлосом и сотр. в Tetr. Lett. 2001, 42, 7489.
Вышеописанные способы имеют определенные недостатки: синтетические пути включают несколько длительных стадий защиты и последующего снятия защиты, необходимость применения опасных веществ и/или применения малостабильных промежуточных веществ. Соответственно, необходимы способы синтеза циклопропановых производных, таких как 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропилметил]-1,9-дигидро-6-H-пурин-6-он, уменьшающие хотя бы одну из вышеприведенных проблем.
Краткое описание изобретения
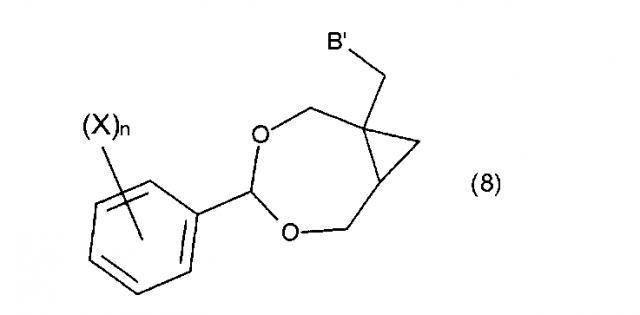
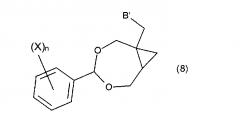
Целью настоящего изобретения является обеспечение нового и улучшенного способа получения 2-амино-9-[[1S,2R)-1,2-бис-(гидроксипропил]метил]-1,9-дигидро-6H-пурин-6-она и связанных соединений. Дополнительной целью изобретения является обеспечение способа, использующего легкодоступные исходные материалы и реакционные условия, подходящие для промышленности. Дополнительной целью изобретения является получение новых и полезных промежуточных соединений, в частности, производных (4-фенил-3,5-диоксабицикло[5.1.0]октан-1-ил)метанола и/или (4-фенил-3,5- диоксабицикло[5.1.0]октан-1-ил)метиламина, которые представлены соединением формулы (5), или его таутомером, рацематом или стереоизомером,
где n - целое число от 0 до 5, X выбран из: C1-6алкил, C1-6галогеналкил, C2-6алкенил, C2-6алкинил, галоген, гидроксил, C1-6алкокси или амино; R11 является гидроксилом или амино.
Авторы настоящего изобретения установили, что при применении фенилацетальной функциональной группы в качестве диольной защитной группы нет необходимости замещения диольной защитной группы в процессе синтеза, к примеру, 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она.
Кроме того, авторы изобретения установили, что установление этой защитной группы является стереоселективным процессом, при котором большая часть стереоизомера может быть легко выделена с помощью кристаллизации. Действительно, [(1S,7R)-4-фенил-3,5-диоксабицикло[5.1.0]-октан-1-ил]метанол и его производные являются полезными синтетическими промежуточными соединениями, которые могут быть легко выделены и являются устойчивыми вследствие их высоко кристаллических свойств.
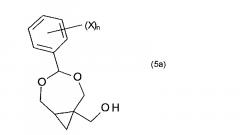
Важно, что соединения формулы (5) могут быть использованы как предшественники в синтезе некоторых аналогов 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она. К примеру, соединения формулы (5a′) или 5(b′) могут быть применены как предшественники в синтезе некоторых аналогов 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она формулы (A′):
где B выбрано из группы, состоящей из пуринила, пиримидила или их аза- или деаза- аналогов, или -NR1R2; при этом каждая группа необязательно замещена одним или более заместителем, независимо выбранными из: галоген, амино, гидроксил, C1-6алкил, аминоС1-6алкил, нитро, формамидо, -NHR18, или OR7; и где углеродный атом указанного пуринила или пиримидила может быть окислен с образованием C=O, где R7 выбран из C1-4алкила, C6-10арилС1-6алкилена или C6-10арила, R18 выбран из C6-10арилС1-6алкилена, C1-6алкилкарбонила, галогенС1-6 алкилкарбонила, C1-6алкилоксикарбонила, 9-флуоренилметилоксикарбонила, или C6-10арилС1-6алкилоксикарбонила; и
R1 выбран из водорода, C6-10арила, C6-10арилС1-6алкилена, C1-4алкила, C6-10галогенарила, C1-4галогеналкила или C6-10галогенарилС1-6алкилена;
R2 выбран из C6-10арила, C6-10арилС1-6алкилена, C1-4алкила, C6-10галогенарила, C1-4галогеналкила или C6-10галогенарилС1-6алкилена;
Дополнительно, соединения формулы (5a′′ или 5(b′′) могут быть применены в синтезе некоторых других аналогов 2-амино-9-[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-она формулы (A′′):
Соответственно, в первом аспекте настоящее изобретение представляет собой соединение формулы (5), как описано выше, либо его таутомера, рацемата или стереомера.
В следующем аспекте настоящее изобретение представляет способ получения соединения формулы (5), либо его таутомера, рацемата или стереомера,
где n, X и R11 имеют определенное в настоящем изобретении значение, включающий стадию превращения группы -COR12 соединения формулы (4)
где R12 является OR3 или амино, а R3 выбран из C1-6алкила, C6-10арила, C6-10арилС1-6алкилена, C6-10галогенарила, C1-6галогеналкила или C6-10галогенарилС1-6алкилена.
В следующем аспекте настоящее изобретение представляет применение производного циклопропана формулы (5) для получения производного циклопропана формулы (A)
где B выбран из группы, состоящей из пуринила, пиримидила или их аза или деаза аналогов, или -NR1R2; при этом каждая группа необязательно замещена одним или более заместителями, независимо выбранными из галогена, амино, гидроксила, C1-6алкила, аминоС1-6алкила, нитро, формамидо, -NHR18, или OR7; и где углеродный атом указанного пуринила или пиримидила может быть окислен с образованием C=O, где R7 выбран из C1-4алкила, C6-10арилС1-6алкилена или C6-10арила, R18 выбран из C6-10арилС1-6алкилена, C1-6алкилкарбонила, галогенС1-6алкилкарбонила, C1-6алкилоксикарбонила, 9-флуоренилметилоксикарбонила, или C6-10арилС1-6алкилоксикарбонила; и
R1 выбран из водорода, C6-10арила, C6-10арилС1-6алкилена, C1-4алкила, C6-10галогенарила, C1-4галогеналкила или C6-10галогенарилС1-6алкилена;
R2 выбран из C6-10арила, C6-10арилС1-6алкилена, C1-4алкила, C6-10галогенарила, C1-4галогеналкила или C6-10галогенарилС1-6алкилена;
Настоящее изобретение также включает способы получения соединения формулы (4).
Подробное описание изобретения
Настоящее изобретение будет описано со ссылкой на конкретные воплощения, но настоящее изобретение ограничивается только формулой изобретения. Любые ссылки в формуле изобретения не должны быть истолкованы, как ограничивающие его объем.
Используемые формы единственного числа включают формы единственного и множественного числа, если из контекста явно не следует иное. Термины «содержащий», «включает» и «состоящий из», используемые здесь, являются синонимами «включающий», «включает» или «содержащий», «содержит» и не исключают дополнительных, не перечисленных членов элементов или этапов способа. Термины «содержащий», «содержит» и «состоящие из» также включают в себя термин «состоящий из». Кроме того, термины «первый», «второй», «третий» и т.п., в описании и формуле изобретения используются для различия подобных элементов и необязательно для описания последовательного или хронологического порядка, если это не отмечено специально. Следует понимать, что термины, используемые таким образом, при соответствующих обстоятельствах являются взаимозаменяемыми, и что описанные здесь воплощения изобретения способны функционировать в иной последовательности, нежели описанные или изображенные здесь.
Термин «примерно», используемый здесь по отношению к измеряемой величине такой, как параметр, количество, продолжительность времени и тому подобное, подразумевает диапазон +/-10 % или менее, предпочтительно +/-5 % или менее, более предпочтительно +/-1 % или менее, и еще более предпочтительно +/-0,1 % или менее от указанного значения, поскольку такие изменения являются оптимальными для выполнения в описанном изобретении. Следует понимать, что величина, по отношению к которой использован термин «примерно», сама по себе конкретна и предпочтительно, раскрыта. Перечисление численных областей конечных величин включает в себя все промежуточные значения этих величин, находящиеся в пределах соответствующих диапазонов, так же, как и перечисленные конечные значения этих величин.
Если специально не оговорено иное, каждый из следующих терминов имеет следующее значение:
Термин «ацил» приписывается радикалу, образованному при удалении гидроксильной группы из карбоновой кислоты (т.е., R-C(=O)-). Предпочтительными ацильными группами являются: ацетил, формил и пропионил, наиболее предпочтительной является ацетил.
Термин «карбонил» используется сам по себе или как часть другого заместителя и приписывается группе -С(=O)-.
Термин «C1-6алкил», как группа или часть группы, приписывается углеводородному радикалу формулы CnH2п+1, где n - число от 1 до 6. Обычно алкильные группы содержат от 1 до 6 углеродных атомов, например, 1-4 углеродных атома. Алкильные группы могут быть линейными или разветвленными и, как здесь указано, могут содержать заместители. Использованный здесь подстрочный знак, следующий за обозначением углеродного атома, относится к числу углеродных атомов, которое может содержать данная группа. Таким образом, символ C1-4алкил означает, что алкильная группа содержит от 1 до 4 углеродных атомов. Примерами алкильных групп являются: метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и его цепочечные изомеры, гексил и его цепочечные изомеры.
Термин «C2-6алкенил», сам по себе или как часть другого заместителя, приписывается ненасыщенной углеводородной группе, которая может быть линейной или разветвленной и содержать одну или более двойных углерод-углеродных связей. Предпочтительные алкенильные группы, таким образом, содержат от 2 до 6 углеродных атомов, предпочтительно, от 2 до 4. Неограничивающие примеры C1-6алкенильных групп включают: этенил, 2-пропенил, 2-бутенил, 3-бутенил, 2-пентенил и его цепочечные изомеры, 2-гексенил и его цепочечные изомеры, 2,4 пентадиенил и его цепочечные изомеры, и т.п.
Термин «C2-6алкинил», сам по себе или как часть другого заместителя, приписывается ненасыщенной углеводородной группе, которая может быть линейной или разветвленной и содержать одну или более тройных углерод-углеродных связей. Предпочтительные алкинильные группы, таким образом, содержат от 2 до 6 углеродных атомов, предпочтительно, от 2 до 4. Неограничивающие примеры C2-6 алкинильных групп включают: этинил, 2-пропинил, 2-бутинил, 3-бутинил, 2-пентинил и его цепочечные изомеры, 2-гексинил и его цепочечные изомеры, и т.п.
Используемый здесь термин «C3-8циклоалкил», сам по себе или как часть другого заместителя, приписывается насыщенному или частично насыщенному циклическому алкильному радикалу, содержащему от 3 до 8 углеродных атомов. Примеры C3-8циклоалкил включают: циклопропил, циклобутил, циклопентил, или циклогексил, циклогептил и циклооктил.
Используемый здесь термин «C6-10арил», сам по себе или как часть другого заместителя, приписывается полиненасыщенной ароматической углеводородной группе, имеющей одно кольцо (т.е. фенил), либо множество конденсированных ароматических колец (например, нафталин), либо связанных ковалентно, обычно содержащих от 6 до 10 атомов, где, по меньшей мере, одно из колец является ароматическим. Арильные кольца могут быть незамещенными или замещенными, имея от 1 до 4 заместителей в кольце. Арильными заместителями могут быть: галоген, циано, нитро, гидрокси, карбокси, амино, ациламино, алкил, гетероалкил, галогеналкил, фенил, арилокси, алкокси, гетероалкокси, карбамил, галогеналкил, метилендиокси, гетероарилокси, или их любая комбинация. Примеры C6-10арил включают: фенил, нафтил, инданил или 1,2,3,4-тетрагидронафтил.
Когда термин «алкил» использован в качестве суффикса, следующего за другим термином, как, например, «гидроксиалкил», подразумевается, что он приписывается алкильной группе, определенной выше, замещенной одним или двумя (предпочтительно, одним) заместителями, выбранными из другой, конкретно названной группы, также определенной здесь. Следовательно, термин «гидроксиалкил» приписывается группе -Ra-OH, где группа Ra является алкиленом, определенным здесь. Используемый здесь термин «C1-6алкокси» или «C1-6алкилокси» приписывается радикалу формулы -ORd, где Rd является C1-6алкилом. Неограничивающие примеры подходящих алкокси групп включают: метокси, этокси, пропокси, изипрококси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси и гексилокси.
Используемый здесь термин «C1-6алкилен», сам по себе или как часть другого заместителя, приписывается бивалентным C1-6 алкильным группам, т.е., двум простым связям для соединения с двумя другими группами. Неограничивающие примеры алкиленовых групп включают: метилен (-CH2-), этилен (-CH2-CH2-), метилметилен (-CH(CH3)-), 1-метил-этилен (-CH(CH3)-CH2-), н-пропилен (-CH2-CH2-CH2-), 2-метилпропилен (-CH2-CH(CH3)-CH2-), 3-метилпропилен (-CH2-CH2-CH(CH3)-), н-бутилен (-CH2-CH2-CH2-CH2-), 2-метилбутилен (-CH2-CH(CH3)-CH2-CH2-), 4-метилбутилен (-CH2-CH2-CH2-CH(CH3)-), пентилен и его цепочечные изомеры, гексилен и его цепочечные изомеры.
Термин «C6-10арилС1-6алкилен», как группа или часть группы, означает определенный здесь радикал C1-6алкил, в котором водородный атом замещен определенным здесь радикалом C6-10арил. Примеры C6-10арилС1-6алкил радикалов включают: бензил, фенэтил, дибензилметил, метилфенилметил, 3-(2-нафтил)-бутил, и т.п.
Использованный здесь термин «C1-6алкилС6-10арилен», сам по себе или как часть другого заместителя, приписывается определенной здесь группе C6-10арил, в которой водородный атом замещен определенным здесь радикалом C1-6алкил. Использованный здесь термин «C3-6циклоалкилен», сам по себе, или как часть другого заместителя, приписывается насыщенному гомоциклическому углеводородному бирадикалу формулы CnH2n-2. Неограничивающие примеры циклоалкиленов включают: 1,2-циклопропилен, 1,1-циклопропилен, 1,1-циклобутилен, 1,2-циклобутилен, 1,3-циклопентилен, 1,1-циклопентилен, или циклогексилен.
Термин «аминоС1-6алкил», сам по себе или как часть другого заместителя, приписывается группе -Rj-NRkRI, где Rj является 1-6алкиленом, Rk является водородом или C1-6алкилом, определенным здесь, a RI является водородом или C1-6алкилом, определенным здесь.
Термин «C1-6алкил эфир»или «C1-6алкоксиС1-6алкил», сам по себе или как часть другого заместителя, приписывается группе C1-6алкил, замещенной одной или двумя группами Rb, где Rb является C1-6алкокси группой, определенной ниже.
Термин «C2-6алкенил эфир» или «C1-6алкенилоксиС1-6алкенил», сам по себе или как часть другого заместителя, приписывается группе C1-6алкенил, замещенной одной или двумя группами Re, где Re является группой C1-6алкенилокси.
«Гало», или «галоген» означает фтор, хлор, бром или иод.
Термин «C1-6алкилсульфинил», «C6-10арилсульфинил» или «C6-10арилС1-6алкиленсульфинил», сам по себе или как часть другого заместителя, приписывается группе -S(O)Rx, где Rx является C1-6алкил, C6-10арил или C6-10арилС1-6алкилен группой, соответственно. Примером C1-6 алкилсульфиниловой группы является метилсульфинил.
Термин «C1-6алкилсульфонил», «C6-10арилсульфонил» или «C6-10арилС1-6алкиленсульфонил», сам по себе или как часть другого заместителя, приписывается группе -S(=O)2Ry, где Ry является C1-6алкил, C6-10арил или C6-10арилС1-6алкилен группой, соответственно. Примером C1-6 алкилсульфониловой группы является метилсульфонил.
Термин «C1-6алкилтио», «C6-10арилтио» или «C6-10арилС1-6алкилентио», сам по себе или как часть другого заместителя, приписывается группе -SRW, где RW является C1-6алкил, C6-10арил или C6-10арилС1-6алкилен группой, соответственно. Неограничивающие примеры подходящих C1-6алкилтиогрупп включают: метилтио, этилтио, пропилтио, изопропилтио, бутилтио, втор-бутилтио, трет-бутилтио, пентилтио и гексилтио.
Термин «C1-6алкилсульфонат», «C6-10арилсульфонат» или «галогенС1-4алкилсульфонат», сам по себе или как часть другого заместителя, приписывается группе -S(=O)2-O-Rv, где Rv является C1-6алкил, C6-10арил или галоС1-3 группой, соответственно. Примером C1-6алкилсульфоната является метилсульфонат. Примерами галогенС1-4алкилсульфоната являются нонафторбутансульфонат (нонафлат) и трифторметансульфонат (трифлат).
Термин «C1-6алкилфосфонат» или «C6-10арилфосфонат», сам по себе или как часть другого заместителя, приписывается группе -OP(=O)(ORt)(ORu), где Rt и Ru являются C1-6алкил и C6-10арил группами, соответственно. Предпочтительно, группы Rt и Ru идентичны. Примером C1-6алкилфосфоната является диэтилфосфонат.
Использованный здесь термин «формамидо» приписывается группе -NH-С(=O)-Н.
Термин «амино», сам по себе или как часть другого заместителя, приписывается группе -NH2.
Использованный здесь термин «фармацевтически приемлемые соли» или «ветеринарно приемлемые соли» означает терапевтически активные нетоксичные аддитивные солевые формы, которые способны образовывать соединения формулы и которые могут быть легко получены обработкой основной формы таких соединений соответствующим основанием или кислотой. Фармацевтически приемлемые соли присоединения кислоты или основания, как выше-, так и нижеупомянутые, означают терапевтически активные нетоксичные соли присоединения кислоты или основания, которые способны образовать соединения формулы (A). Фармацевтически приемлемые соли присоединения кислоты могут быть легко получены обработкой основной формы соответствующей кислотой. Соответствующие кислоты включают, к примеру, неорганические кислоты, такие как галогенводородные, например, хлористоводородная или бромистоводородная кислота, серная, азотная, фосфорная и тому подобные кислоты; или органические, такие, например, как уксусная, пропионовая, гидроксиуксуная, молочная, пировиноградная, щавелевая (т.е. этандиовая), малоновая, янтарная (т.е. бутандиовая кислота), малеиновая, фумаровая, яблочная, винная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памоевая и тому подобные кислоты. И наоборот, упомянутые солевые формы могут быть превращены обработкой соответствующим основанием в свободную основную форму. Соединения формулы (A), содержащие кислый протон, могут быть превращены в их нетоксичные металлические или аминные солевые формы обработкой соответствующими органическими и неорганическими основаниями. Соответствующие основные солевые формы включают, например, соли аммония, соли щелочных и щелочноземельных металлов, например, лития, натрия, калия, магния, солей кальция и т.п., соли органических оснований, например, первичных, вторичных и третичных алифатических и ароматических аминов, таких как метиламин, этиламин, пропиламин, изопропиламин, четыре изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, триметиламин, триэтиламин, трипропиламин, хинуклидин, пиридин, хинолин и изохинолин; бензатин, N-метил-D-глюкамин, соли гидрабамина, и соли аминокислот, например, аргинина, лизина и т.п. И наоборот, солевая форма может быть превращена обработкой кислотой в свободную основную форму.
Кроме того, соли кислот или оснований, не являющихся физиологически приемлемыми, могут также находить применение, например, для получения или очистки физиологически приемлемого соединения. Все соли, независимо от физиологической приемлемости кислоты или основания, находятся в объеме настоящего изобретения.
Использованный здесь термин «изомеры» означает все возможные изомерные формы, которые могут иметь соединения формул (A), (A′), (A′′), от (1) до (8) или от (1′) до (8′). Если специально не оговорено иное, стандартное химическое название относится ко всем возможным стереохимическим изомерным формам, включающим все диастереомеры и энантиомеры (поскольку все описанные здесь соединения могут иметь, по меньшей мере, один хиральный центр) основной молекулярной структуры. В особенности, если не оговорено иное, стереогенные центры могут иметь либо R-, либо S-конфигурацию, а заместители могут иметь либо цис-, либо транс-конфигурацию.
Чистые изомерные формы упомянутых соединений определены, как изомеры, преимущественно свободные от других энантиомерных или диастереомерных форм одной и той же основной молекулярной структуры. В частности, термин «стереоизомерно чистый» или «хирально чистый» относится к соединениям, имеющим стереоизомерный избыток, по меньшей мере, около 80% (т.е., по меньшей мере, 90% одного изомера и не более 10% других возможных изомеров), предпочтительно, по меньшей мере, 90%, более предпочтительно, по меньшей мере, 94%, наиболее предпочтительно - по меньшей мере, 97%. Термины «энантиомерно чистый» и «диастеремерно чистый» следует понимать подобным образом, относительно имеющегося избытка энантиомера или, соответственно, избытка диастереомера в смеси, о которой идет речь. Следовательно, если в процессе любого из последующих способов синтеза получена смесь энантиомеров, она может быть разделена с помощью метода жидкостной хроматографии с применением подходящей хиральной стационарной фазы. Подходящими хиральными стационарными фазами являются, например, полисахариды, в особенности, производные целлюлозы или амилозы. Коммерчески доступными хиральными стационарными фазами на основе
полисахарида являются: ChiralCel™ СА, OA, OB, ОС, OD, OF, OG, OJ и OK, и Chiralpak™ AD, AS, OP(+) и OT(+). Подходящими элюентами или подвижными фазами при использовании в сочетании с указанными полисахаридными хиральными фазами являются: гексан и т.п., модифицированный спиртом типа этанола, изопропанола и т.п. Термины цис- и транс- применяются здесь в соответствии с номенклатурой Chemical Abstracts и относятся к положению заместителей в циклическом радикале. Абсолютная стереохимическая конфигурация соединений формулы может быть легко определена специалистами в данной области техники с помощью известных способов, таких как, например, рентгеновская диффракция.
Специалистам в данной области техники будет также понятно, что соединения по настоящему изобретению могут находиться в различных протонированных формах, зависящих, в частности, от pH среды. В то время как структурные формулы, представленные здесь, описывают соединение только в одной из нескольких возможных протонированных форм, следует понимать, что эти структуры являются лишь иллюстративными, и что изобретение не ограничено какой-либо конкретной протонированной формой, а все формы соединений, включая протонированные, предназначены, чтобы подпадать под объем настоящего изобретения.
Все документы, процитированные в настоящем описании, включены сюда путем ссылки полностью.
Если не определено иное, все термины, используемые в раскрытии изобретения, включая технические и научные термины, имеют значение, которое обычно понимается специалистом с обычной квалификацией в области техники, к которой относится это изобретение. Дополнительные указания и определения терминов, используемых в описании изобретения, включены, чтобы с их помощью лучше понять смысл настоящего изобретения. Термины и определения, используемые в данном документе, приводятся исключительно для оказания помощи в понимании изобретения.
Ссылка в данном описании на «одно воплощение» или «воплощение» означает, что конкретный признак, структура или характеристика, описанные в связи с данным воплощением, включены, по меньшей мере, в одно из воплощений настоящего изобретения. Таким образом, фразы «в одном воплощении» или «в воплощении» в различных местах данного описания не обязательно относятся к одному и тому же воплощению, но могут и относиться. Кроме того, конкретные признаки, структуры или характеристики могут сочетаться любым подходящим способом, понятным для специалиста в данной области техники, в одном или нескольких воплощениях. Кроме того, в то время как некоторые воплощения, описанные здесь, включают некоторые признаки, не включенные в другие воплощения, сочетания особенностей различных воплощений предназначены, чтобы находиться в пределах объема настоящего изобретения, и образуют различные воплощения, понятные для специалистов в данной области техники. Например, в следующей формуле изобретения любое из заявленных воплощений может быть использовано в любом сочетании.
В первом аспекте настоящее изобретение представляет собой соединение формулы (5):
или его таутомер, рацемат или стереоизомер,
где n является целым числом от 0 до 5, а X выбран из C1-6алкила, C1-6галогеналкила, C2-6алкенила, C2-6алкинила, галогена, гидроксила, C1-6алкокси или амино; и R11 является гидроксилом или амино.
В конкретных воплощениях n является 0, 1, 2, 3, 4 или 5. В предпочтительных воплощениях n является 0, 1 или 2, предпочтительно, 0 или 1. В некоторых воплощениях n является 0, 1 или 2, а X выбран из C1-6алкила, C1-6галогеналкила, галогена, гидроксила, C1-6алкокси или амино. В определенных воплощениях n является 0.
В формуле (5) символ «*» указывает на стереогенный центр. Конкретные стереоизомеры (R или S конфигурации) соединений формулы (A) относятся к разделенным энантиомерам соединений по одному или более из этих конкретных стереогенных центров. Соответственно, термин «стереоизомерно чистый», используемый по отношению к соединениям формулы (5), означает, что соединения формулы (5) являются стереохимическими чистыми по одному или более стереогенному центру, обозначенному символом «*». Если группа X включает стереогенный центр, она может иметь R, S или RS конфигурацию, если не указано иное.
В частных воплощениях соединения формулы (5) по настоящему изобретению являются стереоизомерно чистыми. В определенных воплощениях соединение формулы (5) может быть соединением формулы (5′) или (5′′):
В формуле (5′) и (5′′) символ «*» указывает на стереогенный центр, который может иметь R, S или RS конфигурацию.
В следующем аспекте настоящее изобретение представляет собой способ получения соединения формулы (5), либо его таутомера, рацемата или стереомера, включающий стадию превращения группы -COR12 соединения формулы (4) с образованием соединения формулы (5);
где R12 является -OR3 или амино, а R3 выбран из C1-6алкила, C6-10арила, C6-10арилС1-6алкилена, C6-10галогенарила, C1-6галогеналкила или C6-10галогенарилС1-6алкилена.
В некоторых воплощениях получение указанного соединения формулы (4) включает реакцию соединения формулы (2) с соединением формулы (3):
с образованием соединения (4a)
где R19 является -OR23 и R23 выбран из C1-6алкила, C6-10арила, C6-10арилС1-6алкилена, C6-10галогенарила, C1-6галогеналкила или C6-10галогенарилС1-6алкилена, а R4 и R5 независимо выбраны из C6-10арилС1-6алкилена или C6-10арила.
В дополнительном воплощении способ дополнительно включает стадию превращения сложноэфирной группы соединения (4a) в амидную группу с образованием соединения формулы (4b)
где X и n имеют те же значения, что описаны выше.
Соединения формул (5), (5′) или (5′′) особенно ценны в качестве предшественников в синтезе соединений формул (A), (A′) или (A′′), как описано ниже.
В следующем аспекте настоящее изобретение представляет собой способ получения соединения формулы (A):
или его таутомера, рацемата, стереоизомера, фармацевтически приемлемой соли, гидрата или сольвата,
где B выбран из группы, состоящей из пуринила, пиримидила, или их аза или деаза аналогов, или -NR1 R2; при этом каждая группа необязательно замещена одним или более заместителем, независимо выбранным из галоген, амино, гидроксила, C1-6алкила, аминоС1-6алкил, нитро, формамидо, -NHR18, или OR7; и где углеродный атом указанного пуринила или пиримидила может быть окислен с образованием С=O, где R7 выбран из C1-4алкила, C6-10арилС1-6алкилена или C6-10арила, R18 выбран из C6-10арилС1-6алкилена, C1-6алкилкарбонила, галогенС1-6алкилкарбонила, C1-6алкилоксикарбонила, 9-флуоренметилоксикарбонила или C6-10арилС1-6алкилоксикарбонила; и
R1 выбран из водорода, C6-10арила, C6-10арилС1-6алкилена, C1-4алкила, C6-10галогенарила, C1-4галогеналкила или C6-10галогенарилС1-6алкилена;
R2 выбран из C6-10арила, C6-10арилС1-6алкилена, C1-4алкила, C6-10галогенарила, C1-4галогеналкила или C6-10галогенарилС1-6алкилена;
В отдельных воплощениях R18 выбран из 9-флуоренилметилоксикарбонила, трет-бутилоксикарбонила, бензилоксикарбонила, метилкарбонила, бензила и трифенилметила.
В частных воплощениях B представляет собой пуринил или производное пуринила, предпочтительно связанное через положение 9 пуринового кольца, пиримидил или производное пиримидила, либо их аза и/или деаза аналоги. В аза аналогах, по меньшей мере, один из атомов углерода в B замещен атомом азота; в деаза аналогах, по меньшей мере, один из атомов азота в B замещен атомом углерода. Комбинации таких замещений также включены в объем настоящего изобретения.
Предпочтительными производными пуринила являются аденил, гуанил, 2-амино-6-хлорпуринил, 2-аминопуринил, 2,6-диаминопуринил, ксантил или гипоксиксантил. Предпочтительными производными пиримидила являются тиминил, урацил и цитозинил. Соответственно, в частных воплощениях В выбран из группы, включающей пуринил, аденил, гуанил, 2-амино-6-хлорпуринил, 2-аминопуринил, 2,6-диаминопуринил, ксантил или гипоксиксантил, пиримидил, тиминил, урацил и цитозинил.
В определенных воплощениях B представляет собой 2-амино-6-хлорпуринил или гуанил.
Соединение формулы (A) может находиться в как в сольватированной, так и в несольватированной форме. Термин «сольват» употребляется здесь для описания молекулярного комплекса, включающего соединение (A) и стехиометрическое количество одной или более молекул фармацевтически приемлемого растворителя, например, этанола. Термин «гидрат» употребляется, когда указанным растворителем является вода.
В формуле (A) символ «*» указывает на стереогенный центр. Специфические стереоизомеры (R или S конфигурации) соединений формулы (A) относятся к разделенным энантиомерам соединений по этим конкретным стереогенным центрам. Соответственно, термин «стереоизомерно чистый», используемый по отношению к соединениям формулы (A), означает, что соединения формулы (A) являются стереохимическими чистыми по стереогенным центрам, обозначенным символом «*». Если группа В содержит стереогенный центр, она может иметь R, S или RS конфигурацию, если не указано иное.
В конкретных воплощениях соединение формулы (A), являющееся 2-амино-9[[(1S,2R)-1,2-бис(гидроксиметил)циклопропил]метил]-1,9-дигидро-6H-пурин-6-оном, представлено формулой (Ac′).
Настоящее изобретение также включает способ получения соединения формулы (A)
или его таутомера, рацемата, стереоизомера, фармацевтически приемлемой соли, гидрата или сольвата,
где В выбран из группы, состоящей из пуринила, пиримидила или их аза или деаза аналогов, или -NR1R2; при этом каждая группа необязательно замещена одним или более заместителями, независимо выбранными из галогена, амино, гидроксила, C1-6алкила, аминоС1-6алкила, нитро, формамидо, -NHR18, или OR7; и где углеродный атом вышеупомянутого пуринила или пиримидила может быть окислен с образованием C=O, где R7 выбран из C1-4алкила, C6-10арилС1-6алкилена или C6-10арила, R18 выбран из C6-10арилС1-6алкилена, C1-6алкилкарбонила, галогенС1-6 алкилкарбонила, C1-6алкилоксикарбонила, 9-флуоренилметилоксикарбонила, или C6-10арилС1-6алкилоксикарбонила; и
R1 выбран из H, C6-10арила, C6-10арилС1-6алкилена, C1-4алкила, C6-10галогенарила, C1-4галогеналкила или C6-10галогенарилС