Средство против грибковых инфекций
Иллюстрации
Показать всеИзобретение относится к медицине, ветеринарии, растениеводству и промышленности и предназначено для борьбы с грибковой инфекцией. Средство против грибковых инфекций представляет собой соли 2,4-диоксо-5-(2-гидрокси-3,5-дихлорбензилиден)амино-6-метил-1,3-пиримидина
R-4-NO2, 2-OH-5-NO2, 2-OH-3,5-Cl2, 5-Br-4-OH-3-OCH3, 2-ОН-5-Cl, 2,4-Cl2, 3,5-Br2-2-OH.
Использование изобретения обеспечивает эффективное средство против грибковых инфекций широкого спектра действия с высокой растворимостью. 3 табл., 5 пр.
Реферат
Изобретение относится к средствам для борьбы с грибковой инфекцией и может быть использовано для лечения заболеваний, вызванных грибами, а также в сельском хозяйстве ветеринарии и предотвращения порчи грибами различных материалов.
Лечение грибковых инфекций остается нерешенной, серьезной проблемой современной медицины, ветеринарии, растениеводства и промышленности. Это объясняется недостаточной эффективностью известных препаратов и быстрой изменчивостью микробов, приводящей к появлению устойчивых форм, Fidel P.L. Jr, Vazquez J.A., Sobel J.D. Candida glabrata: review of epidemiology, pathogenesis and clinical disease with comparison to C.albicans 1999, 1: 80-96. White T. Antifungal drug resistance in Candida albicans ASM News 8: 427-433.
Известен ряд препаратов для лечения грибковых заболеваний: нистатин, амфотерицин В, флюконазол, тербинафин (Dixon DM, Walsh TJ. Antifungal Agent http://www.ncbi.nlm.nih.gov/books/NBK8263/?report=reader).
Каждый из них имеет существенные недостатки. Флюконазол проявляет, главным образом, фунгистатический эффект и практически не обладает фунгицидными свойствами [Pharmaceutical microbiology. Ed. by W.B. Hugo and A.D. Rassel Blackwell Scientific Publications, Oxford, 1987, 511 p]. Указанное выше затрудняет использование этих препаратов для лечения людей с ослабленной иммунной системой. Флюконазол также может применяться для предотвращения порчи грибами растений и сельскохозяйственных продуктов. Известно также применение флюконазола в архивном деле для обработки бумаги.
Главным недостатком нистатина является низкая активность против многоклеточных грибов.
Амфотерицин В является активным противогрибковым препаратом, однако он весьма токсичен и вызывает ряд серьезных побочных эффектов.
Все эти препараты используются много лет и к ним сформировалась устойчивость у различных бактерий (A. Kanafani1 J.R. Perfect2Resistance to Antifungal Agents: Mechanisms and Clinical Impact Clinical Infectious Diseases 2008: 46 120-126).
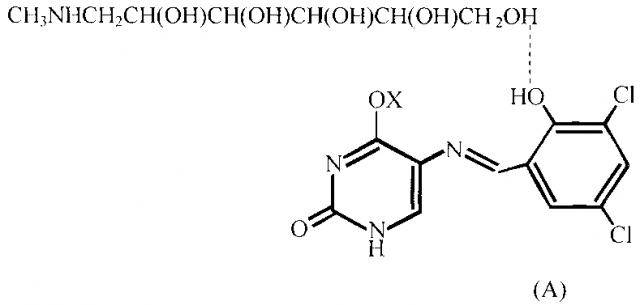
Известно фунгицидное средство, представляющее собой ассоциат соли 5-[3,5-дихлор-2-гидроксибензилиден)амино]-4-гидрокси-1H-пиримидин-2-она с 1,2,3,4,5-пентагидрокси-6-метиламиногексаном
где , RU 2525911 C1, опубл. 20.08.2014.
Данное техническое решение принято в качестве прототипа настоящего изобретения.
Препарат обладает выраженной противогрибковой активностью широкого спектра действия.
Однако это вещество плохо растворяется как в водной среде, так и в жирах. Растворимость известного препарата в воде составляет не более 0,4%, а в масляных растворах - до 0,3%. Недостаточная растворимость фунгицидного средства-прототипа не позволяет получать стабильные растворы, пригодные для практического использования. Вместе с тем, чрезвычайно актуальна задача повышения эффективности использования фунгицидного препарата в виде растворов для применения в медицине и ветеринарии в форме ингаляций и инъекций, а также для обработки различных материалов и сельскохозяйственных продуктов.
Задачей настоящего изобретения является создание эффективного средства против грибковых инфекций широкого спектра действия с более высокой растворимостью.
Согласно изобретению поставленная задача решается путем синтеза фунгицидного средства, которое представляет собой соли 2,4-диоксо-5-(2-гидрокси-3,5-дихлорбензилиден)амино-6-метил-1,3-пиримидина
R-4-NO2, 2-OH-5-NO2, 2-OH-3,5-Cl2, 5-Br-4-OH-3-OCH3, 2-OH-5-Cl,2,4-Cl2, 3,5-Br2-2-OH.
Значения R указаны в табл. 1.
Структура полученных соединений была доказана спектрами протонного магнитного резонанса и ИК-спектроскопии.
Целевые соли 2,4-диоксо-5-арилиденамино-6-метил-1,3-пиримидина получаются взаимодействием натриевой соли 5-амино-6-метилурацила с ароматическими альдегидами. В качестве растворителя использована смесь этанол-вода 3:1. Продукты получались с выходами выше 80% от теоретического. Индивидуальность целевых соединений доказана методом тонкослойной хроматографии: система элюентов - хлороформ-ацетон 3:1. Температуры плавления продуктов - свыше 300°C.
Пример 1: Синтез натриевой соли 2,4-диоксо-5-(4-нитробензилиден)амино-6-метил-1,3-пиримидина (I-1).
В колбу поместили 0.5 г 5-амино-6-метилурацила, 0.5 мл 50%-ного раствора едкого натра. Смесь нагревали при перемешивании до полного растворения исходного вещества. Параллельно в 0.18 мл этанола растворили 0.6 г 4-нитробензальдегида и добавили его к раствору 5-амино-6-метилурацила, при этом в колбе начинал выпадать осадок бордово-красного цвета. Затем реакционную массу перемешивали в течение 30 минут и охладили. Полученный осадок отфильтровали, промыли этанолом и высушивали. Выход продукта составил 83% от теоретического.
Пример 2: Синтез натриевой соли 2,4-диоксо-5-(2-гидрокси-3,5-дихлорбензилиден)амино-6-метил-1,3-гшримидина (I-3).
В реакционную колбу поместили 1.41 г 5-амино-6-метилурацила и 0.4 г едкого натра в 10 мл воды. Смесь нагревали до полного растворения исходного урацила. Одновременно растворили 1.91 г 3,5-дихлорсалицилового альдегида в 30 мл этанола и полученный раствор при перемешивании по каплям прибавили к раствору натриевой соли 5-амино-6-метилурацила. Реакционную массу при перемешивании нагревали в течение 1 ч, затем охлаждали до комнатной температуры и образовавшийся осадок отфильтровывали, промывали этанолом и высушивали. Выход целевого продукта составил 2.86 г (85%).
Пример 3. Лечение заболеваний дыхательных путей.
Исследования проводили на белых беспородных мышах (самки, 6-8 нед.), «Рапполово» (Ленинградская обл.), период карантина составил 2 недели.
Для воспроизведения аспергиллезной пневмонии мыши, в целях создания иммунодефицита, получали однократно внутрибрюшинно раствор циклофосфана (150 мг/кг). Через трое суток мышам вводили однократно внутрибрюшинно раствор гидрокортизона (250 мг/кг). Через сутки после введения гидрокортизона мышей интраназально под эфирным наркозом инфицировали суспензией Aspergillus niger (приблизительно 3×107 кл/мл).
На 5 сутки после инфицирования по 5 животных из каждой группы брали для изучения микробного обсеменения легких (эвтаназию у грызунов осуществляли передозировкой эфира). Из тканей легких готовили гомогенаты, в которых определяли титр грибов рода Aspergillus. Наблюдение за оставшимися мышами проводили в течение 14 суток после инфицирования для учета смертности.
Испытуемые растворы вводили в аэрозольной камере.
В эксперименте были сформированы следующие группы животных:
1 - контроль распыления (К) 3 одинаковые группы (К1, Л2, К3). Животные, инфицированные Aspergillus и получающие аэрозоль изотонического раствора хлорида натрия.
2 - Ассоциат соли 5-[3,5-дихлор-2-гидроксибензилиден)амино]-4-гидрокси-1H-пиримидин-2-она с 1,2,3,4,5-пентагидрокси-6-метиламиногексана -3 одинаковые группы (Е1-3). Животные, инфицированные Aspergillus и получающие аэрозоль 0,1% исследуемого препарата.
3. Водный раствор вещества I-1
4. Водный раствор вещества I-2
5. Водный раствор вещества I-3
6. Водный раствор вещества I-4
7. Водный раствор вещества I-5
8. Водный раствор вещества I-6
9. Водный раствор вещества I-7.
Постановка эксперимента.
Животных помещали в аэрозольные камеры (12 л) сроком на 30 минут, в течение которых через легкие проходит 500 мл воздуха.
В качестве генератора аэрозоля использовали ультразвуковой (УЗ) распылитель «OMRON U1» (Япония). Для поддержания постоянной концентрации аэрозоля препарата в объеме камеры использовали импульсный режим распыления с помощью вихревого пневматического генератора, получая стойкий аэрозоль с размером частиц 3 мкм. Животных помещали в иммобилизационные контейнеры и экспонировали с полученным аэрозолем в течение 30 минут раз 1 в сутки в течение 3 дней, начиная с 1 суток после инфицирования.
Результаты.
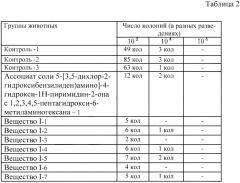
Из образцов гомогенизированных тканей легкого готовили ряд последовательных разведений с последующим высевом на среду Сабуро. Полученные результаты приведены в таблице 2.
Таким образом, в использованных условиях наиболее эффективным противогрибковым препаратом оказалось Вещество I-3.
Пример 4. Кандидамикоз млекопитающих, вызванный Candida albicans.
Кроликов заражали внутрикожно взвесью 48-часовой культуры Candida albicans в дозе 10.000 клеток гриба в 500 мкл 0.9% раствора хлорида натрия. Через 7-10 дней у части животных на месте введения наступало изъязвление, их использовали для эксперимента.
Для исследования были приготовлены масляный (оливковое масло) 0,1% раствор ассоциата соли 5-[3,5-дихлор-2-гидроксибензилиден)амино]-4-гидрокси-1Н-пиримидин-2-она с 1,2,3,4,5-пентагидрокси-6-метиламиногексана и вещество I-3.
В качестве контроля использована стерильная вода.
Продолжительность лечения составила 7 дней, начиная с 1-го дня после изъязвления. Препараты наносили ватным тампоном 2 раза в сутки - утром и вечером.
Критерием микологической излеченности считали отсутствие дрожжевой и мицелиальной форм Malassezia, а критерием полной излеченности - рубцевание очага поражения к 7 дню.
Результаты приведены в таблице 3.
Таким образом, положительный эффект достигнут только при использовании Вещества I-3.
Пример 5. Лечение грибковых поражений растений.
Изучение проведено на бегонии клубневой (Begonia tuberosa hybridum, зараженной мучнистой росой. Мучнистая роса поражает многие растения, в том числе деревья и кустарники. Мучнистая роса поражает хризантемы, бегонии, розы, при этом на зеленых частях растений появляется белый, порой темнеющий, налет. Болезнь передается спорами по воздуху.
Испытуемые растения были заражены спорами гриба (Leveillula tauricd) и выдерживали до появления на листьях белого налета. Заражены были 3 листа на каждом растении. После появления налета растения контрольной группы (3 растения) изолировали от 3-х растений, получавших терапию в виде обработки спреем, представляющим собой водный раствор вещества I-3. Обработку проводили однократно в течение 3 и 7 дней. После завершения обработки наблюдение за растениями было продолжено еще в течение 3-х недель. В ходе наблюдения у контрольных растений зарегистрировано увеличение количества налета, представляющего собой мицелий гриба, и количество пораженных листьев увеличилось, в среднем, до 7-8, при этом налет покрывал и стебли растения. У растений, обработанных испытуемым веществом, увеличение и распространение гриба на другие части растения не происходило. При смыве с листа и посеве на питательную среду роста грибов не зарегистрировано.
Средство против грибковых инфекций, представляющее собой соли 2,4-диоксо-5-(2-гидрокси-3,5-дихлорбензилиден)амино-6-метил-1,3-пиримидина R-4-NO2, 2-OH-5-NO2, 2-OH-3,5-Cl2, 5-Br-4-OH-3-OCH3, 2-ОН-5-Сl, 2,4-Сl2, 3,5-Br2-2-ОН.