Душистые n, n-ди(трет-бутил)биспидин-9-оны
Иллюстрации
Показать всеИзобретение относится к новым душистым N,N-ди(трет-бутил)биспидин-9-онам формулы
где n равно 0 или 1. Изобретение обеспечивает расширение арсенала душистых веществ, которые, в частности, могут использоваться в парфюмерных композициях. 2 пр.
Реферат
Изобретение относится к области органической химии, а конкретно к ранее неизвестным душистым производным N,N-ди(трет-бутил)биспидин-9-онам.
Душистые кетоны, например, такие как 4-фенилбутан-2-он (жасмарол) и его производное 4-(4-метоксифенил)бутан-2-он (анизилацетон), являются природными душистыми веществами [М. Meier, В. Kohlenberg, N.A. Braun. Isolation of Anisyl Acetone from Agarwood Oil // Journal of Essential Oil Research, 2003, Vol. 15, pp. 54-56; Food and Cosmetics Toxicology, 1979, Vol. 17, p. 857], выполняют функцию феромонов [Vargas R.I. et al. Recent Advances in Methyl Eugenol and Cue-Lure Technologies for Fruit Fly Detection, Monitoring, and Control in Hawaii // Vitamins and Hormones, 2010, Vol. 83, pp. 575-595] и могут быть использованы как инсектициды [Barthel W.F. et al. Anisyl acetone, synthetic attractant for male melon fly // Journal of Science, 1957, Vol. 126, p. 654].
Встраивание молекул душистых кетонов в структуру биспидина приводит к усилению их полезных свойств и придает им дополнительные полезные свойства, присущие биспидину. Производные биспидина и его аналоги обладают анальгетической [Smith G.S. et al. A study of the synthesis and antiarrhythmic properties of selected 3,7-diheterabicyclo[3.3.1]nonanes with substituents at the 2,4-positions and at the 9-position // European Journal of Medicinal Chemistry, 1990, Vol. 25, pp. 1-8], нейротрофической [Siener T. Et al. Synthesis and opioid receptor affinity of a series of 2,4-diaryl-substituted 3,7-diazabicylononanones // Journal of Medicinal Chemistry, 2000, Vol. 43, pp. 3746-3751], кардиоваскулярной активностью и могут использоваться в качестве сердечно-сосудистых лекарств [Garrison G.L. et al. Novel 3,7-Diheterabicyclo[3.3.1]nonanes That Possess Predominant Class III Antiarrhythmic Activity in 1-4 Day Post Infarction Dog Models: X-ray Diffraction Analysis of 3-[4-(1H-Imidazol-1-yl)benzoyl]-7-isopropyl-3,7-diazabicyclo[3.3.1]nonane Dihydroperchlorate // Journal of Medicinal Chemistry, 1996, Vol. 39, pp. 2559-2570].
Из уровня техники известен способ получения производных биспидин-9-она [Патент RU 2472793 С1 «1,5-бис[(трет-бутиламино)метил]-N,N′-ди-трет-бутилбиспидин-9-он и способ его получения», опубл. 20.01.2013]. Однако в указанном патенте приведен синтез производных биспидина с двумя заместителями в узловых 5 и 7 положениях.
Наиболее близким техническим решением является синтез N,N′-ди(трет-бутил)биспидин-9-онов [Кузнецов A.И., Сенан И.М., Серова Т.М. Синтез N,N′-ди(трет-бутил)биспидин-9-онов // Известия академии наук. Серия химическая, 2012, №2, С. 307-311].
Однако указанные вещества синтезированы не из душистых кетонов и поэтому не являются душистыми веществами.
Техническим результатом настоящего изобретения является расширение арсенала душистых веществ.
Технический результат заявленного изобретения достигается новыми душистыми 3,7-ди(трет-бутил)-1-{[(трет-бутил)амино]метил}-биспидин-9-онами,
которые могут использоваться в парфюмерных композициях, в качестве субстанций лекарственных средств и как стартовые вещества для получения новых производных биспидина и 1,3-диазаадамантана [Кузнецов А.И, Сенан И.М., Серова Т.М. Синтез N,N′-ди(трет-бутил)биспидин-9-онов // Известия академии наук. Серия химическая, 2014, №12, С. 2689-2692].
Согласно настоящему изобретению заявлены:
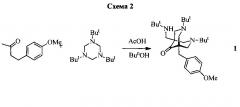
3,7-ди(трет-бутил)-1-{[(трет-бутил)амино]метил}-5-(4-метоксибензил)-3,7-диазабицикло[3.3.1]нонан-9-он (1), и
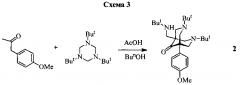
3,7-ди(трет-бутил)-1-{[(трет-бутил)амино]метил}-5-(4-метоксифенил)-3,7-диазабицикло[3.3.1]нонан-9-он (2).
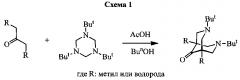
Заявленные душистые N,N-ди(трет-бутил)биспидин-9-оны получают путем конденсации душистых кетонов с 1,3,5-три-(трет-бутил)-1,3,5-триазациклогексаном при нагревании в спирте в присутствии уксусной кислоты, реакцию ведут при нагревании в этаноле или другом спирте, полученный продукт экстрагируют после конденсирования реакционной массы под вакуумом горячим толуолом и перекристаллизовывают из этилового спирта.
Строение полученных соединений доказано данными элементного анализа и совокупностью ИК-, ЯМР 1Н-, и масс-спектров.
Предлагаемое изобретение иллюстрируется следующими примерами.
Пример 1
Получение 3,7-ди(трет-бутил)-1-{[(трет-бутил)амино]метил}-5-(4-метоксибензил)-3,7-диазабицикло[3.3.1]нонан-9-она (1). Раствор 1.78 (10 ммоль) 4-(4-метоксифенил)-2-бутанона и 5.11 г (20 ммоль) 1,3,5-три(трет-бутил)-1,3,5-триазациклогексана и 3.00 г (50 ммоль) уксусной кислоты (АсОН) в 25 мл этилового спирта (EtOH) нагревали при кипении 5 ч. Реакционную массу упаривали, нейтрализовали K2CO3 до pH=10 и экстрагировали кипящим толуолом (3 раза по 15 мл). Растворитель отгоняли, остаток перекристаллизовали из EtOH. Выход: 6.50 г (67%), кристаллы белого цвета. Тпл., °С: 94-96 (EtOH). ИК, ν/см-1: 12555, 1046 (ОСН3), 1611 (Ar), 1713 (C=O), 3350 (NH). ЯМР 1Н (CDCl3), (δ, м.д., J/Гц): 1.02 (с, 18 Н, 2 (CH 3)3CN); 1.08 (с, 9 Н, (CH 3)3CNH); 1.19 (с, 1 Н, NH); 2.55 (с, 2 Н, CH 2NH); 2.66, 2.93 (оба д, 4 Н, 2NCH 2C, J=10.3); 2.75 (с, 2 Н, CH 2Ar); 2.69-2.97 (м, 4 Н, 2 NCH 2C); 3.80 (с, 3 Н, СН 3О); 6.81, 7.09 (оба д, 4 Н, Ar, J=8.1). ЯМР 13С (CDCl3), (δ, м.д.): 217,65 СО(9), 158.06, 131.70, 130.26, 113,52 Ar, 56.01 (С(4), С(6)), 55.59 (С(2), С(8)), 55.30 (ОСН3), 53.60 (3,7-C-N), 50.70 C-NH, 50.24 С(1), 50.04 С(5), 46.14 CH2NH, 38.01 (1-CH2Ph), 29.16 (NHC(CH3)3), 26.67 (2С(СН3)3). Масс-спектр, m/z (Iотн. (%)): 457 [М]+ (55), 439 (100), 400 (7), 384 (12), 336 (30), 357 (16), 327 (70), 285 (27), 228 (23), 121 (55), 100 (25), 57 (40), 41 (15). Найдено, (%): С, 73.69; Н, 10.18; N, 9.23. C28H47N3O2 Вычислено, (%): С, 73.48; Н, 10.35; N, 9.18.
Пример 2
Получение 3,7-ди(трет-бутил)-1-{[(трет-бутил)амино]метил}-5-(4-метоксифенил)-3,7-диазабицикло[3.3.1]нонан-9-она (2). Раствор 1.64 (10 ммоль) 4-(4-метоксифенил)-2-пропанона и 5.11 г (20 ммоль) 1,3,5-три(трет-бутил)-1,3,5-триазациклогексана и 3.00 г (50 ммоль) АсОН в 25 мл EtOH нагревали при кипении 5 ч. Реакционную массу упаривали, нейтрализовали K2CO3 до рН=10 и экстрагировали кипящим толуолом (3 раза по 15 мл). Растворитель отгоняли, остаток перекристаллизовали из EtOH. Выход, %: 5.80 г (66%), кристаллы белого цвета. Т.пл, °С: 80-82 (EtOH). ИК, ν/см-1: 1257, 1042 (ОСН3), 1610 (Ar), 1722 (C=О), 3336 (NH). ЯМР 1Н (CDCl3), (δ, м.д., J/Гц): 1.07 (с, 9 Н, (CH 3)3CNH); 1.18 (с, 18 Н, 2 (CH 3)3CN); 1.25 (с, 1 Н, NH); 2.58 (с, 2 Н, CH 2NH); 2.92, 3.58 (оба д, 4 Н, 2NCH 2C, J=10.3); 3.06-3.12 (м, 4 Н, 2NCH 2C); 3.81 (с, 3Н, CH 3O); 6.90, 7.20 (оба д, 4 Н, Ar, J=8.8). ЯМР 13С (CDCl3), (δ, м.д.): 215.80 СО(9), 158.04, 136.13, 127.83, 113,38 Ar, 57.99 (С(4), С(6)), 56.00 (С(2), С(8)), 55.28 (ОСН3), 55.20 С(1), 53.94 (3,7-C-N), 53.76 С(5), 49.99 C-NH, 46.62 CH2NH, 29.10 (NHC(CH3)3), 26.75 (2С(СН3)3). Масс-спектр, m/z (Iотн. (%)): 443 [М]+ (38), 425 (100), 370 (10), 343 (22), 331 (68), 271 (85), 25718), 216 (48), 186 (18), 121 (20), 100 (75), 57 (78), 41331 (68), 271 (85), 257 (18), 216 (48), 186 (18), 121 (20), 100 (75), 57 (78), 41 (34). Найдено, (%): С, 73.24; Н, 10.07; N, 9.56 C27H45N3O2 Вычислено, (%): С, 73.09; Н, 10.22; N, 9.47.
Синтезированные 3,7-ди(трет-бутил)-1-{[(трет-бутил)амино]метил}-биспидин-9-оны обладали тем же запахом, что и душистые кетоны, используемые при их получении.
Таким образом, предлагаемое изобретение позволяет получить ранее неизвестные душистые производные N,N-ди(трет-бутил)биспидин-9-она, которые могут найти применение в парфюмерии и в качестве промежуточных продуктов при разработке лекарств различного назначения.
Душистые N,N-ди(трет-бутил)биспидин-9-оны, имеющие структуру где n равно 0 или 1.