Способы и композиции для лечения вич-ассоциированной диареи
Иллюстрации
Показать всеНастоящая группа изобретений относится к медицине, а именно к вирусологии и гастроэнтерологии, и касается лечения ВИЧ-ассоциированной диареи. Для этого вводят крофелемер в суточной дозе от 250 до 1000 мг. Это обеспечивает эффективное лечение диареи у данной группы больных, а также уменьшение побочных эффектов за счет использования препарата в низких дозах. 7 н. и 20 з.п. ф-лы, 23 табл., 3 ил., 10 пр.
Реферат
Родственные заявки
По данной заявке испрашивается приоритет согласно предварительной заявке 61/408, 622, поданной 31 октября 2010; предварительной заявке США 61/409,335, поданной 2 ноября 2010; предварительной заявке США 61/416,249, поданной 22 ноября 2010 и предварительной заявке США 61/434, 379, поданной 19 января 2011 года. Все содержание каждой из этих заявок включено в настоящее описание посредством ссылки.
Уровень техники
Диарея остается важной проблемой для ВИЧ-инфицированных субъектов в эпоху высокоактивной антиретровирусной терапии (ВААРТ), негативно сказывающейся на качестве жизни, несмотря на широкое использование антидиарейных препаратов. Причин тому множество и они включают ВИЧ-энтеропатию, чрезмерное развитие нетипичных микробных агентов, злокачественность распространенных кишечных патогенов и побочные эффекты собственно ВААРТ терапии (Kartalija 1999).
В то время как определения и способы отчетности меняются, установлено, что около половины всех ВИЧ-СПИД субъектов имеют диарею в какой-то момент во время их болезни. Хотя заболеваемость диареей не изменялась в течение внедрения ВААРТ, этиологии диареи значительно изменилась с ростом неинфекционных причин и снижения оппортунистических инфекционных заболеваний.
Лечение диареи поможет в повышении общей эффективности противовирусной лекарственной терапии, а также качества жизни, и контроля потери массы у ВИЧ-положительных больных. Диарея может привести к снижению приверженности антиретровирусному лечению и/или привести к необходимости переключения АРВ схем. Диарея также сопровождается снижением уровня антиретровирусных лекарственных препаратов, что подтверждает, что адекватное лечение улучшит абсорбцию АРВ препаратов. На популяционном уровне соблюдение режима лечения лекарственными препаратами и поддержание адекватного уровня АРВ важны для минимизации развития лекарственно устойчивых штаммов вируса. Таким образом, ассоциированная с лекарственными препаратами диарея у ВИЧ-положительных больных представляет собой важную и неудовлетворенную клиническую потребность, требующую более эффективного тактики ведения. В настоящее время предписанное лечение эффективно только частично или осложняется нежелательными побочными эффектами, такими как запор и возможностью привыкания. Разработка лекарственного средства для лечения ВИЧ-ассоциированной диареи с низким потенциалом для лекарственного взаимодействия, влияния на метаболизм лекарственных препаратов или аддиктивного потенциала, могла бы привести значительной пользе для ВИЧ-инфицированных субъектов.
Сущность изобретения
В настоящем изобретении описываются способы профилактики, облегчения и/или лечения диареи. В одном из вариантов представленные в настоящем изобретении способы предотвращают, облегчают или лечат ВИЧ-ассоциированную диарею и диарею, ассоциированную с высокоактивной антиретровирусной терапией (ВААРТ).
В одном аспекте, представленном в настоящем изобретении, способы лечения ВИЧ-ассоциированной диареи или диареи, ассоциированной с высокоактивной антиретровирусной терапией (ВААРТ) у ВИЧ-инфицированного субъекта, включают введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение около 500 мг в день; введение около 1000 мг в день; введение около 125 мг два раза в день; введение около 250 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном аспекте в настоящем изобретении представлены способы лечения консистенции испражнений у ВИЧ-инфицированного субъекта, включающие введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение около 500 мг в день; введение около 1000 мг в день; введение около 125 мг два раза в день; введение около 250 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном аспекте в настоящем изобретении представлены способы улучшения консистенции испражнений у ВИЧ-инфицированного субъекта, включающие введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение около 500 мг в день; введение около 1000 мг в день; введение около 125 мг два раза в день; введение около 250 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном аспекте в настоящем изобретении представлены способы облегчения водянистой диареи у ВИЧ-инфицированного субъекта, включающий введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение около 500 мг в день; введение около 1000 мг в день; введение около 125 мг два раза в день; введение около 250 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном аспекте в настоящем изобретении представлены способы снижения количества испражнений в день у ВИЧ-положительных субъекта, включающий введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение около 500 мг в день; введение около 1000 мг в день; введение около 125 мг два раза в день; введение около 250 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном варианте осуществления введение происходит между около 1 месяца и около 5 месяцев. В одном варианте осуществления введение происходит между около 1 месяца и около 6 месяцев. В одном варианте осуществления введение происходит около 6 месяцев. В другом варианте осуществления введение происходит 6 или более месяцев.
В одном варианте осуществления введение происходит от около 3 дней до 5 месяцев. В одном варианте осуществления введение происходит от около 3 дней до 6 месяцев.
В одном варианте осуществления улучшение симптомов начинается на 3 день.
В одном варианте осуществления улучшение симптомов увеличивается с более длинной продолжительностью введения после 3 дня.
В одном из вариантов осуществления, субъект европеоид или имеет латиноамериканское происхождение.
В одном варианте осуществления крофелемер вводят в течение 8 дней.
В одном варианте осуществления крофелемер вводят от промежутка между 8 и 24 неделями до промежутка от 8 дней до 26 недель.
В одном варианте осуществления субъект считается вылеченным, если субъект демонстрирует уменьшение количества испражнений в день на одно или более, уменьшение количества водянистых испражнений в день, улучшение ежедневной оценки боли или дискомфорта в животе, улучшение ежедневной оценки консистенции испражнений, улучшение оценки консистенции испражнений (от водянистого к сформированному), уменьшение числа дней в неделю, в которые субъекты испытывают неотложные позывы к дефекации, уменьшение числа дней в неделю, в которые субъекты испытывают недержание кала, или уменьшение незапланированных визитов по поводу значительного ухудшения диареи.
В одном варианте осуществления субъект считается вылеченным, если субъект демонстрирует улучшение оценки для ежедневной консистенции испражнений.
В одном варианте осуществления субъект считается вылеченным, если субъект демонстрирует снижение консистенции испражнений.
В одном варианте осуществления субъект считается вылеченным, если субъект демонстрирует уменьшение количества водянистых испражнений за день.
В одном варианте осуществления субъект считается вылеченным, если субъект демонстрирует снижение количества испражнений за день.
В одном варианте осуществления, увеличение или уменьшение симптомов измеряется от исходного уровня.
В одном варианте осуществления введение происходит в течение около 5 месяцев. В другом варианте осуществления введение происходит в течение около 6 месяцев.
В одном варианте осуществления введение происходит около 5 месяцев или дольше. В другом варианте осуществления введение происходит около 6 месяцев или дольше.
В одном варианте осуществления введение происходит в течение продолжительности ВИЧ-инфекции.
В одном варианте осуществления ответ на лечение увеличивается после того, как крофелемер вводили в течение более 4 месяцев.
Другие варианты осуществления раскрыты ниже.
Краткое описание чертежей
На Фиг.1 показаны субъекты с клиническим ответом в перекрестном исследовании фазы без плацебо-контроля на выборке для оценки безопасности.
На Фиг.2 показаны субъекты с ответом по консистенции испражнений в перекрестном исследовании фазы без плацебо-контроля на выборке для оценки безопасности.
На Фиг.3 изображен анализ подгруппы, показывающий разницу в результатах лечения в процентах субъектов, ответивших на лечение (крофелемер 125 мг два раза сутки в сравнении с плацебо) с соответствующими доверительными интервалами и p-величинами.
Подробное описание изобретения
Раскрытые в настоящем изобретении способы включал и введение эффективных количеств проантоцианидиновых полимеров, например, крофелемера, субъектам, например, с ВИЧ-ассоциированной диареей или с диареей, ассоциированной с высокоактивной антиретровирусной терапией (ВААРТ).
Проантоцианидины представляют собой группу конденсированных танинов. Сырые экстракты из лекарственных растений, например, Pycanthus angolenis и Baphia Nitida, как было показано, обладают антидиарейными свойствами в испытаниях на животных (Onwukaeme and Anuforo, 1993, Discovery and Innovation, 5:317; Onwukaeme and Lot, 1991, Phytotherapy Res., 5:254). Сырые экстракты, которые содержат танины, в частности, экстракты из стручков рожкового дерева и сладкого каштана, были предложены в качестве профилактики или лечения (патент США №5043160; Европейский патент №481396).
Проантоцианидины содержат по меньшей мере два или более мономерных звеньев, которые могут быть одинаковыми или различными мономерными структурами. Мономерные единицы (общее название "лейкоантоцианидин"), как правило, являются мономерными флавоноидами, которые включают катехины, эпикатехины, галлокатехины, галлоэпикатехины, флавонолы, флавонолы и флаван-3,4-диолы, лейкоцианидины и антоцианидины. Таким образом, полимерные цепи основываются на различных структурных единицах, которые создают значительные вариации полимерных проантоцианидинов и большое число возможных изомеров (Hemingway et al., 1982, J.С.S. Perkin, 1:1217). Более крупные полимеры флавоноид-3-оловых единиц являются преобладающими в большинстве растений, и как было найдено, обладают средней молекулярной массой более 2000 дальтон, содержащие 6 или более единиц (Newman et al., 1987. Mag. Res. Chem., 25:118).
Проантоцианидиновые полимеры были найдены в самых разнообразных растениях, особенно растениях с древесным характером роста (например, Croton spp.и Calophyllum spp.). Большое количество различных видов деревьев Croton, в том числе Croton sakutaris, Croton gossypifolius, Croton palanostima, Croton lechleri, Croton erythrochilus и Croton draconoides, найденные в Южной Америке, продуцируют красный вязкий латексный сок, называемый Sang re de Dra go или "Dragon′s Blood". Патент США №5211944 впервые описал выделение водорастворимых проантоцианидиновых полимерных композиции из Croton spp.и применение композиции в качестве антивирусного агента (см. также Ubillas et al., 1994, Phytomedicine, 1:77). Было показано, что проантоцианидиновая полимерная композиция обладает антивирусной активностью против различных вирусов, включая респираторно-синцитиальный, вирусы гриппа, парагриппа и герпеса. Патент США №5211944 также раскрывает выделение водорастворимой проантоцианидиновой полимерной композиции из Calophyllum inophylum и применение этой композиции в качестве противовирусного агента.
Типичные проантоцианидиновые полимерные композиции, используемые в способах, представленных в настоящем изобретении, предпочтительно выделяют из Croton spp. или Calophyllum spp любым способом, известным в данной области техники. Например, проантоцианидиновая полимерная композиция может быть выделена из Croton spp. или Calophyllum spp. по способу, раскрытому в патенте США №5211944 или в Ubillas et al., 1994, Phytomedicine 1: 77-106.
Проантоцианидиновые полимерные композиции, используемые в способах, представленных в настоящем изобретении, также могут быть получены in vitro с использованием синтетических методик.
В одном конкретном варианте осуществления проантоцианидиновая полимерная композиция, используемая в способах, представленных в настоящем изобретении, является крофелемером.
Крофелемер представляет собой олигомерный проантоцианидин, экстрагированный и очищенный из красного вязкого латекса растения Croton lechleri семейства Euphorbiace. Растение широко распространено по всей тропической Центральной и Южной Америке и широко известно этноботаникам и местным целителям своими целебными свойствами (McRae 1988), в том числе для лечения диареи. Крофелемер, как полагают, оказывает свой антидиарейный эффект через люминальную блокаду CFTR (муковисцидозного трансмембранного регулятора проводимости) хлоридного (Cl-) канала. Крофелемер продемонстрировал активность in vitro против холерного токсина, форсколина, E coli LT и STa токсин-опосредованной секреции Cl-, и для нормализации аккумуляции электролита и жидкости в СТ-получавших лечение мышах (Gabriel 1999, Fischer 2004, Adam 2005) через его эффекты на CFTR-канал. Крофелемер также значительно улучшал секреторную диарею у людей вследствие энтеротоксигенной E. coli (DiCesare 2002), которая также, как полагают, вызывает секреторную диарею посредством активации CFTR (Kunzelmann 2002). Блокада CFTR-канала, как можно ожидать, имеет негативные последствия у человека, даже напоминая муковисцидоз. Тем не менее, крофелемер практически не имеет системной биодоступности у человека. Во время исследований результаты показали, что крофелемер мало или вообще не абсорбируется из желудочно-кишечного тракта, и что крофелемер хорошо переносится здоровыми мужскими особями. Таким образом, местом приложения действия крофелемера является местное применение в желудочно-кишечном тракте.
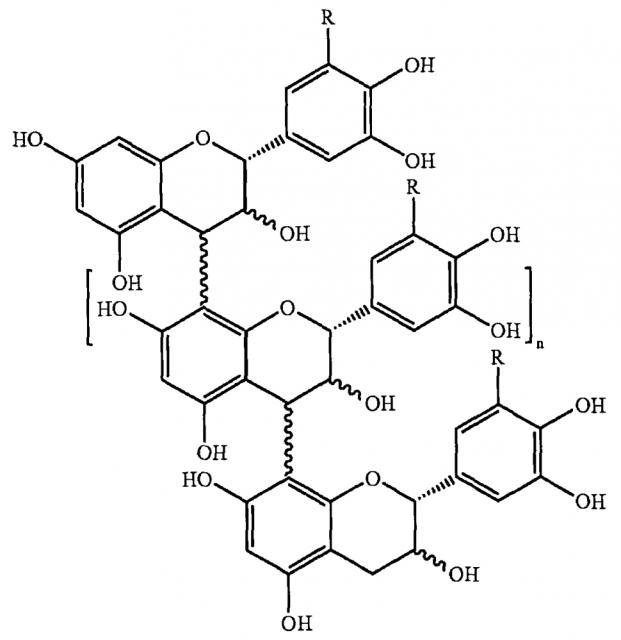
Крофелемер (CAS 148465-45-6) является олигомерными проантоцианидином с различной длиной цепи, получаемым из Dragon′s Blood Croton lecheri семейства молочайных. Крофелемер имеет среднюю молекулярную массу от около 1500 дальтон до около 2900 дальтон. Мономеры, содержащие крофелемер, включают катехин, эпикатехин, галлокатехин и эпигаллокатехин. Длина цепи крофелемера находится в диапазоне от около 3 до около 30 единиц со средней длиной цепи около 8 единиц. Структура крофелемера показана ниже.
R=H или OH
n=3-30
Где средний n=6.
Другой способ выделения крофелемера можно найти в патентной публикации США №2005/0019389, содержание которой явным образом включено в настоящий патент.
В других вариантах осуществления исходный латекс, получаемый из видов Croton или видов Calophyllum, или экстракта, полученного из видов Croton или видов Calophyllum, являются полезными в способах, представленных в настоящем изобретении. Примеры экстрактов описаны в Persinos et al., 1979, J. Pharma. Sci. 68:124 and Sethi, 1977, Canadian J. Pharm. Sci. 12:7.
«Улучшить», «улучшение», «оздоровление» или подобное от носится, например, детектируемым улучшениям или детектируемым изменениям в соответствии с оздоровлением, которое происходит у субъекта, или по меньшей мере у меньшей части субъектов, например, по меньшей мере у около 2%, 5%, 10%, 15%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 100%, или в интервале приблизительно между любыми двумя из этих значений. Такие улучшения или изменения можно наблюдать у получавших лечение (леченых) субъектов по сравнению с субъектами, не получавших лечение крофелемером, где необработанные субъекты имеют или могут получить такое же или аналогичное заболевание, состояние, симптом или подобное вышеперечисленному. Улучшение заболевания, состояния, симптома или параметра анализа может быть определено субъективно или объективно, например посредством самооценки субъекта(ов), по оценке врача или посредством проведения соответствующего анализа или измерения. Улучшение может быть временным, длительным или постоянным или оно может изменяться в соответствующее время в процессе или после того, как крофелемер введут субъекту или используют в анализе или другим описанным в настоящем изобретении способом или цитируемой ссылке, например, в сроки, описанные ниже, или около 1 часа после введения или использования крофелемера до приблизительно 7 дней, 2 недели, 28 дней или 1, 3, 6, 9 месяцев или более после того, как субъект(ы) получил подобную обработку.
"Модуляция", например, симптома, уровня или биологической активности молекулы или т.п., означает, например, что симптом или активность или тому подобное, детектируемо увеличивается или уменьшается. Такое увеличение или уменьшение может наблюдаться у получавших лечение субъектов по сравнению с субъектами, не обработанными крофелемером, где необработанные субъекты имеют или могут получить такое же или аналогичное заболевание, состояние, симптом или подобное перечисленному. Такие увеличения или уменьшения могут быть по меньшей мере около 2%, 5%, 10%, 15%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 98%, 100%, 150%, 200%, 250%, 300%, 400%, 500%, 1000% или более, или в любом диапазоне между любыми двумя из этими значениями. Модуляция может быть определена субъективно или объективно. Модуляция может быть временной, длительной или постоянной или она может варьироваться в соответствующее время в процессе или после того, как крофелемер введут субъекту или используют в анализе или другим описанным в настоящем изобретении способом или цитируемой ссылке, например, в сроки, описанные ниже, или около 1 часа после введения или использования крофелемера до приблизительно 2 недель, 28 дней, 3, 6, 9 месяцев или более после того, как субъект(ы) получил крофелемер.
Выражение "профилактически эффективное количество" соединения означает количество крофелемера, которое является эффективным, после одной или нескольких доз введения субъекту для предотвращения или лечения диареи, например, ВИЧ-ассоциированной диареи.
Используемый в настоящем изобретении термин "субъект" включает организмы, которые способны страдать ВИЧ диареей или ВААРТ ассоциированной диареей или которые могли бы извлечь пользу из введения крофелемера, как описано в настоящем изобретении, таких как люди и животные, не принадлежащих человеческому роду. Термин "животные, не принадлежащие человеческому роду" включает всех позвоночных, например, млекопитающих, таких как приматы, кроме человека, других млекопитающих, например, грызунов и овец, собак и коров, подверженных риску ВИЧ ассоциированной диареи или ВААРТ ассоциированной диареи. Субъект с риском ВИЧ ассоциированной диареи или ВААРТ ассоциированной диареи означает включение субъекта с риском развития или заражения инфекцией ВИЧ
Выражение "профилактически эффективное количество" соединения означает количество крофелемера, которое является эффективным после одной или нескольких доз введения субъекту, для предотвращения или лечения диареи.
Термин "введение" или "вводимый" включает в себя способы введения крофелемера в субъект для осуществления предназначенной им функции. Примеры способов введения, которые могут быть использованы, включают инъекции, пероральный, ингаляции, вагинальный, ректальный и трансдермальный. Фармацевтические препараты могут определяться формой, подходящей для каждого способа введения. Например, эти препараты вводятся в форме таблетки или капсулы, инъекции, ингаляции, мази или суппозитория. Введение также может осуществляться посредством инъекции, инфузии или ингаляции; местно посредством лосьона или мази, а также ректально посредством суппозиториев. Предпочтительным является пероральное введение. В зависимости от способа введения, крофелемер может быть покрыт или он может быть помещен в выбранный материал для защиты от природных условий, которые могут отрицательно влиять на его способность выполнять свои функции. Крофелемер можно вводить отдельно или в сочетании с любым другим препаратом или препаратами, как описано выше, или с фармацевтически приемлемым носителем или с обоими. Типичные формы с кишечнорастворимыми оболочками крофелемера описаны, например, в патенте США 7556831.
Введение "в комбинации с" одним или более дополнительными терапевтическими препаратами включает в себя одновременное (совместное) и последовательное введение в любом порядке.
Как должно быть очевидно специалистам в данной области техники, полезная in vivo дозировка для введения и конкретного способа введения может варьироваться в зависимости от возраста, массы и вида подвергающегося лечению млекопитающего, конкретных используемых соединений и/или конкретного использования, для которых эти соединения применяются. Определение эффективной дозировки, то есть уровней дозировки, необходимых для достижения желаемого результата, может быть достигнуто специалистами в этой области техники с помощью стандартных фармакологических методов и в соответствии с данными, представленными в настоящем патенте. Что касается крофелемера, крофелемер может быть выгодно вводить по 125 мг два раза в день для лечения водянистой диареи, если менее водянистое испражнение желательно в течение недели. Целесообразно также подвергать лечению по 500 мг два раза в день, если желательно улучшение консистенции испражнений.
Термин "получение", как в "получении крофелемера" предназначен для включения приобретения, синтеза, выделения, экстракции или иного обретения крофелемера. Выражение "профилактически эффективное количество" соединения означает количество крофелемера, которое является эффективным после введения одной или нескольких доз субъекту для предотвращения или лечения индикации. В одном варианте осуществления назначением является ВИЧ-ассоциированная диарея.
Способы лечения
В настоящем изобретении приведены способы лечения, предупреждения или облегчения диареи или симптомов, вызванных ВИЧ-инфекцией или ВААРТ терапии ВИЧ-инфекции, включающие введение субъекту, нуждающемуся в этом, эффективного количества крофелемера. Типичная диарея, которая может быть вылечена или предотвращена с использование способов, описанных в настоящем изобретении, включает ВИЧ ассоциированную диарею или диарею, ассоциированную с высокоактивной антиретровирусной терапией.
В одном из вариантов осуществления лечение ВИЧ-ассоциированной диареи включает улучшение следующих симптомов ВИЧ-ассоциированной диареи или ВААРТ ассоциированной диареи, в том числе, например, уменьшение количества испражнений в день (частота), уменьшение количества водянистые испражнения в день, уменьшение частоты симптомов (неотложность позыва, недержание кала), снижение тяжести симптомов (боли в животе или дискомфорта), снижение ежедневной оценки консистенции испражнений (водянистый до сформированный), или уменьшение консистенции испражнений, что ведет к оформленному испражнению от водянистого испражнения.
В одном конкретном варианте осуществления, излечение определяется как два или меньше водянистых испражнений в неделю. В частности, излечение определяется как два или меньше водянистых испражнений в неделю в течение по меньшей мере двух из четырех недель лечения крофелемером.
В других конкретных вариантах осуществления излечение может также включать, например, снижение на одно или больше количества испражнений в день, уменьшение количества водянистого испражнения в день, улучшение ежедневной оценки боли в животе или дискомфорта, улучшение ежедневной оценки для консистенции испражнений, уменьшение числа дней в неделю, в которые субъекты испытывают неотложность позыва, уменьшение числа дней в неделю, в которые субъекты испытывали недержание кала, или уменьшение незапланированных визитов по поводу значительного ухудшения диареи.
В одном аспекте в настоящем изобретении приведены способы лечения ВИЧ-ассоциированной диареи или диареи, ассоциированной с высокоактивной антиретровирусной терапией (ВААРТ) у ВИЧ-положительных субъектов. Излечение диареи может включать, например, снижение количества испражнений в день на одно или более испражнений, уменьшение количества водянистого испражнения в день, улучшение ежедневной оценки боли в животе или дискомфорта, улучшение ежедневной оценки для консистенции испражнений, уменьшение консистенции испражнений, уменьшение числа дней в неделю, в которые субъекты испытывали неотложность позыва, уменьшение числа дней в неделю, в которые субъекты испытывали недержание кала, или снижение уменьшение незапланированных визитов по поводу значительного ухудшения диареи.
В одном аспекте в настоящем изобретении приведены способы лечения консистенции испражнений у ВИЧ-инфицированного субъекта, где субъект считается вылеченным, если есть улучшение в ежедневной оценке для консистенция испражнений и/или уменьшение оценки для консистенция испражнений, измеряемых в течение дня или дней или недель. Это снижение может измеряться от исходного уровня. Исходный уровень может быть определен в ближайшие дни недели до лечения крофелемером. Лечение включает в себя введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение 1000 мг в день; введение около 125 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном аспекте в настоящем изобретении представлены способы улучшения консистенции испражнений у ВИЧ-инфицированного субъекта, в которых субъект считается вылеченным, если есть улучшение в консистенции испражнений и/или уменьшение консистенции испражнений в течение дня или нескольких дней или недель. Это увеличение может быть измерено от исходного уровня. Исходный уровень может быть определен в ближайшие дни недели до лечения крофелемером. Лечение включает в себя введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение 1000 мг в день; введение около 125 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном аспекте в настоящем изобретении представлены способы облегчения водянистой диареи у ВИЧ-инфицированного субъекта, где субъект считается вылеченным, если субъект испытывает уменьшение количества водянистого испражнения в день и/или в течение нескольких дней, недели или недель введения крофелемера. Это снижение может быть измерено от исходного уровня. Исходный уровень может быть определен в ближайшие дни недели до лечения крофелемером. Лечение включает в себя введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение 1000 мг в день; введение около 125 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом.
В одном аспекте в настоящем изобретении представлены способы уменьшения количества испражнений в день, в которых субъект считается вылеченным, если наблюдается снижение количества испражнений в день при измерении от исходного уровня. Исходный уровень может быть определен в ближайшие дни недели до лечения крофелемером.
Лечение включает в себя введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение 1000 мг в день; введение около 125 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту, нуждающемуся в этом. Крофелемер можно вводить, например, один раз в день, два раза в день, три раза в день, или в четыре раза или более часто при необходимости в день. Крофелемер можно вводить в дозах, например, от около между 25 мг два раза в день до около 3000 мг трижды в день, предпочтительно Крофелемер вводят от около 125 мг до около 1000 мг в день. В другом варианте Крофелемер вводят от 125 мг два раза в день до 500 мг два раза в день в зависимости от симптомов. В другом варианте осуществления Крофелемер вводят 125 мг два раза в день. В другом варианте осуществления Крофелемер вводят 500 мг два раза в день. Крофелемер может быть введен перорально, например, в форме таблеток, порошковообразной форме, жидкой форме или в капсулах.
В конкретных вариантах осуществления субъекту вводят 250, 500 или 1000 мг в день крофелемера.
В конкретных вариантах осуществления субъекту вводят 125, 250 или 500 мг р.о. два раза в день (перорально два раза в день). Другие подходящие дозы для способов могут быть определены медицинским работником или субъектом. Количество крофелемера вводимого ежедневно может быть увеличено или уменьшено в расчете на массу, возраст, состояние здоровья, пол и медицинское состояние субъекта. Специалист в данной области техники сможет определить нужную дозу для субъекта на основе настоящего описания и данных, представленных в примерах, которые следуют ниже.
В других вариантах осуществления субъекту вводят крофелемер в течение 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24 или более недель, или 26 или более недель. В одном варианте осуществления субъекту вводят Крофелемер в течение заболевания. Продолжительность лечения может варьироваться в зависимости от типа и продолжительности заболевания, и соответствующая продолжительность лечения может быть легко определена специалистом в данной области техники, имеющим выгоду от этого раскрытия. Лечение может быть до инфицирования, во время инфекции или после подозрения на инфекцию и в течение периода времени, предложенного врачом, чтобы уменьшить или устранить диарею.
Субъекты, нуждающиеся в этом, включают субъектов, имеющие или такие, которые являются чувствительными к или которые имеют ВИЧ-ассоциированную диарею или ВААРТ ассоциированную диарею.
Используемый в настоящем изобретении термин терапевтически эффективное количество означает количество, эффективное при введении в организм человека или животного, не являющимся человеком, чтобы обеспечить терапевтические преимущества, такие как улучшение симптомов, например, в количестве, эффективном для уменьшения симптомов ВИЧ-ассоциированной диареи.
Согласно некоторым вариантам осуществления, крофелемер может быть введен в комбинации с другими соединениями, включая, например, антидиарейные препараты или анти-ВИЧ препараты, включая, например, антиретровирусные препараты.
Согласно одному аспекту в настоящем изобретении представлены способы лечения ВИЧ-ассоциированной диареи или диареи, ассоциированной с высокоактивной антиретровирусной терапией (ВААРТ) у ВИЧ-положительного субъекта, который предварительно использовал ингибиторы протеазы, включающие: введение от около 250 мг до около 1000 мг в день; введение около 250 мг в день; введение около 500 мг в день; введение около 1000 мг в день; введение около 125 мг два раза в день; введение около 250 мг два раза в день или введение 500 мг два раза в день крофелемера субъекту мужского пола, нуждающемся в этом. Используемый в настоящем изобретении термин "предварительно использующий" включает, например, субъектов, которые использовали ингибиторы протеазы (ИП) до терапии крофелемером или, перекрываясь с терапией крофелемером, но использование ИП начали до первой дозы терапии крофелемером.
Фармацевтические препараты
Кроме того, приведенные в настоящем изобретении фармацевтические композиции содержат эффективное количество крофелемера, описанного в настоящем изобретении, и фармацевтически приемлемый носитель. В дополнительном варианте осуществления эффективное количество является эффективным для лечения ВИЧ-ассоциированной диареи и/или ВААРТ-ассоциированной диареи.
Примеры получения и применения крофелемера были описаны в патенте США 7556831, патенте США 20070254050 и патентной публикации США 20080031984, каждый из которых включен в настоящее описание посредством ссылки во всей их полноте.
Один вариант осуществления включает фармацевтические композиции, содержащие крофелемер и фармацевтически приемлемый носитель.
Фармацевтические композиции, описанные в настоящем изобретении, могут также содержать вспомогательные вещества, например, один или более разбавитель, связующее вещество, смазывающее вещество, дезинтегрирующий агент, краситель, ароматизатор или подсластитель. Композиции могут быть составлены для выбранных покрытых и непокрытых таблеток, твердых и мягких желатиновых капсул, драже, пастилок, вафельных листов, гранул и порошков в запечатанном пакете. Например, композиции могут быть составлены для местного применения, например, мази, помады, кремы, гели и лосьоны.
В некоторых вариантах осуществления эти фармацевтические композиции, являются пригодными для местного или перорального введения субъекту. В других вариантах осуществления, как подробно описано ниже, фармацевтические композиции могут быть специально приготовлены для введения в твердой или жидкой форме, в том числе адаптированной для следующих целей: (1) пероральное введение, например, большие дозы (водные или неводные растворы или суспензии), таблетки, болюсы, порошки, гранулы, пасты, (2) парентеральное введение, например, посредством подкожной, внутримышечной или внутривенной инъекции, как например, стерильный раствор или суспензия, (3) местное применение, например, в качестве крема, мази или спрея наносится на кожу, (4) интравагинально или ректально, например, в виде пессария, крема или пены или (5) аэрозоль, например, в виде водного аэрозоля липосомного препарата или твердых частиц, содержащих соединения.
Выражение "фармацевтически приемлемый" относится к крофелемеру, как описано в настоящем изобретении, к композициям, содержащим крофелемер, и/или лекарственным формам, которые, в рамках тщательной медицинской оценки, являются удобными для использования в контакте с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, соразмерных с разумным соотношением польза/риск.
Выражение "фармацевтически приемлемый носитель" включает фармацевтически приемлемое вещество, композицию или носитель, такие как жидкий или твердый наполнитель, разбавитель, вспомогательное вещество, растворитель или инкапсулирующий материал, участвующие в перемещении и транспортировке химического вещества от одного органа или части тела к другому органу или части тела. Каждый носитель должен быть "приемлемым" в смысле совместимости с другими ингредиентами композиции и не вредным для пациента. Некоторые примеры материалов, которые могут служить в качестве фармацевтически приемлемых носителей, включают: (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмалы, такие как кукурузный крахмал и картофельный крахмал; (3) целлюлозу и ее производные, такие как натрийкарбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; (4) порошкообразный трагакант; (5) солод; (6) желатин; (7) тальк; (8) вспомогательные вещества, такие как масло какао и воски для суппозиториев; (9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль; (11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) буферные агенты, такие как гидроксид магния и гидроксид алюминия; (15) альгиновая кислота, (16) апирогенную воду; (17) изотонический солевой раствор, (18), раствор Рингера, (19) этиловый спирт; (20) фосфатные буферные растворы, а также (21) другие нетоксичные совместимые вещества, используемые в фармацевтических препаратах.
Смачивающие агенты, эмульгаторы и смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, разделительные средства, покрывающие агенты, подсластители, вкусовые добавки и ароматизаторы, консерванты и антиоксиданты также могут присутствовать в композициях.
Примеры фармацевтически приемлемых антиоксидантов включают: (1) водорастворимые антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфит натрия, сульфит натрия и тому подобное, (2) растворимые в масле антиоксиданты, такие как аскорбилпальмитат, бутилгидроксианизол (БОА), бутилгидрокситолуол (БОТ), лецитин, пропилгаллат, альфа-токоферол и тому подобное, и (3) металл хелатирующие агенты, такие как лимонная кислота, этилендиаминтетрауксусная кислота (ЭДТА), сорбит, винная кислота, фосфорная кислота, и тому подобное.
Композиции, содержащие крофелемер, включают композиции, пригодные для перорального, назального, местного (включая буккальное и сублингвальное), ректального, вагинального, аэрозольного и/или парентерального введения. Композиции могут быть удобно представлены в форме единичной дозы и могут быть приготовлены любыми способами, известными в области фармации. Количество ак