Лечение легочных инфекций с помощью введения тобрамицина путем аэролизации
Иллюстрации
Показать всеИзобретение относится к медицине и заключается в способе профилактики или лечения бактериальных инфекций в легочной системе. Способ включает введение путем ингаляции аэрозолизированной дозы водного раствора 150-250 мг/мл тобрамицина, где введение осуществляют с использованием дозирующего ингалятора, обеспечивающего образование аэрозоля, имеющего масс-медианный аэродинамический диаметр 4-7 мкм, где дозирующий ингалятор имеет распылительную насадку, обеспечивающую образование указанных аэрозолей путем перенесения композиции через отверстия, имеющие диаметр 1,8-3,9 мкм. Технический результат заключается в быстроте и эффективности введения тобрамицина и в улучшенном режиме дозирования. Средняя максимальная концентрация в плазме является более низкой по сравнению с уровнем техники, что является дополнительным преимуществом, поскольку тобрамицин в плазме обусловливает нежелательные побочные эффекты. 16 з.п. ф-лы, 8 ил., 19 табл., 2 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к лечению легочных инфекций, в частности, в тех случаях, где пациент страдает муковисцидозом.
Предшествующий уровень техники
Бактериальная легочная инфекция является одной из основных проблем и может стать представляющей угрозу жизни для пациента, страдающего хроническими легочными расстройствами, такими как астма, муковисцидоз и хроническая обструктивная болезнь легких.
В частности, муковисцидоз (CF) представляет собой аутосомно-рецессивное наследственное заболевание, которым поражено примерно 30000 человек в США и примерно 40000 в Европе. Мутации CF встречаются в гене, кодирующем белок канала-переносчика для ионов хлора, называемый CF регулятором трансмембранной проводимости (CFTR). Пациенты, гомозиготные по дефектным генам CFTR, типично страдают хроническими рецидивирующими эндобронхиальными инфекциями (в конечном счете, фатальными) и синуситом, а также малабсорбцией вследствие недостаточности поджелудочной железы, повышенной потерей солей с потом, обструктивной болезнью печени и желчных путей и сниженной детородной функцией.
Pseudomonas aeruginosa (Pa) является самым значимым патогенном при легочном заболевании CF. Более 80% пациентов CF, в конечном счете, становится колонизированными Ра, и развитие хронической инфекции легких Pseudomonas aeruginosa является типичным признаком муковисцидоза, который может вызвать дальнейшее повреждение легочной ткани и дыхательную недостаточность, угрожающую жизни.
Тобрамицин представляет собой аминогликозидный антибиотик, продуцируемый в природе Streptomyces tenebrarius. Он действует, прежде всего, посредством прерывания синтеза белка, приводящего к измененной проницаемости клеточной мембраны, прогрессирующему прерыванию клеточной оболочки и, в конечном счете, к гибели клетки. Тобрамицин является бактерицидным при концентрациях, равных его ингибиторным концентрациям, или несколько более высоких.
Для предупреждения и лечения легочных инфекций у пациентов с хроническими легочными расстройствами широко применяют антибиотики, такие как аминогликозидные антибиотики. Парентеральные аминогликозиды являются высоко полярными агентами и слабо приникают в эндобронхиальное пространство. Кроме того, связывание аминогликозида с мокротой (International Cystic Fibrosis [Mucoviscidosis] Association, 1995 Annual Questionnaire, Paris, France; 1995, Collins FS, "Cystic fibrosis molecular biology and therapeutic implications", Science 1992; 256, pp 774-779, Davis PB, et al., "Cystic fibrosis", Amer J. Respir Crit Care Med 1996; 154 (5), pp.1229-56) или с гликопротеинами или ДНК мокроты (Koch С, Hoiby N., "Pathogenesis of cystic fibrosis", Lancet 1993; 341 (8852, pp.1065-1069) снижает биологическую активность и требует локальных концентраций в 10-25 раз выше минимальной ингибиторной концентрации (МИК), чтобы преодолеть сниженную доступность аминогликозида для бактериальных мишеней. Чтобы получить адекватные концентрации лекарства в сайте инфекции при парентеральном введении, сывороточные уровни достигают уровней, которым сопутствуют тяжелые побочные эффекты, такие как нефротоксичность, вестибулотоксичность и ототоксичность (Konstan MW, Berger M. Infection and inflammation of the lung in cystic fibrosis. New York, NY Dekker; 1993, FitzSimmons SC, The changing epidemiology of cystic fibrosis. J Pediatr 1993; 122:1-9).
Введение аминогликозидов путем аэрозолизации предлагает привлекательную альтернативу парентеральному введению, доставляя высокие концентрации антибиотика непосредственно к сайту инфекции в эндобронхиальном пространстве, сводя при этом к минимуму системную биодоступность.
Аминогликозиды, такие как тобрамицин, часто подвергают аэрозолизации, используя небулайзер, то есть устройство с электропитанием, которое преобразует жидкий аминогликозидный препарат в аэрозоль, который затем вводят пациенту путем вдыхания образовавшегося аэрозоля в легкие посредством лицевой маски или мундштука с насадкой для распыления. Общепринято используемый небулайзер для введения аэрозольных препаратов представляет собой струйный небулайзер, также называемый "атомизатором". Струйные небулайзеры соединены с помощью трубок с компрессором, который вызывает продувание сжатого воздуха или кислорода при большой скорости через жидкое лекарство для преобразования его в аэрозоль, вдыхаемый пациентом.
Струйные небулайзеры также используют для введения имеющегося в продаже препарата раствора тобрамицина для ингаляции (TOBI®; 60 мг/мл в 5 мл 1/4 нормального физиологического раствора), разработанного фирмой PathoGenesis Corporation (в настоящее время Novartis). TOBI® был одобрен Администрацией США по пищевым продуктам и лекарственным веществам в 1997 г. для применения два раза в сутки пациентам CF в возрасте старше 6 лет.
Различные препараты растворов тобрамицина для ингаляции также описаны на предшествующем уровне техники. Например, в патенте США №5508269 раскрыт препарат, содержащий от 40 до 100 мг аминогликозида в 1 мл физиологического раствора, разведенный в физиологическом растворе концентрации четверти нормальной, где этот препарат имеет pH от 5,5 до 6,5, и где этот раствор доставляется в 5 мл концентрированной форме путем аэрозолизации.
В US 6987094 раскрыт аэрозольный препарат, состоящий из 75 мг/мл тобрамицина, растворенного в водном растворе, содержащем 0,45% масс./об. хлорида натрия, где pH составляет от 4,0 до 5,5, и осмолярность находится в интервале от 250 до 450 мОсм/л.
В заявке на патент США 2007/0116649 предложены аэрозольные препараты, содержащие от примерно 100 мг/мл до 200 мг/мл антибиотиков против грамотрицательных бактерий. Предложены препараты тобрамицина, но эксперименты с тобрамицином не раскрыты.
В заявке на патент США 2007/0071686 раскрыта композиция тобрамицина, содержащая примерно 80-120 мг/мл тобрамицина, кислый адъювант и только низкую концентрацию хлорида натрия. Кислый адъювант может представлять собой сульфат натрия или фосфат натрия. Согласно US 2007/0071686 концентрация активного агента не должна превышать 120 мг/мл, поскольку указано, что более высокие концентрации тобрамицина обладают отрицательным эффектом на распыление вследствие вязкости композиции. Кроме того, композицию тобрамицина согласно US 2007/0071686 следует вводить пациенту путем использования небулайзера, то есть активный ингредиент вдыхается путем вдохов и выдохов.
В ЕР 2186508 описана, среди прочего, композиция менее чем 4 мл раствора, содержащего 60-200 мг/мл аминогликозидного антибиотика в физиологически приемлемом носителе. Эксперименты, описанные в ЕР 2186508, показывают, что время, необходимое для введения композиции, содержащей 120 мг/мл тобрамицина с использованием струйного небулайзера PARI LC PLUS® (компрессор Pari Boy N, Starnberg, Germany) составляет примерно 10 мин. Хотя это время может быть меньшим, чем время, требующееся для введения имеющегося в продаже TOBI®, это необходимое время все же является слишком длительным с точки зрения соблюдения пациентом режима и схемы лечения и с точки зрения удобства для пациента-пользователя. При использовании активируемого вдохом ингаляционного устройства в ЕР 2186508 описано более быстрое время введения, чем достигаемое вышеупомянутой системой, имеющейся в продаже. Однако время введения, достигаемое при использовании активируемого вдохом ингаляционного устройства (AcroDose™) в экспериментах, описанных в ЕР 2186508, получают, используя композицию, имеющую только низкую концентрацию тобрамицина (60 мг/мл). Кроме того, описано, что при введении композиции 60 мг/мл с использованием системы AcroDose™ может быть также необходимо введение второй аликвоты. Необходимость в заполнении и введении второй аликвоты представляет недостаток с точки зрения удобства для пациента и соблюдения пациентом режима и схемы лечения.
Известны также растворы тобрамицина для местного введения, например, для лечения кератита; см. Davis et al. (1978), Canad. J Ophtal., 13:273, 1978, Davis et al., 1978, Arch Opthalmol, vol 96, page 123-125, and Unter man et al. (1988), J. Cataract Refract. Surg., vol.14, page 500-504.
Хорошо известным недостатком доступных средств введения и режимов лечения является время, требующееся для введения, что влияет, среди прочего, на соблюдение пациентом режима и схемы лечения и на качество жизни пациента.
Авторами Dopfer et al., "Inhalation of Тобрамицин in patients with cyclic fibrosis: Comparison of two methods", Journal of Physiology and Pharmacology, 2007, 58, suppl. 5, pp.141-154, описаны результаты одноцентрового, открытого, перекрестного исследования, где различные количества тобрамицина (TOBI®) вводили, используя различные ингаляционные системы, то есть хорошо известный небулайзер PARI-LC PLUS® (компрессор Pari Boy N, Starnberg, Germany) и AKITA®, комбинированный с небулайзером PARI-LC PLUS® (Activaero, Gemuden, Germany). Это исследование показало, что в результате использования системы AKITA® время, требующееся для аэрозольной ингаляции, было сокращено примерно с 20 минут до примерно 7-8 минут. Исследование, кроме того, показало, что сходные концентрации в сыворотке были получены двумя способами данного клинического исследования.
Хотя использование устройства AKITA® для введения сокращает время, необходимое для введения эффективной дозы тобрамицина по сравнению с общепринятой системой введения, это необходимое время все же является слишком длительным. Поэтому существует необходимость в режиме лечения, гарантирующем более короткие периоды введения, приводящие в результате к лучшему соблюдению пациентом режима и схемы лечения и качеству жизни пациентов с муковисцидозом и пациентов, страдающих другими легочными расстройствами, подлежащими лечению тобрамицином.
Кроме того, системы и способы введения аминогликозидов в легкие пациента путем ингаляции предшествующего уровня техники страдают дополнительными недостатками, как, например, тот, что количество активных ингредиентов, не достигающих сайта действия вследствие того факта, что остатки препаратов задерживаются в устройстве небулайзера после введения препарата тобрамицина или исчезают в окружающей среде пациента. С экономической точки зрения и с точки зрения окружающей среды, таким образом, также существует необходимость в режимах введения, где теряются меньшие количества препарата тобрамицина.
Таким образом, цель настоящего изобретения состоит в разработке улучшенного режима введения для аминогликозидов, который не обременен недостатками предшествующего уровня техники.
Краткое изложение сущности изобретения
В настоящем изобретении предложена новая форма введения и новый режим для лечения и предупреждения легочных инфекций аминогликозидными антибиотиками, в частности, тобрамицином. В настоящем изобретении предложено быстрое и эффективное введение аминогликозидных антибиотиков по сравнению с предшествующим уровнем техники. По сравнению с режимом введения, доступным в продаже (TOBI®, вводимый с использованием небулайзера PARI LC®), режим введения в соответствии с настоящим изобретением обеспечивает эффективную дозировку тобрамицина всего лишь в течение нескольких минут, например, 1-5 минут.
Авторы настоящего изобретения неожиданно обнаружили, что высококонцентрированный раствор тобрамицина в сочетании с малым объемом вводимого препарата обеспечивает эффективный и улучшенный режим дозирования.
Кроме того, форма введения и режим введения в соответствии с настоящим изобретением обеспечивает вдвое больше активного ингредиента, такого как, например, препарат тобрамицина для введения в легкие, по сравнению с режимами введения предшествующего уровня техники. Дополнительное преимущество настоящего режима введения состоит в том, что свободный объем, и, следовательно, отходы, остающиеся в ингаляционном устройстве, используемом в соответствии с настоящим изобретением, пренебрежимо мал по сравнению с режимами введения предшествующего уровня техники. Под отходами также понимают мелкие частицы, которые выдыхаются в воздух при использовании небулайзера Pari. Активное лекарство, и, в частности, антибиотики, должны оставаться в сайте действия и не присутствовать в общем окружающем пространстве. Например, низкие концентрации антибиотиков могут индуцировать устойчивые микроорганизмы.
Еще одно другое преимущество настоящего изобретения состоит в том, что средняя максимальная концентрация в плазме, полученная в соответствии с настоящим изобретением, является более низкой по сравнению со средним максимальным уровнем в плазме, полученным с использованием режимов введения предшествующего уровня техники (тобрамицина с использованием TOBI® и небулайзера PARI LC®).
Согласно одному аспекту изобретения предложена композиция для терапевтического или профилактического лечения бактериальных инфекций в легочной системе пациента, нуждающегося в этом, которая содержит 150-250 мг/мл тобрамицина, где данную композицию следует вводить путем ингаляции.
Согласно одному аспекту изобретения предложена композиция для терапевтического или профилактического лечения бактериальных инфекций в легочной системе пациента, нуждающегося в этом, которая содержит 150-250 мг/мл аминогликозида для терапевтического или профилактического лечения бактериальных инфекций в легочной системе пациента, нуждающегося в этом, где данную композицию следует вводить путем ингаляции, и где данная композиция по существу не содержит хлорида натрия.
Еще в одном другом аспекте настоящего изобретения рассмотрена композиция, которую следует вводить путем ингаляции, в виде монодисперсных капель, образующихся в результате аэрозолизации данной композиции, где эти капли имеют масс-медианный аэродинамический диаметр 4-7 мкм.
В следующем аспекте настоящего изобретения рассмотрена композиция для терапевтического или профилактического лечения бактериальных инфекций в легочной системе пациента, нуждающегося в этом, которая содержит 150-250 мг/мл аминогликозида, которую следует вводить путем ингаляции аэрозолей в форме монодисперсных капель, имеющих масс-медианный аэродинамический диаметр 4-7 мкм.
Согласно одной форме осуществления настоящего изобретения аминогликозид представляет собой тобрамицин.
Согласно еще одной другой форме осуществления настоящего изобретения композиция содержит тобрамицин сульфат, соответствующий 150-250 мг/мл тобрамицина, как, например, соответствующий 180 мг/мл тобрамицина. Такую композицию, согласно одной форме осуществления, можно вводить путем ингаляции, где ингаляцию следует проводить в течение менее чем четырех минут, предпочтительно менее чем трех минут, более предпочтительно менее чем двух минут, более предпочтительно менее чем одной минуты.
Согласно другой форме осуществления настоящего изобретения композиция содержит тобрамицин сульфат, растворенный в воде, и где pH необязательно регулируют таким образом, чтобы pH находился в диапазоне 6-8.
Согласно еще одной другой форме осуществления настоящего изобретения композицию следует вводить путем ингаляции, и где ингаляцию следует проводить в течение 1-5 минут.
Согласно следующей форме осуществления ингаляцию следует проводить в течение менее чем четырех минут, предпочтительно менее чем трех минут, более предпочтительно менее чем двух минут, более предпочтительно менее чем одной минуты.
Согласно другой форме осуществления настоящего изобретения композиция имеет объем вплоть до 500 мкл.
Согласно еще одной форме осуществления настоящего изобретения настоящая композиция обеспечивает введение суммарного количества аминогликозида пациенту, нуждающемуся в этом, в диапазоне 50-80 мг.
Согласно еще одной другой форме осуществления настоящего изобретения настоящая композиция обеспечивает введение стандартной дозы, содержащей 60-70 мг тобрамицина, где введение следует осуществлять в течение менее чем 5 минут.
Согласно еще одной другой форме осуществления настоящего изобретения ингаляция композиции обеспечивает введение 63 мг тобрамицина (180 мг/мл × 0,35 мл) в легочную систему пациента, нуждающегося в этом, где композиция должна вдыхаться пациентом при проведении 7 глубоких медленных вдохов.
Согласно еще одной другой форме осуществления настоящего изобретения композиция имеет осмолярность от 300 до 500 мОсмоль/кг, предпочтительно от 375 до 475 мОсмоль/кг.
Согласно следующей форме осуществления настоящего изобретения композиция полезна для введения с использованием дозирующего ингалятора, имеющего распылительную насадку, обеспечивающую образование аэрозолей путем перенесения композиции через отверстия, имеющие диаметр в интервале 1,8-3,9 мкм.
Композицию согласно настоящему изобретению можно вводить с использованием дозирующего ингалятора, который обеспечивает рабочее давление в диапазоне 20-80 бар (2-8 МПа), как, например, 30-40 бар (3-4 МПа), предпочтительно 35 бар (3,5 МПа).
Композицию согласно настоящему изобретению можно, кроме того, вводить со скоростью тока 10-50 л/мин.
Композицию согласно настоящему изобретению можно вводить с использованием дозирующих ингаляторов, пригодных для ингаляции, активируемой вдохом, или путем координированной ингаляции.
Композиция по настоящему изобретению, кроме того, особенно полезна при лечении инфекций в легочной системе, вызванных бактериями рода Psedomonas.
Композиция по настоящему изобретению, кроме того, особенно полезна при лечении инфекций в легочной системе, где пациент страдает хроническим легочным заболеванием, таким как муковисцидоз.
Краткое описание чертежей
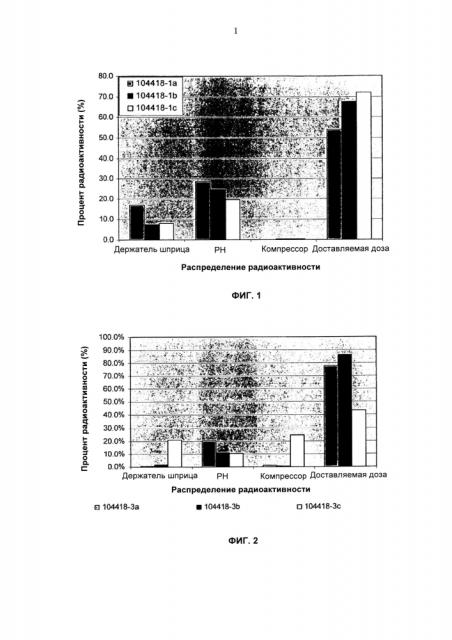
На фиг.1 показан баланс масс радиоактивно меченого раствора тобрамицина 20% масс./об., доставляемого in vitro с использованием устройства Tobrair® (6 активации).
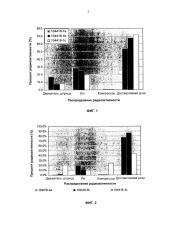
На фиг.2 показан баланс масс радиоактивно меченого раствора тобрамицина, доставляемого in vitro с использованием устройства Tobrair®.
На фиг.3 показан баланс масс радиоактивно меченого раствора тобрамицина 18% масс./об., доставляемого in vitro посредством устройства Tobrair®.
На фиг.4 показан баланс масс радиоактивно меченого раствора тобрамицина, доставляемого in vitro с использованием небулайзера PARI LC® Plus4.
На фиг.5 показаны профили проникновения в легкие для всех субъектов, которым вводили режим лечения А (60 мг тобрамицина, доставляемого с использованием устройства Tobrair®) и режим лечения В (300 мг тобрамицина (TOBI®), доставляемого с использованием системы устройств PARI LC® PLUS).
На фиг.6 показан подходящий ингалятор, включающий компрессор (1) многократного пользования, одноразовый контейнер (2) для лекарства (стандартный шприц) и мундштук (3) с распылительной насадкой.
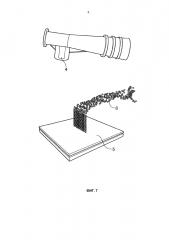
На фиг.7 показан мундштук с распылительной насадкой (4), имеющей силиконовую корзину (5), образующую капли (6) путем рэлеевского диспергирования.
На фиг.8 показан шприц, который можно вставлять в устройство, имеющий защитную крышку (7), которую можно удалять, и поршень (8) для перенесения содержимого шприца (9) в устройство.
Раскрытие изобретения
Определения:
Термин "аминогликозиды", как используют в данной заявке, подразумевают как включающий соединения-антибиотики, содержащие аминосахара, где эти соединения продуцируются в природе Streptomyces или Micromonospora, но также их синтетические и полусинтетические производные. "Аминогликозиды", таким образом, понимают как включающие антибактериальные соединения, такие как, например, тобрамицин, стрептомицин, апрамицин, паромомицин, тодострептомицин, неомицин, канамицин, амикацин, арбекацин, капреомицин и нетилмицин.
Тобрамицин, (2S,3R,4S,5S,6R)-4-амино-2-{[(1S,2S,3R,4S,6R)-4,6-диамино-3-{[2R,3R,5S,6R)-3-амино-6-(аминометил)-5-гидроксиоксан-2-ил]окси}-2-(гидроксиметилциклогексил]окси)-6-(гидроксиметил)оксан-3,5-диол, регистрационный номер 32986-56-4, присвоенный Химической реферативной службой (CAS), может быть представлен приведенной ниже формулой:
"Тобрамицин сульфат" представляет собой соль под регистрационным номером 49842-07-1, присвоенным Химической реферативной службой (CAS). Эта соль в твердой форме содержит тобрамицин и сульфат в отношении 2:5.
Термин "водный тобрамицин сульфат" понимают как включающий водные растворы, содержащие тобрамицин и ионы сульфата в любом соотношении.
"Высококонцентрированный раствор аминогликозида" представляет собой любой раствор, содержащий более 100 мг аминогликозида на мл, как, например, раствор, содержащий 180 мг гентамицина на мл. В отношении тобрамицина высококонцентрированный раствор в данной заявке означает раствор тобрамицина, содержащий 150-250 мг/мл тобрамицина, необязательно в форме тобрамицина сульфата.
Фармацевтический препарат, содержащий тобрамицин, может быть получен путем растворения тобрамицина или тобрамицина сульфата в стерильной воде. pH таких препаратов можно доводить до уровней, подходящих для легочной доставки.
Подходящий pH композиции согласно настоящему изобретению может находиться в диапазоне 6-8. pH препарата аминогликозида, например, в случае, где аминогликозид представляет собой тобрамицин, можно доводить путем добавления серной кислоты.
Подходящая композиция по настоящему изобретению состоит из тобрамицина сульфата и воды, где количество тобрамицина сульфата соответствует 180 мг/мл тобрамицина, и где pH данной композиции находится в диапазоне 6-8.
Согласно одному аспекту изобретения настоящая композиция согласно настоящему изобретению по существу не содержит хлорид натрия. Термин "по существу не содержит хлорид натрия" означает, что хлорид натрия не добавляют к раствору тобрамицина (например, к тобрамицину, растворенному в стерильной воде). Таким образом, в композиции, которая по существу не содержит хлорид натрия, присутствует только хлорид натрия за счет хлорида натрия, присутствующего в воде, используемой для растворения тобрамицина, такого как тобрамицин сульфат.
Термин "терапевтическая доза", как используют в данной заявке, следует понимать как дозу, которая при введении пациенту в соответствии с настоящим изобретением приводит в результате к сниженным уровням бактерий Pseudomonas в легких или приводит в результате к сниженной скорости роста бактерий Pseudomonas в легких.
Среднюю максимальную концентрацию в плазме получают путем введения препарата, содержащего по меньшей мере 100 мг/мл аминогликозида, как, например, 150-200 мг/мл аминогликозида, как, например, 180 мг/мл аминогликозида в соответствии с настоящим изобретением. Средняя максимальная концентрация в плазме согласно данному изобретению ниже, чем полученная в результате режима лечения TOBI® с небулайзером Pari LC® Plus.
Согласно настоящему изобретению композицию, содержащую высококонцентрированный раствор аминогликозида, как, например, 150-250 мг/мл тобрамицина, применяют при лечении и предупреждении легочных инфекций, где данная композиция пригодна для аэрозолизации с получением монодисперсных капель, имеющих масс-медианный аэродинамический диаметр (ММАД) 4-7 мкм. "ММАД", таким образом, следует понимать как масс-медианный аэродинамический диаметр капель/аэрозолей.
Водный дозирующий ингалятор (вДИ) представляет собой устройство, которое доставляет определенное количество лекарства в легкие, в форме кратковременного выброса капель лекарства, которое вдыхается пациентом.
Небулайзер представляет собой устройство, используемое для введения жидкого лекарства в форме аэрозоля, который непрерывно вдыхается в легкие путем вдоха и выдоха. Типичное время введения составляет 20 минут непрерывного и стабильного дыхания через маску. Хорошо известное устройство, применяемое для введения тобрамицина в соответствии с режимами введения предшествующего уровня техники, представляет собой систему устройств PARI LC® PLUS (http://www.pari.com/products/nebulizers/product/detail/info/lc plus reusable nebulizer.html). При введении фармацевтического агента с использованием небулайзера пациенты вдыхают аэрозоли, образуемые этим устройством, путем вдоха и выдоха. Это противоположно дозирующим ингаляторам, пригодным согласно настоящему изобретению, где вдох координирован с активацией ингалятора. Таким образом, введение включает один вдох на каждую активацию устройства. Активация устройства может запускаться различными средствами, известными в данной области техники, например, вручную или с помощью "дыхательных сенсоров".
Когда дозирующий ингалятор приводят в действие путем использования дыхательных сенсоров, и, следовательно, только вдохом, композицию вводят путем "ингаляции, активируемой вдохом". Когда дозирующий ингалятор приводят в действие вручную одновременно с тем, когда пациенты осуществляют один вдох, композицию вводят путем "координированной ингаляции".
Типичное время введения для одной ингаляции вДИ составляет несколько секунд. Это действие можно повторить несколько раз для получения желаемой дозы.
Наиболее предпочтительные вДИ для использования в настоящем изобретении образуют монодисперсные частицы с масс-медианным аэродинамическим диаметром (ММАД) примерно 5-5,7 мкм (ГСО менее 1,6).
Специалисту в данной области техники хорошо известен тот факт, что проникновение в легкие преимущественно зависит от размера частиц и скорости тока ингаляции. Поскольку проникновение в легкие увеличивается при уменьшении размера частиц (ММАД) в пределах диапазона 1-5 мкм, а частицы большего размера обычно ударяются в ротовую часть глотки, крупные дыхательные пути, а частицы менее 1 мкм обычно выдыхаются. Согласно одному аспекту настоящего изобретения композицию следует вводить путем ингаляции монодисперсных капель, образованных путем аэрозолизации данной композиции, где капли имеют масс-медианный аэродинамический диаметр 4-7 мкм, используя подходящий дозирующий ингалятор, обеспечивающий ток 10-50 л/мин. Дозирующий ингалятор может включать суживающее устройство для регуляции скорости тока.
Несколько дозирующих ингаляторов известно специалистам в данной области техники. Дозирующий ингалятор обычно предназначен для введения и доставки определенной дозы фармацевтического препарата в легкие, которая при действии пациента обеспечивает кратковременный выброс аэрозолизированного препарата, вдыхаемого, таким образом, пациентом. В кратком изложении, дозирующий ингалятор обычно включает нижеследующие компоненты:
i) контейнер, содержащий препарат для аэрозолизации, имеющий проксимальное отверстие, дающее возможность композиции выталкиваться из него,
ii) дозирующее устройство, обеспечивающее доставку предопределенного количества препарата для доставки при работе устройства, как, например, путем обеспечения энергии, прилагаемой к аксиально подвижному поршню;
iii) компрессор, состоящий из средств, обеспечивающих дозирование и доставку композиции; и
iv) мундштук, включающий распылительную насадку (РН), обеспечивающую образование аэрозолей, и посредством которого аэрозолизированное лекарство вдыхается пациентом при работе устройства, что, таким образом, приводит в результате к доставке аэрозолей композиции в легкие пациентов.
Средства для обеспечения дозирования и доставки композиции, могут быть, например, снабжены дозировочной кнопкой, которая доступна с наружной стороны дозирующего ингаляционного устройства, обеспечивающей перенос и доставку предопределенного количества лекарства, которое нужно вводить пациенту, и где сконцентрированная энергия, передаваемая от дозировочной кнопки на поршень, создает давление внутри контейнера для лекарства. Такое давление может быть также достигнуто любым источником энергии, хорошо известным специалистам в данной области техники, таким как, например, электрическая энергия (батарея), механическая энергия (мышцы) или физическая энергия (пропеллент).
Любой дозирующий ингалятор, обеспечивающий аэрозоли высококонцентрированного препарата аминогликозида, имеющие масс-медианный аэродинамический диаметр 4-7 мкм, можно использовать в соответствии с настоящим изобретением. Таким образом, подходящий дозирующий ингалятор, полезный для введения композиции по настоящему изобретению, может представлять собой дозирующий ингалятор, подходящий для координированной ингаляции композиции, или подходящий для ингаляции, активируемой вдохом, если этот дозирующий ингалятор включает РН, образующую аэрозоли высококонцентрированного препарата аминогликозида, имеющие масс-медианный аэродинамический диаметр 4-7 мкм, и где данный дозирующий ингалятор включает средства для обеспечения желаемого давления, гарантирующего перенос композиции по настоящему изобретению из контейнера через РН при ингаляции и приведении ингалятора в действие.
Согласно настоящему изобретению "капли" или "аэрозоли" представляют собой аэрозолизированные частицы жидкости, содержащей фармацевтический препарат, такой как высококонцентрированный раствор аминогликозида.
"ГСО" представляет собой геометрическое стандартное отклонение.
"Устройство Tobrair®", как используют в данной заявке, и на которое ссылаются в приведенных ниже примерах, представляет собой водный дозирующий ингалятор (ДИ), который образует монодисперсные капли композиции, содержащей высокие концентрации тобрамицина, имеющие MMAD 4-7 мкм.
Подходящий дозирующий ингалятор, полезный для введения препарата, содержащего высококонцентрированный раствор аминогликозида, такой как раствор 150-250 мг/мл тобрамицина, например, в форме тобрамицина сульфата, описан в WO 2011/043712, которая включена в данную заявку посредством ссылки.
Распылительная насадка (РН) помещена в мундштуке дозирующего ингалятора, используемого согласно настоящему изобретению, обеспечивая создание почти монодисперсных капель при ингаляциях (активируемой вдохом или координированной ингаляции) и работе пациентов с устройством. Более конкретно, при приложении, например, энергии к дозировочной кнопке, запуская, таким образом, приведение в действие компрессора, и путем координированного дыхания, помещая мундштук в рот пациента, работающего с устройством, композиция переносится из контейнера в мундштук и проталкивается через РН, что приводит в результате к образованию аэрозолей, имеющих масс-медианный аэродинамический диаметр 4-7 мкм, которые нужно вдыхать. РН включает множество сквозных отверстий, обеспечивающих образование аэрозоля.
Подходящая распылительная насадка (РН) для использования в дозирующем ингаляторе для обеспечения аэрозолей, имеющих масс-медианный аэродинамический диаметр 4-7 мкм, и содержащих высококонцентрированный раствор аминогликозида, описана в документе WO 02/18058, который включен в данную заявку посредством ссылки.
На фиг.6 показан водный дозирующий ингалятор, который можно использовать в соответствии с настоящим режимом введения. Данное устройство включает компрессор (3) многократного использования, держатель шприца, одноразовый контейнер для лекарства (стандартный шприц (2)) и мундштук (1), включающий распылительную насадку (РН).
вДИ, подходящий для введения композиции согласно настоящему изобретению, способен образовывать отдельные и однородные аэрозольные капли среднего диаметра от 4 до 7 микрон жидкости высокой вязкости. В документе WO 95/13860 описаны мембранные фильтры, снабженные порами, имеющими размер пор обычно от 5 нм до 50 мкм. Мембраны, раскрытые в данном документе, имеющие поры размера, обеспечивающие аэрозоли масс-медианного аэродинамического диаметра 4-7 мкм, можно предпочтительно использовать в распылительной насадке, помещенной в дозирующий ингалятор, такой как, например, дозирующий ингалятор, раскрытый в документе WO 2011/043712, для введения высококонцентрированной композиции тобрамицина согласно настоящему изобретению.
Согласно предпочтительной форме осуществления изобретения предложены аэрозоли, образованные дозирующим ингалятором, с использованием распылительной насадки, которая описана в статье в Respiratory Drug Delivery 8, 2002, авторами Wissink и van Rijn, которая включена в данную заявку посредством ссылки. Использование высокотехнологичных микронасадок, раскрытых в этом документе, обеспечивает отличное рэлеевское диспергирование с помощью отверстий 10 мкм при давлениях, проходящих через насадку, ниже 5 бар (5 МПа), с характеристиками струи со сдвигом от вязкого до кинетического. Для настоящего изобретения, когда композиция содержит 150-250 мг/мл аминогликозида, дозирующий ингалятор предпочтительно обеспечивает рабочее давление 20-80 (2-8 МПа) бар, более предпочтительно 30-40 бар (3-4 МПа).
Согласно настоящему изобретению РН включает средства для образования аэрозолей препарата высококонцентрированного раствора аминогликозида, имеющих масс-медианный аэродинамический диаметр 4-7 мкм (см. Wissink and van Rijn (2008), выше). Согласно одной форме осуществления РН состоит из силиконовой корзины (сетки) (4) и пластмассовых литых деталей из пластмассы марки для медицинского применения (см. фиг.7).
Контейнер, содержащий препарат для аэрозолизации, который нужно вдыхать, согласно одной форме осуществления может представлять собой шприц (10), такой как 1 мл шприц. Подходящий 1 мл шприц, имеющий подвижный поршень (8) и съемную и защитную крышку (7), которую удаляют перед вставкой шприца в дозирующий ингалятор, показан на фиг.8.
Дозирующий ингалятор, подходящий для настоящего режима введения, может включать дозировочную кнопку. Когда пациент прилагает давление к дозировочной кнопке на дозирующем ингаляторе, устройство активируется, и поршень (8) будет передвигаться на предопределенное расстояние, обеспечивая перенос соответствующей дозы из шприца через РН.
Когда устройство активируется, поршень (8) будет передвигаться на определенное расстояние (эквивалентное примерно 50 мкл), и жидкость будет продавливаться через ячейки в силиконовой корзине (сетке), создавая посредством этого капли, которые затем вдыхают. Это можно повторять необходимое число раз, чтобы составить суммарную ингаляционную дозу.
Например, поршень при движении может приводить в результате к тому, что предопределенное количество препарата, содержащего высококонцентрированный раствор аминогликозидов переносится и продавливается через отверстия в РН, обеспечивая образование аэрозолей, имеющих масс-медианный аэродинамический диаметр 4-7 мкм. Аэрозоли, таким образом, образуются при продавливании препарата, содержащего высококонцентрированный раствор аминогликозидов, через ячейки (отверстия) в РН, такой как силиконовая корзина (сетка) (5), создавая за счет этого капли, которые затем вдыхают (фиг.7). Это можно повторять необходимое число раз, чтобы доставить предписанную дозу.
Специалисту в данной области техники понятно, что, чтобы обладать способностью к переносу вязкого раствора через серию ячеек однородного размера, расположенных, например, в силиконовой пластине или мембране в РН для образования серии мелких аэрозолей согласно настоящему изобретению, нужно прилагать соответствующее давление. Дозирующий ингалятор, используемый согласно настоящему изобретению, способен обеспечить рабочее давление в диапазоне 20-80 бар (2-8 МПа). Предпочтительно, когда композицию, содержащую 180 мг/мл тобрамицина сульфата, нужно вдыхать, дозирующий ингалятор, используемый согласно настоящему изобретению, способен обеспечить рабочее давление в диапазоне 30-40 бар (3-4 МПа), предпочтительно 35 бар (3,5 МПа).
Композиция согласно настоящему изобретению при прохождении через РН вДИ будет выходить из ячеек в виде отдельных капель диаметром примерно в 1,8 больше диаметра ячеек. Следовательно, подходящий диаметр отверстий, присутствующих в РН, через которые должна переноситься композиция согласно настоящему изобретению, может находиться в интервале 1,8-3,9 мкм. Затем эти капли направляются по каналам в легкие при активации вдохом через мундштук, в результате чего избегают интенсивного соединения капель.
Подходящие ингаляторы, на которые ссылаются выше, включающие подходящие насадки, будут, следовательно, способны образовывать аэрозоли композиции, обладающей вязкостью вплоть до 5 мПа·с при высоких скоростях сдвига менее 50 с-1.
Подходящие ингаляторы будут обеспечивать скорость тока 10-50 л/мин.
Настоящее изобретение обладает несколькими преимуществами по сравнению с предшествующим уровнем техники. Время введения составляет менее 5 минут по сравнению с 20-30 минутами при использовании общепринятой, имеющейся в продаже системы введения (небулайзера TOBI®/PARI LC® PLUS). Кроме того, путем введения более низкого количества тобрамицина в сумме настоящее изобретение, тем не менее, обеспечивает доставку более высоких количеств тобрамицина в легкие (см. таблицу 12 и таблицу 13). Кроме того, способ по настоящему изобретению приводит в результате к более низким уровням тобрамицина в плазме по ср