Производные фуллеренов с пониженным сродством к электрону и фотовольтаическая ячейка на их основе
Иллюстрации
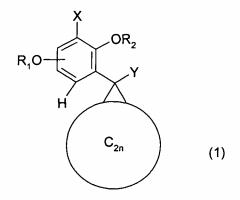
Показать всеНастоящее изобретение относится к новым соединениям общей формулы (1), которые используются в качестве основы тонкой полупроводниковой пленки в структуре солнечной батареи, к композиции, содержащей соединения формулы (1), и к применению новых соединений. В формуле (1): C2n - углеродный каркас фуллерена С60 или С70 с присоединенным циклопропановым аддендом; Y - заместитель, представляющий собой алкильную группу C1-C20, незамещенную фенильную группу, фенильную группу с заместителями в положениях 2 и 4 или 3 и 4, представляющими собой алкоксигруппы C1-C8; R1 и R2 представляют собой алкильную группу С2-С20, если Х=Н; R1 и R2 представляют собой алкильную группу C1-C20, если X является алкоксигруппой C1-C20. 3 н. и 4 з.п. ф-лы, 5 ил., 3 табл., 2 пр.
Реферат
Данное изобретение относится к использованию определенных замещенных фуллеренов в фотовольтаических ячейках, предпочтительно, в органических фотовольтаических ячейках, наиболее предпочтительно, в органических солнечных батареях с объемным гетеропереходом и фотодетекторах, для улучшения фотогенерированного напряжения и эффективности преобразования света в этих устройствах.
Фотовольтаические приборы обеспечивают самое простое и эффективное преобразование солнечной энергии в электричество. Первое поколение солнечных батарей на основе кристаллического кремния известно с середины прошлого века. Однако широкомасштабное распространение таких устройств долгое время лимитировалось их крайне высокой стоимостью. Средняя стоимость установки солнечных батарей на основе технологий кристаллического кремния составляет 2-3 доллара за каждый ватт энергии, генерированной при максимальном (пиковом) солнечном излучении, что обозначается как ватт/пик, Wp. Ожидается, что органические солнечные батареи будут способны производить электричество по цене 20 центов за Wp. К этому уровню можно приблизиться, получив устройства с эффективностью преобразования света 8-16% при очень низкой стоимости модуля (40-60 USD/м2). Дальнейшее усовершенствование солнечных батарей в плане эффективностей, времени жизни, дизайна модулей и технологий производства может привести к прорыву в технологиях возобновляемой энергии. В итоге, энергия, генерируемая при преобразовании солнечного света, должна стать дешевле, чем энергия, которую мы производим в настоящее время при сжигании ископаемого топлива.
Существует много дополнительных преимуществ органических тонкопленочных солнечных батарей, которые можно проиллюстрировать следующим:
- механическая гибкость позволяет адаптировать их к любым изогнутым поверхностям;
- малый вес органических тонкопленочных солнечных батарей делает их идеально подходящими для применений в портативной электронике;
- уже было продемонстрировано их интегрирование в ткань и навесы, используемые военными;
- высокая чувствительность при низких интенсивностях света позволяет применять их внутри помещения для сбора рассеянного света, преимущественно в качестве декоративных энергогенерирующих обоев.
Различные примеры органических солнечных батарей недавно вступили в фазу коммерциализации. Однако рыночный потенциал органических солнечных батарей ограничивается их относительно низкой эффективностью преобразования света и короткими временами жизни. Поэтому требуются значительные усовершенствования комбинаций фотоактивных материалов и архитектуры устройств.
Использование производных фуллеренов с пониженным сродством к электрону является одним из наиболее перспективных путей улучшения характеристик органических фотовольтаических устройств;
Использование производных фуллеренов с пониженным сродством к электрону в органических фотовольтаических ячейках уже было описано в DE 19515305 А1.
В US 6380027 В2 описывается использование производных фуллерена в солнечных батареях. Использование производных фуллерена в качестве материала n-типа в активном слое в фотовольтаических ячейках представлено в US 2010/0043876 А1.
В Science 1995, 270, 1789-1791 описывается использование метилового эфира [6,6]-фенил-С61-масляной кислоты ([60]-PCBM, далее РСВМ, структурная формула представлена на Фиг. 1) для увеличения эффективности преобразования света в полимерных солнечных батареях.
Использование бис-[70]РСВМ и бис-[60]РСВМ (см. Фиг. 2) в фотовольтаических ячейках описано в US 2010/0224252 А1. В Adv.Mater, 2008, 20, 2116 описывается использование бис-аддуктов РСВМ, обладающих пониженным сродством к электрону, для улучшения электрических характеристик органических солнечных батарей;
В WO 2009/086210 А2, Am.Chem.Soc. 2010, 132, 17381-17383; J.Mater.Chem., 2010, 20, 47; J.Mater.Chem., 2010, 20, 475; Adv. Mater. 2010, 22, 2283; Adv. Mater. 2010, 22, 4355; Mol.Cryst.Liq.Cryst. 2010, 519, 266; J.Mater.Chem., 2011, 21, 17345 раскрывается использование других типов бис-аддуктов фуллерена в качестве акцепторов для построения солнечных батарей на основе поли(3-гексилтиофена) P3HT с улучшенными свойствами (см. Фиг. 2, на котором показаны молекулярные структуры некоторых фуллереновых бис-аддуктов, используемых для создания улучшенных органических солнечных батарей).
В Adv. Funct. Mater., 2005, 15, 1979-1987; Org. Lett., 2007, 9, 551-554; J. Mater. Chem., 2010, 21, 1382 впервые было описано использование метоксифенильного или алкоксифенильного заместителей для уменьшения сродства к электрону производных фуллерена и увеличения напряжения в органических солнечных батареях (на Фиг. 3 показаны фуллереновые производные с алкоксифенильными группами, используемые как электроноакцепторные материалы в солнечных батареях).
В WO 2011/160021 А2 продемонстрировано использование фуллереновых производных, содержащих тетраалкоксифенильные заместители, для увеличения напряжения и эффективности преобразования света в органических солнечных батареях (Фиг. 3).
В JP 2012020949 А2 раскрывается использование фуллереновых производных с пониженным сродством к электрону, в частности тех, которые содержат замещенные фенильные группы следующей структуры:
где D=OR, SR, NR2 и R=С1-С30 алкильная группа.
Из Photovoltaics (2010, 89; J. Mater. Chem. (2010), 20(29), 6170; Physical Chemistry Chemical Physics (2010) 12(18), 4656; Physica Status Solidi RRL: Rapid Research Letters (2008), 2(6), 260; Am. Chem. Soc, 2001, 123, 6715; Thin Solid Films 2004, 451-452, 43; J.Org. Chem. 2006, 71, 2995; J. Am. Chem. Soc. 2008, 130, 6447; J. Phys.Chem. C, 2009, 113, 21970; J. Fluor. Chem. 2009, 130, 361, US 20070202413 известно множество других производных фуллерена с пониженным сродством к электрону.
Использование производных фуллерена с алкоксифенильными группами для увеличения напряжения в органических солнечных батареях также уже известно в научно-технической литературе. Однако достичь значительного увеличения эффективности преобразования света органических солнечных батарей при использовании таких производных фуллерена с алкоксифенильными группами не удалось. Как правило, увеличение напряжения холостого хода компенсируется уменьшением тока короткого замыкания и фактора заполнения. Такое поведение наблюдалось для многих соединений, описанных в предьщущих сообщениях. Например, в Adv. Func. Mater., 2005, 15, 1979-1987 и Org. Lett., 2007, 9, 551-554 не наблюдалось улучшения эффективности солнечных батарей в связи с использованием производных фуллерена с алкоксифенильными заместителями. В WO 2011/160021 А2 и JP 2012020949 А2 сообщалось об очень низкоэффективных солнечных батареях с эффективностями преобразования света в интервале 1.0-3.2%. Результатом использования производных фуллерена с алкоксифенильными заместителями было небольшое (50-60 мВ) увеличение напряжения холостого хода и довольно незначительное (0.4% в JP 2012020949 А2 и 0-0.7% в WO 2011/160021 А2) увеличение эффективности преобразования света органических солнечных батарей.
Низкий КПД солнечных батарей на основе производных фуллерена с алкоксифенильными заместителями связан с несбалансированными электронными и физико-химическими свойствами. В настоящее время не ясно, каково оптимально число фенильных заместителей D (см. вышеприведенные формулы) в одной фенильной группе в JP 2012020949 А2 и каковы их оптимальные положения на фенильном кольце, входящего в структуру производного фуллерена. Также недостаточно изучено влияние длины алкильных групп. Некоторые алкоксифенил замещенные циклопропановые производные фуллеренов в соответствии с предыдущей статьей представлены на Фиг. 4.
В связи с вышеописанными недостатками производных фуллерена с пониженным сродством к электрону в результате использования алкоксифенильного замещения, целью данного изобретения являлось создание производных фуллеренов, обладающие следующими свойствами:
1) обеспечивают значительное увеличение напряжения холостого хода органических солнечных батарей по сравнению с контрольными системами, в которых РСВМ
- используется как электронакцепторный материал;
2) имеют хорошую совместимость с различными электрондонорными материалами, например, спряженными полимерами и олигомерами, что позволяет достигать оптимальной морфологии композитов;
3) следовательно, обеспечивают значительное улучшение эффективности преобразования света органических солнечных батарей по сравнению с контрольными системами, в которых РСВМ используется как электронакцепторный материал;
4) имеют подходящие физико-химические свойства, например, достаточную растворимость в органическом растворителе, что требуется для изготовления устройств методом растворных технологий, достаточную термическую стабильность и фотостабильность для увеличения времени эксплуатации органических солнечных батарей и т.д.
Цель достигается с помощью новых соединений формулы (1)
где C2n - углеродный каркас C60 или С70фуллерена, имеющий адденд циклопропанового типа,
X представляет собой заместитель, выбранный из группы атома водорода, атома галогена, произвольным образом замещенной С2-С20 алкильной группы, С2-С20 фторированной алкильной группы, С2-С20 алкил-эфирной группы, С2-С20алкокси группы, С2-С20фторалкокси группы, С2-С20алкилтио группы, С2-С20фтороалкилтио группы, С5-С20алкиленарил группы или С5-С20алкиленгетероарил группы,
Y представляет собой заместитель, выбранный из группы атома водорода, произвольным образом замещенной C1-C20 алкильной цепи, С1-С20 фторированной алкильной группы, С1-С20 алкил-эфирной группы, С1-С20 фторированной алкил-эфирной группы, С5-С20алкиленарил группы или С5-С20алкиленгетероарил группы, незамещенной фенильной группы, фенильной группы, замещенной в позициях 2 и 4, фенильной группы, замещенной в позициях 2 и 5, фенильной группы, замещенной в позициях 2, 3 и 4, 2-тиенил группы, замещенной в позиции 5, (CH2)1-20COOR группы, где R представляет собой произвольным образом замещенную С1-С20алкил группу, С1-С20 фторированную алкил группу, С1-С20 алкил-эфирную группу, или С1-С20 фторированную алкил-эфирную группу, и
R1 и R2 одинаковы или независимы друг от друга и представляют собой произвольным образом замещенную С3-С20 алкильную группу, С3-С20 фторированную алкильную группу, С2-С20 алкил-эфирную группу, С2-С20 фторированную алкил-эфирную группу, С5-С20 алкиленарильную группу или алкиленгетероарильную группу или (CH2)1-20COOR группу, где R представляет собой произвольным образом замещенную С1-С20алкил группу, С1-С20 фторированную алкильную группу, С2-С20 алкил-эфирную группу, или фторированную С2-С20 алкил-эфирную группу.
В предпочтительном варианте осуществления данное изобретение относится к соединению формулы (1), где X и Y имеют вышеприведенные значения при условии, когда Х≠Н, R1 и R2 в формуле (1) одинаковы или независимы друг от друга и представляют собой произвольным образом замещенную С1-С20 алкил группу, С1-С20 фторированную алкильную группу, С1-С20 фторированную алкил-эфирную группу, С1-С20 алкиленарильную группу или алкиленгетероарильную группу или (CH2)1-20COOR группу, где R представляет собой произвольным образом замещенную С1-С20 алкильную группу, С1-С20 фторированную алкильную группу, С1-С20 алкил-эфирную группу, или С1-С20 фторированную алкил-эфирную группу.
В другом предпочтительном варианте осуществления данное изобретение направлено на соединение общей формулы (I), где X и Y имеют значения, указанные выше, при условии, когда X=Н, R1 и R2 в формуле (I) одинаковы или независимы друг от друга и представляют собой произвольным образом замещенную С3-С20 алкильную группу, С3-С20 фторированную алкильную группу, С2-С20 алкил-эфирную группу, С2-С20 фторированную алкил-эфирную группу, С5-С20 алкиленарильную группу или алкиленгетероарильную группу или (CH2)1-20COOR группу, где R представляет собой произвольным образом замещенную С1-С20алкил группу, С1-С20 фторированную алкильную группу, С2-С20 алкил-эфирную группу, или фторированную С2-С20 алкил-эфирную группу.
Для ясности следует отметить, что область настоящего изобретения включает все определения и параметры, представленные в общих условиях или в предпочтительных рамках в данном описании, в любой желаемой комбинации. Кроме того, "[60]" представляет собой C60фуллерен, а "[70]" С70фуллерен, а C2n представляет собой либо C60, либо С70 фуллереновую систему.
В предпочтительном варианте осуществления данного изобретения Y в формуле (1) представляет собой С1-С20 алкильную группу;
В предпочтительном варианте осуществления данного изобретения Y в формуле (1) представляет собой произвольным образом замещенную фенильную или 2-тиенильную группу;
В очень предпочтительном варианте осуществления данного изобретения Y в формуле (1) представляет собой С1-С20 алкильную группу или заместитель, выбранный из группы, состоящей из незамещенной фенильной группы, фенильной группы, замещенной в положениях 2 и 4, фенильной группы, замещенной в положениях 2 и 5, фенильной группы, замещенной в положениях 2, 3 и 4, или 2-тиенильной группы незамещенной или замещенной в положениях 4 и/или 5.
В другом предпочтительном варианте осуществления данного изобретения Y представляет собой 2-тиенильную группу незамещенную или замещенную в положениях 4 и/или 5;
В очень предпочтительном варианте осуществления данного изобретения Y в формуле (1) представляет собой 2,4-(RO)2C6H3 группу или 2,5-(RO)2C6H3 группу, где радикалы R представляют собой независимые друг от друга С3-С20 алкильную группу, С3-С20 фторированную алкильную группу, С2-С20 алкил-эфирную группу, С2-С20 фторированную алкил-эфирную группу, или (CH2)1-20COOR группу, в которой R представляет собой произвольным образом замещенную С1-С20 алкильную группу, С1-С20 фторированную алкильную группу, С2-С20 алкил-эфирную группу, или фторированную С2-С20 алкил-эфирную группу.
В другом очень предпочтительном варианте осуществления данного изобретения Y представляет собой группу формулы (2).
где радикал R′ является С2-С20 алкильной группой, С2-С20 фторированной алкильной группой, С2-С20 алкил-эфирной группой, С2-С20алкокси группой, С2-С20фтороалкокси группой, С2-С20алкилтио группой, С2-С20фторалкилтио группой или (CH2)1-20COOR группой, в которой R представляет собой произвольным образом замещенную С1-С20 алкильную группу, С1-С20 фторированную алкильную группу, С2-С20 алкил-эфирную группу, или фторированную С2-С20 алкил-эфирную группу, в то время как X и R1 имеют вышеназванные значения.
В другом очень предпочтительном варианте осуществления данного изобретения Y представляет собой C1-C8 разветвленную или неразветвленную алкильную группу.
В особенно предпочтительном воплощении данного изобретения Y представляет собой метальную группу.
В предпочтительном воплощении данного изобретения X представляет собой произвольным образом замещенную С2-С20 алкильную группу, С2-С20 фторированную алкильную группу, С2-С20алкокси группу, или С2-С20фторалкокси группу.
В очень предпочтительном воплощении данного изобретения X представляет собой дополнительно замещенную С2-С20алкокси группу.
В другом очень предпочтительном воплощении данного изобретения X представляет собой атом водорода.
В предпочтительном воплощении данного изобретения R1O и R2O прикреплены в позициях 2 и 4 фенильного кольца в формуле (1).
В другом предпочтительном воплощении данного изобретения R1O и R2O прикреплены в позициях 2 и 5 фенильного кольца в формуле (1).
В предпочтительном воплощении данного изобретения R1 и R2 одинаковы или независимы друг от друга и представляют собой произвольным образом замещенную C1-С20алкил группу или С1-С20 фторированную алкильную группу.
В очень предпочтительном воплощении данного изобретения R1 и R2 представляют собой одну и ту же С1-С8 алкильную группу.
В предпочтительном воплощении данного изобретения производные фуллерена в соответствии с данным изобретением используются в смеси по крайней мере двух соединений общей формулы (1), взятых в соответствующих соотношениях.
В очень предпочтительном воплощении данного изобретения производные фуллерена в соответствии с данным изобретением используются в смеси по крайней мере двух соединений общей формулы (1), взятых в соответствующих соотношениях в сочетании с 0.0001-99.9999% третьего компонента, который может быть представлен каким-либо функционализированным высшим фуллереном C>70, каким-либо растворителем, какой-либо обрабатывающей добавкой, кроме любого другого функционального компонента, улучшающего или не влияющего на характеристики производных фуллерена в заявленных оптоэлектронных устройствах, предпочтительно в органических фотовольтаических ячейках.
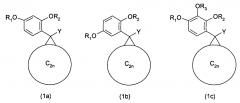
К данному изобретению относятся производные фуллеренов в соответствии с общей формулой (1), предпочтительно те, которые имеют два алкокси заместителя в положениях 2 и 4 фенильного кольца, как показано в формуле (1а), или два алкокси заместителя в положениях 2 и 5 фенильного кольца, как показано в формуле (1b), или три алкокси заместителя в положениях 2, 3 и 4 фенильного кольца, как показано в формуле (1с), где R3 имеет то же самое определение, как указано выше для R1 и R2, и C2n, представляющие собой или C60, или С70 фуллереновые системы, предпочтительно фуллерен C60.
Удивительно, что производные фуллерена в соответствии с данным изобретением имеют неожиданно более низкое сродство к электрону по сравнению с реперным материалом РСВМ. Первый электрохимический потенциал восстановления производного фуллерена, измеренный по методике, приведенной в J.Org.Chem. 1995, 60, 532, можно рассматривать в качестве меры сродства к электрону. В соответствии с Фиг. 1 [60]-РСВМ имеет потенциал восстановления -1.135 V vs Fc/Fc+. Производные фуллерена с более низким сродством к электрону должны обладать более отрицательным первым потенциалом восстановления (например, -1.140 V).
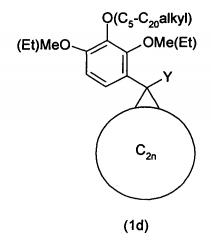
Без ограничения данного изобретения было обнаружено, что производные фуллеренов в соответствии с общей формулой (1), в частности те, которые имеют два С4-С20алкокси заместителя в фенильном кольце, как показано в формулах (1а) и (1b), или те, которые имеют один С5-С20алкокси заместитель в комбинации с двумя С1-С2алкокси заместителями, как показано в формуле (1d), демонстрируют неожиданно значительно улучшенную совместимость с рядом сопряженных полимеров. Примеры из литературы и в вариантах осуществления данного изобретения доказывают, что альтернативное размещение двух алкокси групп (например, в положениях 3, 4 или 2, 6 фенильного кольца) и трех алкоксильных групп (например, в позициях 3, 4, 5 или 2, 4, 6 фенильного кольца) обеспечивают худшую совместимость производных фуллерена с сопряженными полимерами и, следовательно, худшие фотовольтаические свойства.
Производные фуллеренов, описанные в данном изобретении, можно синтезировать, используя известные для специалиста методы. В качестве примера, производное фуллерена формулы (1е) можно получить по следующей схеме:
Коммерчески доступный 2,6-диметоксифенол алкилировали 2-этилгексилбромидом для получения соединения Р1, который далее подвергали взаимодействию с ацетилхлоридом в присутствии AlCl3 с бразованием ацетофенона Р2. Обработка Р2 п-тозилгидразидом позоляет получить P3. Реакция P3 с NaOMe и C60 в смеси 1,2-дихлолбензол/пиридин приводит к образованию соединения (1е) после хроматографического разделения на силикагеле.
Очень предпочтительными объектами данного изобретения являются производные фуллерена общей формулы (1f)
Где Y - метальная группа, R3 и R5 - независимы друг от друга и представляют собой разветвленную или неразветвленную C1-C8 алкильную группу, R4 - разветвленную или неразветвленную С3-С8 алкильную группу, и C2n является фуллереновой системой C60 или С70, предпочтительно фуллереном C60.
Особенно предпочтительными объектами данного изобретения являются производные фуллеренов формулы (1f), где Y - метил, R3 и R5 - метил, этил, изо-пропил, н-пропил, изо-бутил, н-бутил, трет-бутил, н-пентил или изо-пентил, предпочтительно изо-пентил или метил, и R4 - разветвленная или неразветвленная С5-С8 алкильная группа, предпочтительно разветвленная С5 или разветвленная C8 группа.
Особенно предпочтительными являются соединения фуллеренов, соответствующие данному изобретению согласно Таблице 1.
Данные соединения могут обладать такими свойствами, как оптимальная оптические свойства, хорошие зарядово-транспортные характеристики и химическая стабильность при комнатных условиях, возможность обработки при низких температурах, хорошая растворимость в обычных растворителях, а также возможностью использования разнообразных способов их обработки (например, путем использования различных растворных технологий,). В результате, оптоэлектронные устройства, предпочтительно солнечные батареи, которые состоят из одного или более данных соединений в качестве фотоактивного слоя, могут проявлять высокую эффективность в условиях окружающей среды, например, демонстрируя одну или несколько низко-энергетических запрещенных зон, высокий фактор заполнения, высокое напряжение холостого хода и высокую эффективность преобразования света, и предпочтительно, все эти критерии. Кроме того, другие устройства на основе органических полупроводников, такие как органические светоизлучающие транзисторы (OLETs) могут быть эффективно изготовлены с использованием органических полупроводниковых материалов, описанных выше.
Описанные разработки также предлагают методы получения таких соединений и полупроводниковых материалов, а также различных композиций, композитов и устройств, которые включают в себя соединения и полупроводящие материалы, описанные здесь. Следует понимать, что картинки и Фиг. 1-5 представлены только в целях иллюстрации принципов данного изобретения. В любом случае картинки не ограничивают границы данных изобретений. Соединения, представленные в данных разработках могут проявлять полупроводниковоые свойства, такие как оптимальные оптические свойства/разделение зарядов в фотовольтаическом устройстве; транспорт заряда/рекомбинацию/световое излучение в светоизлучающем устройства; и/или высокую подвижность носителя зарядов и/или хорошие характеристики модуляции тока в полевом транзисторе. Кроме того, данные соединения могут обладать определенными преимуществами обработки, такими как растворные технологии и/или высокая стабильность (например, стабильность на воздухе) в условиях окружающей среды. Соединения, представленные в данном изобретении, могут быть использованы для получения полупроводниковых материалов либо р-типа (донорный или дырочно-транспортный), n-типа (акцепторный или электрон-транспортный) или амбиполярных, которые, в свою очередь, можно использовать для изготовления различных органических или гибридных оптоэлектронных устройств, структур или приборов, в том числе органических фотовольтаических устройств и органических светоизлучающих транзисторов. Во всей заявке, при описании композиций, имеющих, или включающих, или состоящих из определенных компонентов, или при описании процессов, имеющих, или включающих, или состоящих из специфических этапов, мы подразумеваем, что композиции данного изобретения также существенно состоят из вышеназванных компонентов, и что процессы данных разработок также состоят из вышеназванных этапов.
В дополнении, если в заявке говорится, что элемент или компонент включен в и/или выбран из списка названных элементов или компонентов, это надо понимать так, что элемент или компонент может быть одним из названных элементов или компонентов, или что элемент или компонент может быть выбран из группы, состоящей из двух или более названных элементов или компонентов. Кроме того, следует понимать, что элементы и/или характерные черты композиции, прибора или метода, описанные здесь, могут комбинироваться различными способами, без отклонения от сути данных разработок, высказано ли это явно или подразумевается.
Использование терминов "включать", "включает", "в том числе", "иметь", "имеет" или "имеющий" следует понимать как допускающее и не ограничивающее изменения, если иное не устанавливается специальным образом.
Использование единственного числа включает множественное число (и наоборот), если иное не оговаривается специальным образом Кроме того, там, где термин "приблизительно" используется перед количественным значением, данные разработки также включают само определенное количественное значение, если иное не оговаривается специальным образом. Использование здесь термина "приблизительно" относится к ±10% отклонению от номинальной величины, если не оговаривается иное. Следует понимать, что порядок этапов или порядок проведения определенных действий несущественен до тех пор, пока данные разработки остаются в рабочем состоянии. Более того, два или более этапов или действий могут проводиться одновременно.
Используемый в заявке термин «полупроводниковый материал р-типа» или «донорный» материал относится к полупроводниковому материалу, например, органическому полупроводниковому материалу, имеющему дырки как основные носители тока или заряда. В некоторых случаях, когда полупроводниковый материал р-типа наносится на субстрат, он может обеспечить подвижность дырок свыше 10-5 см2/Вс. В случае полевых устройств на основе полупроводника р-типа также может наблюдаться соотношение тока вкл/выкл более 10.
Используемый в заявке термин «полупроводниковый материал n-типа» или «акцепторный» материал относится к полупроводниковому материалу, например, органическому полупроводниковому материалу, имеющему электроны как основные носители тока или заряда. В некоторых случаях, когда полупроводниковый материал n-типа наносится на субстрат, он может обеспечить электронную подвижность свыше 10-5 см2/Вс. В случае полевых устройств на основе полупроводника n-типа так же может наблюдаться соотношение тока вкл/выкл более 10.
Используемый в заявке термин «подвижность» относится к скорости, с которой носители заряда, например, дырки (или единицы положительного заряда) в случае полупроводникового материала р-типа и электроны (или единицы отрицательного заряда) в случае полупроводникового материала n-типа, двигаются через материал под влиянием электрического поля. Этот параметр, зависящий от архитектуры устройства, может быть измерен с использованием полевого транзистора или с помощью метода измерения тока, ограниченного объемным зарядом.
Используемый в заявке термин "эффективность преобразования света" (РСЕ) солнечной батареи - это процент энергии, преобразованной из поглощенного света в электрическую энергию. РСЕ солнечной батареи можно рассчитать, разделив величину максимальной мощности (Pm) при облучении светом (Е, в w/m2) в стандартных условиях (STC) и на площадь поверхности солнечной ячейки (Ас, в м2). STC обычно относится к температуре 25°С и освещенности светом мощностью 1000 Вт/м2, соответствующему спектру солнечного света AM 1.5.
Используемый в заявке термин компонент (например, тонкопленочный слой) может считаться «фотоактивным», если он содержит одно или более соединений, которые могут поглощать фотоны, производя экситоны для генерации фототока.
Используемый в заявке термин "имеющий возможность подвергаться растворным технологиям" относится к соединениям, предпочтительно полимерам, материалам или композициям, которые могут быть использованы в различныхпроцессах в растворе, в том числе, спинкоутинг, печать, предпочтительно струйная печать, гравюрная печать, офсетная печать и т.п., покрытие распылением, покрытие электрораспылением, капельное нанесение, нанесение покрытия методом погружения, и с использованием метода блейд-покрытия.
Используемый в заявке термин "полимерное соединение" (или "полимер") относится к молекуле, состоящей из множества одного или нескольких повторяющихся звеньев, связанных ковалентными химическими связями. Полимерный материал можно представить общей формулой
Где М - повторяющееся звено или мономер. Полимерный материал может иметь только один тип повторяющегося звена, а также два или более типов различных повторяющихся звеньев. Когда полимерное соединение может иметь только один тип повторяющегося звена, его называют гомополимер. Когда полимерный материал имеет два или более типов различных повторяющихся звеньев, используется термин "сополимер" или сополимерное соединение". Например, сополимерное соединение может включать повторяющиеся звенья
где Ма и Mb представляют собой два различных повторяющихся звена. Если не оговаривается иное, то соединение повторяющихся звеньев в сополимере может быть голова-к-хвосту, голова-к-голове, или хвост-к-хвосту. Кроме того, если не оговаривается иное, сополимер может быть статистическим сополимером, сополимером с регулярным чередованием мономерных единиц или блок-полимером. Например, можно использовать общую формулу
для представления сополимера Ма и Mb, имеющего мольную долю х Ма и мольную долю у Mb в сополимере, в котором сомономеры Ма и Mb могут чередоваться регулярным, случайным, регио-случайным, регио-регулярным образом. Кроме его состава, полимерное соединение можно далее охарактеризовать степенью полимеризации (n) и молярной массой (например, числовой средний молекулярный вес (Mn) и/или весовой средний молекулярный вес (Mw), в зависимости от методики измерения.
Как это используется в заявке, "гало" или "галоген" относится к фтор, хлор, бром и йод.
Как это используется в заявке, "оксо" относится к кислороду с двойной связью (то есть =O).
Как это используется в заявке, "алкил" относится к неразветвленной или разветвленной насыщенной углеводородной группе. Примерами алкильных групп являются метильная (Me), этильная (Et), пропильная (например, н-пропильная или изо-пропильная), бутильная (например, н-бутильная, изо-бутильная, втор-бутильная, трет-бутильная), пентильная (например, н-пентил, изо-пентил, нео-пентил), гексильная группы, и подобные группы. В различных воплощениях алкильная группа может иметь от 1 дл до 40 атомов углерода (то есть, С1-40 алкильная группа), например, 1-20 атомов углерода (то есть С1-20 алкильная группа). В некоторых воплощениях алкильная группа может иметь от 1 до 6 углеродных атомов, и ее можно называть «низшая алкильная группа». Примерами низших алкильных групп являются метил, этил, пропил (например, н-пропил и изо-пропил) и бутил группы (например, н-бутил, изо-бутил, втор-бутил, трет-бутил). В некоторых воплощениях алкильные группы могут быть замещены, как здесь описано. Обычно алкильная группа не замещается другой алкильной группой, алкенил группой или алкинил группой.
Как это используется в заявке, «галоалкил» относится к алкильной группе, имеющей один или более галогеновые галогеновых заместителизаместителей. В различных воплощениях галоалкильная группа может иметь от 1 до 40 атомов углерода (то есть, С1-40 галоалкильная группа), например, 1-20 атомов углерода (то есть С1-20 галоалкильная группа). Предпочтительными примерами галоалкильных групп являются CF3CHF2, CH2F, CCl3, CHCl2, CH2Cl, C2Cl5 и подобные. Пергалоалкильные группы, т.е., алкильные группы, где все водородные атомы замещены атомами галогена (например, CF3, и C2F5), относятся к определению «галоалкил». Например, С1-40 галоалкильная группа может иметь формулу
-, где Х0 в каждом случае является F, Cl, Br или I, s является целым числом в интервале от 1 до 40, и t - целое число в интервале от 1 до 81, при условии, что t меньше или равно 2s+1. Галоалкильные группы, не являющиеся пергалоалкильными группами, могут быть замещенными, как здесь описано.
Как это используется в заявке, «алкокси» относится к О-алкильной группе. Примеры алкокси-групп включают в себя, но не ограничиваются ими, метокси, этокси, пропокси (например, н-пропокси и изо-пропокси), т-бутокси, пентоксил, гексоксил группы, и подобные. Алкильная группа в О-алкильной группе может быть замещена, как здесь описано.
Как это используется в заявке, «алкилтио» относится к S-алкильной группе. Примеры алкилтио-групп включают в себя, но не ограничиваются ими, метилтио, этилтио, пропилтио (например, н-пропилтио и изо-пропилтио), т-бутилтио, пентилтио, гексилтио группы, и подобные. Алкильная группа в S-алкильной группе может быть замещена, как здесь описано.
Как это используется в заявке, «алкенил» относится к неразветвленной или разветвленной алкильной группе, имеющей одну или более углерод-углеродных двойных связей. Примеры алкенил групп включают этенил, пропенил, бутенил, пентенил, гексенил, бутадиенил, пентадиенил, гексадиенил группы, и подобные. Одна или более углерод-углеродных двойных связей может быть внутренней (как в 2-бутене) или концевой (как в 1-бутене). В различных воплощениях алкенильная группа может иметь от 2 до 40 углеродных атомов (т.е., С2-40 алкенильная группа), например, от 2 до 20 углеродных атомов (т.е., С2-20 алкенильная группа). В некоторых воплощениях алкенильные группы могут быть замещенными, как здесь описано. Обычно алкенильная группа не замещается другой алкенильной группой, алкильной группой или алкинил группой.
Как это используется в заявке, «алкинил» относится к неразветвленной или разветвленной алкильной группе, имеющей одну или более тройных углерод-углеродных связей. Примеры алкинил групп включают этининил, пропинил, бутинил, пентинил, гексинил, и подобные. Одна или более тройных углерод-углеродных связей может быть внутренней (как в 2-бутине) или концевой (как в 1-бутане). В различных воплощениях алкинильная группа может иметь от 2 до 40 углеродных атомов (т.е., С2-40 алкинильная группа), например, от 2 до 20 углеродных атомов (т.е., С2-20 алкинильная группа). В некоторых воплощениях алкинильные группы могут быть замещенными, как здесь описано. Обычно алкинильная группа не замещается другой алкинильной группой, алкильной группой или алкенильной группой.
Как это используется в заявке, «циклоалкил» относится к неароматической карбоциклической группе, включая циклические алкил, алкенил и алдкинил группы. В различный воплощениях, циклоалкильная группа может иметь от 3 до 24 атомов углерода, например, от 3 до 20 атомов углерода (например, С3-14 циклоалкильная группа). Циклоалкильная группа может быть моноциклической (например, циклогексил) или полициклической (