Способ лечения экспериментальной ретинопатии недоношенных
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к офтальмологии, и предназначено для лечения экспериментальной ретинопатии недоношенных (ЭРН). Новорожденным крысятам на фоне изменения концентрации кислорода во вдыхаемом воздухе от 60 до 15% каждые 12 часов при постоянном световом и температурном режиме в первые 14 дней постнатального периода ежедневно интраперитонеально вводят раствор мелатонина в дозе 10 мг/кг в объеме 30 мкл. Использование изобретения обеспечивает нормализацию гематоретинального барьера и антиоксидантного статуса в стекловидном теле крысят с ЭРН на фоне интраперитонеального введения мелатонина в период нарушения постнатального развития и созревания ретинальной сосудистой системы. 2 табл., 6 пр.
Реферат
Предлагаемое изобретение относится к офтальмологии и предназначено для лечения экспериментальной ретинопатии недоношенных и определения новых возможностей медикаментозного воздействия на развитие и прогрессирование ретинопатии недоношенных в клинике.
Ретинопатия недоношенных (РН) - тяжелое инвалидизирующее вазопролиферативное заболевание, многие аспекты патогенеза которого до конца не ясны.
Известно, что ангиогенез сетчатки носит кислородзависимый характер и одним из ключевых звеньев развития РН являются колебания степени оксигенации крови недоношенных детей на этапах выхаживания, являющиеся следствием эпизодов апноэ, бронхопульмональной дисплазии и других респираторных или метаболических осложнений, а также применения неадекватных схем кислородотерапии [Hartnett М.Е., Penn J.S. Mechanisms and Management of Retinopathy of Prematurity. N. Engl. J. Med. 2012; 367 (26): 2515-2526; Hartnett M.E. Studies on the Pathogenesis of Avascular Retina and Neovasculatization into the Vitreous in Peripheral Severe Retinopathy of Prematurity (An American Ophthalmological Society Thesis). Trans. Am. Ophthalmol. Soc. 2010; 108: 96-119]. Кроме того, незрелые нейроваскулярные ткани зрительной системы недоношенных детей, в частности сетчатка, чрезвычайно чувствительны к воздействию образующихся в результате развивающегося оксидативного стресса активных форм кислорода [Penn J.S,. Thum L.A., Naash M.I. Oxygen-Induced Retinopathy in the Rat. Vitamins С and Ε as Potential Therapies. Invest. Ophthalmol. Vis. Sci. 1992; 33 (6): 1836-1845; Saito Y., Geisen P., Uppal Α., Hartnett M.E. Inhibition of NAD(P)H oxidase reduces apoptosis and avascular retina in an animal model of retinopathy of prematurity. Mol. Vis. 2007; 13: 840-53], повреждающее действие которых потенцируется в силу незрелости компонентов антиоксидантной системы недоношенных детей [Saito Y., Geisen P., Uppal Α., Hartnett M.E. Inhibition of NAD(P)H oxidase reduces apoptosis and avascular retina in an animal model of retinopathy of prematurity. Mol. Vis. 2007; 13: 840-53].
Важное значение в изучении патогенеза РН играет экспериментальное моделирование. В настоящее время в исследованиях, посвященных изучению патогенеза РН, наиболее широко применяются модели ретинальной неоваскуляризации на грызунах, в частности на крысятах, в силу довольно высокого сходства развивающейся у них экспериментальной ретинопатии недоношенных (ЭРН) с РН у детей и целого ряда преимуществ работы с мелкими лабораторными животными [Grossniklaus Н.Е., Kang S.J., Berglin L. Animal models of choroidal and retinal neovascularization. Prog. Retin. Eye Res. 2010; 29 (6): 500-19; Barnett J.M., Yanni S.E., Penn J.S. The Development of Rat Model of Retinopathy of Prematurity. Doc. Ophthalmol. 2010; 120 (1): 3-12]. Важно отметить, что ключевую роль в развитии ЭРН у крысят играют именно колебания концентрации подаваемого в ходе эксперимента кислорода [Cunningham S., McColm J.R., Wade J., Sedowofia K., McIntosh N., Fleck В. A novel model of retinopathy of prematurity simulating preterm oxygen variability in the rat. Invest. Ophthalmol. Vis. Sci. 2000; 41 (13): 4275-4280], схемы подачи которого в разных моделях различны.
Наиболее близкой по своему течению к РН у детей является модель Пенна 50/10, в которой новорожденные крысята в течение первых двух недель своей жизни подвергаются воздействию 12-часовых колебаний концентрации кислорода от 50% до 10% [Penn J.S., Tolman B.L., Lowery L.A. Variable oxygen exposure causes preretinal neovascularization in the newborn rat. Invest. Ophthalmol. Vis. Sci. 1993; 34 (3): 576-585]. Данная модель обладает высокой воспроизводимостью, что повышает достоверность результатов проводимых с ее использованием экспериментальных исследований [Grossniklaus Н.Е., Kang S.J., Berglin L. Animal models of choroidal and retinal neovascularization. Prog. Retin. Eye Res. 2010; 29 (6): 500-19].
Актуальность проведения исследований с использованием экспериментальных моделей, помимо изучения вопросов этиопатогенеза РН, обусловлена возможностью поиска новых патогенетически ориентированных подходов к ее профилактике и лечению. Так, в настоящее время в качестве перспективного агента для профилактики и лечения заболеваний, индуцируемых окислительным стрессом, к числу которых относится и РН, активно рассматривается мелатонин [Gitto Ε, Marseglia L, Manti S, D′Angelo G, Barberi I, Salpietro C, Reiter RJ. Protective role of melatonin in neonatal diseases. Oxid Med Cell Longev. 2013; 2013: 980374].
Мелатонин (N-ацетил-5-метокситриптамин) синтезируется преимущественно в эпифизе из нейротрансмиттера серотонина и играет важную роль в регуляции циркадных ритмов, а также функций целого ряда систем организма, включая зрительную, репродуктивную, цереброваскулярную, нейроэндокринную и иммунную [Brzezinski A. Melatonin in humans. The New England Journal of Medicine. 1997; 336 (3): 186-195], обладая широким спектром антиоксидантных, противовоспалительных, нейропротекторных, а также антиангиогенных свойств [Park SY, Jang WJ, Yi ΕΥ, Jang JY, Jung Y, Jeong JW, Kim YJ. Melatonin suppresses tumor angiogenesis by inhibiting HJF-1 alpha stabilization under hypoxia. J Pineal Res. 2010 Mar; 48 (2): 178-84].
Известно, что помимо эпифиза синтез мелатонина осуществляется также в тканях глаза, а именно в сетчатке и цилиарном теле [Siu AW1, Maldonado M, Sanchez-Hidalgo M, Tan DX, Reiter RJ. Protective effects of melatonin in experimental free radical-related ocular diseases. J Pineal Res. 2006 Mar; 40 (2): 101-9], и что в сетчатке взрослых млекопитающих мелатонин способен подавлять продукцию некоторых провоспалительных цитокинов, фактора роста эндотелия сосудов, а также снижать активность индуцибельной NO-синтазы [Sande Р.Н., Fernandez D.C., Aldana Marcos H.J., Chianelli M.S., Aisemberg J., Silberman D.M., ., Rosenstein R.E. Therapeutic effect of melatonin in experimental uveitis // Am J. Pathol. 2008. Vol. 173. №6. P. 1702-1713]. Кроме того, есть данные, свидетельствующие о способности мелатонина стабилизировать гематоретинальный барьер в условиях развития гипоксии [Kaur С, Sivakumar V, Yong Ζ, Lu J, Foulds WS, Ling EA. Blood-retinal barrier disruption and ultrastructural changes in the hypoxic retina in adult rats: the beneficial effect of melatonin administration. J Pathol. 2007 Aug; 212 (4): 429-39].
Мы предположили, что мелатонин, в силу многообразия своих свойств, способен воздействовать на целый ряд факторов патогенеза PH.
Ближайшим аналогом предлагаемого способа является способ лечения ЭРН путем интраперитонеального введения липосомальной супероксиддисмутазы (СОД) (Niesman MR, Johnson KA, Penn JS. Therapeutic effect of liposomal superoxide dismutase in an animal model of retinopathy of prematurity. Neurochem Res. 1997 May; 22 (5): 597-605). Новорожденных крысят с момента рождения помещали в условия постоянной гипероксии (80%). Часть крысят интраперитонеально получала экзогенную СОД, инкапсулированную в полиэтиленгликоль-модифицированных липосомах. Еще одна группа опытных крысят получала липосомы без СОД. Контрольную группу составили крысята, находившиеся с момента рождения в условиях с нормальным содержанием кислорода. Ежедневно на протяжении 14 дней часть крысят выводили из эксперимента, в их сетчатке оценивали содержание общей активности СОД и магний-ассоциированной СОД, также проводили компьютерный анализ плотности сосудистой сети и площади аваскулярной сетчатки. У животных, находившихся в условиях постоянной гипероксии, отмечалось значительное снижение уровня активности ретинальной СОД на 6 сутки жизни по сравнению с крысятами, находившимися в условиях с нормальным содержанием кислорода. На 6 сутки жизни ежедневное введение липосом-инкапсулированной СОД значительно повышало активность ретинальной СОД и снижало степень кислород-индуцированной задержки роста сосудов, что подтверждалось повышением сосудистой плотности и уменьшением площади аваскулярных зон по сравнению с крысятами, подверженными воздействию постоянной гипероксии, но получавшими «контрольные» липосомы (без СОД).
Главным недостатком описанного способа является использование модели ЭРН, не соответствующей современным представлениям о ведущей роли в инициации патологической вазопролиферации при РН именно колебаний кислорода. Механизмы, лежащие в основе развития ЭРН в описанном эксперименте и РН у детей, обладают некоторыми различиями, что ставит под сомнение возможность использования полученных результатов в клинике.
Задачей предлагаемого способа является разработка способа лечения ЭРН с целью обоснования возможности клинического применения мелатонина для профилактики и лечения PH.
Техническим результатом предлагаемого изобретения является нормализация гематоретинального барьера и антиоксидантного статуса в стекловидном теле крысят с ЭРН на фоне интраперитонеального введения мелатонина в период нарушения постнатального развития и созревания ретинальной сосудистой системы.
Технический результат достигается за счет ежедневного интраперитонеального введения раствора мелатонина в дозе 10 мг/кг в объеме 30 мкл крысятам в течение первых 14 суток после рождения на фоне изменения концентрации кислорода во вдыхаемом воздухе от 60 до 15% каждые 12 часов при постоянном световом и температурном режиме.
Исследование было выполнено на 48 крысятах породы Вистар в соответствии с ГОСТ 53434-2009 от 02.12.2009 "Принципы надлежащей лабораторной практики GLP", постановлением главного государственного врача РФ №51 от 29.08.2014 "Об утверждении СП 2.2.1.3218-14" Санитарно-эпидемиологические требования к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев), Федеральным законом №61-ФЗ от 12.04.2010 "Об обращении лекарственных средств". Протокол исследования был утвержден локальным этическим комитетом.
Крысят (n=12) вместе с родившей их самкой, начиная с первых суток после рождения на 14 суток помещали в инкубатор, где каждые 12 часов концентрация кислорода менялась от 60 до 15%. Затем крысят помещали в условия с нормальным содержанием кислорода (21%). На протяжении эксперимента в помещении поддерживали постоянный температурный (+26°C) и световой (12 часов день, 12 часов ночь) режимы. Предлагаемая нами модель является более совершенной по сравнению с моделью в аналоге и с моделью Пенна. Развивающаяся ретинопатия максимально приближена по развитию и механизмам к РН у детей в клинике. С целью моделирования мы применяли колебания концентрации кислорода от 60 до 15%, создавая гипоксию. Контрольную группу составили крысята (n=12), находившиеся с момента рождения в условиях с нормальным содержанием кислорода.
Еще двум группам крысят, находившихся в опытных (n=12) и контрольных (n=12) условиях, с 1 по 14 сутки интраперитонеально вводили раствор мелатонина (Sigma-Aldrich) в стерильном 0,05 M фосфатном буферном растворе (pH 7,4) объемом 30 мкл в дозировке 10 мг/кг. При выборе дозировки интраперитонеальных инъекций мы ориентировались на данные литературы, в которых изучалось влияние интраперитонеального введения экзогенного мелатонина на показатели окислительного стресса крыс в условиях травмы [ and Mustafa . Melatonin reduces traumatic brain injury-induced oxidative stress in the cerebral cortex and blood of rats. Neural Regen Res. 2014 Jun 1; 9 (11): 1112-1116] и при диабетической ретинопатии [Ozremir G, Ergun Y, Bakaris S, Bakaris S, Kilinc M, Durdu H, Ganiyusufoglu E. Melatonin prevent retinal oxidative stress and vascular changes in diabetic rats. Eye (Lond). 2014 Aug; 28 (8): 1020-7]. Важно отметить, что при патологиях, указанных в этих работах, окислительный стресс развивается в зрелых тканях и является следствием поражения сосудистой стенки и перфузионных нарушений иной этиологии, в то время как при РН отмечается первичная «оксидативная» атака и ишемическое повреждение незрелых «недоразвитых» структур.
Данные о применении мелатонина при экспериментальной РН в литературе не обнаружены.
Крысят выводили из эксперимента на 7 (n=16), 14 (n=16) и 18 (n=16) сутки. Всем крысятам проводили бинокулярную энуклеацию, после чего глазное яблоко вскрывали по лимбу, удаляли роговицу и хрусталик, а с помощью полосок фильтровальной бумаги шириной 5 мм проводили забор образцов стекловидного тела. Фрагмент полоски, пропитанный жидкой частью стекловидного тела, взвешивали и помещали в 50-кратный объем 0,05 M фосфатного буферного раствора pH 7,4 для элюирования компонентов стекловидного тела на 20 минут. Затем образец центрифугировали в течение 10 мин при 4000 об/мин и надосадочную жидкость использовали для исследования.
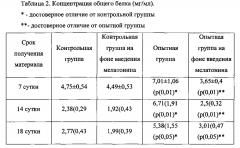
В каждом образце стекловидного тела определяли антиокислительную активность (АОА) по параметрам кинетики хемилюминесценции в модельной системе гемоглобин-H2O2-люминол [Гулидова О.В., Любицкий О.Б., Клебанов Г.И., Чеснокова Н.Б. Изменение антиокислительной активности слезной жидкости при экспериментальной ожоговой болезни глаз. // Бюллетень экспериментальной биологии и медицины. 1999, т. 128, №11, с. 571-574] и концентрацию общего белка по Лоури [Lowry О., Rozebrough Ν., Farr Α., Randell R. Protein measurement with the folin phenol reagent. J. Bio Chem. 1951. Vol. 193. Р. 265-275].
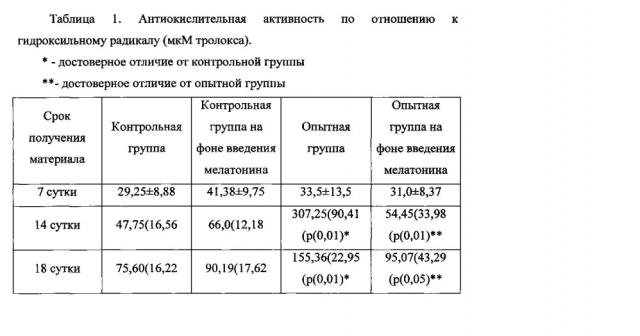
Для измерения показателей антиокислительной активности была использована модельная система гемоглобин-H2O2-люминол, в которой в качестве субстрата окисления выступает люминол [Гулидова О.В., Любицкий О.Б., Клебанов Г.И., Чеснокова Н.Б. Изменение антиокислительной активности слезной жидкости при экспериментальной ожоговой болезни глаз. Бюллетень экспериментальной биологии и медицины. 1999, т. 128, №11, с. 571-574]. Измерения проводили с использованием хемилюминометра "Биотокс-7" (Россия, НПО Энергия). Измеряемым параметром являлась величина латентного периода, характеризующая АОА по отношению к гидроксильному радикалу (АОА-ОН-) [Любицкий О.Б. Определение антиоксидантной активности биологических жидкостей хемилюминесцентным методом. Автореф. канд. дис., 1999]. Для построения калибровочной кривой использовали тролокс, который представляет собой водорастворимый аналог витамина Е. АОА-ОН- биологического материала по отношению к гидроксильному радикалу выражали в эквивалентной концентрации тролокса (мкмоль/л).
Статистическую обработку результатов проводили с использованием статистического пакета Microsoft Excel. Исследуемые выборки подвергнуты тесту на нормальность распределения. Показатели с нормальным распределением представлены как среднее значение (М) и стандартное отклонение (m), достоверность различий между группами с уровнем значимости не менее 95% оценена с помощью параметрического t-критерия Стьюдента.
Проведенные исследования показали, что развитие ЭРН при данном способе моделирования сопровождается резким повышением АОА и концентрации белка в стекловидном теле, что свидетельствует о выраженных нарушениях проницаемости гематоретинального барьера и важной роли окислительного стресса в ее этиопатогенезе. Интраперитонеальное введение мелатонина в дозе 10 мг/кг в объеме 30 мкл в период созревания сосудистой сети сетчатки крысят после рождения привело к тому, что содержание общего белка и уровень АОА в стекловидном теле крысят с ЭРН снизились практически до уровня данного показателя в контрольной группе крысят на всех сроках наблюдения (таб. 1 и 2).
Способ осуществляют следующим образом.
Крысят вместе с родившей их самкой, начиная с первых суток постнатального периода на 14 суток помещают в инкубатор, где каждые 12 часов концентрация кислорода меняется от 60 до 15%. Затем крысят переводят в условия с нормальным содержанием кислорода (21%). На протяжении эксперимента в помещении поддерживается постоянный температурный (+26°C) и световой (12 часов день, 12 часов ночь) режимы.
С 1 по 14 сутки крысятам интраперитонеально вводят раствор мелатонина (Sigma-Aldrich) в стерильном 0,05 M фосфатном буферном растворе (pH 7,4) объемом 30 мкл в дозировке 10 мг/кг.
Примеры.
Пример 1. Крысенок №1 с рождения находился в условиях с нормальным содержанием кислорода, выведен из эксперимента на 14 сутки. Уровень антиокислительной активности (мкМ тролокса) в стекловидном теле правого глаза составил 30,5, левого глаза - 35,5, концентрация белка (мг/мл) - соответственно 2,53 и 2,05. Полученные данные можно рассматривать в качестве нормы для данного срока исследования.
Пример 2. Крысенок №1 с рождения находился в условиях с нормальным содержанием кислорода, выведен из эксперимента на 18 сутки. Уровень антиокислительной активности (мкМ тролокса) в стекловидном теле правого глаза составил 68,5, левого глаза - 86,0, концентрация белка (мг/мл) - соответственно 2,46 и 2,88. Полученные данные можно рассматривать в качестве нормы для данного срока исследования.
Пример 3. Крысенок №3, начиная с первых суток после рождения, на 14 суток помещен в инкубатор, где каждые 12 часов концентрация кислорода менялась от 60 до 15%, выведен из эксперимента на 14 сутки. Уровень антиокислительной активности (мкМ тролокса) в стекловидном теле правого глаза составил 289,0, левого глаза - 321,0, концентрация белка (мг/мл) - соответственно 6,26 и 6,40. Таким образом, на 14 сутки уровень АОА и концентрация общего белка в стекловидном теле крысят с КИР в несколько раз превысили таковые у крысят контрольной группы, что свидетельствует о выраженном нарушении гематоретинального барьера при ЭРН и поступлении компонентов антиокислительной системы в стекловидное тело из патологически измененной ретинальной сосудистой сети, кроме того, определенный вклад может носить возможное увеличение синтеза антиоксидантов in situ в самой сетчатке (супероксиддисмутаза, каталаза, глутатионпероксидаза, мелатонин и др.) в ответ на развивающийся окислительный стресс.
Пример 4. Крысенок №3, начиная с первых суток после рождения, на 14 суток помещен в инкубатор, где каждые 12 часов концентрация кислорода менялась от 60 до 15%, затем переведен в условия с нормальным содержанием кислорода, выведен из эксперимента на 18 сутки. Уровень антиокислительной активности (мкМ тролокса) в стекловидном теле правого глаза составил 156,5, левого глаза - 136,0, концентрация белка (мг/мл) - соответственно 6,69 и 9,44. Таким образом, к 18 суткам у крысят опытной группы отмечалось снижение уровня АОА практически в 2 раза по сравнению с 14 сутками, но при этом он был достоверно выше, чем в контрольной группе. Концентрация общего белка оставалась практически на том же уровне, что и на 14 сутки, что свидетельствует о сохраняющемся на 18 сутки нарушении гематоретинального барьера при ЭРН, на фоне которого снижение АОА говорит скорее не об уменьшении интенсивности процессов перекисного окисления, а о возросших затратах антиоксидантов в борьбе с активными формами кислорода.
Пример 5. Крысенок №5, начиная с первых суток после рождения, на 14 суток помещен в инкубатор, где каждые 12 часов концентрация кислорода менялась от 60 до 15%, ежедневно получал интраперитонеальные инъекции раствора мелатонина (Sigma-Aldrich) в стерильном 0,05 M фосфатном буферном растворе (рН 7,4) объемом 30 мкл в дозировке 10 мг/кг, выведен из эксперимента на 14 сутки. Уровень антиокислительной активности (мкМ тролокса) в стекловидном теле правого глаза составил 17,5, левого глаза - 15,8, концентрация белка (мг/мл) - соответственно 2,79 и 2,27. Таким образом, на фоне инъекций мелатонина уровни изучаемых показателей на 14 сутки у крысенка с ЭРН приблизились к контрольным значениям на том же сроке. Полученные результаты можно объяснить, как способностью мелатонина стабилизировать гематоретинальный барьер при ЭРН, так и проявлением его выраженных антиангиогенных и антиоксидантных свойств.
Пример 6. Крысенок №6, начиная с первых суток после рождения, на 14 суток помещен в инкубатор, где каждые 12 часов концентрация кислорода менялась от 60 до 15%, затем переведен в условия с нормальным содержанием кислорода, ежедневно в течение первых 14 суток жизни получал интраперитонеальные инъекции раствора мелатонина (Sigma-Aldrich) в стерильном 0,05 M фосфатном буферном растворе (pH 7,4) объемом 30 мкл в дозировке 10 мг/кг, выведен из эксперимента на 18 сутки. Уровень антиокислительной активности (мкМ тролокса) в стекловидном теле правого глаза составил 57,0, левого глаза - 71,5, концентрация белка (мг/мл) - соответственно 2,92 и 3,03. Таким образом, на фоне инъекций мелатонина уровни изучаемых показателей на 18 сутки у крысенка с ЭРН приблизились к контрольным значениям на том же сроке. Полученные результаты можно объяснить как способностью мелатонина стабилизировать гематоретинальный барьер при ЭРН, так и проявлением его выраженных антиангиогенных и антиоксидантных свойств.
Таким образом, мелатонин при интраперитонеальном введении его раствора в объеме 30 мкл в дозе 10 мг/кг на протяжении первых 14 суток жизни крысят способствует стабилизации гематоретинального барьера при ЭРН, а также оказывает выраженное антиангиогенное и антиоксидантное действие. Полученные данные позволяют рассматривать мелатонин и его аналоги в качестве потенциального медикаментозного средства для профилактики и лечения РН в клинике.
Способ лечения экспериментальной ретинопатии недоношенных, отличающийся тем, что крысятам на фоне изменения концентрации кислорода во вдыхаемом воздухе от 60 до 15% каждые 12 часов при постоянном световом и температурном режиме в первые 14 дней постнатального периода ежедневно интраперитонеально вводят раствор мелатонина в дозе 10 мг/кг в объеме 30 мкл.