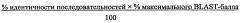Моноклональные антетела к cd44, предназначенные для применения при лечении плоскоклеточной карциномы головы и шеи
Иллюстрации
Показать всеИзобретение относится к области биохимии, в частности к применению моноклонального антитела к CD44 или его антигенсвязывающего фрагмента для лечения плоскоклеточной карциномы головы и шеи (HNSCC) у млекопитающего, где HNSCC отличается экспрессией CD44. Указанное антитело к CD44 можно получать с помощью гибридомы, которая депонирована в АТСС под регистрационным номером РТА-4621, а также оно может представлять собой его химерные или гуманизированные версии. Изобретение обеспечивает возможность эффективного лечения HNSCC с помощью неконъюгированных («голых») антител к CD44. 3 н. и 9 з.п. ф-лы, 15 ил., 6 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к способам предупреждения, лечения или диагностирования плоскоклеточной карциномы головы и шеи (HNSCC) с использованием одного или нескольких модифицирующих злокачественное заболевание антител (cancerous disease modifying antibodies (CDMAB)). В конкретных вариантах осуществления изобретения CDMAB представляет собой антитело, специфическое в отношении CD44. Описаны также способы комбинированной терапии, заключающиеся в том, что применяют CDMAB, предлагаемое в изобретении, необязательно в сочетании с одним или несколькими вторыми CDMAB и/или химиотерапевтическими агентами в качестве средств предупреждения или лечения рака.
Предпосылки создания изобретения
Плоскоклеточная карцинома головы и шеи (HNSCC) представляет собой изнурительное и приводящее к смертельному исходу заболевание, которое присутствует, как правило, в последней стадии и ежегодно поражает 50000 человек в Соединенных Штатах и 500000 человек во всем мире. HNSCC представляет собой заболевание, которое характеризуется выраженными болезненными состояниями, прежде всего связанными с нарушением функции речи и глотательной функции. Общепринятыми путями лечения является хирургическое вмешательство, лучевая терапия, химиотерапия или их комбинация.
Несмотря на применение комбинаций «жестких» методов лечения, включающих хирургическое вмешательство, химиотерапию и лучевую терапию, показатель эффективности лечения на поздних стадиях заболевания достигает лишь 30% и рецидив остается наиболее частой причиной (у 40%-50% пациентов) неблагоприятного исхода после проведения стандартных терапий. Терапия по жизненным показателям включает те же пути лечения, которые применяют для терапии первой линии. Однако паллиативная хирургия часто является сложной и оказывается недостаточной. Кроме того, лучевая терапия редко является осуществимой или оказывает благоприятное воздействие, а химиотерапия не приводит к значительному повышению коэффициента выживаемости страдающих HNSCC пациентов. Прогноз для таких пациентов остается плохим, при этом медианная продолжительность жизни после рецидива составляет лишь примерно шесть месяцев.
Плохой исход может являться результатом неэффективного уничтожения инициирующих образование опухоли клеток или раковых стволовых клеток (CSC). CSC обладают способностью к самообновлению, а также дают потомство с дифференцированным фенотипом и ограниченным самообновлением. CSC, подобно здоровым стволовым клеткам, являются устойчивыми к химиотерапии и лучевой терапии благодаря их обеспечивающим выживаемость преимуществам, таким как повышенная способность к репарации ДНК. Фактически стандартные схемы химиотерапии, например, основанной на применении цисплатина, и лучевой терапии на самом деле увеличивают популяцию стволовых клеток.
CD44 играет решающую роль в онкогенезе. Трансмембранный гликопротеин, CD44, связывает гиалоурановую кислоту (НА) во внеклеточном матриксе и в белках цитоскелета. Взаимодействия между CD44, НА, компонентами цитоскелета и сигнальными молекулами, такими как циклин D1, EGFR, Rho и Ras, ускоряют рост и миграцию. Кроме того, CD44 высвобождается из мембраны в растворимой форме (solCD44) под действие матриксных металлопротеиназ (ММР), что имеет решающее значение для миграции клеток. Установлено также, что CD44 может являться важным маркером CSC, он обнаружен при раке молочной железы, различных видах колоректального рака и HNSCC. На моделях, созданных с использованием ксенотрансплантатов, установлено также, что CD44 обладает активностью в отношении образования опухолей; опухолевые клетки CD44+-HNSCC являются онкогенными для мышей с нарушенным иммунитетом, в то время как контрольные опухолевые клетки CD44--HNSCC не образовывали опухоли при использовании этих же моделей.
VFF-18, обозначенное также как BIWA 1, представляет собой антитело, обладающее высокой аффинностью к v6-варианту CD44, специфическое в отношении области полипептида, включающей положения 360-370. Различные версии или производные BIWA 1 проходили изучение в клинических исследованиях в качестве средств лечения рака. В частности, BIWA 1 применяли в виде меченного с помощью 99mтехнеция конъюгата на фазе 1 клинического исследования, которое проводили с целью оценки безопасности и способности оказывать целевое воздействие с участием 12 пациентов, страдающих плоскоклеточной карциномой головы и шеи. Через 40 ч после инъекции 14% инъецируемой дозы было поглощено опухолью, при этом накопление в других органах, таких как почки, селезенка и костный мозг, оказалось минимальным. Хотя высокая селективность связывания с опухолью позволяет допустить возможность применения BIWA 1 в радиоиммунотерапии, излишне высокая аффинность этого антитела препятствует проникновению указанного антитела в более глубокие слои опухоли. Кроме того, установлено также, что BIWA 1 обладает выраженной иммуногенностью. У одиннадцати из двенадцати пациентов образовались человеческие антимышиные антитела (НАМА), что характеризовалось гетерогенным накоплением в опухоли и приводило к образованию комплексов антитело-растворимый CD44.
B WO 02/094879 описаны гуманизированные версии VFF-18, созданные с целью преодоления НАМА-ответа, которые обозначены как BIWA 4 и BIWA 8. Установлено, что BIWA 4 обладал существенно более низкой аффинностью связывания антигена по сравнению с родительским антителом VFF 18. При этом для обладающего пониженной аффинностью антитела BIWA 4 были выявлены более высокие характеристики поглощения опухолью по сравнению с обладающим более высокой аффинностью BIWA 8. Антитела BIWA 4, меченные с как помощью 99mтехнеция, так и с помощью 186рения, изучали на фазе 1 клинического исследования, выполненного на 33 пациентах, которое проводили с целью оценки безопасности, накопления опухолью, а в случае меченного с помощью 186Re BIWA 4 - максимальной переносимой дозы. Обнаружено зависящее от опухоли поглощение меченного с помощью 99mTc BIWA 4. Не обнаружено никаких ответов опухолей на применение меченного с помощью 186Re BIWA 4 в любых дозах. Хотя в процессе исследования для нескольких пациентов было достигнуто стабильное состояние болезни; была выявлена ограничивающая дозу токсичность, которая составляла 60 мКи/м2. Обнаружено также 50-65% случаев нежелательных явлений, при этом у 12 из 33 пациентов нежелательные явления были классифицированы как серьезные (тромбоцитопения, лейкопения и лихорадка). Кроме того 6 из 12 пациентов, которые все подвергались лечению с использованием меченного с помощью 186Re BIWA 4, умерли в процессе лечения или в последующий период наблюдения из-за прогрессирующего развития заболевания. У двух пациентов обнаружено также образование человеческих античеловеческих антител (НАНА). Таким образом, для меченных с помощью радиоактивных изотопов VFF-18 не удалось продемонстрировать какие-либо клинические действия.
Осуществляли также фазу 1 исследования с использованием возрастающих доз меченного с помощью 186Re BIWA 4 с включением в опыт 20 пациентов. Обнаружены оральный мукозит и ограничивающие дозу тромбоцитопения и лейкоцитопения; у одного пациента обнаружен НАНА-ответ. Стабильное состояние заболевания обнаружено у 5 пациентов, для лечения которых применяли самую высокую дозу 60 мКи/м2. Хотя было установлено, что средство являлось приемлемым как с позиций безопасности, так и переносимости при применении в указанном диапазоне доз, исследования продемонстрировали только стабилизацию заболевания. Кроме того, в указанных исследованиях обнаружена более высокая частота побочных явлений по сравнению с другими изученными в клинических исследованиях терапиями, основанными на применении не включающих радиоизотопы конъюгатов биологических агентов.
В заявке на патент США 2003/0103985 описана гуманизированная версия VFF-18 (BIWA 4), конъюгированная с майтансиноидом, которую обозначили как BIWI 1, предназначенная для противоопухолевой терапии. Установлено, что BIWI 1 обладал выраженным противоопухолевым действием на мышиных моделях человеческой эпидермоидной карциномы вульвы, плоскоклеточной карциномы глотки и карциномы молочной железы. Неконъюгированная версия, т.е. BIWA 4, не обладала противоопухолевым действием. Для конъюгированного варианта BIWI 1 отсутствуют данные о безопасности или эффективности для людей.
МАт U3 6 представляет собой мышиное моноклональное антитело в виде IgG1, которое получали путем иммунизации клетками человеческой карциномы гипофаринкса линии UM-SCC-22B, и которое отбирали по признаку специфичности в отношении типа рака и ткани. Характеризация антигена с помощью клонирования кДНК и анализа последовательности позволила идентифицировать эпитоп МАт U36, расположенный в домене v6 специфического для кератиноцитов сплайсингового варианта CD44, обозначенного как эпикан. Иммуногистохимические исследования продемонстрировали, что распознаваемый эпитоп локализован в клеточной мембране. Было установлено, что МАт U36 обладало выраженной способностью связываться с 94% плоскоклеточных карцином головы и шеи (HNSCC) и в этих опухолях обнаружено однородное окрашивание клеток.
У 10 пациентов, которых в опыте обрабатывали меченным с помощью 99mTc МАт U36, обнаружено избирательное накопление антитела при разных типах HNSCC (20,4±12,4% от инъецируемой дозы/кг через 2 дня); отсутствуют данные о побочных действиях, однако у двух пациентов образовались НАМА. В опыте, в котором использовали мышиное МАт U36, меченное радиоактивным йодом, обнаружено 3 случая НАМА в группе из 18 пациентов и избирательное гомогенное поглощение клетками HNSCC. Для снижения антигенности МАт U36 и снижения уровня НАМА создавали химерное антитело, при этом ни химерное, ни исходное МАт U36, не обладало ADCC-активностью. Однако в исследовании не обнаружена противораковая активность немеченого МАт U36.
Меченное с помощью 186Re химерное МАт U36 использовали для решения вопроса о возможности применения МАт U36 в качестве терапевтического средства. На этой фазе 1 исследования с использованием возрастающих доз 13 пациентам вводили предварительную (пробную) дозу меченного с помощью 99mTc химерного МАт U36, а затем меченного с помощью 186Re-химерного МАт U36. Не обнаружено острых нежелательных явлений. Однако после обработки ограничивающая дозу миелотоксичность (1,5 ГБк/м2) обнаружена у двух из трех пациентов и у одного пациента, обработанного максимальной переносимой дозой (1,0 ГБк/м2) выявлена тромбоцитопения. Хотя обнаружено определенное воздействие на размер опухолей, эти воздействия не удовлетворяли критериям объективных ответов на лечение. В другом исследовании меченного с помощью 186Re химерного МАт U36 применяли стратегию, основанную на использовании реинфузии стимулированной колониестимулирующим фактором цельной крови для достижения удвоенной максимально переносимой активности, составлявшей 2,8 Гр. В этом опыте из девяти пациентов с различным видом рака головы и шеи трем потребовалось переливание крови из-за связанной с лекарственным средством анемии. Другие проявления токсичности включали миелотоксичность 3 степени и мукозит 2 степени. Не обнаружено никаких объективных ответов опухолей, хотя было достигнуто стабильное состояние болезни в течение 3-5 месяцев у 5 пациентов.
Вследствие плохого прогноза для страдающих HNSCC пациентов, воздействия болезни на качество жизни и ограниченных вариантов лечения существует большой интерес и, следовательно, необходимость в разработке новых терапий HNSCC. К настоящему времени отсутствуют данные о так называемых «голых» (т.е. неконъюгированных) антителах к CD44, обладающих эффективностью в отношении HNSCC. Так, хотя CD44, вероятно, является потенциальной мишенью для противораковой иммунотерапии, для достижения противораковых действий антител к CD44 необходимо их применение в виде радиоиммуноконъюгата. Однако исследования, проведенные с меченными с помощью радиоактивных изотопов антителами к CD44, продемонстрировали возникновение ассоциированной с такой терапией нежелательной токсичности, сопровождающей получаемые клинические действия. Таким образом, существует необходимость в разработке новых специфических для HNSCC терапий.
В основу настоящего изобретения была положена техническая задача разработать способы и средства, предназначенные для предупреждения, лечения или диагностирования HNSCC с использованием антител к CD44, и согласно некоторым объектам изобретения, прежде всего немеченых антител к CD44.
Данная техническая задача решается с помощью представленных вариантов осуществления изобретения, охарактеризованных в формуле изобретения.
Краткое изложение сущности изобретения
Настоящее изобретение относится к новым способам предупреждения, лечения или диагностирования плоскоклеточной карциномы головы и шеи (HNSCC), заключающимся в том, что применяют антитела к CD44. Согласно конкретным объектам изобретения применяют антитела к CD44, которые связываются с аминоконцевым доменом внеклеточного домена CD44 и/или которые иммуноспецифически связываются с одним или несколькими, предпочтительно с множеством вариантов человеческого CD44, которые экспрессируются в организме людей. Согласно конкретным объектам изобретения применяют антител к CD44, продуцируемое гибридомой, которая депонирована в АТСС под регистрационным номером РТА-4621, и их варианты и/или производные, например, химерные и гуманизированные версии РТА-4621. Изобретение относится также к применению антител и их антигенсвязывающих фрагментов, которые конкурируют за связывание с РТА-4621.
Антитела и фрагменты, которые применяют в способах, предлагаемых в изобретении, являются специфическим в отношении CD44, в частности CD44, который экспрессируется на поверхности клетки, и предпочтительно являются специфическими в отношении аминоконцевого внеклеточного домена одного или нескольких вариантов человеческого CD44, например, который экспрессируется на поверхности раковых клеток при HNSCC. Согласно конкретным объектам изобретения антитела, которые применяют в способах, представленных в настоящем описании, представляют собой гуманизированные или химерные версии антитела, продуцируемого гибридомой, которая депонирована в АТСС под регистрационным номером РТА-4621. В конкретных вариантах осуществления изобретения антитела, которые применяют в способах, представленных в настоящем описании, или их антигенсвязывающие фрагменты содержат один или несколько из следующих участков:
CDR1 вариабельной области тяжелой цепи (VH), который имеет аминокислотную последовательность RYWMS (SEQ ID NO:3),
CDR2 VH, который имеет аминокислотную последовательность EVNPDSTSINYTPSLKD (SEQ ID NO:4),
CDR3 VH, который имеет аминокислотную последовательность PNYYGSRYHYYAMDY (SEQ ID NO:5),
CDR1 вариабельной области легкой цепи (VL), который имеет аминокислотную последовательность RASQDINNYLN (SEQ ID NO:6),
CDR2 VL, который имеет аминокислотную последовательность YTSRLHS (SEQ ID NO:7); и
CDR3 VL, который имеет аминокислотную последовательность QQGSTLPFT (SEQ ID NO:8).
Антитела, подпадающие под объем изобретения, могут содержать также два или большее количество, три или большее количество, четыре или большее количество, пять или большее количество и в некоторых объектах изобретения все гипервариабельные участки, такие как CDR1 VH, который имеет аминокислотную последовательность, представленную в SEQ ID NO:3, CDR2 VH, который имеет аминокислотную последовательность, представленную в SEQ ID NO:4, CDR3 VH CDR3, который имеет аминокислотную последовательность, представленную в SEQ ID NO:5, CDR1 VL, который имеет аминокислотную последовательность, представленную в SEQ ID NO:6, CDR2 VL, который имеет аминокислотную последовательность, представленную в SEQ ID NO:7, и CDR3 VL, который имеет аминокислотную последовательность, представленную в SEQ ID NO:8.
Антитела и антигенсвязывающие фрагменты, которые применяют в способах, предлагаемых в изобретении, могут содержать:
VH-домен, который имеет аминокислотную последовательность
EVKLLESGGGLVQPGGSLKLSCATSGFDFSRYWMSWVRQAPGKGLEWIGEVNPDSTSINYTPSLKDQFIISRDNAKNTLDLQMSKVSSEDTALYYCTRPNYYGSRYHYYAMDYWGQGTSVTVSS (SEQ ID NO:1),
и/или VL-домен, который имеет аминокислотную последовательность
DIQMTQTTSSLSVSLGDRVTINCRASQDINNYLNWYQQKPDGTVKLLIYYTSRLHSGVPSRFSGSGSGTDFSLTISNLEKEDVATYFCQQGSTLPFTFGSGTKLEIK (SEQ ID NO:2).
Конкретными объектами изобретения является применение антитела к CD44 или его антигенсвязывающего фрагмента, которое/который содержит VH-домен, имеющий аминокислотную последовательность, представленную в SEQ ID NO:1, и VL-домсн, имеющий аминокислотную последовательность, представленную в SEQ ID NO:2.
Изобретение относится также к применению антитела к CD44 или его антигенсвязывающих фрагментов для лечения, предупреждения или диагностирования HNSCC, где антитело к CD44 является гуманизированным.
Согласно некоторым объектам изобретения гуманизированное антитело к CD44 или его антигенсвязывающий фрагмент содержит:
VH-домен, который имеет аминокислотную последовательность
EVQLVESGGGLVQPGGSLRLSCAASGFDFSRYWMSWVRQAPGKGLVWVGEVNPDSTSINYTPSLKDRFTISRDNAKNTLYLQMNSLRAEDTAVYYCTRPNYYGSRYHYYAMDYWGQGTLVTVSS (SEQ ID NO:9) или
EVQLVESGGGLVQPGGSLRLSCATSGFDFSRYWMSWVRQAPGKGLVWIGEVNPDSTSINYTPSLKDQFTISRDNAKNTLYLQMNSLRAEDTAVYYCTRPNYYGSRYHYYAMDYWGQGTLVTVSS (SEQ ID NO:10)
и/или VL-домсн, который имеет аминокислотную последовательность
DIQMTQSPSSLSASVGDRVTITCRASQDINNYLNWYQQKPGKAPKLLIYYTSRLHSGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQGSTLPFTFGQGTKLEIK (SEQ ID NO:11).
Конкретным объектом изобретения является гуманизированное антитело к CD44 или его антигенсвязывающий фрагмент, предназначенное/предназначенный для применения для предупреждения, лечения или диагностирования HNSCC у индивидуума, где гуманизированное антитело к CD44 содержит VH-домен, который имеет аминокислотную последовательность, представленную в SEQ ID NO:9, и VL-домен, который имеет аминокислотную последовательность, представленную в SEQ ID NO:11, или где антитело к CD44 содержит VH-домен, который имеет аминокислотную последовательность, представленную в SEQ ID NO:10, и VL-домен, который имеет аминокислотную последовательность, представленную в SEQ ID NO:11. В конкретных объектах изобретения индивидуум представляет собой человека. Изобретение относится также к применению гуманизированного антитела к CD44 или его антигенсвязывающего фрагмента для предупреждения, лечения или диагностирования HNSCC у индивидуума, где гуманизированное антитело к CD44 содержит VH-домен, который имеет аминокислотную последовательность, представленную в SEQ ID NO:9, и VL-домсн, который имеет аминокислотную последовательность, представленную в SEQ ID NO:11, или где антитело к CD44 содержит VH-домен, который имеет аминокислотную последовательность, представленную в SEQ ID NO:10, и VL-домен, который имеет аминокислотную последовательность, представленную в SEQ ID NO:11.
Согласно некоторым объектам изобретения антитело или его фрагмент, которое/который применяют согласно способам, предлагаемым в изобретении, распознает эпитоп в аминоконцевом домене внеклеточной области CD44, которая имеет аминокислотную последовательность AFDGPITITIV (SEQ ID NO:12).
Антитела к CD44, предназначенные для применения согласно изобретению, можно конъюгировать с активными фрагментами, такими как терапевтические или репортерные фрагменты. Антитела к CD44 можно конъюгировать также с гематогенными клетками из организма индивидуума. Согласно некоторым объектам изобретения терапевтические фрагменты представляют собой фрагменты, для которых в данной области известно благоприятное действие при лечении, предупреждении или диагностировании HNSCC, такие как (но, не ограничиваясь только ими) цитотоксин, фермент, радиоактивный элемент, цитокин, антиметаболит или интерферон.
Изобретение относится также к применению антител к CD44 или их антигенсвязывающих фрагментов в качестве единственного средства лечения или в сочетании с одним или несколькими другими химиотерапевтическими или диагностическими агентами и/или терапиями. Таким образом, изобретение относится к применению антител к CD44 (например, гуманизированных или химерных антител) или их антигенсвязывающих фрагментов в сочетании со стандартным или экспериментальными схемами лечения HNSCC (например, химиотерапия, радиоиммунотерапия или лучевая терапия). Примеры терапевтических агентов, которые являются наиболее предпочтительными для применения в сочетании с CD44-специфическим антителом или его антигенсвязывающим фрагментом согласно способам, представленным в настоящем описании, для предупреждения, лечения или диагностирования HNSCC, включают (но, не ограничиваясь только ими) химиотерапевтические средства, известные в данной области, алкилирующие агенты, антиметаболиты, продукты естественного происхождения и гормоны. Комбинированные терапии, представленные в настоящем описании, могут позволять снижать дозы антитела к CD44 или его антигенсвязывающего фрагмента и/или уменьшать частоту введения антитела к CD44 или его антигенсвязывающего фрагмента индивидууму, который страдает HNSCC, для достижения терапевтического или профилактического действия. Согласно способам, представленным в настоящем описании, антитела к CD44 или их антигенсвязывающие фрагменты можно вводить совместно, вводить одновременно и/или вводить последовательно с одним или несколькими другими химиотерапевтическими или диагностическими агентами, или их можно применять в сочетании с лучевой терапией или хирургическим вмешательством. Введение антител, фрагментов и/или дополнительных агентов или терапий можно осуществлять с помощью любых методов, известных в данной области, которые пригодны для обеспечения достижения конкретным агентом или терапией месту локализации опухоли. Указанное введение может быть парентеральным (например, IV, внутримышечное или подкожное введение), оральным или в некоторых объектах изобретения, представлять собой непосредственное введение вместо опухоли или вместо ожидаемого распространения опухоли или рецидива опухоли. Антитела, фрагменты и/или композиции можно применять также в виде форм с пролонгированным высвобождением.
Изобретение относится также к фармацевтической композиции, предназначенной для предупреждения, лечения или диагностирования HNSCC у индивидуума, которая содержит (I) в терапевтически эффективном количестве антитело к CD44, представленное в настоящем описании (например, химерное или гуманизированное антитело), или его антигенсвязывающий фрагмент; и (II) фармацевтически приемлемый носитель.
В настоящем описании представлены способы диагностирования HNSCC у индивидуума, который, как предполагается, имеет указанное заболевание, заключающиеся в том, что: (I) приводят в контакт биологический образец, полученный из организма индивидуума, с взятым в эффективном количестве антителом к CD44, представленным в настоящем описании, или его антигенсвязывающим фрагментом; и (II) определяют связывание антитела или его фрагмента, где выявление уровня антитела или фрагмента, превышающего фоновый и стандартный уровень, свидетельствует о наличии HNSCC у индивидуума. Для облегчения выявления антитела к CD44 или его фрагмента можно применять выявляемый маркер, известный в данной области. Изобретение относится также к диагностическому или прогностическому набору, предназначенному для выявления HNSCC в образце ткани из организма пациента, для которого известно или предполагается наличие HNSCC-клеток. Согласно некоторым объектам изобретения набор содержит средства выявления CD44, в частности экспрессируемого HNSCC-клетками и/или в образцах ткани из организма индивидуума, для которого известно или предполагается наличие HNSCC-клеток. Набор может содержать (1) моноклональное антитело, продуцируемое гибридомой, которая депонирована в АТСС под регистрационным номером РТА-4621, (2) антитело, которое конкурирует за связывание с моноклональным антителом, продуцируемым гибридомой, которая депонирована в АТСС под регистрационным номером РТА-4621; (3) антитело, которое содержит один или несколько из следующих участков: CDR1 VH, аминокислотная последовательность которого представлена в SEQ ID NO:3, CDR2 VH, аминокислотная последовательность которого представлена в SEQ ID NO:4, CDR3 VH, аминокислотная последовательность которого представлена в SEQ ID NO:5, CDR1 VL, аминокислотная последовательность которого представлена в SEQ ID NO:6, CDR2 VL, аминокислотная последовательность которого представлена в SEQ ID NO:7 и CDR3 VL, аминокислотная последовательность которого представлена в SEQ ID NO:8; или (4) антигенсвязывающий фрагмент антитела, указанного в подпункте (1), (2) или (3). Набор может включать также один или несколько следующих компонентов: субстрат или контейнер для содержания биологического образца, референс-стандарт(ы) или биомаркер(ы) в растворе или в твердой форме (например, CD44 или пептид, специфически связанный с антителом, продуцируемым антителом РТА-4621), одно или несколько антител, специфических в отношении биомаркеров (например, антитело РТА-4621 и его антигенсвязывающийся фрагмент или вариант, или производное), и инструкции по осуществлению анализа(ов), предназначенного(ых) для выявления биомаркеров с использованием содержимого набора.
Еще одним объектом изобретения является предложенный способ лечения HNSCC с помощью антитела РТА-4621 или его антигенсвязывающего фрагмента. Другим объектом изобретения является предложенный способ диагностирования HNSCC с помощью антитела РТА-4621 или его антигенсвязывающего фрагмента. Следующим объектом изобретения является предложенное применение РТА-4621 или его антигенсвязывающего фрагмента для прогнозирования или определения стадии HNSCC. Следующим объектом изобретения является предложенное применение РТА-4621 или его антигенсвязывающего фрагмента для выбора пациента, у которого можно лечить HNSCC.
Согласно некоторым объектам изобретения антитела к CD44 и их антигенсвязывающие фрагменты, предназначенные для применения в способах, представленных в настоящем описании, могут содержать аминокислотную последовательность VH-области и/или VL-области, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% идентична аминокислотной последовательности VH-области и/или VL-области мышиного моноклонального антитела, продуцируемого гибридомой, которая депонирована в АТСС под регистрационным номером РТА-4621, при условии, что антитела к CD44 или их фрагменты обладают способностью специфически связываться с CD44 и/или конкурируют за связывание с РТА-4621. Изобретение относится также к применению антител к CD44 или их антигенсвязывающих фрагментов, которые содержат аминокислотную последовательность VH-области и/или VL-области, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% идентична VH-области, которая имеет аминокислотную последовательность, представленную в SEQ ID NO:1, и/или VL-области, которая имеет аминокислотную последовательность, представленную в SEQ ID NO:2, при условии, что антитела к CD44 или их фрагменты обладают способностью специфически связываться с CD44 и/или конкурируют за связывание с РТА-4621. Некоторыми объектами настоящего изобретения являются антитела или их фрагменты, которые специфически связываются с CD44 и которые содержат аминокислотную последовательность одного или нескольких CDR, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% идентична аминокислотной последовательности одного или нескольких CDR мышиного моноклонального антитела, продуцируемого гибридомой, которая депонирована в АТСС под регистрационным номером РТА-4621, при условии, что антитела или их фрагменты обладают способностью специфически связываться с CD44 и/или конкурируют за связывание с РТА-4621. Изобретение относится также к применению антител к CD44 или их антигенсвязывающих фрагментов, которые содержат аминокислотную последовательность одного или нескольких CDR, которые по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% идентичны одному или нескольким из следующих участков: CDR1 VH, который имеет аминокислотную последовательность SEQ ID NO:3, CDR2 VH, который имеет аминокислотную последовательность SEQ ID NO:4, CDR3 VH, который имеет аминокислотную последовательность SEQ ID NO:5, CDR1 VL, который имеет аминокислотную последовательность SEQ ID NO:6, CDR2 VL, который имеет аминокислотную последовательность SEQ ID NO:7 и CDR3 VL, который имеет аминокислотную последовательность SEQ ID NO:8, при условии, что антитела или их фрагменты обладают способностью специфически связываться с CD44 и/или конкурируют за связывание с РТА-4621.
Настоящее изобретение относится также к применению гуманизированных антител и фрагментов антител, специфических в отношении CD44, или конкурирующих за связывание с антителом РТА-4621, в котором одна или несколько областей одного или нескольких CDR вариабельных доменов тяжелой и/или легкой цепи человеческого антитела (антитело-реципиент) заменена(ы) аналогичными частями одного или нескольких CDR моноклонального антитела-донора, которое специфически связывается с CD44, например, мышиного моноклонального антитела, продуцируемого клоном РТА-4621. Предпочтительно гуманизированное антитело специфически связывается с тем же эпитопом, что мышиное антитело-донор. Как должно быть очевидно специалисту в данной области, изобретение относится в целом к трансплантации CDR антител. Согласно конкретным объектам настоящее изобретения относится к применению гуманизированных антител или фрагментов антител, которые специфически связываются с CD44 и/или конкурируют за связывание с РТА-4621, где гуманизированные антитела или фрагменты антител содержат аминокислотную последовательность VH-области и/или VL-области, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% идентична VH-области, аминокислотная последовательность которой представлена в SEQ ID NO:9 или SEQ ID NO:10, и/или VL-области, аминокислотная последовательность которой представлена в of SEQ ID NO:11.
Антитела к CD44 и их антигенсвязывающие фрагменты, которые можно применять согласно способам, представленным в настоящем описании, могут кодироваться нуклеотидной последовательностью, которая гибридизуется в строгих условиях с нуклеотидной последовательностью, кодирующей VH-область, полную тяжелую цепь, VL-область или полную легкую цепь мышиного моноклонального антитела РТА-4621. Согласно другим объектам изобретение относится к применению антитела к CD44 или его антигенсвязывающего фрагмента, содержащего VH-область, которая кодируется нуклеотидной последовательностью, гибридизующейся в строгих условиях с нуклеотидной последовательностью, которая кодирует аминокислотную последовательность, представленную в SEQ ID NO:1, SEQ ID NO:9 или SEQ ID NO:10. Согласно другим объектам изобретение относится к применению антитела к CD44 или его антигенсвязывающего фрагмента, содержащего VL-область, которая кодируется нуклеотидной последовательностью, гибридизующейся в строгих условиях с нуклеотидной последовательностью, которая кодирует аминокислотную последовательность, представленную в SEQ ID NO:2 или SEQ ID NO:11. Изобретение относится также к применению антитела к CD44 или его антигенсвязывающего фрагмента, содержащего один или несколько CDR, кодируемого(ых) нуклеотидной последовательностью, гибридизующейся в строгих условиях с нуклеотидной последовательностью, которая кодирует один или несколько CDR мышиного моноклонального антитела РТА-4621, или с нуклеотидной последовательностью, кодирующей один или несколько из следующих участков: CDR1 VH, аминокислотная последовательность которого представлена в SEQ ID NO:3, CDR2 VH, аминокислотная последовательность которого представлена в SEQ ID NO:4, CDR3 VH, аминокислотная последовательность которого представлена в SEQ ID NO:5, CDR1 VL, аминокислотная последовательность которого представлена в SEQ ID NO:6, CDR2 VL, аминокислотная последовательность которого представлена в SEQ ID NO:7, и CDR3 VL, аминокислотная последовательность которого представлена в SEQ ID NO:8. Строгие условия гибридизации включают (но не ограничиваясь только ими) (I) гибридизацию со связанной с фильтром ДНК в 6×растворе хлорида натрия/цитрата натрия (SSC) примерно при 45°С, с последующей(ими) одной или несколькими отмывками в 0,2×SSC/0,1% ДСН примерно при 50-65°С; (II) очень строгие условия, такие как гибридизация со связанной с фильтром ДНК в 6×SSC примерно при 45°С, с последующей(ими) одной или несколькими отмывками 0,1×SSC/0,2% ДСН примерно при 60°С, или (III) любые другие строгие условия гибридизации, известные специалистам в данной области.
Изобретение относится также к применению вектора, который содержит нуклеиновые кислоты, представленные в настоящем описании (т.е. нуклеиновые кислоты, кодирующие VL-области, VL-области и/или один или несколько CDR антитела к CD44 или его антигенсвязывающие фрагменты). В определенных вариантах осуществления изобретения указанный вектор представляет собой экспрессионный вектор и нуклеотидные последовательности, которые кодируют аминокислотные последовательности, представленные в настоящем описании, функционально связаны с нуклеотидными регуляторными последовательностями или последовательностями, кодирующими аминокислотные регуляторные последовательности (например, сигналы транскрипции, трансляции, транслокации), необходимые для правильной экспрессии кодируемых аминокислотных последовательностей. Изобретение относится также к клеткам-хозяевам, которые содержат векторы или нуклеотидные последовательности, кодирующие антитела или фрагменты антител, представленные в настоящем описании.
Другие объекты и преимущества настоящего изобретения должны стать очевидными из представленного ниже описания, в котором приведены с целью иллюстрации и примера, определенные варианты осуществления настоящего изобретения.
Определения
В целом, использованные в разделах «Краткое изложение сущности изобретения», «Подробное описание изобретения», «Примеры» и «Формула изобретения» понятия и фразы имеют указанные ниже значения.
Понятие «антитело» в контексте настоящего изобретения применяют в наиболее широком смысле, и оно относится, в частности, к индивидуальным моноклональным антителам (включая агонстические, антагонистические и нейтрализующие антитела, деимунизированные (с пониженной иммуногенностью), мышиные, химерные, гуманизированные или человеческие антитела), композиции антител с полиэпитопной специфичностью, одноцепочечные антитела, димерные антитела (диабоди), тримерные антитела (триабоди), иммуноконъюгаты, синтетические антитела, камелизированные антител, одноцепочечные Fv(scFv), Fab-фрагменты, F(ab')-фрагменты, связанные дисульфидным мостиком Fv(sdFv), внутриклеточные антитела (интрабоди) и антиидиотипические антитела (анти-Id) (включая, например, анти-Id и анти-анти-Id антитела к антителам, предлагаемым в изобретении) и эпитопсвязывающие фрагменты любого из перечисленные выше антител. В частности, антитела включают молекулы иммуноглобулинов и иммунологически активные фрагменты молекул иммуноглобулинов, т.е. молекулы, содержащие антигенсвязывающий сайт. Изобретение относится к применению молекул иммуноглобулинов любого типа (например, IgG, IgE, IgM, IgD, IgA и IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса.
«Фрагмент антитела» или «антигенсвязывающий фрагмент» содержит часть и