Многопараметрическая диагностическая тест-система, предназначенная для обнаружения и мониторинга терапии рака молочной железы и рака яичников, и способ проведения анализа с ее использованием
Иллюстрации
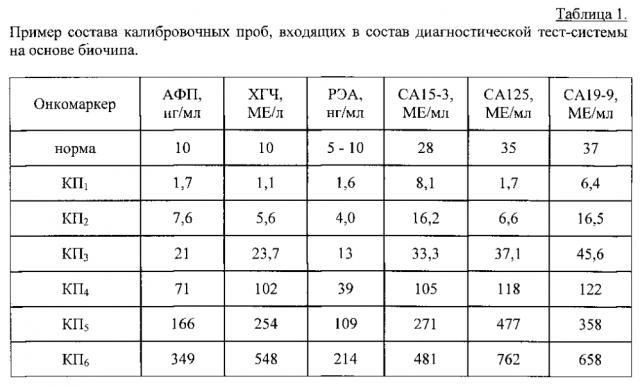
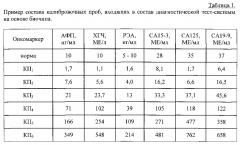
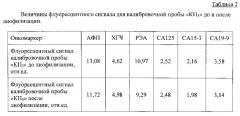
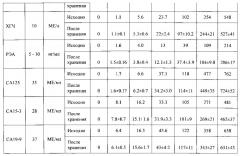
Показать всеИзобретение относится к области биохимии, биотехнологии и медицины, в частности к аналитической биохимии, иммунохимическому анализу и диагностическим средствам для онкологии, и касается многопараметрической диагностической тест-системы, предназначенной для обнаружения и мониторинга терапии рака молочной железы и рака яичников. Система представляет собой набор реагентов, включающий в себя биологический микрочип (биочип) для одновременного определения концентраций нескольких опухолеассоциированных антигенов: АФП, ХГЧ, РЭА, СА125, СА15-3 и СА19-9 в образце сыворотки крови человека, набор калибровочных проб в лиофилизованной форме, изготовленных на основе стабилизированной пулированной донорской сыворотки крови человека, состоящий из нескольких калибровочных проб, содержащих одновременно все анализируемые онкомаркеры, и нулевой калибровочной пробы, не содержащей указанных онкомаркеров и представляющей собой стабилизированную пулированную сыворотку здоровых доноров, абсорбированную на аффинных сорбентах, проявляющую систему, набор буферных растворов и инструкцию по проведению анализа. Предлагаемая тест-система может найти применение при выявлении наиболее распространенных форм онкозаболеваний женской репродуктивной системы, а именно рака молочной железы и рака яичников, в том числе на ранних стадиях опухолеобразования; для скринингового обследования населения, а также для мониторинга эффективности проводимой терапии. 2 н. и 5 з.п. ф-лы, 4 табл., 7 пр., 5 ил.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к области биохимии, биотехнологии и медицины, в частности, к аналитической биохимии, иммунохимическому анализу и диагностическим средствам для онкологии, и касается многопараметрической диагностической иммуноаналитической тест-системы (набора реагентов) для одновременного количественного определения нескольких опухолеассоциированных антигенов (онкомаркеров) в сыворотке крови человека, а также способа многопараметрического анализа образца, осуществляемого с ее помощью. Диагностическая тест-система предназначена для обнаружения и мониторинга терапии рака молочной железы и рака яичников.
Предлагаемая диагностическая тест-система может найти применение в области медицинской диагностики и аналитической биохимии и предназначена для выявления наиболее распространенных форм онкозаболеваний женской репродуктивной системы, а именно рака молочной железы и рака яичников, в том числе на ранних стадиях опухолеобразования; для скринингового обследования населения, а также для мониторинга эффективности проводимой терапии.
Уровень техники
Своевременная дифференциальная диагностика и возможность мониторинга терапии рака молочной железы и рака яичников значительно снижают смертность от этих онкозаболеваний. В современной литературе описаны способы диагностики опухолей женской репродуктивной системы, в том числе рака молочной железы и рака яичников: аппаратурные, in vivo и in vitro обследования, в том числе с взятием биопсийного материала, а также серологические.
Описано использование для in vivo диагностики опухолей различной локализации (предпочтительно глиомы), а также рака молочной железы и рака яичника, наночастиц размером менее 0,1-0,3 мкм, состоящих из покрытого оксидом магнитного металла с хелатирующим металл полимером (желатином) с ковалентно связанными молекулами, способными связывать опухолеспецифический клеточный маркер, и контрастным веществом для рентгеновской визуализации или магнитно-резонансной визуализации (МРТ) или флуоресцентным красителем. Наночастицы могут быть использованы также для рентгеновской визуализации или магнитно-резонансной визуализации (МРТ) и для транспорта лекарственных препаратов (Полимерные наночастицы, покрытые оксидом магнитного металла, и их применение. Заявка на изобретение RU 2010116167/15).
Для диагностики рака молочной железы и рака яичника предлагается полученный от пациента биопсийный биологический образец раковых клеток анализировать in vitro с помощью проточной цитометрии с использованием панели агентов, которые связываются с внеклеточными поверхностными маркерами (Мультиплексная детекция опухолевых клеток с использованием панели агентов, связывающихся с внеклеточными маркерами. Заявка на изобретение RU 2009135780/15). Агентами, специфичными к различным внеклеточным маркерам рака, могут быть моноклональные антитела, поликлональные антитела, фрагменты Fab, фрагменты (Fab′)2, фрагменты Fv, пептиды, белки, молекулы ДНК, полисахариды или любые их сочетания. В качестве маркеров для раковых клеток молочной железы предлагаются СА15-3, СА125, СБА, Ер-САМ, NY-ESO-1, PRL-R, RCAS1, STN и TA-90 и B2M. Применение базы данных позволяет провести идентификацию раковых клеток и выявить метастазы.
В настоящее время в серологической диагностике опухолей нашли широкое применение иммуноаналитические методы, основанные на количественном или полуколичественном определении ряда антигенов, называемых опухолевыми маркерами, уровень которых в крови коррелирует с локализацией опухоли и со стадией патологического процесса. Диагностическая значимость опухолевого маркера зависит от его чувствительности и специфичности. Известно, что повышенная концентрация одного онкомаркера не может служить абсолютным доказательством наличия опухоли (Maruvada Р, Wang W, Wagner PD, Srivastava S. / Biomarkers in molecular medicine: cancer detection and diagnosis. // Biotechniques. 2005. Suppl:9-15), поэтому наиболее информативным является комплексное определение нескольких онкомаркеров в образце {Белохвостое А.С., Румянцев А.Г. / Онкомаркеры. Молекулярно-генетические, иммунохимические, биохимические анализы. Пособие для врачей. // 2003. М.: Макс Пресс; Алексеева М.Л., Гусарова Е.В., Муллабаева С.М., Понкратова Т.С. / Онкомаркеры, их характеристика и некоторые аспекты клинико-диагностического использования. // 2005. Проблемы репродукции. №3. с. 65-79; Карпищенко А.И., Антонов В.Г., Бутенко А.Б., Белохвостое А.С., Шелепина Е.П. / Онкомаркеры и их диагностическое значение. // 1999, Санкт-Петербург, 47 с.; Кушлинский Н.Е. / Возможности, неудачи и перспективы исследования опухолевых маркеров в современной онкологической клинике. Часть 1 // 1999. Клиническая лабораторная диагностика. №3, с. 25-32; Кушлинский Н.Е. / Возможности, неудачи и перспективы исследования опухолевых маркеров в современной онкологической клинике. Часть 2. // 1999. Клиническая лабораторная диагностика. №4, с. 25-32).
Одновременное определение нескольких онкомаркеров увеличивает эффективность анализа и возможности дифференциальной диагностики онкозаболеваний (Клиническое руководство по лабораторным тестам. / Под ред. Н.У. Тица // Юнимед-пресс, Москва, 2003, 942 с.; Кишкун А.А. / Иммунологические и серологические исследования в клинической практике. // Москва, ООО «МИА», 2006, 536 с., с. 239-271).
Описано несколько типов иммуноаналитических систем для детекции онкологических маркеров, в том числе автоматические анализаторы, и множество более простых тест-систем, разработанных на основе принципов твердофазного иммуноферментного анализа (ИФА), аффинных микроколонок, аналитических полосок, микросфер и биологических микрочипов. Иммуноаналитические тест-системы различаются по способу детекции: с использованием ферментов (хромогенных и люминесцентных субстратов), радиоактивных и флуоресцентно меченных соединений, и различных вариантов масс-спектрометрии (SELDI, ICP-MS, MALDI-TOF MS). Под термином «тест-система» в большинстве источников подразумевается само устройство для проведения анализа (микросферы, биочип, аналитические полоски, аффинные колонки, планшет для ИФА и пр.), хотя в ряде случаев имеется в виду набор реагентов, объединяющий все комплектующие и протокол проведения иммуноанализа.
Наиболее распространенные коммерческие тест-системы, основанные на твердофазном ИФА (Fujirebio Diagnostics - CanAg, Швеция, NovaTec, Германия, Abazyme, Needham, США, Biosourse Diagnostics, Бельгия, Alpha Diagnostic Intl., Texas, США; Вектор-Бест, Иммунотех, Амеркард и Хема-Медика, Москва, Россия, Алкор-Био, Санкт-Петербург, Россия), позволяют определять содержание только одного маркера в образце. Фирма Вектор-Бест предлагает набор реагентов «ОНКО - СКРИН - ИФА - БЕСТ Т-8462» для одновременного выявления четырех опухолевых маркеров методом одностадийного сэндвич-ИФА, предназначенный для начального отбора (первичного скрининга) онкологических больных («Набор реагентов для одновременного выявления опухолевых маркеров СА125, РЭА, простат-специфического антигена (ПСА) и АФП в сыворотке крови.». http://www.vector-best.mhost.ru/prod/index.php?page=instr). Однако эта тест-система не является мультиплексной, а представляет собой механическое соединение четырех анализов.
Для определения содержания нескольких онкомаркеров используются автоматические анализаторы, например, фирмы Awareness Technology Inc., США, действующие на основе принципа ИФА, и представляющие собой открытую систему для любых методик и реактивов. Например, анализатор ChemWell использует стандартные микропланшеты для всех типов реакций и способен проводить несколько параллельных исследований, в том числе иммуноферментный анализ опухолевых маркеров: АФП, РЭА, ПСА, СА125, СА15-3, СА19-9, СА242, ферритина, ХГЧ, НСЕ, тканевого полипептидного антигена, бета 2-микроглобулина, UBC (рак мочевого пузыря) в 4-х лунках. Полностью автоматизированный микропланшетный ИФА-анализатор Stat Fax 3200 обеспечивает построение калибровочных кривых, процедуру обсчета результатов, вычитание фона и др., позволяет проводить до 12-и параллельных тестов одновременно. Иммунохемилюминесцентный стриповый анализатор Lumi Stat - CLIA используют для определения 11-и опухолевых маркеров РЭА, ПСАобщ, ПСАсвоб, СА125, АФП, простатической кислой фосфатазы, СА19-9, СА15-3, NMP22 (ядерные матриксные белки), бета-2-микроглобулина, цитокератина 18. Прибор Biomerieux mini VIDAS, Франция, представляет собой мультипараметрический автоматический иммуноанализатор, основанный на технологии энзим-связанного иммунофлюоресцентного анализа (ELFA) и предназначен для выполнения "одиночных" тестов. Определение аналитов происходит с высокой чувствительностью (превышающей на несколько порядков чувствительность ИФА), что позволяет значительно снизить время проведения анализа (до 30 мин.). Приборы этого класса представляют собой механическое соединение нескольких анализов, но не одновременный многопараметрический анализ нескольких аналитов в одном образце.
Описано одновременное определение нескольких аналитов (в том числе онкологических маркеров) с помощью полностью автоматизированных систем Elecsys компании Roche Diagnostics, США/Швейцария, Luminex, США/Нидерланды, и AxSYM компании Abbott, США. Система Elecsys использует принцип гетерогенного иммунохимического анализа на основе электрохемилюминесцентной диагностики - аналитические полоски или микроколонки для аффинной хроматографии. Анализатор Luminex основан на принципе проточной флуориметрии микросфер с иммобилизованными на поверхности лигандами (с использованием различных типов взаимодействия: комплементарное взаимодействие нуклеиновые кислот и оснований, взаимодействие лиганд-рецептор, образование иммунокомплексов, ферментативные реакции), что позволяет проводить одновременный анализ до 100 различных аналитов. Автоматизированные системы AxSYM основаны на иммуноферментном анализе на микрочастицах и/или флюоресцентном поляризационном иммуноферментном анализе. Они обеспечивают быстрое время получения результата (8-30 мин) и высокую производительность (от 80 до 120 тестов в час). Недостатком анализаторов Roche Diagnostics, Luminex и Abbott является то, что они представляют собой «закрытые» системы, состоящие из прибора-анализатора и набора реагентов к нему (используются пробирки, микроколонки, полоски и прочие реагенты только данной фирмы, предназначенные для данной системы или данного конкретного прибора), а также их высокая стоимость (от нескольких десятков до сотен тысяч долларов США), громоздкость аппаратуры, высокие требования к квалификации персонала, что не позволяет их внедрить в широкую клиническую практику.
Патентная заявка WO/2005/016126 (Multifactorial assay for cancer detection. University of Pittsburgh of the commonwealth system of higher education, США) предлагает способ диагностики рака яичников с помощью мультиплексного иммуноанализа на микросферах одного или нескольких опухолеассоциированных антигенов (EGF, G-CSF, IL-6, IL-8, СА125; VEGF, МСР-1, антител против интерлейкинов IL6, IL8, антител против СА125, c-myc, p53, РЭА, антител против СА15-3, MUC-1, сюрвивина, β-ХГЧ, остеопонина, PDGF, Her2/neu, Aktl, цитокератина 19, а также антигенов цитокератин 19, EGFR, РЭА, калликреин-8, M-CSF, FasL, ErB2 и Her2/neu) в сыворотке крови пациента с флуориметрической детекцией или методом квантовых точек с помощью проточного гемоцитометра. Способ позволяет диагностировать рак яичников до его клинического проявления, а также дискриминировать различные формы и локализацию злокачественного процесса. К недостатку тест-системы относится необходимость использования дорогостоящего оборудования, высококвалифицированного персонала, а также громоздкость аппаратуры.
В последнее время наиболее интенсивно развивается метод анализа, связанный с использованием биологических микрочипов. Микрочипы - это массивы индивидуальных микроэлементов, нанесенных на твердую подложку и содержащих различные зонды - ДНК, РНК, олигонуклеотиды, сахара, полипептиды, белки, клетки и ткани, и т.д. Микрочипы позволяют проводить одновременный параллельный анализ образца по многим аналитам, что значительно увеличивает эффективность анализа, позволяет миниатюризировать проведение исследований и значительно снижает требуемое количество исследуемого материала (Мирзабеков А.Д. / Биочипы в биологии и медицине XXI века. // Вестник Российской академии наук, 2003 г., т. 73, №5, с. 412-422). Существует ряд фирм-производителей занимающихся разработкой биочипов, при этом до сих пор не существует явно доминирующей технологии изготовления. Крупнейшими фирмами-изготовителями являются, например, Affymetrix, Inc., США - только ДНК-чипы, RANDOX Laboratories, Ирландия, - ДНК- и белковые чипы для одновременного определения ряда аналитов (Kricka LJ, Master SR, Joos TO, Fortina P. // Current perspectives in protein array technology. // 2006. Ann Clin Biochem. 43(Pt 6):457-67; Информация с сайта: http://www.randox.com/tumour%20markets.php) и др.
Компанией Tripath Imaging, Inc. (США) предложен способ скрининга для выявления пациентов группы риска с повышенной предрасположенностью к раку яичников, основанный на детекции повышенной экспрессии ряда биомаркеров (например, НЕ4, СА125, гликоделин, ММР7, Muc1, PAII, CTHRC1, ингибин A, PLAUR, пролактин, KLKIO, KLK6, SLPI5 и α1-антитрипсин). При этом используются принцип специфического связывания антиген-антитело (метод иммуноанализа на микропланшетах) - для выявления самих белков в сыворотке крови, или ДНК/РНК-гибридизационная техника (микрочипы фирмы Affymetrix) - для выявления нуклеотидных последовательностей, кодирующих экспрессируемые белки. Предлагается двустадийная схема: сначала выявляются пациентки с заведомо положительным содержанием аналитов (отсечение по показателю cut-off), а затем проводится количественный анализ и статистическая обработка данных (Methods for identifying patients with an increased likelihood of having ovarian cancer and compositions therefore. Патентная заявка WO/2007/090076).
Zhang X. с сотр. показали, что в формате микрочипа возможно одновременное иммуноаналитическое определение нескольких онкомаркеров (АФП, Р-ХГЧ и РЭА) и общего IgG человека в плазме с ICP-MS-масс-спектрометрической детекцией с применением лазерной техники с использованием антител, меченных солями редкоземельных металлов (Sm3+, Eu3+) и коллоидным золотом. Определены аналитические характеристики - предел обнаружения, диапазон измерения и коэффициенты вариации внутри серии и между сериями (Zhang S, Zhang С, Xing Z, Zhang X. / Simultaneous determination of alpha-fetoprotein and free beta-human chorionic gonadotropin by element-tagged immunoassay with detection by inductively coupled plasma mass spectrometry. // Clin Chem. 2004 Jul; 50(7): 1214-21; Hu S, Zhang S, Hu Z, Xing Z, Zhang X. / Detection of multiple proteins on one spot by laser ablation inductively coupled plasma mass spectrometry and application to immuno-microarray with element-tagged antibodies. // Anal Chem. 2007 Feb 1; 79(3):923-9). Диапазоны обнаружения для АФП и β-ХГЧ были 4,6-500 и 5,0-170 нг/мл, соответственно, аналитическая чувствительность - 1,2 и 1,7 нг/мл, (определенная как концентрация аналита, соответствующая величине сигнала от нулевой пробы плюс 3 стандартных отклонения). Сравнение метода с IRMAs для АФП и β-ХГЧ показал коэффициенты корреляции (R2) равными 0,97 и 0,95, соответственно.
Song S.-P. и сотр. (Song S.-P., Li В., Hu J., Li M.-Q. I Simultaneous multianalysis for tumor markers by antibody fragments microarray system. // Analytica Chimica Acta. 2004. 510: 147-152) разработали микрочип для одновременного определения шести маркеров онкологических заболеваний. На силиалированные слайды, содержащие альдегидные группы, были нанесены шесть Fab-фрагментов антител против маркеров АФП, РЭА, Р-ХГЧ, СА125, СА19-9 и СА15-3. Использован «сэндвич»-иммуноанализ с применением авидин-биотиновой системы для усиления флуоресцентного сигнала. Несмотря на низкую чувствительность (менее 12 нг/мл для АФП, РЭА и β-ХГЧ, и менее 17 МЕ/мл для СА125, СА19-9 и СА15-3) по сравнению с традиционными иммуноаналитическими системами - ИФА и РИА, авторы получили хорошую корреляцию с данными радиоиммунного анализа.
В работе Wilson M.S. и др. (Wilson M.S., Nie W. / Multiplex measurement of seven tumor markers using an electrochemical protein chip. // Anal. Chem. 2006, 78, 6476-6483) описан сенсорный чип, состоящий из электродных элементов с иммобилизованными антигенами, с помощью которого осуществляется одновременное определение концентраций семи онкомаркеров: АФП, ферритина, РЭА, β-ХГЧ, СА15-3, СА125 и СА19-9 методом конкурентного ферментного иммуноанализа. Чип показал хорошую точность и надежность результатов в сравнении с независимым количественным определением тех же онкомаркеров в ИФА-тестах: коэффициент вариации составил 1,9-8,1% внутри серии; чувствительность составила не более 2 нг/мл (или 2 МЕ/мл) для большинства аналитов.
Патентная заявка WO/2005/083440 описывает способ диагностирования рака и дискриминации между здоровыми лицами и раковыми больными на основе одновременной идентификации множества биомаркеров, продукция которых в организме резко возрастает при онкологических заболеваниях. Для прогнозирования и мониторинга рака яичников, рака молочной железы и рака прямой кишки был предложен ряд биомаркеров лептин, пролактин, ферменты химотрипсиного ряда, калликреины, онкомаркеры СА125, СА15-3, СА19-9, MUC1, OVX1, РЭА, M-CSF, OPN и IGF-II, простатин, СА54-61, СА72, HMFG2, интерлейкины IL-6, IL-10, LSA, M-CSF, NB70K, PLAP, TAG72, факторы TNF, TPA, UGTF, VEGF, CLDN3, NOTCH3, E2F и др., которые идентифицируются с использованием новой уникальной скрининговой технологии. Предварительно установленным отрицательным стандартом являются уровень экспрессии данных биомаркеров у здоровых индивидов и уровень экспрессии данных биомаркеров в здоровых тканях онкологических больных. Экспрессию выбранных биомаркеров определяли методами ELISA, RCA иммуноанализом, хемилюминесценцией, оптическим биосенсором в тонких пленках, протонным резонансом и т.д.. Был создан чип для идентификации 169 биомаркеров и на нем протестированы 46 образцов сывороток (18 больных раком яичников и 28 здоровых доноров) методом РСА иммуноанализа, причем из 169 биомаркеров в качестве наиболее значимых были отобраны 35 маркеров. В следующей серии экспериментов (100 больных раком и 106 здоровых доноров) были отобраны 4 наиболее значимых для диагностики и мониторинга рака яичников и рака молочной железы параметров (лептин, пролактин, OPN, IGF-11), к которым был добавлен СА 125 (Identification of cancer protein biomarkers using proteomic techniques, патентная заявка WO/2005/083440).
В работе (Balachandra К, Laisupasin P, Dhepakson P, Warachit J, Jantraraksri U, Issaragrisil S, Yang XL, Hus GX. I Preliminary clinical evaluation of a protein chip for tumor marker serodiagnosis of various cancers // Asian Рас J Allergy Immunol. 2003 Sep; 21(3):171-178) описано применение белкового микрочипа для серодиагностического определения нескольких онкомаркеров. Исследованы чувствительность и специфичность созданного микрочипа и показана принципиальная возможность клинического его применения среди тайской популяции для 10 типов рака. Чиповая диагностика применима для рака легких, шеи, молочной железы, яичников, простаты, поджелудочной железы, печени, пищевода, желудка, колоректального рака. Были обследованы 165 онкологических больных и 50 здоровых человек. Чувствительность и специфичность серодиагностического белкового чипа составила 82,4% и 94,0%, соответственно. Доля успешных попыток диагностики рака составила от 57% до 100% для всех 10 типов рака. Чувствительность определения на чипе каждого из онкомаркеров в смеси была не ниже чувствительности его индивидуального определения. Таким образом, белковый чип весьма перспективен как для скринингового обследования, так и для обследования онкологических больных вплоть до стадии появления метастазов.
Sun и др. (Sun Z, Fu X, Zhang L, Yang X, Liu F, Hu G. I A protein chip system for parallel analysis of multi-tumor markers and its application in cancer detection. // Anticancer Res. 2004 Mar-Apr; 24(2C):1159-65) разработали микрочип для одновременного иммунологического определения 12 онкомаркеров (С12-биочип). Чип предназначен для скринингового обследования онкологических больных и групп популяций с высоким риском злокачественных заболеваний. На нитроцеллюлозной мембране были иммобилизованы двенадцать моноклональных антител против маркеров СА125, СА15-3, СА19-9, СА242, РЭА, АФП, ПСАобщ, ПСАсвоб, ХГЧ, β-ХГЧ, НСЕ и ферритина. Было протестировано 1147 образцов сыворотки крови онкологических больных с клинически подтвержденным диагнозом. Тест-система на основе микрочипа оказалась высокочувствительной к раку печени, раку поджелудочной железы и раку яичников, и низкоспецифичной к раку желудочно-кишечного тракта. Далее с помощью данного микрочипа авторами было проведено скрининговое обследование 15867 человек, причем у 436 обследованных были выявлены повышенный уровень того или иного онкомаркера. Из них дальнейшее обследование прошли только 138 пациентов, у 16 пациентов был обнаружен рак различной локализации, у 41 пациента - заболевания нераковой природы. У 81 пациента не было выявлено каких-либо заболеваний.
Данный С12-биочип использовали для диагностики и мониторинга разных типов раковых заболеваний (Yu DY. / Application of multi-tumor markers protein chip assistance diagnostic system for detection of various tumors // China Trop Med 2005; 5:414-16; Liang Z, Wang HF, Wu AZ, Fu SM. I Clinical value of 12 tumor markers protein biochip detection of digestive system neoplasm. // China Trop Med 2005; 5:407-09; Jiang ZJ, Zhou W X, Lin W, Huang QXI Application of multi-tumor markers protein chip diagnose system in the diagnosing of intestinal neoplasms // J Mod Lab Med 2005; 20:17-19; Mou JH, Li ZP, Wang D, Ma Y, Xiao HL, Zhang QH. I Combined detection of multiple tumor marker and its diagnostic value in colorectal cancer. // J Digest Surg 2005; 4:268-70; Zhong ZY, Wang D, Li ZP, Li MX, Dai N, Cao XJ, et al. / Clinical significance of C-12 multiple tumor marker protein chip detective system in diagnosing colorectal carcinoma // Chongqing Med 2007; 36:2406-08). Был исследован уровень 12 онкомаркеров в сыворотке крови 170 пациентов с колоректальным раком и показано, что биочип С12 позволяет выявлять 41,8% случаев рака, при этом процент выявления на ранних стадиях (0-I) был ниже - 12,9%. Среди всех анализируемых онкомаркеров чувствительность к данному виду рака была выше всего у РЭА - 36,5%. Использование различных комбинаций онкомаркеров не привели к значительному улучшению чувствительности теста; уровни наиболее информативных для рака толстой кишки онкомаркеров (РЭА, СА19-9, СА242) хорошо коррелировали между собой. Было также показано, что уровни СА242 и β-ХГЧ повышались у пациентов с метастазами в лимфатические узлы. Авторы сделали заключение, что С12-биочип пригоден для диагностики и мониторинга поздних стадий колоректального рака, но не эффективен для его ранней диагностики (Chen С, Chen LQ, Yang GL, Li Y. / The application of C12 biochip in the diagnosis and monitoring of colorectal cancer: Systematic evaluation and suggestion for improvement. // J Postgrad Med. 2008. 54(3):186-190).
Те же авторы использовали С12-биочип для диагностики и мониторинга рака желудка. Был проанализирован уровень онкомаркеров у 100 пациентов с различными стадиями рака желудка. Диагностическая чувствительность системы для выявления рака желудка на основе С12-биочипа составила 37%. Для пациентов с I стадией рака чувствительность составила всего 7,8%, для II, III и IV стадий - 29,4%, 35,5% и 50%, соответственно. Среди всех 12 онкомаркеров наилучшая чувствительность (23%) была у СА19-9. С12-микрочип оказался менее чувствителен к ранним стадиям рака желудка и пригоден для диагностики и мониторинга поздних стадий данного заболевания (Chen С, Chen LQ, Chen LD, Yang GL, Li Y. / Evaluation of tumor markers biochip C12 system in the diagnosis of gastric cancer and the strategies for improvement: analysis of 100 cases. // Hepatogastroenterology. 2008, 55(84):991-997).
Относительно новым для серологической диагностики рака молочной железы является определение с помощью микрочипа с нанесенными на него гликанами наличия в крови пациента антител к специфичной и чувствительной комбинации опухолеассоциированных гликанов на фоне индивидуальных особенностей конкретного больного (Способ диагностики рака молочной железы. Патент RU 2504785 С1). Диагностика осуществляется по наличию уровня антител одновременно ко всем гликанам выше порогового, что позволяет улучшить чувствительность и специфичность диагностики рака молочной железы.
Все вышеперечисленные тест-системы используют «двумерные» чипы, где антитела иммобилизованы на поверхности твердофазного носителя с некоторой потерей биологической активности из-за агрегации, денатурации, стерических затруднений, ограничивающих доступ аналитов к активным центрам иммобилизованного белка (Zhang S. / Hydrogels: Wet or let die. // Nat Mater. 2004 Jan; 3(1):7-8; Rubina A.Yu., Kolchinsky A., Makarov A.A., Zasedatelev A.S. I Why 3-D? Gel-based microarrays in proteomics. // Proteomics 2008, Feb; 8(4):817-831, Jonkheijm P., Weinrich D., Schroder K, Niemeyer С M., Waldmann H. I Chemical Strategies for Generating Protein Biochips // Angew. Chem. Int. Ed., 2008, 47, 9618-9647).
В ряде работ описано создание «трехмерных» гелевых микрочипов, обладающих рядом преимуществ по сравнению с «двумерными» чипами (Rubina A., Dementieva Е., Stomakhin A., Darii Е., Pan′kov S., Bar sky V., Ivanov S., Konovalova E., Mirzabekov A. / Hydrogel-based protein microchips: manufacturing, properties, and applications. // BioTechniques, 2003, 34 (5), 1008-1022; Rubina A.Yu., Kolchinsky A.M., Makarov A.A, Zasedatelev A.S. / Why 3-D? Gel-based microarrays in proteomics // Proteomics, 2008, v. 8, p. 817-831). Так, использование для идентификации и анализа опухолеассоциированных маркеров (фактор фон Виллебрандта, IgM, α1-антихимотрипсин, IgG) с целью диагностики рака предстательной железы, 3D-микрочипов, содержащих иммобилизованные в полиакриламидном геле антитела, показало 6-и кратное увеличение показателя дискриминации (отношения величины флуоресцентного сигнала пробы к величине флуоресцентного сигнала шума) по сравнению с 2D-чипами, в которых антитела иммобилизованы на поверхности стекла, обработанного поли-лизином (Miller J.С, Zhou К, Kwekel J., Cavallo R., Burke J., Butler E.B., Teh B.S., Haab В В. I Antibody microarray profiling of human prostate cancer sera, // Proteomics, 2003, 3, 56-63).
Применение 3D-микрочипов для одновременного количественного определения нескольких опухолеассоциированных маркеров описано в работах группы Рубиной А.Ю. и др. (Дементьева Е.И., Рубина А.Ю., Дарий Е.Л. и др. / Применение белковых микрочипов для количественного определения опухолеассоциированных маркеров // Докл. Акад. Наук, 2004, т. 395, с. 542-547, Коновалова Е.В., Савватеева Е.Н., Дементьева Е.И., Филиппова М.А., Турыгин А.Ю., Осипова Т.В., Рябых Т.П., Рубина А.Ю., Заседателев А.С. / Разработка биочипа для количественного определения двух форм простата-специфического антигена с использованием внутренней калибровочной кривой // Молекуляр. биология, т. 41, №4, Июль-Август 2007, с. 734-738; Савватеева Е.Н., Дементьева Е.П., Цибульская М.В., Осипова Т.В., Рябых Т.П., Турыгин А.Ю., Юрасов Р.А., Заседателев А.С., Рубина А.Ю. / Биологический микрочип для одновременного количественного иммунологического анализа маркеров онкологических заболеваний в сыворотке крови человека // Бюлл. Эксп. Биол. Мед., 2009, т. 147, №6, с. 679-683).
В патенте РФ №2363955 (Биологический микрочип для множественного параллельного иммунологического анализа соединений и способы иммуноанализа, в которых он используется, ИМБ РАН им. В.А. Энгельгардта, РФ) описано создание и применение гидрогелевого микрочипа для различных типов множественного параллельного иммуноанализа (прямого, конкурентного, сэндвич-анализа).
Помимо приведенных выше источников, касающихся описания микрочипов для одновременного количественного определения нескольких онкомаркеров, существуют несколько патентов, в которых описаны наборы реагентов, включающие микрочип, проявляющую систему, панель калибровочных проб для количественного анализа, положительный и отрицательный контроли и буферы для отмывки. Так, компаниями Bayer Healthcare Lie (США) и Mayo Foundation For Medical Education And Research (США) описан комбинированный чип (ДНК-белок) и набор реагентов для определения уровня экспрессии полипептидов или нуклеотидных последовательностей, кодирующих опухолеспецифичные маркеры, которые могут быть использованы для диагностики и мониторинга злокачественных заболеваний, в том числе рака разного типа (аденокарцинома, лимфома, бластома, меланома, саркома, лейкемия) и различной локализации (рака молочной железы, рака яичников, рака толстой кишки и многих др.). Набор также содержит положительный и отрицательный контроли, различные комбинации проявляющих флуоресцентно меченных специфических последовательностей и/или антител и инструкцию для проведения анализа и интерпретации результатов (Use of differentially expressed nucleic acid sequences as biomarkers for cancer, патентная заявка WO/2005/044990).
Компанией Shanghai Health Digit Co., Ltd (Китай) описана детектирующая тест-система, состоящая из белкового чипа, проявляющей смеси различных белков, меченных пероксидазой, отмывающего буфера (0,9% NaCl, 1.21%) Tris, 0,1% Tween20, рН 7,5), буфера для разведения образцов биологических жидкостей (0,9% NaCl, 1.21%) Tris, 0,1%) Tween20, 0,1% тирозин, рН 7,5), химической композиции, обеспечивающей протекание реакции хемилюминесценции, детергента и серии калибровочных проб, содержащих определяемые маркеры, протокола сэндвич-иммуноанализа. Белковый чип содержит моноклональные антитела, иммобилизованные на поверхности нитроцеллюлозной мембраны (Protein chips, method producing it and detection system of the protein chips, and operating method of the detection system. Патент CN 01105023.3).
Продолжением этого патента является патентная заявка WO/2004/038413 (Protein chips detecting system which can simultaneously detect multi target) китайской компании Shanghai Health Digit Co. Ltd (Китай), которая описывает диагностическую тест-систему для одновременного параллельного анализа множества показателей на основе белковых микрочипов, включающую в себя белковый микрочип, проявляющую систему (готовая смесь белков, содержащих люминесценые метки), серии стандартных образцов (смешанных белков в известных повышающихся концентрациях) и раствор для промывки белковых чипов. В качестве примера приводится тест-система для одновременного параллельного определения шести онкомаркеров АФП, РЭА, ПСАобщ, ПСАсвоб, СА125, СА15-3, где зондами являются антитела к шести онкомаркерам, нанесенные на подложку. В описанной тест-системе авторы используют «двумерные» чипы, подробно описывают способы их изготовления и применения, но нет данных о проведении иммуноанализа сывороток больных, не определены технические и аналитические характеристики диагностической тест-системы.
В патентной заявке WO 03/104808 компаниями Chengdu Kuachang Science And Technology Co., Ltd (Китай), Human Plasma Product Services Ltd (Гонконг) и Chengdu Kuachang Medical Industrial Co., Ltd (Китай) описана мультиплексная тест-система, состоящая из биологического чипа, проявляющей системы (флуоресцентная, хемилюминесцентная, электролюминесцентная, радиоактивная или магнитная метки), медиаторов и системы усиления сигнала (коллоидное золото с добавлением солей серебра, авидин-биотиновая система, белок А, белок G, псорален, дигоксин), отрицательного и положительного контролей, референсного материала, буферов для отмывки и т.д. В качестве примера предложен биочип для одновременного анализа шести онкомаркеров (ХГЧ, РЭА, СА50, СА242, СА15-3, СА125) и одного антитела (против вируса EBV), связанных с опухолями, в одном реакторе. Отрицательным контролем служила сыворотка крови, выбранная по результатам тестирования с помощью 7-и ИФА-тест-наборов. Положительный контроль не описан (Biochip kit comprising biochip based on antigen-antibody reactions, and its usage, патентная заявка WO 03/104808, США 20050153382, патент РФ 2316000).
Помимо тест-систем (набора реагентов) для одновременного количественного определения нескольких онкомаркеров в одном образце, описаны также калибровочные пробы, необходимые для построения калибровочных кривых. Калибровочные пробы должны обладать достаточной стабильностью при хранении, устойчивостью и воспроизводимостью для всех аналитов. Патентный поиск по способам изготовления панели калибровочных проб, используемых для построения калибровочных кривых для одновременного количественного определения нескольких аналитов, выявил следующие патентные документы, касающиеся создания калибровочных проб для различных тест-систем:
В патенте РФ 2242006 РОНЦ им. Н.Н. Блохина описан набор для количественного определения ПСАобщ в сыворотке крови человека методом одностадийного твердофазного иммуноферментного анализа и способ создания панели калибровочных проб, необходимых для построения калибровочных кривых для количественной интерпретации результатов иммуноанализа, содержащих известные концентрации ПСА (0; 2,5; 5; 10 и 30 нг/мл ПСА). Калибровочные пробы были изготовлены в трис-буфере с 1%-м бычьим сывороточным альбумином. К недостаткам данного способа относится то, что он разработан только для одного онкомаркера, а также наличие в матриксной среде инородного для человека белка - бычьего альбумина.
Патентная заявка РФ 2007106670 ООО Научно-производственного объединения "Диагностические системы" (РФ) предусматривает изготовление лиофилизированного отраслевого стандартного образца (ОСО) поверхностного антигена вируса гепатита В (HBsAg) для контроля качества тест-систем и количественного определения содержания антигена в сыворотке (плазме) и препаратах крови человека методом ИФА. ОСО включает в себя 1%-й водный раствор BSA, содержащий 0,75% глицина, 0,01% тимеросала, а также плазменный или рекомбинантный поверхностный антиген вируса гепатита В HBsAg до концентрации 20 МЕ/мл. Техническим результатом заявленного изобретения является увеличение длительности хранения и обеспечение возможности неоднократного использования препарата. Преимуществом является наличие раствора для разведения ОСО - негативной сыворотки человека. Недостатком данного способа также является то, что описанное изобретение касается только одного аналита - поверхностного антигена вируса гепатита В HBsAg. Кроме того, набор содержит только один флакон, содержащий ОСО и 9 флаконов с раствором для разведения ОСО, то есть, нет всей панели калибровочных проб, а есть только сток-флакон, из которого предлагается пользователю готовить калибровочные пробы самостоятельно, что неизбежно приведет к появлению мануальных ошибок.
Патентная заявка WO/2004/038413 китайской компании Shanghai Health Digit Co. Ltd (Китай) в составе тест-системы на основе белкового чипа описывает способ создания панели калибровочных проб для количественного параллельного анализа нескольких онкомаркеров - стандартных растворов антигенов, содержащих смесь двух или более белков в точно известных возрастающих концентрациях. Стандартные растворы антигенов изготавливают в две стадии. Сначала изготовляют сток-раствор смеси антигенов с высокой концентрацией в буферном растворе, содержащем 40%-60% фетальной телячьей сыворотки и 0,002-0,01% NaN3, или в К,Na-фосфатном буфере: 0,05М KH2PO4-Na2HPO4, рН 7,0-7,8, содержащем 2-30% БСА, 1,5-2,5% сахарозы, 0,002-0,01% NaN3. В качестве примера описано изготовление и испытание на стабильность при лиофилизации и хранении стандартных растворов антигенов для одновременного параллельного определения трех онкомаркеров (АФП, РЭА и НСЕ). Калибровочные растворы антигенов готовили путем добавления 60 мкл сток-раствора смеси антигенов к большому объему буфера в двух буферных системах: в буферном растворе на основе 60%-й фетальной телячьей сыворотки и 0,005% NaN3 или в К,Na-фосфатном буфере: 0,05М KH2PO4-Na2HPO4, рН 7,0-7,8, содержащем 15% БСА, 2,5% сахарозы, 0,005% NaN3. Последовательно разведенные стандартные растворы антигенов лиофилизовали и хранили в течение 3 мес. при +4°C. После хранения лиофилизованные стандартные растворы антигенов анализировали на микрочипах. После проведения иммуноанализа уровень сигналов, регистрируемых с помощью автоматического анализатора хемилюминесценции, не снижался при использовании обеих буферных систем.
Известные диагностические тест-системы (наборы реагентов) и панели калибровочных проб для одновременного количественного определения нескольких онкомаркеров в биологических жидкостях человека имеют ряд недостатков.
Недостатки
Большинство описанных в мировой практике неинвазивных способов обнаружения и мониторинга терапии рака молочной железы и рака яичников, осуществляемые с помощью многопараметрических диагностических тест-систем (наборов реагентов), не являются достаточно разработанными и надежными. Большинство иммунохимических тест-систем позволяет выявлять содержание только одного маркера в одном клиническом образце. Одновременное определение нескольких онкомаркеров повышает эффективность скринингового анализа и расширяет возможности дифференциальной диагностики онкозаболеваний.
Недостатком существующих «закрытых» диагностических систем - анализаторов для проведения многопараметрического анализа (США, Япония, Китай), является их высокая стоимость, громоздкость аппаратуры и требование использования реагентов и комплектующих только фирмы-производителя, что не позволяет их внедрить в широкую клиническую практику.
К недостаткам описанных к настоящему времени диагностических многопараметрических тест-систем с иммобилизованными на поверхности носителя белками (РФ, США, Китай), например, на основе микросфер, относится их высокая стоимость и то, что среди них нет коммерчески доступных тест-систем. Недостатком диагностических тест-систем на основе планарных микрочипов являются низкая воспроизводимость и недостаточная стабильность при хранении.
В большинстве изобретений запатентован только сам микрочип, описан способ его изготовления и применения, но не описаны проявляющая система, калибровочные пробы, используемые для построения калибровочных кривых, растворы для разведения образцов. Например, в патенте РФ №2363955 ИМБ РАН им. В.А. Энгельгардта (Биологический микрочип для множест