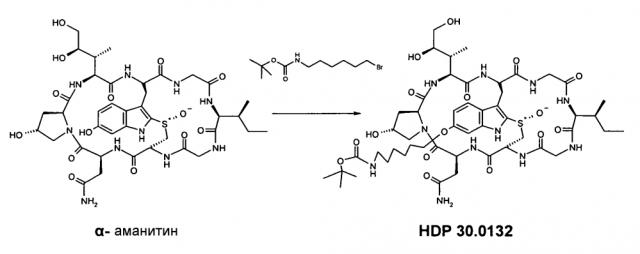
Конъюгаты аматоксинов с улучшенными линкерами
Иллюстрации
Показать всеИзобретение относится к противоопухолевой терапии. В одном аспекте настоящее изобретение относится к конъюгатам аматоксина и части, связывающей мишень, например, антитела, соединенные линкером, включающим остаток мочевины, которые предназначены для лечения рака. В другом аспекте изобретение относится к фармацевтическим композициям, включающим такие конъюгаты, и способу получения указанных конъюгатов. Конъюгаты имеют высокую стабильность в плазме, что приводит к уменьшению вредного побочного действия на клетки. 4 н. и 10 з.п. ф-лы, 9 ил., 6 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к противоопухолевой терапии. В одном аспекте настоящее изобретение относится к конъюгатам аматоксина и связывающей мишень части, например, антитела, соединенные линкером, включающим остаток мочевины, которые применимы при лечении рака. В другом аспекте изобретение относится к фармацевтическим композициям, включающим такие конъюгаты.
Предпосылки создания изобретения
Аматоксины представляют собой циклические пептиды, состоящие из 8 аминокислот. Их можно выделить из грибов Amanita phalloides или получить синтетически. Анатоксины специфически ингибируют ДНК-зависимую РНК-полимеразу II клеток млекопитающих и посредством этого также транскрипцию и биосинтез белка пораженных клеток. Ингибирование транскрипции в клетках вызывает остановку роста и пролиферации. Хотя ковалентной связи нет, комплекс между аманитином и РНК-полимеразой II является весьма прочным (KD=3 нМ). Отсоединение аманитина от фермента является очень медленным, причем таким образом восстановление пораженной клетки становится невозможным. Когда ингибирование транскрипции слишком запаздывает, клетка будет подвержена запрограммированной гибели (апоптоз).
Использование аматоксинов в качестве цитотоксических частей для противоопухолевой терапии уже исследовалось в 1981 путем соединения антитела против Thy 1.2 с α-аманитином с использованием линкера, присоединенного к индольному циклу Trp (аминокислота 4; см. фигуру 1) через диазотирование (Davis & Preston, Science, 1981, 213, 1385-1388).
В заявке на патент ЕР 1859811 А1 (опубликованной 28 ноября 2007) описываются конъюгаты, в которых γ-атом С аминокислоты 1 аматоксина β-аманитина соединен непосредственно, т.е. без линкерной структуры, с альбумином или моноклональным антителом НЕА125, ОКТ3 или РА-1. Кроме того, показано ингибирующее действие таких конъюгатов на пролиферацию клеток рака молочной железы (MCF-7), клеток лимфомы Беркитта (Raji) и клеток Т-лимфомы (Юрката). Предлагалось использование линкеров, в том числе линкеров, включающих такие элементы, как амид, сложный эфир, простой эфир, простой тиоэфир, дисульфид, мочевина, тиомочевина, углеводородные группы и т.п., но такие конструкции фактически не показаны и не приводятся такие детали, как места присоединения на аматоксинах.
Известно, что аматоксины относительно нетоксичны, когда соединены с носителями крупными биомолекулами, такими как молекулы антител, и что они проявляют свою цитотоксическую активность только после отщепления носителя-биомолекулы. В свете токсичности аматоксинов, в частности, для клеток печени, важно, что конъюгаты аматоксинов для таргетной противоопухолевой терапии остаются весьма устойчивыми после введения в плазму, и что высвобождение аматоксина происходит после интернализации в клетках-мишенях. В таком контексте небольшие улучшения устойчивости конъюгатов могут иметь радикальные последствия для терапевтического окна и безопасности конъюгатов аматоксинов для терапевтических целей.
Цель изобретения
Таким образом, на известном уровне технике имелась высокая потребность в конъюгатах связывающей мишень части и аматоксина, которые устойчивы в плазме, так что вредное побочное действие на клетки-не-мишени минимизируется.
Сущность изобретения
В первом аспекте настоящее изобретение относится к конъюгату, включающему связывающую мишень часть, соединенную через линкер L с аматоксином, где линкер L соединен с аматоксином через
(i) γ-атом С аминокислоты 1 аматоксина, в частности, через амидную связь;
(ii) атом кислорода, связанный с δ-атомом С аминокислоты 3 аматоксина, в частности, через сложноэфирную связь, простую эфирную связь или уретановую связь; или
(iii) 6'-атом С аминокислоты 4 аматоксина, в частности, через атом кислорода, связанный с 6'-атомом С аминокислоты 4 аматоксина;
где в каждом случае линкер L соединен с частью, связывающей мишень, через остаток мочевины.
Во втором аспекте настоящее изобретение относится к фармацевтической композиции, включающей конъюгат по настоящему изобретению.
В еще одном аспекте настоящее изобретение относится к конъюгирующей молекуле аматоксина, включающей линкер L, соединенный с аматоксином через
(i) γ-атом С аминокислоты 1 аматоксина, в частности, через амидную связь;
(ii) атом кислорода, связанный с δ-атомом С аминокислоты 3 аматоксина, в частности, через сложноэфирную связь, простую эфирную связь или уретановую связь; или
(iii) 6'-атом С аминокислоты 4 аматоксина, в частности, через атом кислорода, связанный с 6'-атомом С аминокислоты 4 аматоксина;
где в каждом случае линкер L включает производное карбаминовой кислоты -NH-C(O)-X, где Х представляет собой удаляемую группу, которую можно заменить первичным амином части, связывающей мишень.
В еще одном аспекте настоящее изобретение относится к способу синтеза конъюгата по настоящему изобретению, включающему стадию осуществления реакции конъюгирующей молекулы аматоксина по настоящему изобретению со связывающей мишень частью, включающей первичную аминогруппу.
Краткое описание чертежей
Фиг. 1 показывает структурные формулы различных аматоксинов. Цифры, выделенные жирным шрифтом (1-8), обозначают стандартную нумерацию восьми аминокислот, образующих аминотоксин. Также показаны стандартные обозначения атомов в аминокислотах 1, 3 и 4 (греческие буквы α-γ, греческие буквы α-δ и числа от 1' до 7', соответственно).
Фиг. 2 показывает цитотоксическую активность различных конъюгатов аманитин-герцептин с различными линкерными группами на клетках SKOV-3 в анализе с BrdU после инкубации в течение 72 час.
Фиг. 3 показывает цитотоксическую активность различных конъюгатов аманитин-герцептин с различными линкерными группами на клетках SK-BR-3 в анализе с BrdU после инкубации в течение 72 час.
Фиг. 4 показывает цитотоксическую активность различных конъюгатов аманитин-герцептин с различными линкерными группами на клетках NCI-N87 в анализе с BrdU после инкубации в течение 72 час.
Фиг. 5 показывает цитотоксическую активность различных конъюгатов аманитин-герцептин с различными линкерными группами на клетках MDA-MB231 в анализе с BrdU после инкубации в течение 72 час.
Фиг. 6 и фиг. 7 показывают количество аманитина, высвобожденного из различных конъюгатов аманитин-герцептин с различными линкерными группами после инкубации в плазме до 14 суток.
Фиг. 8 показывает сравнение цитотоксической активности различных конъюгатов аманитин-герцептин с различными линкерными группами на клетках SKOV-3 в анализе с BrdU до и после инкубации в плазме.
Фиг. 9 показывает сравнение активности двух различных конъюгатов аманитин-герцептин с различными линкерными группами in vivo на модели с ксенотрансплантатом SKOV-3.
Подробное описание изобретения
Перед обращением к приведенному ниже подробному описанию настоящего изобретения следует иметь в виду, что данное изобретение не ограничивается определенной методологией, протоколами и реагентами, описанными в данном описании, так как они могут изменяться. Также следует иметь в виду, что терминология, используемая в данном описании, используется только с целью описания определенных воплощений и не предназначена для ограничения объема настоящего изобретения, который будет ограничиваться только прилагаемой формулой изобретения. Если не дается иного определения, все технические и научные термины, используемые в данном описании, имеют те же значения, какие им обычно придают специалисты в данной области техники.
Предпочтительно, термины, используемые в данном описании, определяются так, как описано в «A multilingual glossary of biotechnological terms: (IUPAC Recommendations)», Leuenberger H.G.W., Nagel B. and Kölbi H., eds. (1995), Helvetica Chimica Acta, CH-4010 Basel, Switzerland).
В данном описании и следующей за ним формуле изобретения, если не указано иное, слово «включать» и такие варианты, как «включает» и «включающий», будут пониматься как подразумевающие включение указанных целого числа или стадии или группы целых чисел или стадий, но не исключающие какое-либо другое целое число или стадию или группу целых чисел или стадий.
В тексте данного описания цитируются некоторые документы. Каждый из документов, цитированных в данном описании (включая все патенты, заявки на патент, научные публикации, предписания изготовителей, инструкции, представления инвентарных номеров последовательностей GenBank и т.д.) выше или ниже, включен в данное описание в качестве ссылки в степени, возможной в связи с соответствующим законом о патентах. Ничего в данном описании не следует истолковывать как признание, что изобретение не дает права датировать задним числом такое раскрытие на основании предшествующего изобретения.
Теперь настоящее изобретение будет описываться дополнительно. В последующих разделах различные аспекты изобретения определяются подробнее. Каждый аспект, определенный таким образом, может быть объединен с любым другим аспектом или аспектами, если четко не указано иное. В частности, любая особенность, указанная как предпочтительная или выгодная, может быть объединена с любой другой особенностью или особенностями, указанными как предпочтительные или выгодные.
В первом аспекте настоящее изобретение относится к конъюгату, включающему часть, связывающую мишень соединенную через линкер L с аматоксином, при этом линкер L соединяется с аматоксином через
(iv) γ-атом С аминокислоты 1 аматоксина, в частности, через амидную связь;
(v) атом кислорода, связанный с δ-атомом С аминокислоты 3 аматоксина, в частности, через сложноэфирную связь, простую эфирную связь или уретановую связь; или
(vi) 6'-атом С аминокислоты 4 аматоксина, в частности, через атом кислорода, связанный с 6'-атомом С аминокислоты 4 аматоксина;
где в каждом случае линкер L соединен с частью, связывающей мишень, через остаток мочевины.
В контексте настоящего изобретения термин «конъюгат» относится к молекуле, включающей, по меньшей мере, две различные молекулы, соединенные ковалентной связью.
Термин «часть, связывающая мишень», используемый в данном описании, относится к любой молекуле или части молекулы, которая может специфически связываться с молекулой-мишенью или эпитопом-мишенью. Предпочтительными частями, связывающими мишень, в контексте настоящей заявки являются (i) антитела или их антигенсвязывающие фрагменты; (ii) антителоподобные белки и (iii) аптамеры нуклеиновой кислоты. «Части, связывающие мишень», подходящие для применения в настоящем изобретении, обычно имеют молекулярную массу 40000 Да (40 кДа) или более.
Используемое в данном описании первое соединение (например, антитело) считают «специфически связанным» со вторым соединением (например, антигеном, таким как белок-мишень), если оно имеет константу диссоциации KD ко второму соединению 100 мкМ или менее, предпочтительно 50 мкМ или менее, предпочтительно 30 мкМ или менее, предпочтительно 20 мкМ или менее, предпочтительно 10 мкМ или менее, предпочтительно 5 мкМ или менее, предпочтительно 1 мкМ или менее, предпочтительнее 900 нМ или менее, предпочтительнее 800 нМ или менее, предпочтительнее 700 нМ или менее, предпочтительнее 600 нМ или менее, предпочтительнее 500 нМ или менее, предпочтительнее 400 нМ или менее, предпочтительнее 300 нМ или менее, предпочтительнее 200 нМ или менее, даже предпочтительнее 100 нМ или менее, даже предпочтительнее 90 нМ или менее, даже предпочтительнее 80 нМ или менее, даже предпочтительнее 70 нМ или менее, даже предпочтительнее 60 нМ или менее, даже предпочтительнее 50 нМ или менее, даже предпочтительнее 40 нМ или менее, даже предпочтительнее 30 нМ или менее, даже предпочтительнее 20 нМ или менее, и даже предпочтительнее 10 нМ или менее.
В контексте настоящей заявки термины «молекула-мишень» и «эпитоп-мишень», соответственно, относятся к антигену и эпитопу антигена, соответственно, которые специфически связываются частью, связывающей мишень. Предпочтительно, молекула-мишень представляет собой опухолеспецифический антиген, в частности, антиген или эпитоп, который присутствует на поверхности опухолевых клеток одного или нескольких типов в повышенной концентрации и/или в другой пространственной конфигурации по сравнению с поверхностью неопухолевых клеток. Предпочтительно указанный антиген или эпитоп присутствует на поверхности опухолевых клеток одного или нескольких типов, но не на поверхности неопухолевых клеток. В отдельных воплощениях часть, связывающая мишень, специфически связывается с эпитопом HER-2/neu или молекулой фактора адгезии эпителиальных клеток (ЕрСАМ). В других воплощениях указанный антиген или эпитоп преимущественно экспрессируется на клетках, вовлеченных в аутоиммунные заболевания. В таких частных воплощениях часть, связывающая мишень, специфически связывается с эпитопом рецептора IL-6 (IL-6R).
Термин «антитело или его антигенсвязывающий фрагмент», используемый в данном описании, относится к молекулам иммуноглобулинов и иммунологически активным частям молекул иммуноглобулинов, т.е. молекулам, которые содержат антигенсвязывающий сайт, который иммуноспецифически связывает антиген. Также включаются иммуноглобулиноподобные белки, которые отбираются методами, включающими, например, фаговый дисплей к специфической связи с молекулой-мишенью, например, с белком-мишенью Her-2/neu или ЕрСАМ. Молекулы иммуноглобулинов по изобретению могут представлять собой молекулу иммуноглобулина любого типа (например, IgG, IgE, IgM, IgD, IgA и IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса. «Антитела и их антигенсвязывающие фрагменты», подходящие для применения в настоящем изобретении, включают, но не ограничиваются указанным, поликлональные, моноклональные, одновалентные, биспецифические, гетероконъюгатные, полиспецифические, человеческие, гуманизированные (в частности, CDR-привитые), деиммунизированные или химерные антитела, одноцепочечные антитела (например, scFv), фрагменты Fab, фрагменты F(ab')2, фрагменты, полученные Fab-экспрессирующей библиотекой, диатела или тетратела (Holliger P. et al., 1993), нанотела, антиидиотипические (анти-id) антитела (включая, например, анти-id антитела к антителам по изобретению) и эпитопсвязывающие фрагменты любых из вышеуказанных антител и фрагментов.
В некоторых воплощениях антигенсвязывающие фрагменты являются антигенсвязывающими фрагментами человеческих антител по настоящему изобретению и включают, но не ограничиваются указанным, Fab, Fab' и F(ab')2, Fd, одноцепочечные Fv (scFv), одноцепочечные антитела, дисульфидсвязанные Fv (dsFv) и фрагменты, включающие или VL-, или VH-домен. Антигенсвязывающие фрагменты антител, в том числе одноцепочечных антител, могут включать вариабельный(ые) домен(ы) один(одни) или в сочетании с полным или частью следующего: шарнирный участок, CL, домены CH1, CH2 и СН3. В изобретение также включены антигенсвязывающие фрагменты, также включающие любую комбинацию вариабельного(ых) домена(ов) с шарнирным участком, CL, доменами CH1, CH2 и СН3.
Антитела, применимые в изобретении, могут происходить от любого животного, включая птиц и млекопитающих. Предпочтительно антитела происходят от человека, грызуна (например, мыши, крысы, морской свинки или кролика), курицы, свиньи, овцы, козы, верблюда, коровы, лошади, осла, кошки или собаки. Особенно предпочтительно, когда антитела имеют человеческое или мышиное происхождение. Как используется в данном описании, термин «человеческие антитела» включает антитела с аминокислотной последовательностью человеческого иммуноглобулина и включают антитела, изолированные из библиотек человеческих иммуноглобулинов или из животных, трансгенных в отношении одного или нескольких человеческих иммуноглобулинов, и которые не экспрессируют эндогенные иммуноглобулины, как описано, например, в патенте США № 5939598, Kucherlapati & Jakobovits.
Термин «антителоподобный белок» относится к белку, который создан методами инженерии (например, мутагенезом петель) для специфического связывания с молекулой-мишенью. Обычно такой антителоподобный белок включает, по меньшей мере, одну вариабельную пептидную петлю, присоединенную к обоим концам каркаса белка. Такое двойное структурное ограничение значительно повышает аффинность связывания антителоподобного белка до уровней, сравнимых с уровнями антитела. Длину вариабельной пептидной петли обычно составляют 10-20 аминокислот. Каркасный белок может представлять собой любой белок с хорошими свойствами растворимости. Предпочтительно каркасный белок представляет собой небольшой глобулярный белок. Антителоподобные белки включают, без ограничения, аффинные антитела, антикалины и сконструированные белки анкиринового повтора (для общего представления см. Binz et al., 2005). Антителоподобные белки можно получить из больших библиотек мутантов, например, извлечь из больших библиотек фаговых дисплеев, и можно выделить по аналогии с регулярными антителами. Также антителоподобные связывающие белки можно получить комбинаторным мутагенезом выставленных на поверхность остатков в глобулярных белках.
Термин «аптамер нуклеиновой кислоты» относится к молекуле нуклеиновой кислоты, которая создана методами инженерии через повторные циклы отбора in vitro или SELEX (систематическое изменение лигандов путем экспоненциального обогащения) на связывание с молекулой-мишенью (для общего представления см. Brody and Gold, 2000). Нуклеотидный аптамер может представлять собой молекулу ДНК или РНК. Аптамеры могут содержать модификации, например, модифицированные нуклеотиды, такие как 2'-фторзамещенные пиримидины.
Используемое в данном описании определение «химическое производное» (или коротко «производное») соединения относится к разновидности, имеющей химическую структуру, схожую со структурой соединения, содержащую также по меньшей мере одну химическую группу, не присутствующую в соединении, и/или с отсутствием, по меньшей мере, одной химической группы, которая в соединении присутствует. Соединение, с которым сравнивают производное, известно как «исходное» соединение. Обычно «производное» можно получить из исходного соединения в одну или несколько химических реакционных стадий.
«Аналог» соединения, как используется в данном описании, структурно родственен, но не идентичен соединению и проявляет по меньшей мере одну активность соединения. Соединение, с которым сравнивают аналог, известно как «исходное» соединение. Вышеуказанные активности включают, без ограничения, активность связывания с другим соединением; активность ингибирования, например, активность ингибирования фермента; токсичное действие; активность, например, фермент-активирующую активность. Не требуется, чтобы аналог проявлял такую активность в такой же степени, как исходное соединение. Соединение рассматривают как аналог в контексте настоящей заявки, если оно проявляет релевантную активность в степени, по меньшей мере, 1% (предпочтительнее, по меньшей мере, 5%, предпочтительнее, по меньшей мере, 10%, предпочтительнее, по меньшей мере, 20%, предпочтительнее, по меньшей мере, 30%, предпочтительнее, по меньшей мере, 40%, предпочтительнее, по меньшей мере, 50%) от активности исходного соединения. Таким образом, термин «аналог аматоксина», используемый в данном описании, относится к соединению, которое структурно родственно любому соединению из α-аманитина, β-аманитина, γ-аманитина, ε-аманитина, аманина, аманинамида, амануллина и амануллиновой кислоты, показанных на фиг. 1, и проявляет активность на уровне, по меньшей мере, 1% (предпочтительнее, по меньшей мере, 5%, предпочтительнее, по меньшей мере, 10%, предпочтительнее, по меньшей мере, 20%, предпочтительнее, по меньшей мере, 30%, предпочтительнее, по меньшей мере, 40%, предпочтительнее, по меньшей мере, 50%) ингибирующей активности против РНК-полимеразы II млекопитающих по сравнению с, по меньшей мере, одним соединением из α-аманитина, β-аманитина, γ-аманитина, ε-аманитина, аманина, аманинамида, амануллина и амануллиновой кислоты. «Аналог аматоксина», подходящий для применения в настоящем изобретении, даже может проявлять большую ингибирующую активность против РНК-полимеразы II млекопитающих, чем любое одно соединение из α-аманитина, β-аманитина, γ-аманитина, ε-аманитина, аманина, аманинамида, амануллина или амануллиновой кислоты. Ингибирующую активность можно измерить, определяя концентрацию, при которой происходит ингибирование на 50% (величина IC50). Ингибирующую активность против РНК-полимеразы II млекопитающих можно определить косвенно путем измерения ингибирующей активности в отношении пролиферации клеток. Подходящий анализ для измерения пролиферации клеток описан в примерах.
Термин «полусинтетический аналог» относится к аналогу, который получают химическим синтезом с использованием в качестве исходного материала соединений из природных источников (например, растительных материалов, бактериальных культур или клеточных культур). Обычно «полусинтетический аналог» по настоящему изобретению синтезируют, исходя из соединения, выделенного из гриба семейства Amanita. Напротив, термин «синтетический аналог» относится к аналогу, синтезированному так называемым полным синтезом из небольших (типично нефтехимических) строительных блоков. Обычно такой полный синтез выполняют без помощи биологических процессов.
Используемый в данном описании термин «конъюгат аптамера» относится к конъюгату связывающей мишень части с токсином, в котором часть, связывающая мишень, представляет собой аптамер нуклеиновой кислоты согласно указанной выше альтернативе (iii).
Термин «линкер» в контексте настоящего изобретения относится к молекуле, которая соединяет два компонента, причем каждый присоединяется к одному концу линкера, и которая увеличивает расстояние между двумя компонентами и уменьшает пространственное взаимное влияние между указанными компонентами, например, в данном случае, между частью, связывающей мишень, и аматоксином. В отсутствие линкера прямая связь аматоксина с частью, связывающей мишень, может снизить возможность взаимодействия аматоксина с РНК-полимеразой II. В отдельных воплощениях линкер имеет длину своей основной цепи в 1-30 атомов (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 атомов), т.е. длина линкера определяется как самое короткое соединение, измеренное числом атомов или связей между аматоксиновой группой и частью, связывающей мишень, при этом одна сторона основной цепи линкера прореагировала с аматоксином и другая сторона с частью, связывающей мишень. В контексте настоящего изобретения линкер предпочтительно представляет собой С1-20-алкиленовую, С1-20-гетероалкиленовую, С2-20-алкениленовую, С2-20-гетероалкениленовую, С2-20-алкиниленовую, С2-20-гетероалкиниленовую, циклоалкиленовую, гетероциклоалкиленовую, ариленовую, гетероариленовую, аралкиленовую или гетероаралкиленовую группу, необязательно замещенную. Линкер может содержать один или несколько структурных элементов, таких как карбоксамидные, сложноэфирные, простые эфирные, простые тиоэфирные, дисульфидные, мочевинные, углеводородные группы и т.п. Линкер также может содержать комбинации из двух или большего числа таких структурных элементов. Каждый из указанных структурных элементов может присутствовать в линкерной группе более одного раза, например, дважды, три раза, четыре раза, пять раз или шесть раз. В некоторых воплощениях линкер может включать дисульфидную связь. Следует представлять, что линкер должен быть присоединен к аматоксину и к части, связывающей мишень, или в одну стадию или две или больше последовательных стадий. С такой целью линкер должен будет иметь две группы, предпочтительно, у проксимального и дистального конца, которые могут (i) образовывать ковалентную связь с группой, присутствующей в одном из соединяемых компонентов, предпочтительно, активированной группой на аматоксине или части, связывающей мишень, или (ii) которые активированы или могут быть активированы для образования ковалентной связи с группой на аматоксине. Соответственно, предпочтительно, что у дистального и проксимального конца линкера находятся химические группы, которые являются результатом такой реакции сочетания, например, сложноэфирная, простая эфирная, уретановая, пептидная связь и т.д.
В контексте настоящего изобретения термин «аматоксин» включает все циклические пептиды, состоящие из 8 аминокислот, выделенные из рода Amanita и описанные Wieland T. и Faulstich H. (Wieland T., Faulstich H., CRC Crit. Rev. Biochem., 1978, Dec, 5(3): 185-260), и кроме того, включает все их химические производные; а также все их полусинтетические аналоги, также их синтетические аналоги, построенные из строительных блоков в соответствии с главной структурой природных соединений (циклическая, 8 аминокислот), также все синтетические и полусинтетические аналоги, содержащие негидроксилированные аминокислоты вместо гидроксилированных аминокислот, также все синтетические и полусинтетические аналоги, в которых простая тиоэфирная сульфоксидная группа заменена сульфидной, сульфоновой или атомами иными, чем сера, например, атомом углерода, как в карба-аналогах аманитина, при этом в каждом случае любое такое производное или аналог является функционально активным, ингибируя РНК-полимеразу II млекопитающих.
Функционально аматоксины определяют как пептиды или депсипептиды, которые ингибируют РНК-полимеразу II млекопитающих. Предпочтительными являются аматоксины с функциональной группой (например, карбоксильной группой, аминогруппой, гидроксигруппой, тиольной или тиолозахватывающей группой), которую можно ввести во взаимодействие с молекулами линкера или частями, связывающими мишень, как определено выше. Аматоксинами, которые особенно подходят для конъюгатов по настоящему изобретению, являются α-аманитин, β-аманитин, γ-аманитин, ε-аманитин, аманин, аманинамид, амануллин и амануллиновая кислота, показанные на фиг. 1, а также их соли, химические производные, полусинтетические аналоги и синтетические аналоги. Особенно предпочтительными аматоксинами для применения в настоящем изобретении являются α-аманитин, β-аманитин и аманинамид.
В контексте настоящего изобретения термин «соединенный с частью, связывающей мишень через мочевинную группу» относится к соединению между линкером и частью, связывающей мишень, где часть, связывающая мишень, непосредственно присоединена к линкеру через группу -NH-C(O)-NH-.
В отдельных воплощениях настоящего изобретения конъюгат имеет структуру, выбранную из одной из следующих структур:
аматоксин-γС(О)-NH-L-NH-C(O)-NH-(часть, связывающая мишень);
аматоксин-δС-О-С(О)-L-NH-C(O)-NH-(часть, связывающая мишень);
аматоксин-δС-О-L-NH-C(O)-NH-(часть, связывающая мишень);
аматоксин-δС-О-С(О)-NH-L-NH-C(O)-NH-(часть, связывающая мишень) и
аматоксин-6'С-О-L-NH-C(O)-NH-(часть, связывающая мишень).
В отдельных воплощениях настоящего изобретения часть, связывающая мишень, соединяется с линкером L через аминогруппу, присутствующую в части, связывающей мишень, при этом аминогруппа образует часть указанной мочевинной группы.
В отдельных воплощениях настоящего изобретения аматоксин выбирают из α-аманитина, β-аманитина, γ-аманитина, ε-аманитина, аманина, аманинамида, амануллина или амануллиновой кислоты или их солей или аналогов.
В отдельных воплощениях настоящего изобретения линкер L включает одну или несколько групп, в частности, одну, две или три группы, выбранные из списка, включающего алкиленовую, алкениленовую, алкиниленовую, циклоалкиленовую, гетероалкиленовую, гетероалкениленовую, гетероалкиниленовую, гетероциклоалкиленовую, ариленовую, гетероариленовую, аралкиленовую и гетероаралкиленовую группу, при этом каждая группа может быть необязательно независимо замещенной.
Термин «алкилен» относится к двухвалентным линейным насыщенным углеводородным группам с 1-20 атомами углерода, включая группы с 1-10 атомами углерода. В некоторых воплощениях алкиленовые группы могут представлять собой низшие алкиленовые группы. Термин «низшие алкиленовые группы» относится к алкиленовым группам с 1-6 атомами углерода, и в некоторых воплощениях с 1-5 или 1-4 атомами углерода. Примеры алкиленовых групп включают, но не ограничиваются указанным, метилен (-СН2-), этилен (-СН2-СН2-), н-пропилен, н-бутилен, н-пентилен и н-гексилен.
Термин «алкенилен» относится к двухвалентным линейным группам с 2-20 атомами углерода, при этом, по меньшей мере, одна из углерод-углеродных связей представляет собой двойную связь, в то время как другие связи могут быть простыми или также двойными связями. Термин «алкинилен» в данном описании относится к группам с 2-20 атомами углерода, при этом, по меньшей мере, одна из углерод-углеродных связей представляет собой тройную связь, в то время как другие связи могут быть простыми, двойными или тройными связями. Примеры алкениленовых групп включают этенилен (-СН=СН-), 1-пропенилен, 2-пропенилен, 1-бутенилен, 2-бутенилен, 3-бутенилен и т.п. Примеры алкиниленовых групп включают этинилен, 1-пропинилен, 2-пропинилен и т.д.
Предполагается, что «циклоалкилен», когда используется в данном описании, относится к двухвалентному циклу, являющемуся частью любой устойчивой моноциклической или полициклической системы, где такой цикл имеет от 3 до 12 атомов углерода, но не имеет гетероатомов, и где такой цикл является полностью насыщенным, и предполагается, что термин «циклоалкенилен» относится к двухвалентному циклу, являющемуся частью любой устойчивой моноциклической или полициклической системы, где такой цикл имеет от 3 до 12 атомов углерода, но не имеет гетероатомов, и где такой цикл является, по меньшей мере, частично ненасыщенным (но за исключением любого ариленового цикла). Примеры циклоалкиленов включают, но не ограничиваются указанным, циклопропилен, циклобутилен, циклопентилен, циклогексилен и циклогептилен. Примеры циклоалкениленов включают, но не ограничиваются указанным, циклопентенилен и циклогексенилен.
Предполагается, что используемые в данном описании термины «гетероциклоалкилен» и «гетероциклоалкенилен» относятся к двухвалентному циклу, являющемуся частью любой устойчивой моноциклической или полициклической системы, где такой цикл имеет от 3 до примерно 12 атомов, и где такой цикл состоит из атомов углерода и, по меньшей мере, одного гетероатома, в частности, по меньшей мере, одного гетероатома, независимо выбранного из группы, состоящей из N, O и S, причем гетероциклоалкилен относится к такому циклу, который является полностью насыщенным, и гетероциклоалкенилен относится к циклу, который является, по меньшей мере, частично ненасыщенным (но за исключением любого ариленового или гетероариленового цикла).
Предполагается, что термин «арилен» обозначает двухвалентный цикл или циклическую систему, являющуюся частью любой устойчивой моноциклической или полициклической системы, где такой цикл или циклическая система имеет от 3 до 20 атомов углерода, но не имеет гетероатомов, и такой цикл или циклическая система состоит из ароматической группы, определяемой правилом «4n+2» π-электронов, включая фенилен.
Используемый в данном описании термин «гетероарилен» относится к двухвалентному циклу или циклической системе, являющейся частью любой устойчивой моно- или полициклической системы, где такой цикл или циклическая система имеет от 3 до 20 атомов, и такой цикл или циклическая система состоит из ароматической группы, определяемой правилом «4n+2» π-электронов, и содержит атомы углерода и один или несколько гетероатомов азота, серы и/или кислорода.
В контексте настоящего изобретения термин «замещенный» предназначается для того, чтобы показать, что один или несколько атомов водорода, присутствующих в основной цепи линкера, заменены на выбор указанной(ыми) группой(ами), при условии, что нормальная валентность указанного атома или соответствующего атома группы, который замещен, не превышается, и что замещение приводит к устойчивому соединению. Термин «необязательно замещенный» предназначается для обозначения того, что линкер является или незамещенным или замещен, как определено в данном описании, одним или несколькими заместителями, как определено в данном описании. Когда заместителем является кетогруппа (или оксогруппа, т.е. =О), тио- или иминогруппа или подобная группа, тогда замещаются два атома водорода в основной цепи линкера. Примеры заместителей включают, например, алкил, алкенил, алкинил, циклоалкил, гетероциклоалкил, арил, гетероарил, аралкил, гетероаралкил, ацил, ароил, гетероароил, карбоксил, алкокси, арилокси, ацилокси, ароилокси, гетероароилокси, алкоксикарбонил, галоген, (тио)сложноэфирную группу, циано, фосфорил, амино, имино, (тио)амидо, сульфгидрил, алкилтио, ацилтио, сульфонил, сульфатную группу, сульфонатную группу, сульфамоил, сульфонамидо, нитро, азидо, галогеналкил, включая перфторалкил (такой как трифторметил), галогеналкокси, алкилсульфанил, алкилсульфинил, алкилсульфонил, алкилсульфониламино, арилсульфониламино, фосфорил, фосфатную группу, фосфонатную группу, фосфинатную группу, алкилкарбокси, алкилкарбоксиамидную группу, оксо, гидрокси, меркапто, амино (необязательно моно- или дизамещенный, например, алкилом, арилом или гетероарилом), имино, карбоксамидную группу, карбамоил (необязательно моно- или дизамещенный, например, алкилом, арилом или гетероарилом), амидино, аминосульфонил, ациламино, ароиламино, (тио)уреидо, арил(тио)уреидо, алкил(тио)уреидо, циклоалкил(тио)уреидо, арилокси или -О(СН2)n-OH, -O(CH2)n-NH2, -O(CH2)nCOOH, -(CH2)nCOOH, -C(O)O(CH2)nR, -(CH2)nN(H)C(O)OR или - N(R)S(O)2R, где n равен 1-4, и R независимо выбирают из водорода, -алкила, -алкенила, -алкинила, -циклоалкила, -циклоалкенила, -(С-присоединенного гетероциклоалкила), -(С-присоединенного гетероциклоалкенила), -арила и -гетероарила, причем допускается несколько степеней замещения. Специалистам в данной области техники будет понятно, что заместители, такие как гетероциклоалкил, арил, гетероарил, алкил и т.д., или функциональные группы, такие как -ОН, -NHR и т.д., сами могут быть замещенными в соответствующем случае. Специалистам в данной области техники также будет понятно, что сами замещенные группы также могут быть замещены в соответствующем случае.
В отдельных воплощениях настоящего изобретения линкер L, в частности, линкер L, показанный в абзаце [0042] или абзаце [0081], включает m групп, выбранных из следующего списка: алкиленовая, алкениленовая, алкиниленовая, циклоалкиленовая, гетероалкиленовая, гетероалкениленовая, гетероалкиниленовая, гетероциклоалкиленовая, ариленовая, гетероариленовая, аралкиленовая и гетероаралкиленовая группы, при этом каждая группа может быть, необязательно, независимо замещенной, линкер также включает n групп, выбранных независимо из одной из следующих групп: дисульфидная (-S-S-), простая эфирная (-О-), простая тиоэфирная (-S-), аминная (-NH-), сложноэфирная (-О-С(=О)- или -С(=О)-О-), карбоксамидная (-NH-C(=О)- или -C(=O)-NH-), уретановая (-NH-C(=O)-O- или -О-С(=О)-NH-) и мочевинная (-NH-C(=O)-NH-) группы, при этом m=n+1. В отдельных воплощениях m равен 2 и n равен 1, или m=3 и n равен 2. В отдельных воплощениях линкер включает 2 или 3 незамещенные алкиленовые группы, и 1 или 2, соответственно, дисульфидные, простые эфирные, простые тиоэфирные, аминные, сложноэфирные, карбоксамидные, уретановые или мочевинные группы, соединяющие незамещенные алкиленовые группы.
В отдельных воплощениях линкер L, в частности, линкер L, показанный в абзаце [0042], представляет собой линейную цепь с 2-20 атомами, выбранными независимо из C, O, N и S, в частности, с 2-16 атомами, в более частном случае, с 5-14 атомами, и даже в более частном случае, с 6-12 атомами. В отдельных воплощениях, по меньшей мере, 60% атомов в линейной цепи являются атомами С. В отдельных воплощениях атомы в линейной цепи соединяются простыми связями.
В отдельных воплощениях атомы С в линейной цепи являются независимо частью необязательно замещенных метиленовых групп (-СН2-). В отдельных таких воплощениях необязательные заместители выбирают независимо из галогена и С1-6-алкила, в частности, метила.
В отдельных воплощениях линкер L, показанный в абзаце [0042] или абзаце [0081], выбирают из следующей группы линкеров:
сторона аматоксина: -(СН2)2- сторона части, связывающей мишень;
сторона аматоксина: -(СН2)3- сторона ча