Средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к средствам, обладающим антимикробным, сорбционным, обезболивающим и ранозаживляющим действием на местные гнойно-воспалительные процессы мягких тканей и слизистых оболочек, используемым в хирургии, дерматологии, акушерстве и гинекологии, оториноларингологии. Заявленное средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек является пленкой и содержит в качестве лечебных компонентов антисептик хлоргексидина биглюконат 0,05% и стимулятор регенерации метилурацил, содержит в качестве основы полиэтиленоксид с молекулярной массой 400 (ПЭО-400) и натриевую соль карбоксиметилцеллюлозы (Na-КМЦ), также в качестве лечебного компонента - метронидазол, в качестве анестетика содержит лидокаина гидрохлорид, в качестве стабилизатора - глицерин, в указанных в формуле изобретения количествах. Техническим результатом изобретения является создание эффективного средства в форме пленки, обладающего противомикробным, сорбционным, обезболивающим и ранозаживляющим действием. 3 табл.
Реферат
Изобретение относится к области медицины, а именно к средствам, обладающим антимикробным, сорбционным, обезболивающим и ранозаживляющим действием на местные гнойно-воспалительные процессы мягких тканей и слизистых оболочек, используемых в хирургии, дерматологии, акушерстве и гинекологии, оториноларингологии.
В современной хирургии одной из актуальных проблем является проблема лечения гнойных ран, что связано с распространенностью ран различной этиологии, гнойными осложнениями, высокой летальностью, большими материальными затратами на лечение. По данным некоторых авторов от всех хирургических заболеваний гнойные осложнения составляют 28-34%, а летальность от них достигает 22%.
На сегодняшний день все большее внимание отводится антисептикам для местного применения, в связи с тем, что частое использование антибиотиков приводит к преобладанию в ране малочувствительной или нечувствительной к ним микрофлоры. Без сомнения современные препараты должны обладать разнонаправленным действием: широкая антимикробная активность, высокая дегидратирующая способность, стимуляция регенерации тканей, местная анестезия.
С целью абсорбции гнойного экссудата и дренированию раневой поверхности в лекарственных препаратах (мази, гели и др.) для наружного применения в настоящее время широко используют полиэтиленоксиды (ПЭО), углеродные сорбенты, производные целлюлозы и др. Более того современные тенденции диктуют необходимость разработки удобных форм препаратов, таких как раневые покрытия (губки, пленки и др.).
Прототипом нашего изобретения рассматривается лекарственное средство, которое содержит в качестве основы - энтеросгель, в качестве лечебных компонентов антисептик 0,05% раствор хлоргексидина биглюконата и стимулятор регенерации метилурацил. (Патент РФ №2445083 «СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ МЯГКИХ ТКАНЕЙ И СЛИЗИСТЫХ ОБОЛОЧЕК»).
Однако данное средство представляет собой мазь, которая не обладает анестезирующим свойством и содержит всего один антисептик, что снижает область его применения при микст инфекции, которая все чаще встречается в раневом отделяемом.
Техническим результатом изобретения является создание эффективного средства в форме пленки, обладающего противомикробным, сорбционным, обезболивающим и ранозаживляющим действием.
Технический результат достигается тем, что средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек является пленкой и содержит в качестве лечебных компонентов антисептик хлоргексидина биглюконат 0,05% и стимулятор регенерации метилурацил, содержит в качестве основы полиэтиленоксид с молекулярной массой 400 (ПЭО-400) и натриевую соль карбоксиметилцеллюлозы (Na-КМЦ), также в качестве лечебного компонента - метронидазол, в качестве анестетика содержит лидокаина гидрохлорид, в качестве стабилизатора - глицерин в следующих массовых долях:
| Метронидазол | 1,0 |
| (ФС 42-2283-93) | |
| Лидокаина гидрохлорид | 2,0 |
| (ФС 42-0251-07) | |
| Метилурацил | 2,0 |
| (ФС 42-0256-07) | |
| Глицерин | 1,0 |
| (ФС 42-2202-99) | |
| Полиэтиленоксид с молекулярной массой 400 | 1,0 |
| (ФС 42-1242-96) | |
| Натриевая соль карбоксиметилцеллюлозы | 1,75 |
| (ТУ 6-55-221-1453-96) | |
| Раствор хлоргексидина биглюконата (0,05%) | 91,25 |
| (ТУ 9158-002-76922630-2005) |
Характеристика объектов
Метронидазол. Антибактериальный химиотерапевтический препарат, производное 5-нитроимидазола, обладает высокой активностью в отношении широкого спектра бактерий и простейших. Доказано, что анаэробы сохранили к нему 100% чувствительность. Механизм действия заключается в биохимическом восстановлении 5-нитрогруппы метронидазола внутриклеточными транспортными протеинами анаэробных микроорганизмов и простейших. Восстановленная 5-нитрогруппа метронидазола взаимодействует с ДНК клетки микроорганизмов, ингибируя синтез их нуклеиновых кислот, что ведет к гибели бактерий.
Лидокаина гидрохлорид обладает местноанестезирующим действием, блокирует потенциалзависимые натриевые каналы, что препятствует генерации импульсов в окончаниях чувствительных нервов и проведению импульсов по нервным волокнам. Подавляет проведение не только болевых импульсов, но и импульсов других модальностей. Анестезирующее действие лидокаина в 2-6 раз сильнее, чем прокаина (действует быстрее и дольше - до 75 мин). При местном применении расширяет сосуды, не оказывает местнораздражающего действия.
Метилурацил. Белый кристаллический порошок без запаха. Мало растворим в воде (до 0,9 % при температуре +200°С) и спирте. По химическому строению метилурацил относится к производным пиримидина. Согласно экспериментальным данным, ряд препаратов этой группы обладает анаболической и антикатаболической активностью, ускоряет процессы клеточной регенерации; ускоряет заживление ран, стимулирует клеточные и гуморальные факторы защиты. Они оказывают также противовоспалительное действие. Характерной особенностью соединений этого ряда является стимуляция эритро- и особенно лейкопоэза, в связи с чем их обычно относят к группе стимуляторов лейкопоэза.
Глицерин бесцветная, без запаха, сладковатая на вкус, сиропообразная жидкость нейтральной реакции, растворяется во всех пропорциях в воде и спирте, сильно гигроскопичен. Оказывает на кожу и образовавшиеся на ее поверхности струпы размягчающее действие. В высоких концентрациях обладает антисептическими свойствами, благодаря чему применяется как консервирующая среда. Глицерин относится к группе стабилизаторов, обладающих свойствами сохранять и увеличивать степень вязкости и консистенции.
Полиэтиленоксиды (ПЭО) обладают дегидратирующим действием, причём в гнойной ране оно распространяется не только на ее ткани, но и на содержащиеся в ней микробные клетки. ПЭО-основа обезвоживает микробную клетку, резко снижает ее биологическую активность и ослабляет сопротивляемость к различным лекарственным средствам. В результате чего существенно возрастает антимикробная активность многих антибиотиков, сульфаниламидов и антисептиков. Благодаря способности ПЭО абсорбировать экссудат, а вместе с ним и микробные токсины, продукты распада тканей, биологически активные вещества - лизосомальные ферменты и другие медиаторы воспалительного процесса, «обрывая» тем самым его прогрессирующее течение, они обуславливают потенцирующее влияние на лечебный эффект лекарственного препарата в целом.
Натриевая соль карбоксиметилцеллюлозы (Na-КМЦ) растворима в воде, в водных растворах щелочей, в органических растворителях и минеральных маслах - не растворяется. При этом натриевая соль карбоксиметилцеллюлозы образует вязкие прозрачные растворы, характеризуемые псевдопластичностью, а для некоторых сортов продукта - и тиксотропией (т.е. способностью самопроизвольно восстанавливать разрушенную механическим воздействием исходную структуру). В виде геля Na-КМЦ взаимодействует с тканями и содержимым раны, равномерно распределяется по раневой поверхности, обеспечивает быструю и полную доставку лекарственных веществ к месту поражения, проявляет осмотическое действие при аппликации на рану, поглощая раневое отделяемое.
Хлоргексидина биглюконат. Является одним из наиболее активных местных антисептических средств. В химическом отношении является дихлорсодержащим производным бигуанида. Хлоргексидин оказывает быстрое и сильное бактерицидное влияние на грамположительные и грамотрицательные бактерии. Не действует на вирусы и споры. Препарат стабилен и после обработки им кожи сохраняется на ней в некотором количестве, продолжающем давать бактерицидный эффект. Препарат сохраняет активность в присутствии крови, гноя. Хлоргексидин эффективен также в отношении возбудителей венерических болезней.
СПОСОБ ОСУЩЕСТВЛЯЕТСЯ СЛЕДУЮЩИМ ОБРАЗОМ
Технология осуществлялась в асептических условиях и включала несколько этапов:
1. Навеску полимера натриевой соли карбоксиметил целлюлозы (Na-КМЦ) заливали раствором хлоргексидина биглюконата, в котором предварительно растворяли лидокаина гидрохлорид, добавляли глицерин и оставляли до набухания полимера, массу гомогенизировали медленно перемешивая и делили на две равные части;
2. Предварительно измельченный метилурацил диспергировали с первой частью приготовленного раствора полимера на хлоргексидина биглюконате, содержащего лидокаина гидрохлорид;
3. Предварительно измельченный метронидазол диспергировали с по-лиэтиленоксидом с молекулярной массой 400 (ПЭО-400) и к полученной суспензии по частям добавляли вторую часть раствора полимера на хлоргексидина биглюконате, содержащего лидокаина гидрохлорид;
4. Полученные композиции смешивали и после деаэрации массы ее выливали в чашки Петри на подготовленную подложку (тонкий слой вазелинового масла). Высушивали до остаточной влажности 10%, после чего разрезали на пластинки размером 2×2 см и герметично упаковывали в стерильный полимерный пакет.
ПРИМЕР ПО СПОСОБУ ПОЛУЧЕНИЯ
1. Навеску полимера натриевой соли карбоксиметилцеллюлозы (Na-КМЦ) (1,75 массовых долей) заливали раствором хлоргексидина биглюконата 0,05% (91,25 массовых долей), в котором предварительно растворяли лидокаина гидрохлорид (2,0 массовые доли), добавляли глицерин (1,0 массовые доли) и оставляли до набухания полимера, массу гомогенизировали медленно перемешивая и делили на две равные части.
2. Предварительно измельченный метилурацил (2,0 массовые доли) диспергировали с первой частью раствора полимера, приготовленного согласно пункту 1.
3. Предварительно измельченный метронидазол (1,0 массовых долей) диспергировали с полиэтиленоксидом с молекулярной массой 400 (1,0 массовых долей) и к полученной суспензии по частям добавляли вторую часть раствора полимера, приготовленного согласно пункту 1.
4. Полученные композиции смешивали и после деаэрации массы ее выливали в чашки Петри на подготовленную подложку (тонкий слой вазелинового масла). Высушивали до остаточной влажности 10%, после чего разрезали на пластинки размером 2×2 см и герметично упаковывали в стерильный полимерный пакет.
ОПРЕДЕЛЕНИЕ МИКРОБИОЛОГИЧЕСКОЙ АКТИВНОСТИ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ МЯГКИХ ТКАНЕЙ И СЛИЗИСТЫХ ОБОЛОЧЕК
Антимикробное действие разработанного средства изучалось методом диффузии в агар (ГФ XII, 2007) в отношении тест-штаммов St. aureus АТСС 6538-Р, Вас. cereus АТСС 10702, Е. coli АТСС 25922, Proteus vulgaris и Pseudomonas aeruginosa ATCC 9027, Candida albicans ATCC 885-653. Результаты определения представлены в табл. 1.
Из данных, представленных в табл. 1, следует, что разработанное нами средство обладает достаточно сильным противомикробным действием в отношении всех исследуемых тест-штаммов. Зона ингибирования роста при изучении спектра антимикробной активности наиболее выражена в отношении тест-штаммов St. aureus ATCC 653 8-Р, Вас. cereus ATCC 10702, Е. coli ATCC 25922, Proteus vulgaris, что достоверно превосходит зоны задержки роста при исследовании прототипа.
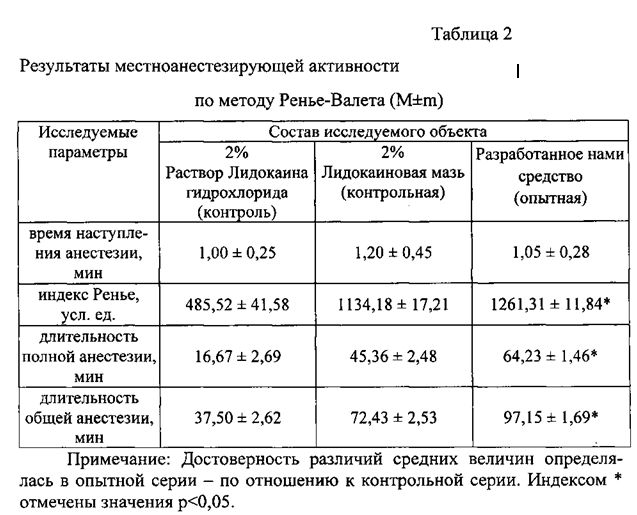
Местноанестезирующую активность разработанного нами средства изучали в опытах in vivo (кролики породы Шиншилла, в количестве 20 штук) методом Ренье-Валета, в основе которого лежит изменение чувствительности роговицы глаза кролика при нанесении на нее исследуемого образца, выражающееся в ответной реакции на раздражитель в виде смыкания века.
В конъюктивальный мешок глаза кролика вносили исследуемую пленку (разработанное нами средство) размером 2×2 см. Используя калиброванные волоски, на роговицу наносили ритмичные раздражения с частотой 100 ударов в минуту через 1, 2, 5, 8, 10, 12, 15 мин и далее через каждые 5 мин до начала смыкания век (табл. 2).
Исходя из статистически обработанных данных, представленных в таблице 2, можно отметить, что наибольшие показатели силы и продолжительности анестезии имеют место при использовании разработанного нами средства.
ПРИМЕР ЭКСПЕРИМЕНТАЛЬНОГО ПРИМЕНЕНИЯ
Изучение ранозаживляющей активности разработанного средства проводили в эксперименте на крысах-самцах породы «Вистар», массой 180-200 г, у которых моделировалась гнойная рана по методике П.И. Толстых. Экспериментальные животные были разделены на три серии, по 36 животных в каждой.
В 1-ой серии (модель) лечение не проводилось.
Во 2-ой серии (контроль) проводили лечение прототипом.
В 3-ей серии (опытная) проводили лечение разработанным нами средством (пленки размером 2×2 см).
Течение раневого процесса у экспериментальных животных оценивали планиметрическим (метод Л.И. Поповой), микробиологическим, гистологическим методами. Результаты исследований обработаны статистически (рассчитаны средние величины, критерий достоверности).
Животные выводились из эксперимента путем передозировки эфирного наркоза на 1, 3, 5, 8, 10, 15 сутки.
После моделирования на 1-е сутки во всех сериях отмечалась гиперемия краев раны, отек окружающих тканей, дно ран было покрыто налетом фибрина с участками некроза, наблюдалось гнойное отделяемое.
В процессе лечения происходило очищение поверхности раны от гнойно-некротических масс, купировался отек, появлялись грануляции и краевая эпителизация.
Данные планиметрического исследования свидетельствуют о более быстром уменьшении площади ран в опытной серии по сравнению с моделью и контролем (исходная площадь ран была 250±2,35 мм2). Так, с 10-х суток площади ран в контрольной и опытной сериях имели статистически значимые различия. Процесс заживления протекал быстрее в опытной серии по сравнению с контрольной и моделью. Результаты планиметрического исследования представлены в табл. 3.
Таким образом, полученные данные планиметрического исследования подтверждают высокую эффективность разработанного нами средства (опытная серия) в лечении гнойных ран. К 15-м суткам площадь ран в опытной серии сократилась в среднем на 99,2%, что было выше скорости заживления ран в среднем в 1,5 раза, по сравнению с контрольной серией.
Данные микробиологического исследования показали, что в опытной серии микробная обсемененность ран достоверно меньше, чем в контрольной серии, начиная с 8-х суток и на протяжении всего срока наблюдения. В опытной серии на 10-е сутки микробная обсемененность ран в 1,4 раза меньше, чем в контрольной серии. Таким образом, установлено, что разработанное нами средство в 1,4 раза сокращает микробную обсемененность ран по сравнению с прототипом.
Для полной оценки состояния раны в динамике был использован гистологический метод исследования раневых биоптатов, дающий возможность объективно оценить динамику течения раневого процесса.
На 3-ьи сутки при лечении с использованием прототипа на поверхности раны непосредственно под слоем препарата обнаруживался мощный слой инфильтрата, состоящий в подавляющем большинстве из гранулоцитов, также отмечаются очаги кровоизлияния в верхних слоях. На 15-е сутки наблюдалось полное покрытие грануляций эпидермисом практически у всех животных, эпидермис состоял из 2-х слоев клеток (причем верхний слой несколько инфильтрирован полиморфно-ядерными лейкоцитами), производные эпидермиса отсутствовали по всей площади раневого дефекта.
На 3-ьи сутки при лечении с использованием разработанного нами средства (опытная серия) отмечается незначительная инфильтрация свежих грануляций полиморфно-ядерными лейкоцитами. На 15-е сутки рана полностью эпителизирована, наблюдалось полное восстановление кожи за исключением ее производных.
Применение разработанного средства в лечении гнойных ран в I и II фазу раневого процесса повышает скорость заживления ран, сокращает микробную обсемененность ран, ускоряет формирование и созревание грануляционной ткани, способствует ранней и быстрой эпителизации раневой поверхности по сравнению с лечением прототипом. Более того, применение разработанного нами средства в виде пленки значительно облегчает процесс перевязки, при нанесении пленки не травмируется молодой эпителий и грануляции, как это происходит при намазывании мази на рану.
Средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек является пленкой и содержит в качестве лечебных компонентов антисептик хлоргексидина биглюконат 0,05% и стимулятор регенерации метилурацил, содержит в качестве основы полиэтиленоксид с молекулярной массой 400 и натриевую соль карбоксиметилцеллюлозы, также в качестве лечебного компонента - метронидазол, в качестве анестетика содержит лидокаина гидрохлорид, в качестве стабилизатора - глицерин в следующих массовых долях:
| Метронидазол | 1,0 |
| Лидокаина гидрохлорид | 2,0 |
| Метилурацил | 2,0 |
| Глицерин | 1,0 |
| Полиэтиленоксид с молекулярной массой 400 | 1,0 |
| Натриевая соль карбоксиметилцеллюлозы | 1,75 |
| Раствор хлоргексидина биглюконата (0,05%) | 91,25 |