Способ получения лекарственного средства для коррекции нарушений функций щитовидной железы
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности и касается способа получения лекарственного средства из растительного сырья для коррекции нарушений функций щитовидной железы. Способ получения лекарственного средства для коррекции нарушений функций щитовидной железы путем экстрагирования корней и корневищ лапчатки белой, корней шлемника байкальского и корней и корневищ родиолы розовой в соотношении 50 масс.%, 25 масс.%, 25 масс.% соответственно, которые измельчают и экстрагируют 50-60% этиловым спиртом при определенных условиях. Средство, полученное вышеописанным способом, характеризуется повышенным содержанием биологически активных веществ, эффективно корректирует нарушения функций щитовидной железы. 7 табл., 3 пр.
Реферат
Известно, что увеличение заболеваний щитовидной железы связано с геохимическими, социальными, экологическими и другими факторами [4]. Щитовидная железа является не только одним из самых крупных эндокринных органов по своим размерам и массе, но и одним из наиболее значимых с позиций роли для организма секретируемых гормонов - йодтиронинов. В наибольшей степени на частоту тиреоидной патологии влияет уровень потребления йода населением. Во всем мире дополнительным средством профилактики является йодирование пищевой поваренной соли, а также назначение таблетированных препаратов йода наиболее уязвимым слоям населения (дети, беременные и кормящие женщины). В России более 30% территории, где почти у 80% населения наблюдается массовое поражение щитовидной железы, в основном, это эндемический зоб. По мировой статистике различными заболеваниями щитовидной железы (повышенная или пониженная функция железы, узловые образования) страдают не менее 3% населения. Известно, что недостаточное содержание в организме тиреоидных гормонов приводит к расстройству структурно-функциональных взаимосвязей нервной, сердечно-сосудистой, иммунной и других систем [5]. Гормоны щитовидной железы крайне необходимы для роста тканей, в процессах закладки и функционировании мозга, формировании интеллекта, регуляции и поддержании обмена веществ. Фармакологическая коррекция гипотиреоидного состояния организма основана на восполнении дефицита йода и тиреоидных гормонов. Несмотря на обширный арсенал современных лекарственных средств с тиреотропным действием, применяемых для лечения заболеваний щитовидной железы, необходимость в эффективных и безопасных средствах сохраняется. Учитывая клинические проявления, при гипотиреозе целесообразно использовать комплексный подход в лечении, целью которого является не только нормализация тиреоидного гормонального статуса, но и улучшение состояния нейровегетативной, сердечно-сосудистой, иммунной систем, коррекция когнитивных нарушений и эмоционально-аффективных расстройств. При комплексном лечении больных с указанным профилем расстройств назначают эффективную седативную и метаболическую терапию. Для этой цели используют седативные препараты растительного происхождения, анаболические препараты, транквилизаторы, преимущественно бензодиазепинового ряда, антидепрессанты. Используемые препараты не всегда отличаются достаточной клинической эффективностью и при длительном применении могут вызывать побочные эффекты. В связи с этим оправдан значительный интерес к поиску новых средств, способных предупреждать и корригировать гипофункцию щитовидной железы.
Лекарственные растения являются наиболее перспективным источником биологически активных веществ тиреотропного действия. Одним из растений, применяемых в народной медицине для лечения и профилактики заболеваний щитовидной железы, является лапчатка белая (Potentilla alba L., семейство розоцветные - Rosaceae). Установлено, что извлечения из Potentilla alba L. могут применяться при коррекции гипофункции и гиперфункции щитовидной железы [3, 6]. Наряду с этим, учитывая зависимость ментальных процессов и клинических проявлений гипотиреоза от уровня тиреоидных гормонов в крови, развития вторичного иммунодефицита, целесообразными представляются вопросы коррекции патологических проявлений гипотиреоза средствами, обладающими иммуномодулирующим (Rodiola) и ноотропным (Scutellaria,) действием. Объектом исследования служило комплексное растительное средство «Тиреотон-1» (условное название), состоящее из экстракта лапчатки белой сухого, экстракта шлемника байкальского сухого и экстракта родиолы розовой сухого в соотношении 50%, 25%, 25% соответственно и его влияние на течение экспериментального гипотиреоза. В «Тиреотоне-1» основным действующим компонентом является лапчатка белая, а шлемник байкальский и родиола розовая являются усиливающими и модулирующими действие первого.
В качестве прототипа использовали ламинарию в таблетках («Эвалар», Россия) в дозе 3 мг/кг, которая компенсирует суточную норму йода на 133% (согласно аннотации к препарату).
Технический результат изобретения - расширение ассортимента лекарственных средств растительного происхождения, имеющих надежную и обеспеченную сырьевую базу и корректирующих нарушения функций щитовидной железы, влияя на основные звенья патогенеза заболевания за счет многокомпонентности лекарственного средства. Заявляемое лекарственное средство включает высушенный измельченный экстракт из следующих растений: корневищ и корней лапчатки белой, корневищ и корней родиолы розовой, корней шлемника байкальского. Для достижения указанной цели, растительное сырье - корневища и корни лапчатки белой, соответствующие требованиям проекта ГОСТ Р 51074-2003, корневища и корни родиолы розовой, соответствующие требованиям ГФ XI вып. 2, ст. 75, и корни шлемника байкальского, соответствующие требованиям ФС 42-453-91, взятые в соотношении 50, 25, 25% соответственно, измельчают на мельнице для размола сухих проб МРП-2 до размера частиц не более 2 мм и экстрагируют 50-60% этиловым спиртом в соотношении сырье-экстрагент, равном 1:(14-16) (с учетом коэффициента водопоглощения), при температуре 55-65°C и постоянном перемешивании. Процесс повторяют трижды. Время экстракции при 1-ом и 2-ом контактах фаз - 60 мин, при 3-ем контакте фаз - 30 мин. Извлечения фильтруют через серошинельное сукно, объединяют, упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке и измельчают на мельнице пропеллерного типа. Выход готового продукта составляет 27.0±0.5% от массы растительного сырья. Конечный продукт представляет собой мелкодисперсный порошок коричневого цвета с приятным запахом и горьковатым вяжущим вкусом, с содержанием влаги не более 5%. Полученный нами продукт характеризуется как средство, корректирующее нарушения функций щитовидной железы.
Для качественной оценки полученного фитоэкстракта нами были использованы: хроматография в тонком слое сорбента. Хроматографический анализ проводили на пластинках «Сорбфил ПТСХ-АФ-А-УФ» с использованием различных систем растворителей: хлороформ - этанол - вода (26:16:3), н-бутанол - ледяная уксусная кислота - вода (4:1:2).
Фитостериновые соединения детектировали после обработки хроматографических пластинок 20% раствором серной кислоты и нагревания при 100°C в течение 15 минут в виде розовых пятен с величиной Rf около 0,7 на уровне стандартного образца β-ситостерина. Идентифицированы - β-ситостерин и олеаноловая кислота.
Фенольные соединения детектировались после обработки хроматографических пластин раствором алюминия хлорида в виде желто-зеленых пятен. Идентифицировали рутин; кверцетин; цинарозид.
Фенолы производные детектировали в системе растворителей (хлороформ-метанол-вода (26:14:3)) после обработки хроматограммы 10% раствором натрия карбоната и нагревали в сушильном шкафу при 100°C две минуты, затем опрыскивали пластинку диазотированным сульфацилом и еще нагревали при 110°C в течение 2 минут. На хроматограмме 1 пятно красноватого цвета с Rf 0.42, соответствующее салидрозиду [1].
Количественное определение.
Простые фенолы (Салидрозид). К 0.5 г экстракта сухого «Тиреотон-1» добавляли 10 мл воды и нагревали на водяной бане с обратным холодильником 15 минут. Охлажденный фильтрат помещали в колбу, объемом 50 мл, добавляли 6 мл 10% раствора ацетата свинца, 2 мл насыщенного раствора натрия сульфата, перемешивали, доводили водой до метки (А). 5 мл раствора А переносили в колбу, объемом 25 мл, добавляли 2.5 мл 2% раствора натрия карбоната, 2.5 мл диазотированного сульфанила, доводили объем раствора водой до метки, перемешивали и измеряли оптическую плотность раствора при длине волны 486 нм, в кювете с толщиной слоя 10 мм, в качестве раствора сравнения использовали воду. Содержание салидрозида (X %) вычисляли по формуле:
, где
D - оптическая плотность испытуемого раствора;
kv - коэффициент разведения, равный 250;
М - навеска экстракта;
253 - удельный показатель поглощения салидрозида;
W - потеря массы при высушивании.
Стероиды (β-ситостерин). К 0.5 г экстракта сухого «Тиреотон-1» добавляли 10 мл хлороформа и нагревали на водяной бане с обратным холодильником 15 минут. Хлороформное извлечение, упаренное до сухого остатка, помещали в колбу объемом 25 мл и растворяли в концентрированной серной кислоте. Полученный раствор перемешивали и измеряли оптическую плотность при длине волны 310 нм, в кювете с толщиной слоя 10 мм, в качестве раствора сравнения использовали концентрированную серную кислоту. Содержание стериновых соединений (Х%), в пересчете на β-ситостерин рассчитывали по формуле:
, где
D0 - оптическая плотность испытуемого раствора;
kv - коэффициент разведения экстракта, равный 25;
D1 - оптическая плотность на β-ситостерина;
kvст - коэффициент разведения β-ситостерина, равный 25;
М - навеска экстракта;
W - потеря массы при высушивании экстракта.
Определено, что количественное содержание стериновых соединений в пересчете на β-ситостерин составило около 3,4%.
Методика количественного определения суммарного содержания флавоноидов.
0.5 г экстракта сухого «Тиреотон-1» помещали в коническую плоскодонную колбу вместимостью 100 мл с притертой пробкой, прибавляли 60 мл 60% спирта этилового, нагревали содержимое колбы на кипящей водяной бане в течение 1 ч. После охлаждения извлечение фильтровали в мерную колбу вместимостью 200 мл через бумажный фильтр, который промывали 10 мл 60% спирта этилового. Извлечение повторяли в тех же условиях еще раз и доводили объем объединенного фильтрата до метки 60% спиртом этиловым (раствор А). 2 мл раствора А переносили в мерную колбу вместимостью 25 мл и доводили до метки 60% спиртом этиловым (раствор Б). Оптическую плотность раствора Б измеряли на спектрофотометре при длине волны 281 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения использовали 60% спирт этиловый. Параллельно определяли оптическую плотность раствора стандартного образца байкалина при длине волны 281 нм. Суммарное содержание флавоноидов (X, %) в пересчете на байкалин и абсолютно сухое сырье рассчитывали по формуле
, где
D0 - оптическая плотность испытуемого раствора;
kv - коэффициент разведения экстракта, равный 2500;
Е - удельный показатель поглощения байкалина, равный 610;
М - навеска экстракта, г;
W - потеря массы при высушивании экстракта.
Определено, что количественное содержание флавоноидов в пересчете на байкалин в экстракте сухом «Тиреотон-1» составило 4.15%.
Количественная оценка проводилась по выходу флавоноидов, в пересчете на байкалин, фенолов, в пересчете на салидрозид, и экстрактивных веществ. Метрологические характеристики представлены в таблице 1.
Известен способ получения сухого экстракта «Тиреотон» [1], однако нами предложен более экономичный ресурсосберегающий вариант, позволяющий увеличить выход биологически активных веществ (табл. 2)
Пример 1.
500 г корневищ и корней лапчатки белой, соответствующих требованиям ГОСТ Р 51074-2003, 250 г корневищ и корней родиолы розовой, соответствующих требованиям ГФ XI вып. 2, ст. 75, и 250 г корней шлемника байкальского соответствующего требованиям ФС 42-453-91, взятые в соотношении 50, 25, 25% соответственно, измельчают на мельнице для размола сухих проб МРП-2 до размера частиц не более 2 мм (сито №20 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 14 л 50% этилового спирта в соотношении сырье-экстрагент, равном 1:14 с учетом коэффициента водопоглощения сырья. Экстрагируют при температуре 60°C и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще две экстракции в течение 60 и 30 мин, подавая каждый раз в экстрактор 50% спирт в количестве, равном объему слитого извлечения (1-ый слив - 10.85 л, 2-ой слив - 11.05 л, 3-ий слив - 9.87 л). Объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°C в течение 8 ч и измельчают на мельнице пропеллерного типа. Получают 270.3 г готового продукта, что составляет 27.3% от веса исходного сырья. Сухой экстракт представляет собой мелкодисперсный порошок коричневого цвета с приятным запахом и горьковатым вяжущим вкусом, комкуется, содержание влаги - 4.5%.
Острую токсичность «Тиреотона-1» определяли с использованием метода Першина [6] на белых крысах линии Wistar массой 180±11 г. Животные находились под постоянным наблюдением в течение 14 дней. В результате проведенных экспериментов установлено, что DL50 «Тиреотон-1» - 450 мг/кг. Животные погибали преимущественно на 1-2 сутки. При этом в первые часы после введения испытуемого средства у животных наблюдали признаки интоксикации в виде снижения двигательной активности, тахикардии, учащения дыхания. Гибель животных наступала от остановки дыхания. При макроскопическом исследовании внутренних органов наблюдались полнокровие сосудов с явлениями стаза, мелкоточечные кровоизлияния под эпикардом, вздутие петель кишечника, полнокровие мезентериальных сосудов и печени. При патоморфологическом исследовании внутренних органов отмечали резкое полнокровие осмотренных органов, более выраженное в легких и печени.
При введении белым крысам «Тиреотон-1» per os в максимально возможных дозах 4500 мг/кг гибели животных в течение 14 суток не наблюдали. В первые 2-5 часов после введения животным «Тиреотон-1» отмечали явления гиподинамии, учащенное мочеиспускание, отказ от корма.
Таким образом, полученные данные позволяют отнести «Тиреотон-1» к группе малотоксичных веществ по действующей классификации.
Учитывая DL50 «Тиреотон-1», составляющую 450 мг/кг, результаты предыдущих экспериментов для изучения влияния его на течение экспериментального гипотиреоза крыс были использованы дозы 10 и 50 мг/кг. В качестве препарата сравнения использовали ламинарию в таблетках («Эвалар», Россия) в дозе 3 мг/кг, что компенсирует суточную норму йода на 133% (согласно аннотации к препарату).
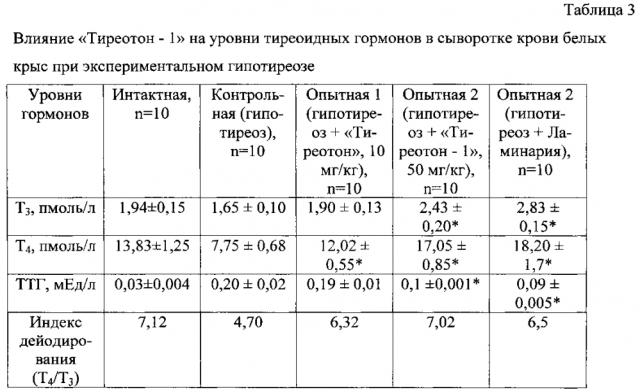
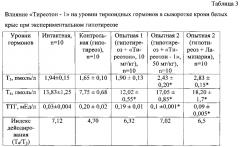
Для изучения тиреотропного действия «Тиреотон-1» воспроизведена модель экспериментального гипотиреоза [7]. В результате введения мерказолила перорально белым крысам линии Wistar в дозе 10 мг/кг в течение 28 дней отмечается достоверное снижение Т3 на 15%, Т4 - на 43%, увеличение ТТГ в 6,0 раз по сравнению с данными животных интактной группы. Введение животным «Тиреотон-1» перорально в дозе 50 мг/кг в течение 21 дня сопровождается повышением уровня Т4 в крови крыс в 2,2 раза, Т3 - на 47%, ТТГ уменьшается на 50% по сравнению с данными контрольной группы. Индекс дейодирования составил 7,02, что практически соответствует индексу дейодирования интактной группы животных (7,12). «Тиреотон» в дозе 10 мг/кг оказывает менее выраженную фармакотерапевтическую эффективность по сравнению с таковой в дозе 50 мг/кг. Уровень Т4 повышается на 55,1%, Т3 - на 15%, но уровень ТТГ при этом оставался высоким, уменьшаясь всего на 5% по сравнению с показателями животных контрольной группы. Масса тела крыс уменьшалась незначительно по сравнению с контролем. Полученные данные приведены в табл. 3.
Таким образом, в результате проведенного эксперимента установлено, что «Тиреотон-1» повышает функциональную активность щитовидной железы, нормализуя уровень тиреоидных гормонов. Курсовое введение «Тиреотон-1» в дозе 50 мг/кг приводит к повышению индекса дейодирования и практически соответствует таковому интактной группы крыс. «Тиреотон-1» оказывает аналогичное действие в сравнении с ламинарией.
Пример 2.
500 г корневищ и корней лапчатки белой, соответствующих требованиям ГОСТ Р 51074-2003, 250 г корневищ и корней родиолы розовой, соответствующих требованиям ГФ XI вып. 2, ст. 75, и 250 г корней шлемника байкальского, соответствующего требованиям ФС 42-453-91, взятые в соотношении 50, 25, 25% соответственно, измельчают на мельнице для размола сухих проб МРП-2 до размера частиц не более 2 мм (сито №20 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 14 л 60% этилового спирта в соотношении сырье-экстрагент, равном 1:15 с учетом коэффициента водопоглощения сырья. Экстрагируют при температуре 60°C и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще две экстракции в течение 60 и 30 мин, подавая каждый раз в экстрактор 60% спирт в количестве равном объему слитого извлечения (1-ый слив - 10.95 л, 2-ой слив - 11.35 л, 3-ий слив - 9.95 л). Объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°C в течение 8 ч и измельчают на мельнице пропеллерного типа. Получают 27.1 г готового продукта, что составляет 27.1% от веса исходного сырья. Сухой экстракт представляет собой мелкодисперсный порошок коричневого цвета с приятным запахом и горьковатым вяжущим вкусом; комкуется, содержание влаги - 4.12%.
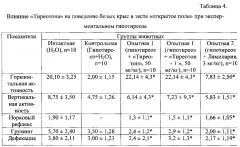
Далее рассматривается возможность влияния «Тиреотон-1» на состояние центральной нервной системы крыс при экспериментальном гипотиреозе. Исследование проводили с помощью методик: «открытое поле», «приподнятый крестообразный лабиринт» (ПКЛ), УРПИ.
Трехнедельное введение белым крысам «Тиреотона» в дозе 50 мг/кг приводит к повышению практически всех показателей. Общая двигательная активность (горизонтальная и вертикальная) увеличивается в 4,5 раза, появился норковый рефлекс, указывающий на появление исследовательской активности. Уменьшение актов груминга на 31% с предшествующей исследовательской активностью говорит о «комфортной» природе груминга. Уровень дефекации также снижается в опытной группе. Ориентировочно-исследовательская активность крыс опытной группы превышает таковые показатели в группе сравнения.
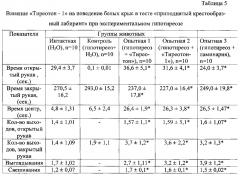
«Приподнятый крестообразный лабиринт» позволяет выявить степень тревожности животного. В настоящем разделе сравним показатели теста ПКЛ опытных групп, получавших на фоне экспериментального гипотиреоза «Тиреотон», «Тиреотон-1» в дозе 50 мг/кг и ламинарию в дозе 3 мг/кг.
Как видно из таблицы 5, курсовое введение «Тиреотон-1» в дозе 50 мг/кг в течение 21 дня уменьшает время проведения в закрытых рукавах лабиринта на 20% по сравнению с контролем. Достоверно увеличивается время проведения в открытых рукавах и на центральной площадке лабиринта в 4,0 раза по сравнению с показателями контрольной группы животных. Также необходимо отметить, что при введении «Тиреотон-1» увеличивается время пребывания в открытых рукавах лабиринта, количество выходов в открытый рукав лабиринта по сравнению с показателями животных в контрольной группе. Отмечена наибольшая исследовательская активность крыс, выраженная в количестве свешиваний и заглядываний под лабиринт. Тем самым можно утверждать о наличии более выраженной анксиолитической активности «Тиреотон-1», по сравнению с экстрактом лапчатки белой, что обусловлено входящими в его состав экстрактами шлемника байкальского и родиолы розовой, которые усиливают и модулируют действие первого.
В тесте УРПИ достоверно отмечено, что «Тиреотон-1» способствует сохранению памятного следа в эксперименте. Так, выявлено, что через 24 часа латентный период увеличился на 70%, на 3 сутки - в 2,7 раза, на 7 сутки - в 2 раза по сравнению с показателями контрольной группы (табл. 6). Данные показатели были аналогичными таковым у препарата сравнения.
Таким образом, введение «Тиреотон-1» на фоне экспериментального гипотиреоза способствует увеличению ориентировочно-исследовательской активности, стимулированию анксиолитической активности и выработке и сохранению памятного следа.
Пример 3.
500 г корневищ и корней лапчатки белой, соответствующих требованиям ГОСТ Р 51074-2003, 250 г корневищ и корней родиолы розовой, соответствующих требованиям ГФ XI вып. 2, ст. 75, и 250 г корней шлемника байкальского, соответствующего требованиям ФС 42-453-91, взятые в соотношении 50, 25, 25%, соответственно, измельчают на мельнице для размола сухих проб МРП-2 до размера частиц не более 2 мм (сито №20 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 16 л 65% этилового спирта в соотношении сырье-экстрагент, равном 1:16 с учетом коэффициента водопоглощения сырья. Экстрагируют при температуре 60°C и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще две экстракции в течение 60 и 30 мин, подавая каждый раз в экстрактор 65% спирт в количестве, равном объему слитого извлечения (1-ый слив - 11.85 л, 2-ой слив - 11.65 л, 3-ий слив - 10.00 л). Объединенные извлечения упаривают до 1/3 первоначального объема и очищают сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема, высушивают в вакуумной сушилке при температуре 60°C в течение 8 ч и измельчают на мельнице пропеллерного типа. Получают 26.6. г готового продукта, что составляет 26.6% от веса исходного сырья. Сухой экстракт представляет собой мелкодисперсный порошок коричневого цвета с приятным запахом и горьковатым вяжущим вкусом, комкуется, содержание влаги - 4.55%.
Изучение особенностей функционирования оксидантно-антиоксидантных систем организма крыс проводили при экспериментальном гипотиреозе и в условиях коррекции лекарственных средств «Тиреотон» и «Тиреотон-1». Определяли концентрацию МДА, уровень каталазы и восстановленного глутатиона в сыворотке крови и СОД в эритроцитах крови.
При курсовом введении «Тиреотон-1» в течение 21 дня при экспериментальном гипотиреозе отмечается тенденция к уменьшению содержания МДА в сыворотке крови на 21% с одновременным увеличением активности каталазы в сыворотке крови в 1,4 раза и СОД - в 2,1 раза по сравнению с данными показателями в контрольной группе. Уровень восстановленного глутатиона увеличивается на 7% по сравнению с контролем (табл. 7). Такие данные позволяют сделать вывод о повышении антиоксидантной системы организма и уменьшении свободнорадикальных процессов при коррекции экспериментального гипотиреоза «Тиреотоном-1».
Таким образом, курсовое введение «Тиреотон-1» в дозе 50 мг/кг повышает функциональную активность щитовидной железы при экспериментальном гипотиреозе, повышая уровень тиреоидных гормонов в сыворотке крови крыс и уменьшая уровень ТТГ в два раза по сравнению с показателями контрольной группы. Также «Тиреотон» способствует улучшению показателей поведенческих реакций животных на фоне гипотиреоидного состояния: увеличению ориентировочно-исследовательской активности, снижению тревожности животных, сохранению памятного следа в эксперименте, стимулированию антиоксидантной системы организма при экспериментальном гипотиреозе.
Таким образом, экспериментально установлено, что «Тиреотон-1» оказывает комплексное воздействие на организм при экспериментальном гипотиреозе, влияя на основные звенья патогенеза заболевания.
Используемая литература
1. Архипова Э.В. Влияние экстракта Potentilla alba L. и комплексного средства "Тиреотон" на течение экспериментального гипотиреоза. Автореферат диссертации на соискание ученой степени кандидата медицинских наук / Институт общей и экспериментальной биологии Сибирского отделения Российской академии наук. - Улан-Удэ, 2012. - 20 с.
2. Государственная фармакопея СССР: вып. 2. Общие методы анализа. Лекарственное растительное сырье. 11-е изд., доп. - М., 1987. - 400 с.
3. Захария А.В. Исследование лапчатки белой как перспективного средства для лечения заболеваний щитовидной железы: Автореф. дисс… канд. биол. наук. - Львов, 1997. - 24 с.
4. Мелик-Гусейнов В.В. Атлас растений. Растения в народной медицине России и сопредельных государств. Пятигорск: СНЕГ, 2011. 607 с.
5. Приходько Е.И. Лечение больных тиреотоксикозом травой пестрач белый применяющейся при заболеваниях щитовидной железы // Врачебное дело. №6. 1976. С. 66-71.
6. Семенова Е.Ф. Химический состав лапчатки белой и применение ее с лечебной целью / Е.Ф. Семенова, Е.В. Преснякова // Химия и компьютерное моделирование. Бутлеровские сообщения. - 2001. - №5. - С. 32-34.
7. Требования по доклиническому изучению общетоксического действия новых фармакологических веществ. - М., 1984. - 49 с.
8. Чугунова Л.Г., Рябков А.Н., Савилов К.В. Способ моделирования гипотиреоза // Патент 2165648 Российская Федерация. МПК G09B 23/28, A61K 31/4164. - Рязанский государственный медицинский университет. - №97120428/14. - 2001.
Способ получения лекарственного средства для коррекции нарушений функций щитовидной железы путем экстрагирования растительного материала, отличающийся тем, что в качестве растительного материала используют корни и корневища лапчатки белой, корни шлемника байкальского и корни и корневища родиолы розовой в соотношении 50 масс.%, 25 масс.%, 25 масс.% соответственно, которые измельчают до размера частиц не более 2 мм и экстрагируют 50-60% этиловым спиртом в соотношении растительный материал - экстрагент, равном 1:(14-16), первый и второй раз по 60 минут, третий - 30 минут при температуре 60-65°С.