Диагностика феномена "no-reflow" с помощью метода двухмерного стрейна
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к кардиологии. Проводят ультразвуковое исследование с синхронизированной электрокардиограммой и мультичастотным датчиком. При этом ультразвуковое исследование проводят из пяти стандартных доступов - по короткой оси на уровне митрального клапана и папиллярных мышц, а также 2-, 4- и 5-камерных позиций. На полученных изображениях определяют деформационные характеристики миокарда каждого из 16 сегментов левого желудочка. Затем вычисляют показатели глобальной продольной (GLS), циркулярной (GCS) и радиальной (GRS) деформации миокарда. При значении GLS менее 17,7, GCS менее 21,09 и GRS меньше 31,31 диагностируют феномен «no reflow». Способ обладает большой информативностью в анализе посегментарного сокращения миокарда, что позволяет выявить нарушение региональной сократимости в зоне сохраняющегося нарушения миокардиального кровотока и оценить эффективность проведенной реперфузии. 3 ил., 1 пр.
Реферат
Изобретение относится к области медицины (раздел «Неотложная кардиология»). Его задача заключается в выявлении отсутствия адекватного кровотока в миокарде на микроциркуляторном уровне после успешного проведения реваскуляризации инфаркт-связанной артерии.
Проведение своевременной и успешной реваскуляризации при ОКС с подъемом сегмента ST (OKCпST) является залогом эффективного восстановления нормального кровотока в инфаркт-связанной артерии и уменьшения площади и глубины некроза сердечной мышцы. Однако успешная реваскуляризация по шкале TIMI не всегда сопровождается восстановлением кровотока на микроциркуляторном уровне.
Одним из таких примеров неэффективной реперфузии миокарда является феномен «no-reflow». Феномен «nо-reflow» или феномен «невосстановленного кровотока» активно изучается в настоящее время, так как его несвоевременная диагностика приводит к возникновению систолической дисфункции миокарда, патологическому ремоделированию ЛЖ, формированию аневризмы и ряду других проблем, что делает лечение инфаркта миокарда безуспешным и значительно снижает качество жизни больных. Поэтому раннее выявление «nо-reflow» имеет несомненную клиническую ценность с целью проведения его своевременного лечения, что во многом будет определяющим фактором в исходе OKCnST.
По данным разных авторов выявлено, что невосстановленный кровоток может достигать 66% от общего числа эффективных реваскуляризаций инфаркт-обусловившей артерии (L. Galiutano et al., 2003). В руководстве Европейского общества кардиологов (European Society of Cardiology, ESC) по ведению больных инфарктом миокарда с подъемом сегмента ST (2008) говорится, что «nо-reflow» встречается в 10-40% случаев реваскуляризации.
Данный феномен имеет существенное влияние на ближайший и отдаленный прогноз пациента, являясь независимым предиктором неблагоприятных исходов, среди которых немалую роль играет рецидив ОКС. Рефрактерный «nо-reflow» ассоциирован со значительным повышением риска смерти, осложнений ИМ (особенно желудочковых аритмий), ухудшения систолической функции левого желудочка, развития сердечной недостаточности (Н. Ito el al., 1996; К.С. Wu et al., 1998; I. Morishima et al., 2000).
Диагностика феномена может осуществляться клинически по возобновлению или усилению болевого синдрома после проведения реперфузионных мероприятий, а также с учетом данных электрокардиографии, где отмечается снижение сегмента ST на протяжении 4 часов после процедуры реваскуляризации менее чем на 70%. Но опираться только на эти данные нецелесообразно, так как сделать достоверные выводы о недостаточности миокардиальной перфузии (MBG 0-3) на их основании не представляется возможным (P. Sorajja et al., 2005).
Для более точной диагностики «nо-reflow» могут использоваться различные методы визуализации миокарда (сцинтиграфия, контрастная эхокардиография), которые недоступны для повседневной рутинной практики.
Благодаря сцинтиграфии миокарда можно отличить зону некроза миокарда от зоны недостаточного кровоснабжения после предварительного внутривенного введения добутамина или его аналогов. Проба с физической нагрузкой не рассматривается с учетом ограничения двигательной активности больных OKCпST после проведения реперфузионной терапии. Чаще всего используемыми изотопами являются таллий-201 и меченые технецием-99m перфузионные радиоактивные индикаторы. После внутривенного введения только 5% радиоактивного изотопа накапливается в тканях сердечной мышцы, где происходит активный обмен веществ. В дальнейшем, если на сцинтиграмме виден дефект наполнения, необходимо выяснить, является ли он постинфарктной рубцовой тканью миокарда или зоной недостаточного кровоснабжения. По истечении 2-4 часов делают новый снимок, а при необходимости - через сутки после повторной инъекции радиоактивного индикатора. За время полураспада галлия, составляющего 73 часа, он по-новому распределяется в организме человека, что позволяет точно диагностировать дефект, запечатленный ранее. Наполнение дефекта изотопом указывает на наличие зоны недостаточного кровоснабжения миокарда или гипоксии сердечной мышцы, а не зоны некроза, что позволяет судить о целесообразности дальнейшего проведения лечебных мероприятий.
Недостатком данного метода является его инвазивность и длительность оценки результатов исследования, что ограничивает возможность оказания своевременной помощи при выявлении вышеуказанных изменений.
Особое значение имеет контрастная эхокардиография, являющаяся «золотым стандартом» в диагностике «nо-reflow». Данная методика предполагает наличие ультразвуковой аппаратуры, оснащенной технологией, позволяющей поэтапно использовать ультразвук низкой и высокой мощности. В начале исследования применение ультразвука низкой мощности позволяет контрастировать полости сердца, затем ультразвук высокой мощности в течение нескольких секунд разрушает введеное контрастное вещество (flash-эффект), находящееся в полостях, что в дальнейшем способствует визуализации миокардиальной стенки при непосредственном поступлении контраста в миокард. Эхоконтраст, состоящий из наполненных газом сфер с липидной оболочкой и диаметром, аналогичным или меньшим, чем у эритроцитов, вводят внутривенно, болюсно или с помощью инфузомата, в зависимости от объема исследования. Граница раздела «газ-оболочка» обеспечивает хорошее отражение ультразвука. Оценку данных, полученных при контрастировании миокарда, можно проводить качественно (визуально), полуколичественно и количественно. Количественную оценку перфузии миокарда осуществляют на рабочих станциях с помощью соответствующих программ, позволяющих проводить полный анализ и цифровую обработку изображений в избранных зонах интереса. Также обращает на себя внимание инвазивность и достаточно высокая стоимость проводимого обследования.
Техническим результатом изобретения является диагностика феномена «nо-reflow» у больных OKCпST после проведения тромболитической терапии и/или ЧКВ с оценкой результатов ангиографии по шкале TIMI.
Данный способ основан на быстром и неинвазивном выявлении нарушения микроциркуляции миокарда с помощью методики двухмерного стрейна за счет оценки нарушения деформационных характеристик миокарда в зоне ишемии, несмотря на успешно проведенную реваскуляризацию. Методика двухмерного стрейна в отличие от вышеперечисленных методов исследования является доступной в применении в повседневной врачебной практике и входит в оснащение УЗ-прибора. Метод обладает большой информативностью в анализе посегментарного сокращения миокарда, что позволяет выявить нарушение региональной сократимости в зоне сохраняющегося нарушения миокардиального кровотока и оценить эффективность проведенной реперфузии.
Данный метод реализуется следующим образом. Всем больным OKCпST после проведения эффективной реперфузионной терапии проводят УЗИ сердца с синхронизированной ЭКГ и мультичастотным датчиком 2,5-3,5 МГц. Регистрируют цифровые сигналы динамического изображения сердца в диапазоне частоты кадров 50-64 в сек. Используют 5 стандартных доступов: по короткой оси на уровне митрального клапана и папиллярных мышц, а также 2-, 4-, и 5-камерные апикальные позиции. Анализ данных заключается в обработке полученных видеозаписей сокращения миокарда левого желудочка в исследуемых позициях. Оценка деформационных характеристик миокарда проводится в 16 сегментах ЛЖ. Анализ данных происходит в полуавтоматическом режиме после указания эндокардиальных границ зон интереса в пяти позициях (одной позиции соответствует 6 сегментов). Зоны интереса определяются при трассировке эндокарда в одном кадре. Ширина зоны интереса определяется в соответствии с толщиной миокарда. Эпикард трассируется системой автоматически с последующей ручной корректировкой при необходимости.
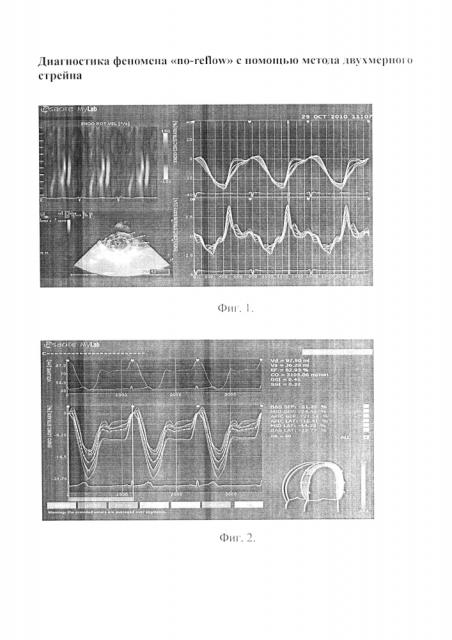
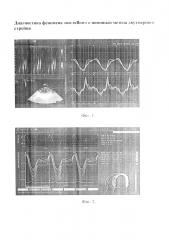
В дальнейшем покадрово рассчитывается смещение полученных границ миокарда в пределах выбранной зоны интереса из 6 сегментов на протяжении всего сердечного цикла (Фиг. 1). Независимо от полученных результатов необходима визуальная оценка - проверка двухмерного изображения на наличие стационарных артефактов с возможной их коррекцией. Сегменты с неудовлетворительным изображением исключаются из анализа. После оптимизации зоны интереса отображаются кривые стрейна для каждого из сегментов с получением региональных, глобальных, амплитудных и временных показателей, а также рассчитываются их значения в цифровом эквиваленте (Фиг. 2).
В ходе исследования проводят оценку глобальной продольной (GLS), циркулярной (GCS) и радиальной (GRS) деформации миокарда с последующим анализом полученных данных и сопоставлением их с нормативными показателями, полученными при обследовании контрольной группы здоровых добровольцев, где GLS составила 20,3±2,6, GCS - 25,1±4,01, GRS - 33,5±2,19, соотвественно. Было отмечено, что несмотря на успешно проведенную реваскуляризацию (TIMI 2-3) в ряде случаев отмечается значительное снижение всех деформационных характеристик миокарда, что свидетельствует о сохраняющемся нарушении кровотока на микроциркуляторном уровне. В дальнейшем при динамическом отслеживании данных больных выявляется прогрессирующее снижение конграктильной функции миокарда, нарастание дилатации камер сердца и снижения фракции выброса ЛЖ, что является закономерным следствием «nо-reflow». В связи с этим своевременная диагностика данного феномена имеет большое прогностическое значение для предотвращения патологического ремоделирования миокарда на ранних этапах с сохранением его конграктильной функции.
ПРИМЕР 1
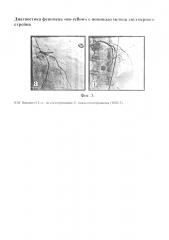
Больной П., 59 лет поступил в экстренном порядке в кардиологическое отделение Пензенской областной клинической больницы с жалобами на впервые возникшую выраженную жгучую боль в грудной клетке. Па ЭКГ бригадой скорой помощи зарегистрированы признаки инфаркта миокарда (QS в V1-V5, патологический з. Q в V6, подъем ST V2-V6). По данным КАГ: ствол проходим. Тип кровообращения - правый. ПНА - окклюзия в проксимальном сегменте, дистальное русло не визуализируется (инфаркт-связанная артерия). OA-проходима. ПКА - проходима. Выполнено прямое стентирование ПНА стентом 3,0·24 мм, 16 атм. Получен хороший ангиографический результат (TIMI 3) без диссекции и эмболизации (Фиг. 3).
Несмотря на полученный удовлетворительный результат реваскуляризации коронарного кровотока и купирование болевого синдрома состояние больного имело слабоположительную динамику, сохранялись признаки декомпенсированной сердечной недостаточности. По результатам УЗИ сердца сохранялся акинез всех сегментов МЖП, передней ст. ЛЖ, средних сегментов боковой ст. ЛЖ. ФВ по Simpson составила 30%. Диастолическая дисфункция ЛЖ по 1 типу. Тромб верхушки ЛЖ.
Больному был проведено исследование деформационных характеристик миокарда методом двухмерного стрейна, при анализе показателей которого отмечалось снижение глобальной продольной деформации на 50% (N - 20,3±2,6), циркулярной на 59% (N - 25,1±4,01), а радиальной на 20% (N - 33,5±2,19). Полученные параметры в значительной степени объясняют сохраняющуюся тяжесть состояния пациента из-за развившегося феномена «nо-reflow», несмотря на успешное проведение ЧКВ.
При повторном обследовании пациента через 6 месяцев после инфаркта отмечалось снижение глобальной продольной, циркулярной и радиальной деформации на 81%, 78% и 71% от нормы, что свидетельствует о значительном прогрессирующем снижении контрактильной функции миокарда вследствие невосстановленного кровотока на микроциркуляторном уровне с исходом в патологическое ремоделирование левого желудочка.
Способ диагностики феномена «no reflow» с помощью технологии двухмерного стрейна, включающий проведение ультразвукового исследования с синхронизированной электрокардиограммой и мультичастотным датчиком, во время которого регистрируют цифровые сигналы динамического изображения сердца, отличающийся тем, что ультразвуковое исследование проводят из пяти стандартных доступов - по короткой оси на уровне митрального клапана и папиллярных мышц, а также 2-, 4- и 5-камерных позиций, на полученных изображениях определяют деформационные характеристики миокарда каждого из 16 сегментов левого желудочка, затем вычисляют показатели глобальной продольной (GLS), циркулярной (GCS) и радиальной (GRS) деформации миокарда и при значении GLS менее 17,7, GCS менее 21,09 и GRS меньше 31,31 диагностируют феномен «no reflow».