Субстрат для иммобилизации функциональных веществ и способ приготовления данного субстрата
Иллюстрации
Показать всеИзобретение относится к субстрату для иммобилизации функциональных групп, а также к способам приготовления данного субстрата и картриджу с сорбентом для использования в устройстве диализа. Субстрат содержит соединения, предназначенные для иммобилизации функциональных молекул, при этом каждое соединение содержит цепочку, включающую: функциональную группу R, химически связанную с субстратом, при этом указанная функциональная группа R выбирается из группы, включающей: эфир, сложный эфир, карбонильную группу, сложный эфир карбоната, тиоэфир, дисульфид, сульфинил, сульфонил и карбонотиоил, амин, амид, карбамат, мочевины и гуанидины; и эпоксидсодержащую функциональную группу, соединенную с функциональной группой R сшивающим агентом, включающим, по крайней мере, одну нуклеофильную группу, выбранную из группы включающей амин, гидроксил и тиол; при этом функциональная молекула состоит из фермента, который выбирается из группы, включающей уреазу, уриказу, креатининазу, липазы, эстеразы, целлюлазы, амилазы, пектиназы, каталазы, ацилазу, каталазу, эстеразу, пенициллинамидазу, протеиназу К. 6 н. и 43 з.п. ф-лы, 4 ил., 3 табл.
Реферат
Область техники
Изобретение в общем относится к субстрату для иммобилизации функциональных веществ. Настоящее изобретение также относится к способам приготовления данного субстрата.
Предпосылки изобретения
При проведении биологических и химических анализов и процессов, аналитически или препаративно используемых в исследовательских, клинических, диагностических и производственных целях, зачастую требуется фиксация или иммобилизация функционального вещества на твердофазной подложке (или субстрате). Такая фиксация зачастую повышает устойчивость и универсальность вещества без снижения его эффективности и активности и дает возможность многократного использования вещества. Например, функциональные вещества, включающие биологические вещества, такие как ферменты, как правило, иммобилизуются на инертной подложке, такой как кремний или полиакриламидный гель, для повышения их устойчивости к изменению показателя pH или температурных условий при применении в производственных процессах катализации ферментами и упрощения последующего их отделения от продуктов реакции. Это обеспечивает повторное использование иммобилизованных ферментов и значительно упрощает очистку продукта, в результате обеспечивая более эффективные с точки зрения затрат процессы.
Иммобилизация функционального вещества, включающего биологическое вещество, может быть осуществлена путем физической или химической иммобилизации. Одной из форм физической иммобилизации является физическая адсорбция (физосорбция), при которой функциональное или биологическое вещество соединяется с субстратом посредством инкапсуляции или электростатическими, гидрофобными или ван-дер-ваальсовыми силами. Хотя физическая адсорбция и предоставляет относительно простой способ иммобилизации с широкой областью применения для целого ряда функциональных и/или биологических веществ, она часто не обеспечивает иммобилизацию с достаточной устойчивостью и подвержена выщелачиванию иммобилизованных функциональных и/или биологических веществ.
Более стабильным способом иммобилизации функциональных и/или биологических веществ является химическая иммобилизация, которая ковалентно связывает функциональное и/или биологическое вещество с субстратом в результате химической реакции. Химическая иммобилизация приводит, как правило, к повышенной активности, сниженной неспецифической адсорбции и повышенной устойчивости функционального и/или биологического вещества. Однако для химической иммобилизации в большинстве случаев требуется химическая модификация функционального и/или биологического вещества или субстрата для обеспечения эффективной связи.
Модификация поверхности материала твердофазной подложки, или «предактивация» твердофазной подложки, для улучшения ее связи с функциональным и/или биологическим веществом, как правило, приводит к включению в поверхность в целом слабо реагирующего полимерного материала реакционноспособных химических функциональных групп. Поверхностная модификация может быть достигнута физическими средствами, такими как нековалентное закрепление аффинного спейсера, или химическими средствами, такими как глутаральдегидная активация, цианогенбромидная активация, бромоацетилирование, диазотирование, вызванное ионизирующим излучением окисление и химическая прививочная сополимеризация.
Однако нековалентное закрепление аффинного спейсера сопровождается плохой воспроизводимостью и/или неустойчивой связью с поверхностью субстратов. Некоторые способы ковалентного закрепления, среди которых следует отметить имины и, в меньшей степени, сложные эфиры, могут быть гидролизованы в условиях реакции, применяемых для ферментативных реакций, приводя к частичной потере иммобилизованных ферментов и утечке ферментов в реакционную среду. Такие проблемы могут отрицательно отразиться, прежде всего, на способах иммобилизации на основе глутаральдегидной активации и бромоацетилирования. Хотя при диазотировании, циагенбромидной активации, вызванном ионизирующим излучением окислении и химической прививочной сополимеризации образуются ковалентные связи, являющиеся более устойчивыми по сравнению с нековалентными связями, данные способы подразумевают использование опасных, дорогих, сложных и/или жестких условий реакции.
Некоторые из данных способов также приводят к образованию высокого результирующего заряда на твердофазной подложке, что приводит к образованию нежелательных неспецифических электростатических связей функционального и/или биологического вещества при последующих процедурах биологического/химического процесса. Еще одной общей проблемой, связанной с применением жестких условий реакции, является неблагоприятное изменение свойств поверхности, что может затруднить закрепление функционального и/или биологического вещества, в частности, вещества с большой длиной полимерной цепочки. Это может привести к низкой концентрации функционального и/или биологического вещества на субстрате. Однако другими проблемами, характерными для некоторых коммерчески доступных твердофазных подложек, являются низкая устойчивость, ярко выраженная токсичность и недостаточная биологическая совместимость, что приводит к малому сроку годности, сложностям в обращении и ограниченному применению в медицинских целях.
Некоторые из данных способов основываются на дальнейшей модификации «предактивированных» подложек эпоксисилановым аппретом для иммобилизации гидрофильных молекул. Другие способы основываются на приготовлении субстрата путем реакции с бис-эпоксиоксирановым сшивающим агентом для иммобилизации молекулы к субстрату. Алифатические сшивающие агенты, применяемые в данных способах, вызывают снижение количества реакционноспособных групп, доступных для иммобилизации, снижение биологической совместимости и снижение воспроизводимости.
Возникает необходимость в предложении способов приготовления субстрата для иммобилизации функциональных и биологических веществ, устраняющих или, по крайней мере, смягчающих один или более из вышеописанных недостатков.
Возникает необходимость в предложении способов, которые являются подходящими, экономически эффективными, устойчивыми и надежными для приготовления субстрата для иммобилизации функциональных и биологических веществ.
Возникает также необходимость в предложении субстратов, которые являются устойчивыми, удобными в обращении, экономически эффективными, нетоксичными, биологически совместимыми и биоразлагаемыми для иммобилизации функциональных и биологически активных веществ и которые можно использовать для иммобилизации широкого диапазона веществ при высоких плотностях заполнения с улучшенной активностью и реакционной способностью.
Краткое изложение сущности изобретения
В соответствии с первым аспектом изобретения предлагается субстрат, содержащий соединения, предназначенные для иммобилизации функциональных молекул, при этом каждое соединение содержит цепочку, включающую: функциональную группу R, химически связанную с субстратом, указанная функциональная группа R выбирается из группы, включающей: эфир, сложный эфир, карбонильную группу, сложный эфир карбоната, тиоэфир, дисульфид, сульфинил, сульфонил и карбонотиоил; и эпоксидсодержащую функциональную группу, соединенную с функциональной группой R сшивающим агентом, включающим, по крайней мере, одну нуклеофильную группу.
В одном варианте осуществления субстрат содержит дополнительную эпоксидсодержащую группу, соединенную с цепочкой. В другом варианте осуществления количество дополнительных эпоксидсодержащих групп выбирается из числа 1, 2, 3, 4 и 5. В одном варианте осуществления сшивающий агент содержит дополнительные нуклеофильные группы, к которым указанные дополнительные эпоксидсодержащие группы присоединяются в указанной цепочке. Преимущество настоящего изобретения заключается в том, что плотность эпоксидсодержащих групп, способных вступать в реакцию с функциональной молекулой, увеличивается, и, следовательно, количество точек иммобилизации, доступных для иммобилизации вещества, также увеличивается.
Преимущество настоящего изобретения заключается в том, что сшивающий агент увеличивает длину связи между функциональной молекулой и субстратом и помогает укрепить связь функциональной молекулы с субстратом.
В еще одном варианте осуществления сшивающий агент содержит динуклеофильные частицы. В одном варианте осуществления динуклеофильный сшивающий агент выбирается, по крайней мере, из одного алкилдиамина и алкендиамина. Предпочтительно диаминовый сшивающий агент может предоставить дополнительные участки для эпоксиактивации. Не вдаваясь в теорию, предполагается, что до пяти молекул эпоксидсодержащего соединения (такого как эпихлоргидрин) может прореагировать с одной молекулой диаминового сшивающего агента. Это предпочтительно, поскольку обеспечивает увеличение плотности, например, эпоксидсодержащего соединения и, вследствие этого, количества точек иммобилизации, доступных для иммобилизации функциональной молекулы.
В еще одном варианте осуществления сшивающий агент содержит полинуклеофильные частицы. В еще одном варианте осуществления полинуклеофильные частицы могут являться полиаминами, такими как путресцин, спермидин, спермин, кадаверин, диэтилентриамин, триэтилентетрамин, тетраэтиленпентамин и тетрагидрофурфуриламин.
Введение аминогрупп сшивающего агента также выполняет благотворную роль внутреннего буфера рН для иммобилизируемого вещества. Дальнейшим преимуществом является то, что аминогруппы также действуют как ионообменники, обеспечивая условия стабилизации для иммобилизируемого вещества. Дальнейшим преимуществом является то, что аминогруппы являются сильно нуклеофильными, что делает более эффективным образование связи первого и второго эпоксидсодержащих соединений по сравнению с другими нуклеофильными группами, например группами ОН. Сильная нуклеофильная природа аминогрупп сшивающего агента является дальнейшим преимуществом, поскольку обеспечивает использование длинных сшивающих агентов при поддержании реакционной способности с эпоксидсодержащим соединением. Это является дальнейшим преимуществом, поскольку использование более длинных сшивающих агентов обеспечивает дальнейшее снижение стерических затруднений между субстратом и иммобилизованным веществом. Более предпочтительно, диамины, такие как гександиамин, относительно дешевые по сравнению с другими сшивающими агентами и являются коммерчески доступными материалами массового спроса. Низкая стоимость гександиамина обеспечивает массовое производство описанного в настоящем изобретении субстрата при относительно низких затратах.
Дальнейшим преимуществом является то, что связь «алкил-амин», образующаяся между эпоксидсодержащим соединением и гександиаминовым сшивающим агентом, устойчива к гидролизу при физиологических условиях, так что его можно использовать в водных системах, например, устройствах для диализа. Дальнейшим преимуществом является то, что субстрат в соответствии с сущностью изобретения является биологически инертным.
В соответствии со вторым аспектом предлагается способ иммобилизации функциональной молекулы на субстрате, содержащем этап экспонирования функциональной молекулы на субстрат в соответствии с сущностью данного изобретения.
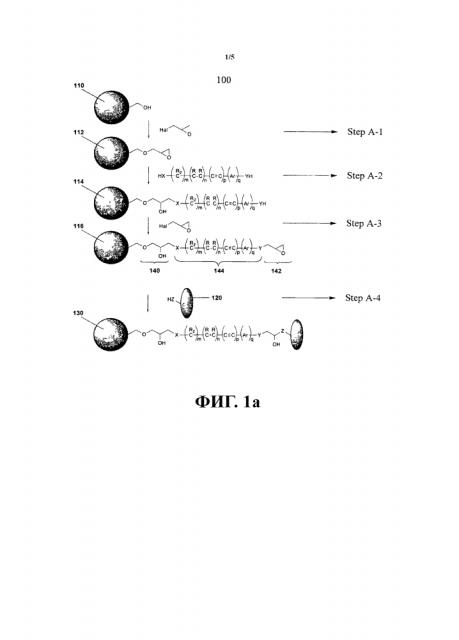
В соответствии с третьим аспектом предлагается способ приготовления субстрата для иммобилизации на нем функциональных молекул, включающий: (i) обеспечение электрофильных соединений, соединенных с поверхностью субстрата; (ii) обеспечение участия электрофильных соединений в реакции нуклеофильного замещения для получения посредством нее нуклеофильной группы и тем самым повышения нуклеофильности поверхности субстрата; (iii) осуществление участия нуклеофильной группы в реакции нуклеофильного замещения с другим электрофильным соединением для получения электрофильной группы на поверхности субстрата и тем самым повышения электрофильности субстрата.
Преимуществом способа является то, что удлиненный спейсер, прикрепленный к электрофильным группам субстрата, обеспечивает повышенную доступность функционального соединения к электрофильной группе, и одновременно обеспечивает повышение плотности и реакционной способности электрофильной группы к функциональной молекуле, тем самым осуществляя иммобилизацию функциональной молекулы на субстрате. Дальнейшим преимуществом является то, что этап (iii) способа также обеспечивает повышенную доступность функциональной молекулы к электрофильной группе для последующей иммобилизации на субстрате.
В одном варианте осуществления этапы (ii) и (iii) повторяются n-е количество раз для образования n поколений электрофильных групп на указанном субстрате. Это предпочтительно, поскольку обеспечивает удлинение спейсера и увеличение плотности электрофильных групп и, следовательно, количества участков иммобилизации, доступных для иммобилизации функциональной молекулы к субстрату.
Дальнейшим преимуществом является то, что этап (iii) способа обеспечивает относительно более быструю реакцию между сшивающим агентом и вторым электрофильным соединением. Это приводит к снижению уровня гидролиза электрофильных соединений и увеличению количества негидролизованных электрофильных групп, включенных в субстрат. Это является дальнейшим преимуществом, поскольку также обеспечивает повышение плотности электрофильных групп на субстрате для иммобилизации функциональной молекулы.
Дальнейшим преимуществом способа является то, что электрофильные группы смещены по отношению к субстрату таким образом, что способность функциональной молекулы к иммобилизации вследствие этого увеличивается по сравнению с субстратом, обладающим только одним электрофильным соединением, непосредственно соединенным с субстратом. Дальнейшим преимуществом является то, что это относительное смещение также обеспечивает повышенную доступность функциональной молекулы к электрофильной группе для последующей иммобилизации на субстрате.
В соответствии с четвертым аспектом предлагается картридж с сорбентом для использования в устройстве диализа, картридж с сорбентом, включающий субстрат, как описано в настоящем изобретении, для иммобилизации уреазы.
В соответствии с пятым аспектом предлагается способ диализа, включающий этапы: экспонирование диализата, содержащего мочевину, на субстрате, как описано в настоящем изобретении; и удаление диализата из указанного субстрата.
В соответствии с шестым аспектом предлагается диализатор для использования в устройстве диализа, диализатор, содержащий субстрат, как описано в настоящем изобретении, для иммобилизации уреазы. Таким образом, уреаза может быть иммобилизована на диализной мембране, такой как ацетатцеллюлозный мембранный фильтр, расположенной внутри диализатора.
В соответствии с шестым аспектом предлагается способ модифицирования диализной мембраны для иммобилизации на ней функциональных молекул, состоящий из следующих шагов:
(i) соединение электрофильных соединений с поверхностью мембраны;
(ii) обеспечение участия электрофильных соединений в реакции нуклеофильного замещения для получения посредством нее нуклеофильной группы, и тем самым повышения параметра нуклеофильности поверхности мембраны; и
(iii) обеспечение участия нуклеофильной группы в реакции нуклеофильного замещения с другим электрофильным соединением для получения электрофильной группы на поверхности мембраны, и тем самым повышения параметра нуклеофильности поверхности мембраны для иммобилизации на ней функциональных молекул. В одном варианте осуществления мембрана является ацетатцеллюлозной мембраной.
Предпочтительно способ может быть использован для модифицирования стандартной диализной мембраны, такой как ацетатцеллюлозная мембрана, диализатора. Этот этап модифицирования обеспечивает повышенную способность к иммобилизации на диализной мембране функциональных молекул, таких как диализатные ферменты, при использовании в диализаторе.
В соответствии с восьмым аспектом предлагается использование субстрата, как описано в настоящем изобретении, в устройстве диализа.
В одном варианте осуществления предлагается способ приготовления субстрата для иммобилизации на нем функциональных веществ, способ, включающий: соединение первого электрофильного соединения с субстратом; и химическое соединение второго электрофильного соединения с первым электрофильным соединением, соединенным с субстратом, при котором указанное второе электрофильное соединение при соединении с указанным первым электрофильным соединением сконфигурировано для иммобилизации на нем функционального вещества.
Предпочтительно первое и второе электрофильные соединения выбираются смещенными относительно друг друга таким образом, чтобы увеличить способность к иммобилизации функционального вещества по сравнению с субстратом только с одним электрофильным соединением, непосредственно соединенным с субстратом. Более предпочтительно первое и второе электрофильные соединения выбираются смещенными друг относительно друга таким образом, чтобы эффекты стерических затруднений поблизости от второго электрофила были снижены или минимизированы для усиления связи функционального вещества со вторым используемым электрофильным соединением.
Более предпочтительно первое и/или второе электрофильное соединение может быть диэлектрофилом, который эффективно конвертирует слабо нуклеофильный субстрат в сильно электрофильный субстрат. Это определяет изменения в полярности и реакционной способности субстрата.
Более предпочтительно, способ является простым и экономичным способом получения субстрата, обладающего относительно высокой реакционной способностью для иммобилизации на нем по сравнению с субстратами, полученными известными способами. Более предпочтительно второе электрофильное соединение способно образовывать устойчивые связи с функциональным веществом, включая биологическое вещество, такое как фермент. Еще более предпочтительно, второе электрофильное соединение предоставляет участок соединения для функционального вещества, расположенный на соответствующем расстоянии от субстрата, снижая, таким образом, стерические затруднения. В одном варианте осуществления плотность электрофильных групп на грамм субстрата составляет от 0,1 до 1 ммоль/г.
Это в свою очередь снижает препятствия во время иммобилизации функционального вещества и упрощает прикрепление функционального вещества к субстрату посредством второго эпоксидсодержащего соединения. Кроме того, это увеличивает доступность и структурную гибкость связанного вещества (фермент), тем самым повышая его активность. Описанный в настоящем изобретении способ также пригоден для получения субстратов, которые способны иммобилизовывать хиральные лиганды, аффинные лиганды и/или ионообменные частицы.
В одном варианте осуществления первое и второе электрофильные соединения являются эпоксидсодержащими соединениями. В одном варианте осуществления описанный в настоящем изобретении способ включает этап использования сшивающего агента для соединения второго эпоксидсодержащего соединения с первым эпоксидсодержащим соединением. Это увеличивает длину связи между активным оксирановым участком и субстратом, и помогает укрепить связь функциональной молекулы с оксирановым участком. Это также повышает доступность, а вследствие этого и активность связанного вещества, такого как фермент. Предпочтительно сшивающий агент может содержать дополнительные функциональные группы для придания субстрату необходимых химических свойств. Например, сшивающий агент может содержать аминогруппы, обладающие буферными свойствами, которые могут быть полезны, когда субстрат используется в таких устройствах, как устройства диализа. Сшивающий агент может также содержать группы, действующие как антиоксиданты или акцепторы металлов, дополняющие функции субстрата в определенных случаях применения. Более предпочтительно сшивающий агент может также предоставить большее количество участков для присоединения второго электрофильного соединения и/или последующих эпоксидсодержащих соединений. Фактически сшивающий агент может увеличить количество эпоксидсодержащих соединений, присоединенных к субстрату, что, в свою очередь, повышает вероятность и силу иммобилизации функционального вещества. Сшивающий агент может также быть нейтральным и инертным, что не сказывается отрицательным образом на функциональных или биологических свойствах соединенного с ним функционального или биологического вещества.
В одном варианте осуществления сшивающий агент не содержит эпоксидную группу. Функциональный сшивающий агент может также содержать нуклеофильную группу. Предпочтительно нуклеофильная группа реакционноспособна и может образовывать химические связи с электрофильными (эпоксидсодержащими) соединениями. В одном варианте осуществления функциональный сшивающий агент является динуклеофильным сшивающим агентом. Присутствие двух нуклеофильных групп позволяет сшивающему агенту создавать связи как с первым, так и со вторым эпоксидсодержащими соединениями, формируя мостик между двумя эпоксидсодержащими соединениями. В одном варианте осуществления, по крайней мере, один из нуклеофилов динуклеофильного сшивающего агента выбирается из группы, включающей NH, NR, NHO, NRO, O, S, Se, COO, CONH, CONR, CSS, COS, CONHO, CONRO, CONHNH, CONRNH, CONR1NR2, CNO, PH и PR,
где R, R1 и R2 независимо выбираются из группы, включающей водород, опционально замещенный алкил, опционально замещенный алкенил, опционально замещенный алкинил, опционально замещенный арил и опционально замещенный гетероарил.
Динуклеофильный сшивающий агент может также иметь общую формулу (I):
где X и Y независимо выбираются из группы, включающей NH, NR, NHO, NRO, O, S, Se, COO, CONH, CONR, CSS, COS, CONHO, CONRO, CONHNH, CONRNH, CONRNR, CNO, РН и PR;
R выбирается из группы, включающей водород, опционально замещенный алкил, опционально замещенный алкенил, опционально замещенный алкинил, опционально замещенный арил и опционально замещенный гетероарил;
n является целым числом от 0 до 25.
В другом варианте осуществления динуклеофильный сшивающий агент обладает общей формулой (II):
где X и Y независимо выбираются из NH, NR, NHO, NRO, О, S, Se, COO, CONH, CONR, CSS, COS, CONHO, CONRO, CONHNH, CONRNH, CONRNR, CNO, PH, PR;
где R, R1, R2, R3, R4 независимо выбираются из группы, включающей водород, опционально замещенный алкил, опционально замещенный алкенил, опционально замещенный алкинил, опционально замещенный арил и опционально замещенный гетероарил; и
m, n, p и q являются целыми числами, независимо выбираемыми от 0 до 25.
В одном варианте осуществления динуклеофильный сшивающий агент является алкилдиамином, таким как гександиамин или этилендиамин. Предпочтительно диаминовый сшивающий агент может предоставлять дополнительные участки для эпоксиактивации. Не вдаваясь в теорию, предполагается, что до пяти молекул эпоксидсодержащего соединения (такого как эпихлоргидрин) может прореагировать с одной молекулой диаминового сшивающего агента. Это предпочтительно, поскольку обеспечивает увеличение плотности, например, эпоксидсодержащего соединения и, вследствие этого, количества участков иммобилизации, доступных для иммобилизации вещества. Введение аминогрупп сшивающего агента также выполняет благотворную роль внутреннего буфера pH для иммобилизуемого вещества. Дальнейшим преимуществом является то, что аминогруппы также действуют как ионообменники, обеспечивая условия стабилизации для иммобилизуемого вещества. Дальнейшим преимуществом является то, что аминогруппы являются сильно нуклеофильными, что делает более эффективным образование связи первого и второго эпоксидсодержащих соединений по сравнению с другими нуклеофильными группами. Сильная нуклеофильная природа аминогрупп сшивающего агента является дальнейшим преимуществом, поскольку обеспечивает использование длинных сшивающих агентов при поддержании реакционной способности с эпоксидсодержащим соединением. Это является дальнейшим преимуществом, поскольку использование более длинных сшивающих агентов обеспечивает дальнейшее снижение стерических затруднений между субстратом и иммобилизованным веществом. Более предпочтительно гександиамин является относительно дешевым по сравнению с другими сшивающими агентами и коммерчески доступным материалом массового спроса. Низкая стоимость гександиамина обеспечивает массовое производство описанного в настоящем изобретении субстрата при относительно низких затратах. Дальнейшим преимуществом является то, что связь «алкил-амин», образующаяся при использовании гександиаминового сшивающего агента, устойчива к гидролизу при физиологических условиях, так что его можно использовать в водных системах, например, устройствах для диализа. Дальнейшее преимущество гександиаминового сшивающего агента заключается в том, что он является биологически совместимым и биологически разлагаемым.
В одном варианте осуществления, по крайней мере, одно электрофильное соединение и второе электрофильное соединения являются эпигалогенгидринами. Предпочтительно эпигалогенгидрин является эпихлоргидрином. Аналогично эпихлоргидрин относительно дешевый по сравнению с другими эпигалогенгидринами и легко доступен, в связи с тем, что он является коммерчески доступным материалом массового спроса. Опять же низкая стоимость эпигалогенгидрина обеспечивает массовое производство описанного в настоящем изобретении субстрата при относительно низких затратах. Для эпихлоргидрина также характерна очень быстрая и исчерпывающая реакция с образованием только нетоксичных продуктов (глицерин и аминоглицерины), вследствие чего он пригоден для использования при приготовлении субстрата, который будет в итоге применяться для медицинских целей. Кроме того, в связи с тем, что эпихлоргидрин частично смешивается с водой и полностью смешивается со спиртами, весь избыточный эпихлоргидрин можно относительно легко удалить путем промывания субстрата водой и/или спиртом. Кроме того, эпихлоргидрин и его продукты гидролиза являются летучими, вследствие чего они легко могут быть удалены испарением.
В одном варианте способ включает выбор слабо реакционноспособного субстрата. Субстрат описанного в настоящем изобретении способа может представлять собой, шарики, микроразмерные частицы, наноразмерные частицы, мембрану, сетку, каркасную структуру или любую твердофазную подложку, которую можно приготовить с использованием описанного в настоящем изобретении способа для иммобилизации на ней функционального вещества, включая биологическое вещество. В одном варианте осуществления субстрат выбирается из группы, включающей субстрат на основе сложного полиэфира, полиамидный субстрат, субстрат на основе эпоксидной смолы, полиакрилатный субстрат, гидрокси-функционализированный субстрат и субстрат на основе полисахарида. Субстрат на основе полисахарида может быть выбран из группы, включающей хлопковый пух, хлопковую целлюлозу, хлопчатобумажные ткани, целлюлозное волокно, целлюлозные шарики, целлюлозный порошок, микрокристаллическую целлюлозу, целлюлозные мембраны, вискозное волокно, целлофан, ацетатцеллюлозу, ацетатцеллюлозные мембраны, хитозан, хитин, производные декстрана и производные агарозы. Субстраты могут также быть биоразлагаемыми и, вследствие этого, экологически чистыми, что дает возможность их применения в экологически уязвимых областях, таких как сельскохозяйственные работы или переработка отходов. Субстрат также может быть биоразлагаемым, так что при имплантировании субстрата в тело человека или при взаимодействии с телом человека, например, при диализе он оказывает незначительное или не оказывает никакого неблагоприятного воздействия на здоровье.
Этапы химического соединения описанных в настоящем изобретении способов могут быть осуществлены в температурном диапазоне от -30°C до 100°C, предпочтительно от 0°C до 100°C. В одном варианте осуществления этап химического присоединения первого электрофильного соединения к субстрату выполняется при температуре от приблизительно 50°C до 60°C; этап химического присоединения сшивающего агента осуществляется при температуре от приблизительно 20°C до 40°C; этап химического присоединения второго электрофильного соединения к сшивающему агенту осуществляется при температуре от приблизительно 20°C до 40°C и этап химического присоединения функционального вещества к второму электрофильному соединению осуществляется при температуре от приблизительно 2°C до 6°C. Предпочтительно субстрат может быть произведен или приготовлен при мягких условиях, например, при комнатной температуре и нормальном атмосферном давлении. Это снова находит отражение в снижении затрат на производство и повышении удобства в обращении. Более предпочтительно заключительная реакция иммобилизации может быть осуществлена при очень мягких условиях, например, в водном буфере при 2-6°C и нормальном атмосферном давлении, не требуя дополнительных реагентов. Это исключает риск деактивации или денатурации биологически активного вещества в связи с экстремальными условиями или наличием сильных реагентов, что может представлять проблему в других способах иммобилизации. Еще более предпочтительно, поскольку способ может быть осуществлен при температурах окружающей среды, иммобилизация биоактивных веществ на субстрате также может осуществляться одновременно или последовательно по отношению к активации субстрата.
В одном варианте осуществления функциональные вещества являются биологически активными веществами, такими как ферменты, например, уреаза. Предпочтительно при уреазе, иммобилизованной на субстрате, субстрат, содержащий иммобилизованную уреазу, можно использовать для целей диализа, например, для регенерации перитонеального диализата или гемодилизата. Ферменты также могут являться одним из следующих: уриказа, креатининаза, липаза, эстераза, целлюлаза, амилаза, пектиназа, каталаза, ацилаза, пенициллинамидаза, протеиназа K.
В одном варианте осуществления описанный в настоящем изобретении способ далее включает этап химического присоединения одного или более дополнительных электрофильных соединений как к первому, так и ко второму электрофильным соединениям, где указанные дополнительные электрофильные соединения при присоединении к указанным как первому, так и второму электрофильным соединениям сконфигурированы для иммобилизации на них функционального вещества. Например, третье, четвертое, пятое, шестое электрофильное соединение и т.д. могут быть присоединены как к первому, так и ко второму электрофильным соединениям одновременно. Электрофильные группы, как описано в настоящем изобретении, могут содержать, по крайней мере, одну эпоксидную группу.
В другом варианте осуществления предлагается способ иммобилизации функциональной молекулы на субстрате, способ, включающий этапы приготовления субстрата, содержащего соединения, приготовленные по способу, описанному в настоящем изобретении, каждое из указанных соединений включает эфирсодержащую функциональную группу, химически соединенную с субстратом, и эпоксидсодержащую функциональную группу, соединенную с эфирной функциональной группой; и введение раствора, содержащего указанную функциональную молекулу к указанным соединениям, расположенным на указанном субстрате, при котором эпоксидсодержащая функциональная группа образует химическую связь с указанной функциональной молекулой для ее иммобилизации.
Предпочтительно эта химическая связь может быть негидролизуемой ковалентной связью, такой как аминосвязь. Соответственно функциональная молекула иммобилизуется на субстрате с достаточной устойчивостью и не может быть легко удалена с субстрата.
Способ второго аспекта может также может содержать этап нанесения на поверхность субстрата в основном гомогенной смеси стабилизирующих добавок для стабилизации указанной функциональной молекулы. В одном варианте осуществления этап нанесения в основном гомогенной смеси добавок включает испарение растворителя указанных добавок на субстрате. Стабилизирующие добавки могут быть выбраны из группы, включающей сахар, такой как глюкоза, органическую кислоту, такую как этилендиаминтетрауксусная кислота, аминокислоту, такую как цистеин, и сахарную кислоту, такую как аскорбиновая кислота, и тиолы, такие как меркаптоэтанол.
В другом варианте осуществления предлагается субстрат, содержащий соединения, расположенные на нем, для иммобилизации функциональной молекулы, каждое соединение включает эфирсодержащую функциональную группу, химически соединенную с субстратом, и эпоксидсодержащую функциональную группу, соединенную с эфирной функциональной группой посредством сшивающего агента, включающего, по крайней мере, одну нуклеофильную группу, причем указанная эпоксидсодержащая функциональная группа смещена по отношению к указанной эфирсодержащей функциональной группе для иммобилизации функциональной молекулы к указанной эпоксидсодержащей функциональной группе без существенных стерических затруднений, вызванных указанной эфирсодержащей функциональной группой или субстратом. Предпочтительно субстрат обладает повышенной устойчивостью и может быть произведен с относительно низкими затратами по сравнению с известными субстратами, которые могут эффективно иммобилизовать функциональные вещества. Более предпочтительно субстрат может быть использован повторно без существенной потери его ферментных свойств в связи с высокой устойчивостью связи между биомолекулой и эпоксидсодержащей функциональной группой. Кроме того, в связи с отсутствием выщелачивания потенциально опасных веществ субстрат доступен для применения в медицинских целях, таких как перитонеальный диализ.
В одном варианте осуществления сшивающий агент является не водородом - гидразин, гидроксиламин, аммиак, вода или сероводород.
В одном варианте осуществления сшивающий агент является насыщенной или ненасыщенной алифатической цепочкой, содержащей от 2 до 18 атомов углерода, от 2 до 16 атомов углерода, от 2 до 14 атомов углерода, от 2 до 12 атомов углерода, от 2 до 10 атомов углерода, от 2 до 8 атомов углерода, от 2 до 6 атомов углерода и от 2 до 4 атомов углерода. В одном варианте осуществления сшивающий агент является насыщенной алифатической цепочкой, содержащей от 4 до 8 атомов углерода, более предпочтительно 6 атомов углерода. Нуклеофильная группа указанного сшивающего агента может быть расположена на одном из терминальных концов алифатической цепочки или между терминальными концами алифатической цепочки. В одном варианте осуществления нуклеофильная группа указанного сшивающего агента может быть химически соединена с алифатической цепочкой с помощью протянутого от нее разветвления цепи. В одном варианте осуществления на указанном сшивающем агенте расположены две нуклеофильные группы, предпочтительно на терминальных концах алифатической цепочки. В одном варианте осуществления, по крайней мере, одна нуклеофильная группа расположена на терминальном конце алифатической цепочки и соединена с эфир- или эпоксидсодержащей функциональной группой дополнительной алифатической цепочкой сшивающего агента. Дополнительная алифатическая цепочка сшивающего агента может содержать от 1 до 3 атомов углерода.
Субстрат может также содержать покрытие, расположенное на указанном субстрате, покрытие, включающее в основном гомогенную смесь стабилизирующих добавок. Стабилизирующие добавки могут быть выбраны из группы, включающей сахар, такой как глюкоза, органическую кислоту, такую как этилендиами