Способ определения концентрации свинца в легких крупного рогатого скота
Иллюстрации
Показать всеИзобретение относится к области аналитической химии и касается способа определения концентрации свинца в легких крупного рогатого скота черно-пестрой породы. Сущность способа заключается в определении в волосе концентрации Mn и/или Na методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой. Затем рассчитывают уравнение регрессии, при этом по содержанию марганца или натрия определяют концентрацию свинца в легких по формуле y=0,0179х-0,0067, где х - содержание Mn (мг/кг) в волосе, где y - содержание Pb (мг/кг) в легких или по формуле y=0,0000334х+0,007551, где х - содержание Na (мг/кг) в волосе, y - содержание Pb (мг/кг) в легких. Использование способа позволяет с высокой точностью определить содержание свинца в легких крупного рогатого скота черно-пестрой породы. 3 табл.
Реферат
Предлагаемое изобретение относится к животноводству, экологии, ветеринарии и предназначено для использования в качестве прижизненного неинвазивного теста уровня аккумуляции свинца в легких крупного рогатого скота.
Свинец находится в организме животных в мобильной и фиксированной формах. В мобильной форме он способен к диффузии, а в фиксированной - нет. Более 90% свинца в крови содержится в связанном с эритроцитами виде (Castellino N., Aloj S., 1964). Большая часть свинца находится в эритроцитах, в строме - меньшая. В организме свинец транспортируется схожим с кадмием способом. Он образует комплексы с металлотионеином, транспортером дивалентных ионов металлов и с транспортером цинка, благодаря чему мигрирует в места своей аккумуляции (Espinoza A. et al., 2012).
Наибольшая аккумуляция свинца в норме происходит в почках, печени и костной ткани (Kehoe R.A., 1964). В экспериментах, проведенных на лабораторных животных, установлено, что через час после внутривенного введения свинца, его содержание в почках составляет 8,3%, в бедренной кости - 3,2%, в печени - 2,2%, в сыворотки крови - 1,5%. Через 24 часа концентрация этого металла была следующей: 6,3%, 3,2%, 0,7%, 0,4% соответственно (Москалев Ю.И., 1985, с. 156).
В элементологии сельскохозяйственных животных большое внимание уделяется поиску малоинвазивных и неинвазивных маркеров аккумуляции тяжелых металлов в различных органах (Патент РФ №2342659, Патент РФ №2426119, Патент РФ №2421726).
Свинец оказывает сильное токсическое воздействие на организм животных и человека. Это проявляется в высоком нейротоксичном, нефротоксичном, гематотоксичном, гепатотоксичном, мутагенном и канцерогенном действии, а также он отрицательно влияет на опорно-двигательную, репродуктивную, сердечно-сосудистую и пищеварительную системы (Патент №2285920).
Существуют способы определения свинца в пищевом сырье (Продукты пищевые. Методика определения токсических элементов атомно-эмиссионным методом. - М.: Госстандарт России, 1997. - С. 10-21). Однако этим методом определяют содержание свинца после забоя животных. Известен способ определения свинца в печени свиней (Патент РФ №2285920). Данный метод разработан для определения свинца в печени свиней, а для других видов животных не пригоден.
От рассмотренных выше методов предлагаемый нами способ отличается тем, что проводят определение химического состава волоса крупного рогатого скота методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой. Устанавливают концентрацию Mn и Na в волосе для определения свинца в легких и рассчитывают уравнение регрессии:
y=0,0179х-0,0067, где х - содержание Mn (мг/кг) в волосе,
y - содержание Pb (мг/кг) в легких,
y=0,0000334х+0,007551, где х - содержание Na (мг/кг) в волосе,
y - содержание Pb (мг/кг) в легких.
Заявленным способом решается задача оценки накопления свинца в легких крупного рогатого скота черно-пестрой породы. Поставленная задача достигается с помощью определения концентрации Mn и Na в волосе с последующим расчетом уровня свинца в легких с использованием уравнения регрессии.
Пример выполнения
Содержание элементов в пробах определяли методом атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой (ИСП-АЭС) в лаборатории аналитической геохимии Объединенного института геологии, геофизики и минералогии СО РАН. Исследования проб легких и волоса выполняли на спектрометре серии IRIS Advantage производства Thermo Jarrell Ash.
Пробоподготовка для атомно-эмиссионного анализа происходила в следующей последовательности: посуду после мойки в мыльном растворе промывали водопроводной водой и ополаскивали бидистиллированной водой, потом сушили. Пробы (весом 1 г) измельчались до однородной массы, затем высушивались в печи при температуре 100°C около 12 часов до постоянной массы. Затем полученный сухой остаток озоляли в муфельной печи при температуре 480-500°C. Через 10-15 часов минерализация заканчивалась, зола приобретала серый или белый цвет. После этого пробы остывали при комнатной температуре. В кварцевые чашки с пробами вносили 5 мл азотной кислоты, сверху накрывали фторопластовой крышечкой и оставляли на 12 часов. Затем пробы нагревали на электроплитке до получения сухого осадка. Далее добавляли 1 мл хлорной и 5 мл азотной кислоты, сверху накрывали фторопластовой крышечкой. Содержимое чашек упаривали на электроплитке. Когда раствор становится прозрачным, в каждую чашку вносили 5 мл соляной кислоты 1:1. Это повторяли до влажного осадка солей желтоватого цвета. Затем добавляли 5 мл 5%-ной соляной кислоты и нагревали на электроплитке до растворения осадка. Полученные пробы оставляли остывать при комнатной температуре. Затем добавляли 2 мл скандия. Конечная концентрация скандия в растворе была 2 мкг/мл. Полученный раствор разбавляли бидистиллированной водой до 10 мл. Готовый раствор исследовался на элементный состав.
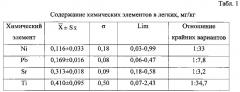
В легких черно-пестрого скота наибольшая концентрация микроэлементов наблюдалось у титана, а у никеля - наименьшая (таблица 1). По уровню концентрации химических элементов в легких можно расположить в виде возрастающего ряда: Ni<Pb<Sr<Ti, в соотношении 1:1,5:2,7:3,5. В то же время фенотипическая изменчивость более всего выражена для Ni, а менее всего - для Sr. Выявлены значительные различия между отдельными животными по способности к аккумуляции никеля и титана, что отражает широкое отношение крайних вариант этих элементов.
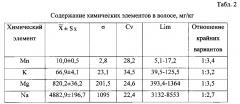
В таблице 2 приведены данные о содержании химических элементов в волосе. По уровню аккумуляции микроэлементы можно представить в виде убывающего ранжированного ряда: Na>Mg>K. Следовательно, в волосе в набольшей степени накапливается натрий, а в наименьшей - марганец. Более высокая фенотипическая изменчивость характерна для Mg, а относительно низкая - для Na.
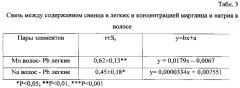
В таблице 3 показано, что между изученными показателями имеются достаточно высокие положительные корреляции. С целью прогнозирования уровня свинца в легких были рассчитаны уравнения регрессии. По уровню марганца и/или натрия в волосе можно вычислить концентрацию свинца в легких.
Таким образом, предложенные уравнения регрессии позволяют провести прижизненную неинвазивную оценку интерьера животных по содержанию свинца в легких, используя при этом только пробы волоса.
Литература
1. Москалев Ю.И. Минеральный обмен. - М.: Медицина, 1985. - С. 156.
2. Castellino N. Kinetics of the distribution and excretion of lead in the rat. / N. Castellino, S. Aloj // Brit. J. ind. Med., 1964. - Vol. 21. - P. 308-314.
3. Espinoza A. Iron, copper, and zinc transport: inhibition of divalent metal transporter 1 (DMT1) and human copper transporter 1 (hCTR1) by shRNA / A. Espinoza, S. Le Blanc, M. Olivares et al. // Biol. Trace Elem. Res., 2012. - Vol. 146 (2). - P. 281-286.
4. Kehoe R.A. Normal metabolism of lead / R.A. Kehoe // Arch. Environ. Health, 1964. - Vol. 8. - P. 44.
Способ определения концентрации свинца в легких крупного рогатого скота, включающий анализ биосубстрата, отличающийся тем, что проводят микроэлементный анализ волоса крупного рогатого скота черно-пестрой породы, определяют в волосе концентрацию марганца и/или натрия и рассчитывают уравнение регрессии:y=0,0179х-0,0067, где х - содержание Μn (мг/кг) в волосе,y - содержание Pb (мг/кг) в легких,у=0,0000334х+0,007551, где x - содержание Na (мг/кг) в волосе,y - содержание Pb (мг/кг) в легких.