Способ получения катализатора реакций гидрогенизации
Иллюстрации
Показать всеИзобретение относится к способам получения и применения нанесенного катализатора на основе никеля в реакциях восстановления основных классов промышленно важных органических соединений: при получении капролактама, анилина, спиртов и жиров. В способе получения катализатора реакций гидрогенизации, заключающемся в пропитке носителя раствором никеля, его сушке, последующем прокаливании и восстановлении, согласно изобретению носитель используют в виде дисперсного порошка, пропитывают его 0,3-2,3 М водным раствором нитрата никеля в соотношении 5-10 г носителя на 100 г раствора нитрата никеля однократно, фильтруют, сушат при 80-100°С, восстанавливают (активируют) при 350-450°С в токе водорода 20-40 см3/мин, пассивируют путем внесения его в атмосфере водорода в жирные одноатомные спирты С16-18 при 80-100°С, размешивают и охлаждают готовый катализатор до комнатной температуры. Технический результат - повышение каталитических свойств, упрощение и удешевление процесса получения, значительное увеличение сроков хранения, улучшение транспортировки. 2 ил., 3 табл., 3 пр.
Реферат
Изобретение относится к способам получения и применения нанесенного катализатора на основе никеля в реакциях восстановления основных классов промышленно важных органических соединений: при получении капролактама, анилина, спиртов и жиров.
Известен способ получения никелевого катализатора гидрирования, содержащий 50% NiO (39,3% Ni), заключающийся в смешении основного карбоната никеля с алюмооксидным носителем (смесь α-Al2O3 и γ-Al2O3 при соотношении 0,05:0,95) в присутствии пептизатора - водного раствора аммиака, с последующей сушкой при 100-120°С и прокалкой при 300-500°С, измельчении, смешении с графитом и таблетировании [Патент №2102145 РФ, МПК B01J 37/04. Способ получения никелевого катализатора гидрирования / Кипнис М.А., Газимзянов Н.Р., Алешин А.И., Агоронов B.C.; заявитель и патентообладатель ЗАО НПФ «Химтэк». - №96117610/04; заяв. 05.09.1996; опубл. 20.01.1998].
Наиболее близким к настоящему патенту по сущности и техническому результату является способ получения селективного катализатора гидрирования для селективного гидрирования ацетиленовых примесей в неочищенных олефиновых или диолефиновых потоках, содержащий только никель или никель и один или больше элементов, выбранных из группы, состоящего из Cu, Re, Pd, Zn, Mg, Mo, Ca и Bi, нанесенных на носитель, представляющий оксид алюминия, имеющий следующие физические свойства: площадь поверхности по БЭТ от 30 до примерно 100 м2/г, общий объем пор по азоту от 0,4 до примерно 0,9 см3/г и средний диаметр пор от примерно 110 до , где указанный катализатор содержит от примерно 4 до примерно 20 вес. % никеля. Способ получения катализатора включает пропитку носителя, представляющего оксид алюминия, имеющего указанные выше физические свойства, растворимыми солями только никеля или никеля и одного или больше элементов, выбранных из группы, состоящей из Cu, Re, Pd, Zn, Mg, Mo, Ca и Bi, из одного или больше растворов с получением пропитанного носителя, где указанный катализатор содержит от примерно 4 до примерно 20 вес. % никеля. А способ селективного гидрирования ацетиленовых соединений включает контактирование исходного сырья, содержащего ацетиленовые соединения и другие ненасыщенные соединения, с описанным выше катализатором. [Патент №2333796 РФ, МПК B01J 23/80, 23/78, 23/873, 23/88, 23/89, 23/755, 21/04, 37/02; С07С 5/08, 5/09. Никелевые катализаторы гидрирования, способ получения и применение / Риу Дж. Юн, Путмэн Хью М.; заявитель и патентообладатель Каталитик Дистиллейшн Технолоджиз (US). - №2006106735(04; заяв. 26/05/2004; опубл. 20.09.2008, Бюл. №26].
Известные способы синтеза каталитических систем на основе переходных металлов обладают общим рядом недостатков: имеют относительно высокую стоимость, трудоемки, в ходе синтеза образуется большое количество побочных веществ (отходы), кроме того, полученные катализаторы гидрогенизации не подлежат длительному хранению или требуют активирования перед использованием, также следует отметить, что все катализаторы, не содержащие в своем составе железо или никель, трудоемки в сепарировании из объема готового продукта.
Задачей настоящего изобретения является получение относительно дешевого катализатора на основе никеля с устраненными вышеперечисленными недостатками.
Технический результат - повышение каталитических свойств, упрощение способа получения, значительное увеличение сроков хранения, улучшение транспортировки, удешевление процесса получения.
Указанный результат достигается тем, что в способе получения катализатора реакций гидрогенизации, заключающемся в пропитке носителя раствором никеля, его сушке, последующем прокаливании и восстановлении, согласно изобретению носитель используют в виде дисперсного порошка, пропитывают его 0,3-2,3 М водным раствором нитрата никеля в соотношении 5-10 г носителя на 100 г р-ра нитрата никеля однократно, фильтруют, сушат при 80-100°С, восстанавливают (активируют) при 350-450°С в токе водорода 20-40 см3/мин, пассивируют путем внесения его в атмосфере водорода в жирные одноатомные спирты С16-18 при 80-100°С, размешивают и охлаждают готовый катализатор до комнатной температуры.
Технический результат достигается за счет уменьшения числа стадий приготовления, что упрощает и удешевляет процесс, использования адсорбционных свойств носителя (т.е. при пропитке наносится не больше ионов никеля, чем способен адсорбировать носитель из раствора соли никеля), более точного установления режима восстановления, применения легкоудаляемого пассивирующего агента (жирные спирты).
Выбор жирных спиртов в качестве пассивирующего агента обусловлен следующими моментами.
1. Жирные спирты С16-18 безвредны для человека.
2. Инертны к активной поверхности катализатора.
3. Относительно легко, по сравнению с маслами, полимерами и парафинами, поддаются выделению из массы гидрогенизата и могут быть возвращены в производство.
4. Обладают большим сродством к катализатору, позволяя получать стойкую эмульсию катализатора, одновременно полностью блокируя доступ окислителя к металлическому никелю.
5. Относительно доступны.
Изобретение поясняется чертежами, где на фиг. 1 показаны кинетические зависимости реакций гидрирования малеата натрия на катализаторах, полученных в трех приведенных примерах при атмосферном давлении и температуре 30°C; на фиг. 2 - кинетические зависимости реакций гидрирования малеата натрия на катализаторах, полученных в трех приведенных примерах при избыточном давлении 0,8 МПа и температуре 30°C.
Способ осуществляют следующим образом
Пример 1. Катализатор состава Ni/Al2O3 с w(Ni)=7% получают следующим образом. Готовят водный раствор Ni(NO3)2 с концентрацией 2,3 М. Отмеряют 15 мл раствора на 1 грамм Al2O3 (Алюминий оксид ТУ 6-09-3428-73). Далее проводят насыщение катализатора. Насыщение идет путем выдерживания носителя в растворе соли в течение 4 часов при температуре 30°C и перемешивании с частотой 1 Гц.
Отделяют пропитанный нитратом никеля носитель от раствора следующим образом. Используют фильтр Шотта с величиной пор менее чем средний размер частиц носителя. Также возможно отстаивание с последующей декантацией. Далее проводят сушку. Подложку (носитель) с нанесенным на нее Ni(NO3)2 сушат при t=100°C до получения нанесенных кристаллогидратов. Затем осуществляют температурное разложение кристаллогидратов, т.е. прокаливание, которое производят следующим способом. Полупродукт помещают в печь и выдерживают в атмосфере азота при t=350°C до прекращения выделения NO2 (2 ч±30 мин). Активацию (восстановление) катализатора проводят следующим образом. Помещают в трубчатую печь носитель (подложку) с нанесенным никелем и восстанавливают в токе водорода 20 см3/мин при t=350°C до прекращения выделения H2O (1 ч±30 мин). На этой стадии полученный катализатор Ni/Al2O3 уже обладает значительной активностью, однако для долговременного хранения используют его пассивацию. Активированный катализатор вносят в атмосфере водорода в жирные одноатомные спирты C16-18 при температуре 80°С в соотношении спирт: катализатор - 3:1 по массе. Полученную массу размешивают и затем охлаждают до комнатной температуры.
Пример 2. Катализатор состава Ni/SiO2 с w(Ni)=9% получают следующим образом. Готовят водный раствор Ni(NO3)2 с концентрацией 2,3 М. Отмеряют 15 мл раствора на 1 грамм SiO2 (Л 5/40 м). Далее проводят насыщение катализатора. Насыщение идет путем выдерживания носителя в растворе соли в течение 4 часов при температуре 30°C и перемешивании с частотой 1 Гц.
Отделяют пропитанный нитратом никеля носитель от раствора следующим образом. Используют фильтр Шотта с величиной пор менее чем средний размер частиц носителя. Также возможно отстаивание с последующей декантацией. Далее проводят сушку. Подложку (носитель) с нанесенным на нее Ni(NO3)2 сушат при t=80°C до получения нанесенных кристаллогидратов. Затем осуществляют температурное разложение кристаллогидратов, т.е. прокаливание, которое производят следующим способом. Полупродукт помещают в печь и выдерживают в атмосфере азота при t=350°C до прекращения выделения NO2 (2 ч±30 мин). Активацию (восстановление) катализатора проводят следующим образом. Помещают в трубчатую печь носитель (подложку) с нанесенным никелем и восстанавливают в токе водорода 40 см3/мин при t=350°C до прекращения выделения H2O (1 ч±30 мин). На этой стадии полученный катализатор Ni/Al2O3 уже обладает значительной активностью, однако для долговременного хранения используют его пассивацию. Активированный катализатор вносят в атмосфере водорода в жирные одноатомные спирты C16-18 при температуре 80°C, в соотношении спирт: катализатор - 3:1 по массе. Полученную массу размешивают и затем охлаждают до комнатной температуры.
Пример 3. Катализатор состава Ni/SiO2 с w(Ni)=9% получают следующим образом. Готовят водный раствор Ni(NO3)2 с концентрацией 2,3 М. Отмеряют 15 мл раствора на 1 грамм SiO2 (Л 5/40 м). Далее проводят насыщение катализатора. Насыщение идет путем выдерживания носителя в растворе соли в течение 4 часов при температуре 30°C и перемешивании с частотой 1 Гц.
Отделяют пропитанный нитратом никеля носитель от раствора следующим образом. Используют фильтр Шотта с величиной пор менее чем средний размер частиц носителя. Так же возможно отстаивание с последующей декантацией. Далее проводят сушку. Подложку (носитель) с нанесенным на нее Ni(NO3)2 сушат при t=80°C до получения нанесенных кристаллогидратов. Затем осуществляют температурное разложение кристаллогидратов, т.е. прокаливание, которое производят следующим способом. Полупродукт помещают в печь и выдерживают в атмосфере азота при t=350°C до прекращения выделения NO2 (2 ч±30 мин). Активацию (восстановление) катализатора проводят следующим образом. Помещают в трубчатую печь носитель (подложку) с нанесенным никелем и восстанавливают в токе водорода 40 см3/мин при t=450°C до прекращения выделения H2O (2 ч±30 мин). На этой стадии полученный катализатор Ni/SiO2 уже обладает значительной активностью, однако для долговременного хранения используют его пассивацию. Активированный катализатор вносят в атмосфере водорода в жирные одноатомные спирты C16-18 при температуре 100°C в соотношении спирт: катализатор - 3:1 по массе. Полученную массу размешивают и затем охлаждают до комнатной температуры.
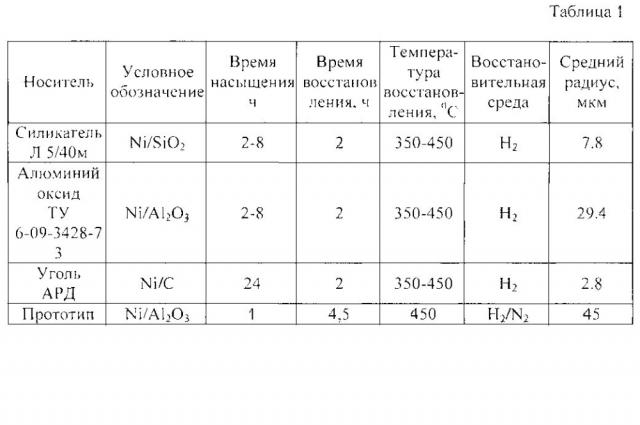
В таблице 1 сведены условия приготовления никелевых катализаторов на различных носителях.
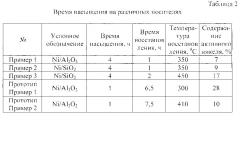
В таблице 2 сведены условия приготовления катализаторов в примерах 1-3.
Полученный по способу в примере 3 катализатор обладает каталитической активностью, отнесенной к массе активного металла, превышающей в 4 раза скелетные металлические катализаторы на основе переходных металлов и в 2-3 раза нанесенные палладиевые катализаторы, используемые в промышленности. Кинетические зависимости гидрирования малеата натрия в воде для катализаторов, приготовленных в примерах, приведены на фиг. 1 для давления 0,1 МПа и на фиг. 2 для давления 0,9 МПа. Параметры каталитической активности никелевых катализаторов в реакции восстановления малеата натрия в воде при 30°C приведены в таблице 3.
где:
rн o - наблюдаемая скорость реакции модельного соединения (малеата натрия) в начальный момент времени (степень превращения 0÷0,05) (моль·с-1·кг-1);
kн o - наблюдаемая константа скорости реакции (с-1).
При этом ,
где dn(H2) - количество моль водорода, пошедшего на реакцию;
dτ-1 - время за которое поглотилось dn(H2);
mNi -1 - масса никеля, участвовавшая в катализе выбранной реакции (гидрирование малеата натрия).
где ρ - кажущаяся плотность катализатора (г/см3);
α - коэффициент Бунзена для водорода при 303 К в моль Н2/см3 жидкой фазы;
PH2 - давление водорода в системе (мм рт.ст.).
В качестве каталитической активности принимали скорость реакции гидрогенизации малеата натрия и диэтилового эфира малеиновой кислоты в воде при температуре 30°C и атмосферном давлении водорода, отнесенной к 1 грамму активного металла. Данные соединения были выбраны в качестве модельных, так как реакция их гидрогенизации идет в одну стадию без образования промежуточных продуктов и кинетика данных процессов хорошо изучена.
Концентрация металлического никеля в полученном катализаторе составляет от 7 до 17% в зависимости от природы подложки. Более низкие концентрации металла приводят к резкому сокращению срока службы катализатора, более высокие экономически не целесообразны.
Предлагаемый катализатор обладает улучшенными характеристиками, такими как активность, селективность и стабильность, а также удобен при хранении и транспортировке.
Способ получения катализатора реакций гидрогенизации, заключающийся в пропитке носителя раствором никеля, его сушке, последующем прокаливании и восстановлении, отличающийся тем, что носитель используют в виде дисперсного порошка, пропитывают его 0,3-2,3 М водным раствором нитрата никеля в соотношении 5-10 г носителя на 100 г раствора нитрата никеля однократно, фильтруют, сушат при 80-100°C, восстанавливают (активируют) при 350-450°C в токе водорода 20-40 см3/мин, пассивируют путем внесения его в атмосфере водорода в жирные одноатомные спирты C16-18 при 80-100°C, размешивают и охлаждают готовый катализатор до комнатной температуры.