Антитела против cd70
Иллюстрации
Показать всеДанное изобретение относится к области иммунологии. Предложены антитело и его антигенсвязывающий фрагмент, которые связываются с CD70 человека, охарактеризованные аминокислотными последовательностями CDR вариабельных доменов тяжелой и легкой цепи. Рассмотрен выделенный полинуклеотид, который кодируют антитело или антигенсвязывающий фрагмент по изобретению, а также вектор экспрессии, клетка-хозяин, бесклеточная экспрессионная система и способ продукции антитела или его антигенсвязывающего фрагмента по изобретению. Также представлена фармацевтическая композиция, способ ингибирования роста опухолевых клеток и способ истощения CD70-экспрессирующих клеток у пациента. Данное изобретение может найти дальнейшее применение в терапии и диагностике заболеваний, в частности рака и аутоиммунных заболеваний, характеризующихся экспрессией CD70. 9 н. и 18 з.п. ф-лы, 24 ил., 29 табл., 21 пр.
Реферат
Область техники
Настоящее изобретение относится к антителам и их антигенсвязывающим фрагментам, которые связываются с белком CD70 человека с высокой аффинностью и демонстрируют сильное ингибирование роста опухолевых клеток.
Предпосылки создания изобретения
Рецептор цитокинов CD27 является членом суперсемейства рецепторов факторов некроза опухолей (TFNR), которые играют роль в росте и дифференциации клеток, а также апоптозе. Лигандом CD27 является CD70, который относится к семейству факторов некроза опухолей - лигандов. CD70 представляет собой полипептид из 193 аминокислот, содержащий гидрофильный N-концевой домен из 20 аминокислот и C-концевой домен, содержащий 2 потенциальных сайта N-гликозилирования (присоединения сахара к атому N) (Goodwin, R.G. et al. (1993) Cell 73: 447-456; Bowman et al. (1994) Immunol 152: 1756-1761). На основе этих особенностей было установлено, что CD70 является трансмембранным белком типа II, содержащим экстраклеточную C-концевую часть.
CD70 кратковременно обнаруживается на активированных T- и B-лимфоцитах и дендритных клетках (Hintzen et al. (1994) J. Immunol. 152: 1762-1773; Oshima et al. (1998) Int. Immunol. 10: 517-26; Tesselaar et al. (2003) J. Immunol. 170: 33-40). Помимо экспрессии в нормальных клетках экспрессия CD70 была описана в различных типах раков, включая почечно-клеточные карциномы, метастатические раки молочной железы, опухоли головного мозга, лейкозы, лимфомы и карциномы носоглотки (Junker et al. (2005) J. Urol. 173: 2150-2153; Sloan et al. (2004) Am J Pathol. 164: 315-323; Held-Feindt and Mentlein (2002) Int J Cancer 98: 352-356; Hishima et al. (2000) Am J Surg Pathol. 24: 742-746; Lens et al. (1999) Br J Haematol. 106: 491-503). Также взаимодействие CD70 с CD27, как было предположено, играет роль в клеточноопосредованном аутоиммунном заболевании и ингибировании продукции TNF-альфа (Nakajima et al. (2000) J. Neuroimmunol. 109: 188-196).
Соответственно, CD70 представляет собой мишень в случае лечения рака, аутоиммунных нарушений и ряда других заболеваний, характеризующихся экспрессией CD70.
В WO 2006/0044643 описываются антитела против CD70, содержащие эффекторный домен антитела, который может опосредовать одну или более из ADCC, ADCP, CDC или ADC и или проявлять цитостатический или цитотоксический эффект по отношению к CD70-экспрессирующему раку, или проявлять имммуносупрессорный эффект по отношению к иммунологическому нарушению, характеризующемуся экспрессией CD70, в отсутствие конъюгации с цитостатическим или цитотоксическим агентом. Приводимые здесь в качестве примера антитела основаны на антигенсвязывающих областях двух моноклональных антител, обозначенных 1F6 и 2F2.
В WO 2007/038637 описываются полностью человеческие моноклональные антитела, которые связываются с CD70. Эти антитела характеризуются связыванием с CD70 человека с KD, составляющей 1×10-7 M или менее. Антитела также связываются с линиями опухолевых клеток почечноклеточной карциномы, которые экспрессируют CD70, такими как 786-О, и подвергаются интернализации в них.
Краткое изложение сущности изобретения
Здесь обеспечиваются антитела, или их антигенсвязывающие фрагменты, (называемые здесь антителами против CD70), которые связываются с белком CD70 человека и демонстрируют характеристики, отличные и, как правило, лучшие, (от) таковых антител против CD70, описанных в известном уровне техники. Лучшие характеристики этих антител являются преимущественными, что касается применения для лечения людей, особенно лечения CD70-экспресссирующих раков, а также иммунологических нарушений.
Описываемые здесь антитела против CD70 характеризуются очень высокой аффинностью к CD70 человека. Все предпочтительные варианты осуществления, описываемые здесь, демонстрируют аффинность к рекомбинантному CD70 человека (измеряемую с помощью поверхностного плазмонного резонанса с использованием BiacoreTM, описываемого здесь), которая значительно выше таковой самых сильных антител против CD70 известного уровня техники, предложенных для лечения людей, в том числе антител против CD70 «полностью человеческого происхождения» известного уровня техники. Кроме того, все предпочтительные варианты антител против CD70, описываемые здесь, демонстрируют лучшее связывание (т.е. с большей аффинностью) с CD70, представленным на поверхности линий клеток человека, особенно линий раковых клеток человека, по сравнению с антителами против CD70 известного уровня техники, предложенными для лечения людей. Это лучшее связывание с CD70 на клеточной поверхности особенно заметно относительно линий раковых клеток человека, которые экспрессируют CD70 в «низкой копийности», и имеет прямое отношение к применению антител для лечения людей. Более того, предпочтительные варианты антител против CD70, описываемые здесь, демонстрируют в значительной степени увеличенное связывание с раковыми клетками, изолированными от являющихся людьми пациентов, в частности, раковыми клетками, изолированными от пациентов с хроническим лимфолейкозом (CLL), по сравнению с антителами против CD70 известного уровня техники, предложенными для лечения людей.
Следовательно, в первом аспекте настоящего изобретения обеспечивается связывающееся с CD70 человека антитело или его антигенсвязывающий фрагмент, включающее(ий) по крайней мере один вариабельный домен тяжелой цепи (VH) и по крайней мере один вариабельный домен легкой цепи (VL), причем указанные VH- и VL-домены, при исследовании в виде Fab-фрагмента, демонстрируют скорость диссоциации (koff, измеряемую с использованием BiacoreTM) от CD70 человека, составляющую менее 7×10-4 сек-1, используя стандартный протокол BiacoreTM, описываемый здесь.
В предпочтительном варианте осуществления антитело или антигенсвязывающий фрагмент включает по крайней мере один вариабельный домен тяжелой цепи (VH) и по крайней мере один вариабельный домен легкой цепи (VL), причем указанные VH- и VL-домены демонстрируют скорость диссоциации от CD70 человека, составляющую 5×10-4 сек-1 или менее, или 2×10-4 сек-1 или менее, или 1×10-4 сек-1 или менее. Наиболее предпочтительно, когда антитело против CD70, при исследовании в виде Fab-фрагмента, будет демонстрировать скорость диссоциации от CD70 в диапазоне от 0,4×10-4 сек-1 до 4,8×10-4 сек-1.
Также обеспечивается связывающееся с CD70 человека антитело, включающее две Fab-области, причем каждая из Fab-областей связывается с CD70 человека и демонстрирует, при исследовании в виде Fab-фрагмента, скорость диссоциации от CD70 человека, составляющую 5×10-4 сек-1 или менее, или 2×10-4 сек-1 или менее, или 1×10-4 сек-1 или менее, а предпочтительно находящуюся в диапазоне от 0,4×10-4 сек-1 до 4,8×10-4 сек-1. Две Fab-области могут быть идентичными, или они могут отличаться по характеристикам связывания, например, аффинности к CD70 человека. Две Fab-области могут связываться с одним и тем же эпитопом или перекрывающимися эпитопами CD70 человека, или они могут связываться с отличными, не перекрывающимися эпитопами CD70 человека. Две Fab-области могут отличаться друг от друга по аминокислотной последовательности в одном или обоих VH- и VL-доменах.
Предпочтительные варианты антител против CD70, обеспечиваемых здесь, могут, помимо очень высокой аффинности к CD70, демонстрировать сильное блокирование или ингибирование взаимодействия между CD70 или его лигандом CD27. Предпочтительные антитела против CD70, которые демонстрируют как связывание с высокой аффинностью с CD70, так и сильное блокирование взаимодействия CD70/CD27, являются особенно преимущественными в качестве терапевтических средств для лечения показаний-заболеваний, в случае которых блокирование передачи сигнала от CD70/CD27 увеличивает терапевтическую эффективность (например, помимо уничтожения клеток, опосредуемого эффекторными функциями антитела против CD70), например, аутоиммунных заболеваний и раков, которые коэкспрессируют CD70 и CD27.
Не все из антител против CD70, описываемых здесь, демонстрируют сильное блокирование взаимодействия CD70/CD27 помимо связывания с высокой аффинностью с CD70. Здесь также описывается ряд антител против CD70, которые демонстрируют связывание с очень высокой аффинностью с CD70, но не демонстрируют значительное блокирование взаимодействия CD70/CD27. Характеристики этих антител описываются здесь в другом месте. Наличие не блокирующих антител против CD70 с высокой аффинностью может расширить диапазон возможностей терапевтического применения.
Предпочтительные варианты антител против CD70, описываемых здесь, демонстрирующие очень высокую аффинность к CD70 человека, также характеризуются сочетанием характеристик связывания, которое не демонстрируют антитела против CD70 известного уровня техники, предложенные для терапевтического применения для людей. Соответственно, предпочтительные антитела против CD70, описываемые здесь, характеризуются:
(a) связыванием в пределах аминокислотной последовательности HIQVTLAICSS (SEQ ID NO: 342) в CD70 человека;
(b) перекрестной реактивностью с гомологами CD70 у макака-резус (Macaca mulatta) и яванского макака (Macaca cynomolgus);
(c) связыванием как со встречающимся в природе CD70 человека, так и с подвергнутым тепловой денатурации рекомбинантным CD70 человека.
Это сочетание характеристик связывания, которое не демонстрируют антитела известного уровня техники, предложенные для терапевтического применения для людей, указывает на связывание с новым эпитопом CD70, который отличен от эпитопов, с которыми связываются антитела против CD70 известного уровня техники.
Сочетание характеристик связывания, которое демонстрируют предпочтительные антитела против CD70, является преимущественным в рамках разработки лекарственных средств для людей. В частности, перекрестная реактивность с гомологами CD70 у обезьян дает возможность проводить токсикологические исследования антител против CD70, предложенных для терапевтического применения для людей, в моделях на приматах.
Предпочтительные антитела против CD70, описываемые здесь, кроме того, демонстрируют подходящие характеристики, которые имеют отношение к промышленному производству в виде терапевтического продукта в виде антитела. Как здесь описывается в другом месте, предпочтительные антитела против CD70, обеспечиваемых здесь, демонстрируют экспрессию на очень высоком уровне в рекомбинантных экспрессионных системах, используемых для промышленного производства терапевтических продуктов в виде антител клинической стадии. Уровни экспрессии, достигаемые в случае предпочтительных антител против CD70, в значительной степени превышают уровни, обычно достигаемые даже в случае терапевтических продуктов в виде «полностью человеческих» антител. Кроме того, продукты в виде предпочтительных антител против CD70 (продуцированных в результате рекомбинантной экспрессии в формате, подходящем для терапевтического применения для людей) демонстрируют исключительную термостабильность, которая превосходит таковую типичных терапевтических продуктов в виде антител.
Обеспечиваемые здесь антитела против CD70 с более высокой аффинностью к CD70 человека и другими преимущественными характеристиками, перечисленными выше, происходят от животных семейства Camelidae (верблюдовых) (например, происходят от лам). Происходящие от верблюдовых антитела против CD70 могут быть выделенными или рекомбинантно экспрессированными моноклональными антителами. Предпочтительные варианты осуществления могут быть гуманизированным (или приведенным к зародышевому типу) моноклональным антителом (например, гуманизированным вариантом происходящего от верблюдовых антитела против CD70), химерным антителом (например, животное семейства верблюдовых-человек химерным антителом) или гуманизированным химерным антителом (например, химерным антителом, включающим гуманизированные варианты VH- и VL-доменов верблюдовых и константные домена антитела человека).
Происходящие от верблюдовых антитела против CD70 могут включать по крайней мере один гипервариабельный петлевой участок или определяющий комплементарность участок, полученный из VH-домена или VL-домена вида семейства Camelidae. В конкретном варианте осуществления антитело против CD70, или его антигенсвязывающий фрагмент, может включать вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), причем VH- и VL-домены, или один или более их CDR, происходят от верблюдовых. В конкретных вариантах осуществления антитело или его антигенсвязывающий фрагмент могут включать VH- и VL-домены ламы, или приведенные к человеческому зародышевому типу варианты VH- и VL-доменов ламы. Это антитело, или антигенсвязывающий фрагмент, может проявлять «высокую степень гомологии с антителом человека», как здесь описывается.
Происходящие от верблюдовых антитела против CD70, описываемые здесь, обычно демонстрируют аминокислотные последовательности VH- и/или VL-областей, идентичные на по крайней мере 90% (например, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%) ближе всего соответствующей последовательности антитела человека зародышевого типа.
Дальнейшие предпочтительные варианты осуществления настоящего изобретения включают гуманизированные (или приведенные к человеческому зародышевому типу) варианты происходящих от верблюдовых антител против CD70. В частности, настоящим изобретением обеспечиваются гуманизированные или приведенные к человеческому зародышевому типу варианты происходящих от ламы антител против CD70, описываемых здесь.
В дальнейшем аспекте настоящего изобретения обеспечивается химерное животное семейства верблюдовых-человек антитело, которое связывается с CD70 человека, причем антигенсвязывающие части антитела (например, VH- и/или VL-домены или их CDR) происходят от верблюдовых, а константные области антитела происходят из антитела человека. В частности, настоящим изобретением обеспечивается химерное лама-человек антитело, которое связывается с CD70 человека.
В дальнейшем аспекте настоящего изобретения обеспечивается гуманизированный вариант химерного животное семейства верблюдовых-человек антитела, которое связывается с CD70 человека, причем антигенсвязывающие части антитела (например, VH- и/или VL-домены или их CDR) являются гуманизированными вариантами происходящих от верблюдовых последовательностей, а константные области антитела происходят из антитела человека. В частности, настоящим изобретением обеспечивается гуманизированный вариант химерного лама-человек антитела, которое связывается с CD70 человека.
Предпочтительные (но не ограничивающие) варианты антител против CD70, или их антигенсвязывающие фрагменты, определены ниже в соответствии с конкретными структурными характеристиками, т.е. точно определенными аминокислотными последовательностями либо CDR (одной или более из SEQ ID NO: 49-59, 262 или 263 (CDR3 тяжелой цепи), или SEQ ID NO: 26-37, 249, 258 или 259 (CDR2 тяжелой цепи), или SEQ ID NO: 10-20, 248, 256 или 257 (CDR1 тяжелой цепи), или одной из последовательностей CDR, представленных в виде SEQ ID NO: 148-168, 271 или 273 (CDR3 легкой цепи), или SEQ ID NO: 109-128 или 270 (CDR2 легкой цепи), или SEQ ID NO: 77-95 или 250-253, 267 или 268 (CDR1 легкой цепи), либо полноразмерных вариабельных доменов (одной или более из SEQ ID NO: 177-188, 212-223, 274 или 275 (VH) или SEQ ID NO: 189-211, 230-245, 276 или 277 (VL)). Все из этих антител связываются с CD70 человека с высокой аффинностью, демонстрируя, при исследовании в виде Fab-фрагмента, скорость диссоциации от CD70 человека, составляющую 5×10-4 сек-1 или менее, и типично находящуюся в диапазоне от 0,4×10-4 сек-1 до 4,8×10-4 сек-1.
Настоящим изобретением также обеспечиваются гуманизированные/приведенные к зародышевому типу варианты этих антител, плюс варианты аффинности и варианты, содержащие консервативные аминокислотные замены, определенные здесь. В частности, обеспечиваются химерные антитела, содержащие VH- и VL-домены, происходящие от верблюдовых, или их приведенные к человеческому зародышевому типу варианты, слитые с константными доменами антител человека, в частности, IgG1, IgG2, IgG3 или IgG4. Вариабельные домены тяжелой цепи, определенные выше, могут использоваться в качестве однодоменных антител, или могут быть включены в обычное четырехцепочечное антитело или другие антигенсвязывающие белки, такие как, например, Fab-, Fab′-, F(ab′)2-, биспецифические Fab′- и Fv-фрагменты, диатела, линейные антитела, одноцепочечные молекулы антител, одноцепочечный вариабельный фрагмент (scFv) и полиспецифические антитела.
Предпочтительными вариантами антител против CD70 являются антитела, или их антигенсвязывающие фрагменты, включающие вариабельный домен тяжелой цепи, включающий CDR3 вариабельного домена тяжелой цепи, CDR2 вариабельного домена тяжелой цепи и CDR1 вариабельного домена тяжелой цепи, причем указанный CDR3 вариабельного домена тяжелой цепи включает аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO: 49, SEQ ID NO: 50, SEQ ID NO: 51, SEQ ID NO: 52, SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 55, SEQ ID NO: 56, SEQ ID NO: 57, SEQ ID NO: 58, SEQ ID NO: 59, SEQ ID NO: 262 и SEQ ID NO: 263, и вариантов любой из приведенных последовательностей, причем вариант последовательности включает одну, две или три аминокислотных замены в приведенной последовательности;
указанный CDR2 вариабельного домена тяжелой цепи необязательно включает аминокислотную последовательность, выбираемую из группы, состоящей из аминокислотных последовательностей SEQ ID NO: 306 [X1X2X3X4X5X6X7X8X9YYADSVKX10], где
X1 представляет собой любую аминокислоту, предпочтительно D, T, S или E,
X2 представляет собой любую аминокислоту, предпочтительно I,
X3 представляет собой любую аминокислоту, предпочтительно N, S, T или Y,
X4 представляет собой любую аминокислоту, предпочтительно N, M, S или T,
X5 представляет собой любую аминокислоту, предпочтительно E, D, Y или H,
X6 представляет собой любую аминокислоту, предпочтительно G, D, S или N,
X7 представляет собой любую аминокислоту, предпочтительно G, Y, S, D или M,
X8 представляет собой любую аминокислоту, предпочтительно T, E, S, N, Y или R,
X9 представляет собой любую аминокислоту, предпочтительно T, A или R, и
X10 представляет собой любую аминокислоту, предпочтительно G или S,
и аминокислотных последовательностей SEQ ID NO: 30, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 249, SEQ ID NO: 258 и SEQ ID NO: 259 и вариантов любой из приведенных последовательностей, причем вариант последовательности включает одну, две или три аминокислотных замены в приведенной последовательности; и
указанный CDR1 вариабельного домена тяжелой цепи необязательно включает аминокислотную последовательность, выбираемую из группы, состоящей из аминокислотных последовательностей SEQ ID NO: 307 [X1YYMN], где
X1 представляет собой любую аминокислоту, предпочтительно V, G or A,
аминокислотных последовательностей SEQ ID NO: 308 [X1X2AMS], где
X1 представляет собой любую аминокислоту, предпочтительно D, T, S, N или G, и
X2 представляет собой любую аминокислоту, предпочтительно Y, S или P,
и аминокислотных последовательностей SEQ ID NO: 10, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 248, SEQ ID NO: 256 и SEQ ID NO: 257 и вариантов любой из приведенных последовательностей, причем вариант последовательности включает одну, две или три аминокислотных замены в приведенной последовательности.
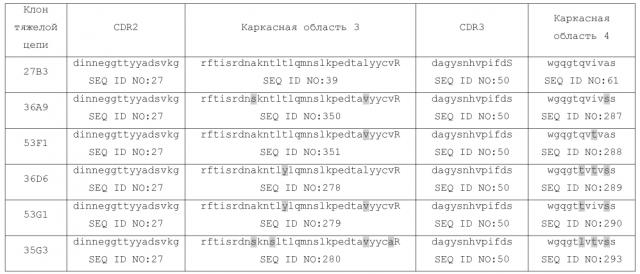
Вариабельный домен тяжелой цепи может включать любую из перечисленных последовательностей CDR3 вариабельного домена тяжелой цепи (HCDR3) в сочетании с любой из последовательностей CDR2 вариабельного домена тяжелой цепи (HCDR2) и любой из последовательностей CDR1 вариабельного домена тяжелой цепи (HCDR1). Однако особенно предпочтительными являются некоторые сочетания HCDR3 и HCDR2 и HCDR1, которые являются встречающимися в природе сочетаниями, которые происходят из одного общего VH-домена. Эти предпочтительные сочетания перечислены в таблице 6 и таблице 14A.
Антитело или его антигенсвязывающий фрагмент может, кроме того, включать вариабельный домен легкой цепи (VL), который спаривается с VH-доменом с образованием антигенсвязывающего домена. Предпочтительными вариабельными доменами легкой цепи являются те, которые включают CDR3 вариабельного домена легкой цепи, CDR2 вариабельного домена легкой цепи и CDR1 вариабельного домена легкой цепи, причем указанный CDR3 вариабельного домена легкой цепи включает аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO: 148, SEQ ID NO: 149, SEQ ID NO: 150, SEQ ID NO: 151, SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156, SEQ ID NO: 157, SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161, SEQ ID NO: 162, SEQ ID NO: 163, SEQ ID NO: 164, SEQ ID NO: 165, SEQ ID NO: 166, SEQ ID NO: 166, SEQ ID NO: 168, SEQ ID NO: 271 и SEQ ID NO: 273, и вариантов любой из приведенных последовательностей, причем вариант последовательности включает одну, две или три аминокислотных замены в приведенной последовательности;
указанный CDR2 вариабельного домена легкой цепи необязательно включает аминокислотную последовательность, выбираемую из группы, состоящей из
(а) аминокислотных последовательностей SEQ ID NO: 310 [X1TX2X3RHS], где
X1 представляет собой любую аминокислоту, предпочтительно N или S,
X2 представляет собой любую аминокислоту, предпочтительно N, S или A, и
X3 представляет собой любую аминокислоту, предпочтительно S, N или T,
(b) аминокислотных последовательностей SEQ ID NO: 311 [YYSDSX1X2X3QX4S], где
X1 представляет собой любую аминокислоту, предпочтительно Y, V или L,
X2 представляет собой любую аминокислоту, предпочтительно K или S,
X3 представляет собой любую аминокислоту, предпочтительно H или N, и
X4 представляет собой любую аминокислоту, предпочтительно G или S,
(c) аминокислотных последовательностей SEQ ID NO: 312 [X1NX2NRPS], где
X1 представляет собой любую аминокислоту, предпочтительно V, I или Y, и
X2 представляет собой любую аминокислоту, предпочтительно N или T,
(d) аминокислотных последовательностей SEQ ID NO: 313 [GDNX1X2PL], где
X1 представляет собой любую аминокислоту, предпочтительно Y, и
X2 представляет собой любую аминокислоту, предпочтительно R или M,
(e) аминокислотных последовательностей SEQ ID NO: 314 [X1DDX2RPS], где
X1 представляет собой любую аминокислоту, предпочтительно D или G, и
X2 представляет собой любую аминокислоту, предпочтительно S или I,
и аминокислотных последовательностей SEQ ID NO: 113, SEQ ID NO: 116, SEQ ID NO: 120 и SEQ ID NO: 270, и вариантов любой из приведенных последовательностей, причем вариант последовательности включает одну, две или три аминокислотных замены в приведенной последовательности; и
указанный CDR1 вариабельного домена легкой цепи необязательно включает аминокислотную последовательность, выбираемую из группы, состоящей из
(а) аминокислотных последовательностей SEQ ID NO: 315 [GLX1SGSX2TX3X4X5YPX6], где
X1 представляет собой любую аминокислоту, предпочтительно S или T,
X2 представляет собой любую аминокислоту, предпочтительно V или A,
X3 представляет собой любую аминокислоту, предпочтительно S или T,
X4 представляет собой любую аминокислоту, предпочтительно S, T или G,
X5 представляет собой любую аминокислоту, предпочтительно N или H,
X6 представляет собой любую аминокислоту, предпочтительно G, D или E,
(b) аминокислотных последовательностей SEQ ID NO: 316 [TLX1SX2X3X4X5GX6YDIS], где
X1 представляет собой любую аминокислоту, предпочтительно S, N или I,
X2 представляет собой любую аминокислоту, предпочтительно G или A,
X3 представляет собой любую аминокислоту, предпочтительно N или D,
X4 представляет собой любую аминокислоту, предпочтительно N или S,
X5 представляет собой любую аминокислоту, предпочтительно V или I,
X6 представляет собой любую аминокислоту, предпочтительно N или S,
(c) аминокислотных последовательностей SEQ ID NO: 317 [QGGNLX1LYGAN], где
X1 представляет собой любую аминокислоту, предпочтительно G или W,
(d) аминокислотных последовательностей SEQ ID NO: 318 [RGDX1LX2X3YX4X5N], где
X1 представляет собой любую аминокислоту, предпочтительно S или T,
X2 представляет собой любую аминокислоту, предпочтительно E или R,
X3 представляет собой любую аминокислоту, предпочтительно R или N,
X4 представляет собой любую аминокислоту, предпочтительно G или H,
X5 представляет собой любую аминокислоту, предпочтительно T или A,
(e) аминокислотных последовательностей SEQ ID NO: 319 [GX1X2SGSVTSX3NFPT], где
X1 представляет собой любую аминокислоту, предпочтительно V или L,
X2 представляет собой любую аминокислоту, предпочтительно K или T,
X3 представляет собой любую аминокислоту, предпочтительно T или D,
и аминокислотных последовательностей SEQ ID NO: 82, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 250, SEQ ID NO: 251, SEQ ID NO: 252, SEQ ID NO: 253, SEQ ID NO: 267 и SEQ ID NO: 268, и вариантов любой из приведенных последовательностей, причем вариант последовательности включает одну, две или три аминокислотных замены в приведенной последовательности.
Вариабельный домен легкой цепи может включать любую из перечисленных последовательностей CDR3 вариабельного домена легкой цепи (LCDR3) в сочетании с любой из последовательностей CDR2 вариабельного домена легкой цепи (HCDR2) и любой из последовательностей CDR1 вариабельного домена легкой цепи (LCDR1). Однако особенно предпочтительными являются некоторые сочетания LCDR3 и LCDR2 и LCDR1, которые являются встречающимися в природе сочетаниями, которые происходят из одного общего VL-домена. Эти предпочтительные сочетания перечислены в таблице 7 и таблице 15A.
Любое конкретное антитело против CD70 или его антигенсвязывающий фрагмент, включающее(ий) VH-домен, спаренный с VL-доменом с образованием центра связывания с антигеном CD70, будет включать сочетание 6 CDR: CDR3 вариабельного домена тяжелой цепи (HCDR3), CDR2 вариабельного домена тяжелой цепи (HCDR2), CDR1 вариабельного домена тяжелой цепи (HCDR1), CDR3 вариабельного домена легкой цепи (LCDR3), CDR2 вариабельного домена легкой цепи (LCDR2) и CDR1 вариабельного домена легкой цепи (LCDR1). Хотя все сочетания 6 CDR, выбираемых из групп последовательностей CDR, перечисленных выше, являются допустимыми и находятся в объеме настоящего изобретения, особенно предпочтительными являются некоторые сочетания 6 CDR, которые являются встречающимися в природе сочетаниями в одном Fab, демонстрирующем связывание с высокой аффинностью с CD70 человека.
Предпочтительные сочетания 6 CDR включают, но без ограничения, сочетания CDR3 вариабельного домена тяжелой цепи (HCDR3), CDR2 вариабельного домена тяжелой цепи (HCDR2), CDR1 вариабельного домена тяжелой цепи (HCDR1), CDR3 вариабельного домена легкой цепи (LCDR3), CDR2 вариабельного домена легкой цепи (LCDR2) и CDR1 вариабельного домена легкой цепи (LCDR1), выбираемые из группы, состоящей из:
(i) HCDR3, включающего SEQ ID NO: 50, HCDR2, включающего SEQ ID NO: 27, HCDR1, включающего SEQ ID NO: 11, LCDR3, включающего SEQ ID NO: 160, LCDR2, включающего SEQ ID NO: 119, и LCDR1, включающего SEQ ID NO: 250;
(ii) HCDR3, включающего SEQ ID NO: 49, HCDR2, включающего SEQ ID NO: 26, HCDR1, включающего SEQ ID NO: 10, LCDR3, включающего SEQ ID NO: 148, LCDR2, включающего SEQ ID NO: 109, и LCDR1, включающего SEQ ID NO: 77;
(iii) HCDR3, включающего SEQ ID NO: 50, HCDR2, включающего SEQ ID NO: 27, HCDR1, включающего SEQ ID NO: 11, LCDR3, включающего SEQ ID NO: 149, LCDR2, включающего SEQ ID NO: 110, и LCDR1, включающего SEQ ID NO: 78;
(iv) HCDR3, включающего SEQ ID NO: 50, HCDR2, включающего SEQ ID NO: 28, HCDR1, включающего SEQ ID NO: 11, LCDR3, включающего SEQ ID NO: 150, LCDR2, включающего SEQ ID NO: 111, и LCDR1, включающего SEQ ID NO: 79;
(v) HCDR3, включающего SEQ ID NO: 50, HCDR2, включающего SEQ ID NO: 28, HCDR1, включающего SEQ ID NO: 11, LCDR3, включающего SEQ ID NO: 151, LCDR2, включающего SEQ ID NO: 110, и LCDR1, включающего SEQ ID NO: 80;
(vi) HCDR3, включающего SEQ ID NO: 51, HCDR2, включающего SEQ ID NO: 29, HCDR1, включающего SEQ ID NO: 12, LCDR3, включающего SEQ ID NO: 152, LCDR2, включающего SEQ ID NO: 110, и LCDR1, включающего SEQ ID NO: 80;
(vii) HCDR3, включающего SEQ ID NO: 52, HCDR2, включающего SEQ ID NO: 30, HCDR1, включающего SEQ ID NO: 13, LCDR3, включающего SEQ ID NO: 153, LCDR2, включающего SEQ ID NO: 112, и LCDR1, включающего SEQ ID NO: 81;
(viii) HCDR3, включающего SEQ ID NO: 53, HCDR2, включающего SEQ ID NO: 31, HCDR1, включающего SEQ ID NO: 14, LCDR3, включающего SEQ ID NO: 154, LCDR2, включающего SEQ ID NO: 113, и LCDR1, включающего SEQ ID NO: 82;
(ix) HCDR3, включающего SEQ ID NO: 54, HCDR2, включающего SEQ ID NO: 32, HCDR1, включающего SEQ ID NO: 15, LCDR3, включающего SEQ ID NO: 155, LCDR2, включающего SEQ ID NO: 114, и LCDR1, включающего SEQ ID NO: 83;
(x) HCDR3, включающего SEQ ID NO: 55, HCDR2, включающего SEQ ID NO: 33, HCDR1, включающего SEQ ID NO: 16, LCDR3, включающего SEQ ID NO: 156, LCDR2, включающего SEQ ID NO: 115, и LCDR1, включающего SEQ ID NO: 84;
(xi) HCDR3, включающего SEQ ID NO: 56, HCDR2, включающего SEQ ID NO: 34, HCDR1, включающего SEQ ID NO: 17, LCDR3, включающего SEQ ID NO: 157, LCDR2, включающего SEQ ID NO: 116, и LCDR1, включающего SEQ ID NO: 85;
(xii) HCDR3, включающего SEQ ID NO: 57, HCDR2, включающего SEQ ID NO: 35, HCDR1, включающего SEQ ID NO: 18, LCDR3, включающего SEQ ID NO: 158, LCDR2, включающего SEQ ID NO: 117, и LCDR1, включающего SEQ ID NO: 84;
(xiii) HCDR3, включающего SEQ ID NO: 58, HCDR2, включающего SEQ ID NO: 36, HCDR1, включающего SEQ ID NO: 19, LCDR3, включающего SEQ ID NO: 159, LCDR2, включающего SEQ ID NO: 118, и LCDR1, включающего SEQ ID NO: 86;
(xiv) HCDR3, включающего SEQ ID NO: 50, HCDR2, включающего SEQ ID NO: 27, HCDR1, включающего SEQ ID NO: 11, LCDR3, включающего SEQ ID NO: 161, LCDR2, включающего SEQ ID NO: 120, и LCDR1, включающего SEQ ID NO: 88;
(xv) HCDR3, включающего SEQ ID NO: 50, HCDR2, включающего SEQ ID NO: 27, HCDR1, включающего SEQ ID NO: 11, LCDR3, включающего SEQ ID NO: 162, LCDR2, включающего SEQ ID NO: 121, и LCDR1, включающего SEQ ID NO: 89;
(xvi) HCDR3, включающего SEQ ID NO: 50, HCDR2, включающего SEQ ID NO: 27, HCDR1, включающего SEQ ID NO: 11, LCDR3, включающего SEQ ID NO: 163, LCDR2, включающего SEQ ID NO: 122, и LCDR1, включающего SEQ ID NO: 90;
(xvii) HCDR3, включающего SEQ ID NO: 51, HCDR2, включающего SEQ ID NO: 29, HCDR1, включающего SEQ ID NO: 12, LCDR3, включающего SEQ ID NO: 164, LCDR2, включающего SEQ ID NO: 123, и LCDR1, включающего SEQ ID NO: 91;
(xviii) HCDR3, включающего SEQ ID NO: 51, HCDR2, включающего SEQ ID NO: 29, HCDR1, включающего SEQ ID NO: 12, LCDR3, включающего SEQ ID NO: 164, LCDR2, включающего SEQ ID NO: 124, и LCDR1, включающего SEQ ID NO: 91;
(xix) HCDR3, включающего SEQ ID NO: 59, HCDR2, включающего SEQ ID NO: 37, HCDR1, включающего SEQ ID NO: 12, LCDR3, включающего SEQ ID NO: 165, LCDR2, включающего SEQ ID NO: 125, и LCDR1, включающего SEQ ID NO: 92;
(xx) HCDR3, включающего SEQ ID NO: 59, HCDR2, включающего SEQ ID NO: 37, HCDR1, включающего SEQ ID NO: 20, LCDR3, включающего SEQ ID NO: 165, LCDR2, включающего SEQ ID NO: 126, и LCDR1, включающего SEQ ID NO: 93;
(xxi) HCDR3, включающего SEQ ID NO: 59, HCDR2, включающего SEQ ID NO: 37, HCDR1, включающего SEQ ID NO: 20, LCDR3, включающего SEQ ID NO: 166, LCDR2, включающего SEQ ID NO: 127, и LCDR1, включающего SEQ ID NO: 92;
(xxii) HCDR3, включающего SEQ ID NO: 59, HCDR2, включающего SEQ ID NO: 37, HCDR1, включающего SEQ ID NO: 20, LCDR3, включающего SEQ ID NO: 167, LCDR2, включающего SEQ ID NO: 128, и LCDR1, включающего SEQ ID NO: 94;
(xxiii) HCDR3, включающего SEQ ID NO: 59, HCDR2, включающего SEQ ID NO: 37, HCDR1, включающего SEQ ID NO: 20, LCDR3, включающего SEQ ID NO: 168, LCDR2, включающего SEQ ID NO: 110, и LCDR1, включающего SEQ ID NO: 95;
(xxiv) HCDR3, включающего SEQ ID NO: 262, HCDR2, включающего SEQ ID NO: 258, HCDR1, включающего SEQ ID NO: 256, LCDR3, включающего SEQ ID NO: 271, LCDR2, включающего SEQ ID NO: 110, и LCDR1, включающего SEQ ID NO: 267;
(xxv) HCDR3, включающего SEQ ID NO: 263, HCDR2, включающего SEQ ID NO: 259, HCDR1, включающего SEQ ID NO: 257, LCDR3, включающего SEQ ID NO: 273, LCDR2, включающего SEQ ID NO: 270, и LCDR1, включающего SEQ ID NO: 268.
Дополнительные предпочтительные антитела против CD70, демонстрирующие связывание с высокой аффинностью с CD70 человека, включают выделенные антитела или их антигенсвязывающие фрагменты, включающие вариабельный домен тяжелой цепи, имеющий аминокислотную последовательность, выбираемую из группы, состоящей из аминокислотных последовательностей SEQ ID NO: 177, SEQ ID NO: 178, SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 181, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 184, SEQ ID NO: 185, SEQ ID NO: 186, SEQ ID NO: 187, SEQ ID NO: 188, SEQ ID NO: 212, SEQ ID NO: 213, SEQ ID NO: 214, SEQ ID NO: 215, SEQ ID NO: 216, SEQ ID NO: 217, SEQ ID NO: 218, SEQ ID NO: 219, SEQ ID NO: 220, SEQ ID NO: 221, SEQ ID NO: 222, SEQ ID NO: 223, SEQ ID NO: 224, SEQ ID NO: 225, SEQ ID NO: 226, SEQ ID NO: 227, SEQ ID NO: 228, SEQ ID NO: 229, SEQ ID NO: 274 и SEQ ID NO: 275, и аминокислотных последовательностей, идентичных на по крайней мере 90%, 95%, 97%, 98% или 99% одной из приведенных последовательностей, и необязательно включающие вариабельный домен легкой цепи, имеющий аминокислотную последовательность, выбираемую из группы, состоящей из аминокислотных последовательностей SEQ ID NO: 189, SEQ ID NO: 190, SEQ ID NO: 191, SEQ ID NO: 192, SEQ ID NO: 193, SEQ ID NO: 194, SEQ ID NO: 195, SEQ ID NO: 196, SEQ ID NO: 197, SEQ ID NO: 198, SEQ ID NO: 199, SEQ ID NO: 200, SEQ ID NO: 201, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 204, SEQ ID NO: 205, SEQ ID NO: 206, SEQ ID NO: 207, SEQ ID NO: 208, SEQ ID NO: 209, SEQ ID NO: 210, SEQ ID NO: 211, SEQ ID NO: 223, SEQ ID NO: 230, SEQ ID NO: 231, SEQ ID NO: 232, SEQ ID NO: 233, SEQ ID NO: 234, SEQ ID NO: 234, SEQ ID NO: 236, SEQ ID NO: 237, SEQ ID NO: 238, SEQ ID NO: 239, SEQ ID NO: 240, SEQ ID NO: 241, SEQ ID NO: 242, SEQ ID NO: 243, SEQ ID NO: 244, SEQ ID NO: 245, SEQ ID NO: 245, SEQ ID NO: 247, SEQ ID NO: 248, SEQ ID NO: 276 и SEQ ID NO: 277, и аминокислотных последовательностей, идентичных на по крайней мере 90%, 95%, 97%, 98% или 99% одной из приведенных последовательностей.
Хотя все возможные спаривания VH-доменов и VL-доменов, выбираемых из групп последовательностей VH- и VL-доменов, перечисленных выше, являются допустимыми и находятся в объеме настоящего изобретения, особенно предпочтительными являются некоторые сочетания VH и VL, которые являются встречающимися в природе сочетаниями в одном Fab, демонстрирующем связывание с высокой аффинностью с CD70 человека. Соответственно, предпочтительными антителами против CD70, или их антигенсвязывающими фрагментами, демонстрирующими связывание с высокой аффинностью с CD70 человека, являются те, которые включают сочетание вариабельного домена тяжелой цепи (VH) и вариабельного домена легкой цепи (VL), причем сочетание выбирают из группы, состоящей из:
(i) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 223, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 241;
(ii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 177, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 189;
(iii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 178, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 190;
(iv) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 179, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 191;
(v) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 179, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 192;
(vi) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 180, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 193;
(vii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 181, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 194;
(viii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 182, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 195;
(ix) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 183, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 196;
(x) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 184, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 197;
(xi) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 185, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 198;
(xii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 186, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 199;
(xiii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 187, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 200;
(xiv) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 178, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 201;
(xv) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 178, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 202;
(xvi) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 178, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 203;
(xvii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 178, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 204;
(xviii) вариабельного домена тяжелой цепи, включающего аминокислотную последовательность SEQ ID NO: 180, и вариабельного домена легкой цепи, включающего аминокислотную последовательность SEQ ID NO: 205;
(