Способ очистки никелевого электролита от примесей железа (iii) и меди (ii) экстракцией смесью олеиновой кислоты и триэтаноламина
Иллюстрации
Показать всеИзобретение относится к извлечению веществ органическими экстрагентами из водных растворов и может быть использовано в цветной и черной металлургии, а также для очистки промышленных и бытовых стоков. Способ включает обработку электролита и экстрагента, контакт электролита и экстрагента, при этом селективное извлечение ионов Fe (III) и Cu (II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина осуществляют в две стадии: 1 стадия - извлечение Fe (III) при 3<рН≤4, соотношении объемов водной В и органической О фаз 1≤В:O≤4 и t 40°С, 2 стадия - извлечение Cu (II) при 5≤рН≤6, 1≤В:O≤4 и t 40°С. Совместное извлечение ионов Fe (III) и Cu (II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина осуществляют при рН 5-6, 1≤B:O≤4 и t 40°С. Способ обеспечивает повышение эффективности селективного и совместного извлечения ионов Fe (III) и Cu (II) из никелевого электролита. 2 н.п. ф-лы, 2 табл., 4 ил.
Реферат
Изобретение относится к извлечению веществ органическими экстрагентами из водных растворов и может быть использовано в цветной и черной металлургии, а также для очистки промышленных и бытовых стоков.
Ионы меди из никелевого электролита обычно удаляют методом цементации более электроотрицательным металлом - никелем. Для этой цели используют никелевый порошок. Очистка электролита от железа проводится путем окисления хлором для перевода железа в трехвалентное состояние и последующего осаждения в виде основных солей переменного состава, нейтрализацию кислоты гидролиза осуществляют карбонатом никеля [Вольдман Г.М., Зеликман А.Н. Теория гидрометаллургических процессов. - М., Металлургия, 1993, с. 303-307].
Недостатками способов является то, что селективное извлечение ионов железа и цветных металлов из таких растворов осаждением затруднено. Ионы Fe(II) осаждаются гидролитически совместно с основными ионами цветных металлов. Ионы Fe(III) осаждаются в более кислой области, но вместе с ними также осаждаются ионы цветных металлов и органические примеси, так как ионы Fe(III) являются коагулянтами.
Наиболее близким техническим решением является экстракционное извлечение ионов металлов из водных растворов смеси солей [Воропанова Л.А., Величко Л.Н. Экстракция меди (II), никеля (II), кобальта (III), хрома (III), железа (II и III) из водных растворов с использованием в качестве экстрагента технической смазки. Журнал Прикладной Химии, 1999 г., вып. 11, №6. С. 1858-1863], в котором даны результаты извлечения ионов Fe(III) и Cu(II) из водных растворов технологической смазкой марки СП-3.
Недостатком способа является то, что не выявлены оптимальные условия селективного и совместного извлечения ионов Fe(III) и Cu(II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине.
Задачей изобретения является определение оптимальных условий селективного и совместного извлечения ионов Fe(III) и Cu(II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине.
Технический результат, который может быть получен при использовании изобретения, заключается в эффективности селективного и совместного извлечения ионов Fe(III) и Cu(II) из никелевого электролита с использованием недорогого экстрагента.
1. Данный технический результат достигается тем, что в известном способе очистки никелевого электролита от примесей ионов Fe(III) и Cu(II) экстракцией, включающем обработку раствора и экстрагента, контакт раствора и экстрагента, селективное извлечение ионов Fe(III) и Cu(II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине осуществляют в две стадии:
1 стадия - извлечение Fe(III) при 3≤рН≤4, соотношении объемов водной В и органической О фаз 1≤В:O:≤4 и t 40°C,
2 стадия - извлечение Cu(II) при 5≤рН≤6, соотношении объемов водной В и органической О фаз 1≤В:O≤4 и t 40°C;
2. Данный технический результат достигается тем, что в известном способе очистки никелевого электролита от примесей ионов Fe(III) и Cu(II) экстракцией, включающем обработку раствора и экстрагента, контакт раствора и экстрагента, совместное извлечение ионов Fe(III) и Cu(II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине осуществляют при pH 5-6, соотношении объемов водной В и органической О фаз 1≤B:O≤4 и t 40°C.
Сущность способа поясняется данными фиг. 1-3 и табл. 1-2, в которых указаны время контакта фаз, остаточная концентрация С, г/дм3, ионов металлов в рафинате, коэффициент распределения D=Сорг/Свод=(С0/С-1)(В:O), извлечение металлов в органическую фазу Е, мас.% от исходного, коэффициент разделения в зависимости от величины рН, соотношения объемов водной В и органической О фаз В:O. Отмечали также окраску равновесных фаз - рафината и экстракта.
Примеры практического применения
В качестве экстрагента использовали смесь олеиновой кислоты и триэтаноламина в керосине в объемном соотношении 6:3:41 соответственно. Для приготовления растворов использовали соли CuSO4·5H2O, FeCl3·6H2O и NiSO4·7H2O.
Концентрация ионов металлов в исходном растворе C0 составила, г/дм3: 1,02 Cu(II), 0,56 Fe(III) и 63,5 Ni(III). Температура исходного раствора 22°C, величина рН 2,2-2,4.
Экстракцию осуществляли при перемешивании и регулировании постоянной величины рН 50 мин, в качестве нейтрализаторов использовали растворы NaOH и H2SO4. Нагрев осуществляли постепенно от комнатной температуры до 40-45°C. Исследованиями установлено, что при комнатной температуре экстракция осуществляется менее эффективно.
Пример 1 (табл. 1, фиг. 1)
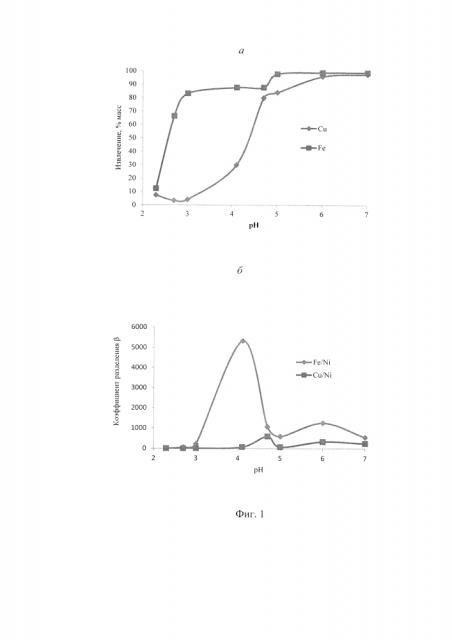
В табл. 1 и на фиг. 1 дана зависимость результатов экстракции ионов меди (II) и Fe(III) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине от величины рН раствора.
На фиг. 1 обозначено: а - извлечение, б - коэффициент разделения.
Извлечение Е, в мас.% от исходного, для никеля не превышает 0,1-6% при 3≤рН≤6, в то время как извлечение железа 83-99% при рН 3-7, а меди - 84-98% при рН 5-7. В тех же интервалах рН наблюдаются наибольшие коэффициенты разделения β этих металлов с никелем.
Смесью олеиновой кислоты и триэтаноламина в керосине возможно селективное извлечение из никелевого электролита преимущественно железа при рН 3-4,5 (при этом извлекается меньше 2% никеля) и меди при рН 5-7 (при этом извлекается меньше 7% никеля), или совместное извлечение железа и меди при рН 4-7 (при этом извлекается 0,1-7% никеля).
Пример 2 (табл. 2, фиг. 2)
В табл. 2 и на фиг. 2 дана зависимость результатов экстракции ионов Fe(III) и Cu(II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине от отношения В:O в интервале рН 5,5-6,0. На фиг. 2 обозначено: а - извлечение, б - коэффициент разделения Совместное извлечение ионов железа (III) и меди (II) возможно при соотношении 1≤В:O≤4, при соотношении В:O≥5 в водной фазе выпадает осадок, в последнем случае извлечение из водной фазы ионов металлов рассчитывали совместно в органическую фазу и осадок.
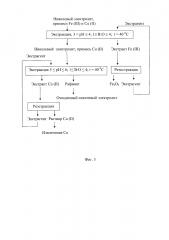
Исходя из полученных экспериментальных данных разработана принципиальная технологическая схема процесса экстракционного селективного (фиг. 3) и совместного (фиг. 4) извлечения ионов меди (II) и железа (III) из никелевого электролита.
1. Способ очистки никелевого электролита от примесей ионов Fe(III) и Cu(II) экстракцией, включающий обработку электролита и экстрагента, контакт электролита и экстрагента, отличающийся тем, что селективное извлечение ионов Fe(III) и Cu(II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине осуществляют в две стадии:1 стадия - извлечение Fe(III) при 3<рН≤4, соотношении объемов водной В и органической О фаз 1≤В:O≤4 и t 40°C,2 стадия - извлечение Cu(II) при 5≤рН≤6, соотношении объемов водной В и органической О фаз 1≤В:O≤4 и t 40°C.
2. Способ очистки никелевого электролита от примесей ионов Fe(III) и Cu(II) экстракцией, включающий обработку электролита и экстрагента, контакт электролита и экстрагента, отличающийся тем, что совместное извлечение ионов Fe(III) и Cu(II) из никелевого электролита смесью олеиновой кислоты и триэтаноламина в керосине осуществляют при рН 5-6, соотношении объемов водной В и органической О фаз 1≤В:O≤4 и t 40°C.