Электрохимический биосенсор для прямой регистрации миоглобина на основе углеродных нанотрубок и молекулярно импринтированного полимера на основе о-фенилендиамина и способ его получения
Иллюстрации
Показать всеГруппа изобретений относится к области аналитической химии, электрохимиии и медицинской диагностики и может быть использована для диагностики ранних стадий инфаркта миокарда. Электрохимический биосенсор для прямой регистрации миоглобина в водных буферных растворах путем измерения высоты пика электровосстановления миоглобина методом квадратно-волновой вольтамперометрии представляет собой графитовый электрод, модифицированный углеродными нанотрубками и аналогом антител к миоглобину, представляющим собой молекулярно импринтированный для миоглобина полимер о-фенилендиамина. Группа изобретений касается также способа получения указанного биосенсора, включающего модификацию поверхности графитового электрода суспензией углеродных нанотрубок, последующую модификацию полученного электрода путем электрополимеризации о-фенилендиамина в присутствии миоглобина, осуществляемой на поверхности модифицированного нанотрубками электрода, и инкубацию полученного электрода в растворе, содержащем этанол и 0,25 М NaOH при их соотношении 2:1. При этом суспензию углеродных нанотрубок получают методом ультразвуковой дезинтеграции углеродных нанотрубок в органическом растворителе. Группа изобретений обеспечивает повышение чувствительности биосенсора. 2 н.п. ф-лы, 2 ил., 2 пр.
Реферат
Изобретение относится к области клинической биохимии и аналитической химии и касается электрохимического биосенсора на основе углеродных нанотрубок и молекулярно импринтированного полимера (МИП) на основе о-фенилендиамина для прямого определения миоглобина и способа получения указанного биосенсора.
Изобретение может быть использовано в медицинской практике для диагностики ранних стадий инфаркта миокарда с помощью анализа раннего маркера инфаркта миокарда - миоглобина [1].
Специфичность биохимического анализа определяется, как правило, использованием принципа «ключ-замок», где роль «замка» играют такие биореагенты, как антитела, аптамеры, сомамеры, альтернативные каркасные белки [2]. Антитела, альтернативные каркасные белки, аптамеры являются природными полимерами, что может снижать их стабильность за счет чувствительности к протеазам (белки), нуклеазам (олигонуклеотиды) при работе различных сенсорных систем.
В связи с этим в настоящее время развивается новое направление - создание сенсоров на основе синтетических биомимических (или «биоподражательных») материалов, осуществляющих, как и биореагенты, селективное комплементарное связывание определяемых веществ по принципу «ключ-замок» (http://www.mipdatabase.com). Такими биомимическими материалами являются полимеры с молекулярными отпечатками или молекулярно импринтированные полимеры (МИП) [2]. В качестве мономеров для получения МИП описаны следующие вещества: замещенные акриламиды, пиррол, анилин, замещенные фенолы, допамин, о-фенилендиамин, тиофен (http://www.mipdatabase.com)].
Для повышения чувствительности биосенсорного анализа (предела определяемых концентраций) синтетические биораспознающие молекулы на основе полимеров конъюгируют с различными типами наноматериалов [3-7].
На сегодняшний день на рынке представлены следующие тесты и системы иммуноанализа белков-кардиомаркеров, выпускаемые зарубежными производителями: Stratus® CS STAT (Dade Behring Inc), i-STAT® (Abbott), Triage® Cardiac Panel (Biosite), RAMP® (Response Biomedical Corp), Cardiac Reader™ (Roche), PATHFAST® (Mitsubishi Chemical Europe GmbH), MGL-CHECK-1 (Vedalab), HEXAGON TROPONIN (HUMAN GmbH). Все вышеперечисленные методы анализа миоглобина основаны на использовании антител, обеспечивающих специфичность анализа.
Ранее нами были разработаны электрохимические сенсоры на основе антител к миоглобину для определения миоглобина в водных буферных растворах и в плазме крови здоровых доноров и больных острым инфарктом миокарда.
Так, описан электрохимический биосенсор для прямого определения миоглобина в водных буферных растворах и способ его получения, заключающийся в том, что на поверхность рабочего электрода, предварительно модифицированного коллоидным золотом, стабилизированным диметилдидодециламмоний бромидом (ДДАБ), и моноклональными антителами к миоглобину, наносят анализируемый водный буферный раствор, содержащий миоглобин в определенной концентрации [8].
Описан также способ экспресс-определения кардиомиоглобина в плазме крови здоровых доноров и больных инфарктом миокарда с помощью электрохимического иммуносенсора, заключающийся в том, что на поверхность рабочего электрода, предварительно модифицированного коллоидным золотом, стабилизированным диметилдидодециламмоний бромидом (ДДАБ), и моноклональными антителами к миоглобину, наносят анализируемую плазму крови [9].
Недостатками описанных биосенсоров является использование моноклональных антител, которые являются нестабильными и дорогостоящими белковыми молекулами, что сказывается на стоимости анализа, стабильности сенсора и возможности его многократного использования.
Задачей настоящего изобретения является разработка электрохимического биосенсора для регистрации миоглобина, лишенного указанных недостатков, так как распознающим элементом является полимер с молекулярными отпечатками миоглобина (МИП на миоглобин). Для повышения чувствительности биосенсора используется МИП на миоглобин, сопряженный с углеродными нанотрубками.
В соответствии с изобретением описывается электрохимический биосенсор для прямой регистрации миоглобина в водных буферных растворах путем измерения высоты пика электровосстановления миоглобина методом квадратно-волновой вольтамперометрии, представляющий собой графитовый электрод, модифицированный углеродными нанотрубками и аналогом антител к миоглобину, представляющий собой молекулярно импринтированный для миоглобина полимер о-фенилендиамина (МИП на миоглобин).
Описывается также способ получения указанного электрохимического биосенсора для прямой регистрации миоглобина, заключающийся в том, что поверхность графитового электрода модифицируют суспензией углеродных нанотрубок, полученной методом ультразвуковой дезинтеграции углеродных нанотрубок в органическом растворителе, с последующей модификацией полученного электрода путем электрополимеризации о-фенилендиамина в присутствии миоглобина, осуществляемой на поверхности печатного графитового электрода с углеродными нанотрубками.
Разработан электрохимический биосенсор на основе печатного графитового для прямой регистрации миоглобина в водных буферных растворах с использованием в качестве биораспознающего элемента молекулярно импринтированного для миоглобина полимера о-фенилендиамина (МИП на миоглобин), представляющего собой аналог антител к миоглобину.
Аналитическим сигналом служит величина измеряемого тока электровосстановления миоглобина на поверхности электрода, модифицированного углеродными нанотрубками и молекулярно импринтированным для миоглобина полимером на основе о-фенилендиамина. Полимер получают методом электрополимеризации на поверхности электрода [10-12].
Электрохимический биосенсор для безреагентного определения миоглобина изготавливается на основе одноразовых графитовых электродов, полученных методом трафаретной печати, которые модифицируют углеродными нанотрубками для усиления аналитического электрохимического сигнала и молекулярно импринтированным для миоглобина полимером (МИП на миоглобин).
Метод анализа основан на взаимодействии МИП, полученного электрополимеризацией о-фенилендиамина в присутствии миоглобина, как молекулы-шаблона, удалении миоглобина из полимера с последующей электрохимической регистрацией миоглобина в анализируемых водных буферных растворах за счет взаимодействия миоглобина с полостями в полимере, соответствующими молекуле миоглобина.
ПРИМЕР 1. Методика модификации рабочего графитового электрода углеродными нанотрубками (УНТ) и МИП на основе о-фенилендиамина.
Электрохимические измерения проводили с помощью потенциостата AUTOLAB 12 (Metrohm Autolab, Нидерланды), снабженного программным обеспечением GPES (версия 4.9.7).
Для приготовления биосенсоров используют трехконтактные электродные структуры, полученные методом трафаретной печати (ООО «АвтоКом», Россия, http://www.membrans.ru) с графитовыми рабочим и вспомогательным электродами (графит фирмы Acheson), и хлорсеребряным электродом сравнения. Диаметр рабочего электрода 2 мм. Все потенциалы приведены относительно хлорсеребряного Ag/AgCl электрода сравнения.
Приготовление предполимеризационной смеси мономер - миоглобин.
Для синтеза МИП на основе о-фенилендиамина и миоглобина были приготовлены исходные растворы реагентов: 100 мкМ миоглобин в 0,1 М калий-фосфатном буфере, рН=7,4, 10 мМ раствор о-фенилендиамина в 0,5 М ацетатном буфере, рН 5,2. Меньшие концентрации миоглобина и мономера получали при разведении исходных растворов теми же буферными растворами. Предполимеризационную смесь готовили смешиванием 30 мкл 1×10-7 М раствор миоглобина с 30 мкл 1×10-6 М о-фенилендиамина.
Получение суспензии углеродных нанотрубок.
Для получения суспензии углеродных нанотрубок была приготовлена смесь 1 мг УНТ/1 мл хлороформа, затем смесь озвучивали с помощью ультразвукового дезинтегратора (модель Elmasonic "Elma" S10H). Время озвучивания 5 минут.
Модификация рабочего графитового электрода.
На поверхность рабочего графитового электрода наносили 2 мкл озвученной суспензии УНТ в хлороформе (1 мг/мл) и инкубировали 15 мин при 37°С; затем на электрод наносили 60 мкл предполимеризационной смеси о-фенилендиамин:миоглобин в соотношении 10:1. Электросинтез пленок осуществлялся методом циклической вольтамперометрии (ЦВА), 20 сканов при сканировании в диапазоне потенциалов от 0 В до +1,1 В со скоростью сканирования 50 мВ/с. После полимеризации, модифицированный электрод промывали деионизованной водой с последующей инкубацией полученного электрода в растворе, содержащем этанол и 0,25 М NaOH при их соотношении 2:1 в течение 15 мин при 50°С с последующим промыванием водой в течение 15 мин при комнатной температуре. Модифицированные электроды высушивались под аргоном и хранились при +4°С (МИП/УНТ-электроды). Электроды без молекулярных отпечатков или молекулярно не импринтированные электроды (НИП) получали аналогично, используя вместо раствора миоглобина соответствующий объем 0,5 М ацетатного буфера, рН 5,2.
ПРИМЕР 2. Регистрация миоглобина с помощью электрохимического сенсора на основе углеродных нанотрубок и молекулярно импринтированного полимера (МИП) в качестве аналогов антител (МИП/УНТ-электроды).
Подготовка к измерению
Для встраивания анализируемой молекулы (миоглобина) в полимер с молекулярными отпечатками на модифицированный электрод (МИП/УНТ-электрод) наносят 2 мкл раствора миоглобина различной концентрации. Через 35 минут при 37°С электрод переносят в водный буферный раствор (0,1 М калий-фосфатный буфер, рН=7,4) на 15 мин, затем проводят измерения сигнала.
Параметры измерения сигнала
В программе к прибору устанавливают следующие параметры измерения сигнала.
- Метод: Квадратно-волновая вольтамперометрия (КВВА);
- Время инкубации: 900 с;
- Частота: 10 Гц;
- Начальный потенциал: 0.1 В;
- Конечный потенциал: -0.6 В;
- Шаг потенциала: 0.005 В;
- Амплитуда: 0.020 В;
Измерение сигнала
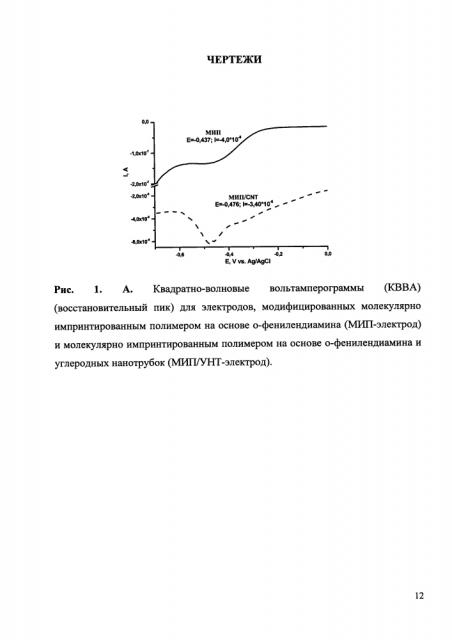
В ячейку вносят 1 мл фосфатного буферного раствора. Закрепляют биосенсор с нанесенной пробой в измерительной ячейке, опускают в буферный раствор и запускают процедуру измерения сигнала. Полученную вольтамперометрическую кривую запоминают в виде самостоятельного файла (Рис. 1).
Построение калибровочных кривых для определения миоглобина.
Если на полученной вольтамперограмме наблюдается пик (Еmах=-400÷-500 мВ), то с помощью программы к прибору GPES (версия 4.9.7) производят определение высоты полученного пика восстановления миоглобина. При использовании МИП/УНТ-сенсора аналитический сигнал регистрации миоглобина по сравнению с сенсором без УНТ возрастает в 80±5 раз (Рис. 1А). НИП/УНТ-электрод, полученный без миоглобина и не содержащий молекулярных отпечатков, менее эффективно связывал миоглобин (Рис. 1Б).
Квадратно-волновые вольтамперограммы прописывали после инкубации с 10-8 M миоглобином (Рис. 1А) и 10-7 M миоглобином (Рис. 1Б) и стадии отмывки для удаления неспецифической сорбции.
На основе зависимости высоты восстановительного пика миоглобина от концентрации проводят построение калибровочной кривой для определения диапазона определяемых концентраций и нижнего предела определяемых концентраций миоглобина. Диапазон определяемых концентраций миоглобина с помощью разработанного биосенсора на основе МИП и УНТ (МИП/УНТ-электрод) составил 10-10-10-6 М, а нижний предел определяемых концентраций составил 0,5×10-10 М.
Литература
1. Qureshi, Α., Gurbuz, Υ., and Niazi, J.H. (2012). Biosensors for cardiac biomarkers detection: A review. Sensors and Actuators B: Chemical, 171-172, 62-76.
2. О.Д. Гендриксон, A.B. Жердев, Б.Б. Дзантиев, Молекулярно импринтированные полимеры и их применение в биохимическом анализе. Успехи биологической химии, т.46, 2006, с. 149-192.
3. Y. Lv et al., Molecular imprinting of proteins in polymers attached to the surface of nanomaterials for selective recognition of biomacromolecules. Biotechnology Advances, 2013, 31, 1172-1186.
4. Zhang, X., Y. Peng, J. Bai et al., A novel electrochemical sensor based on electropolymerized molecularly imprinted polymer and gold nanomaterials amplification for estradiol detection. Sensors and Actuators B, 2014, 200, 69-75.
5. J. Luo, Sisi J. Xiaoya Liu, Electrochemical sensor for bovine hemoglobin based on a novel graphene-molecular imprinted polymers composite as recognition element / // Sensors and Actuators, 2014, 203, 782-789.
6. Choong C.-L. James S. Bendall, William I. Milne, Carbon nanotube array: A new MIP platform. Biosensors and Bioelectronics, 2009, 25, 652-656.
7. Liu, Y., S. Kumar, Polymer/Carbon Nanotube Nano Composite Fibers-A Review, ACS Appl. Mater. Interfaces, 2014, 6, 6069-6087.
8. Патент RU №2367958, 20.09.2009
9. Патент RU №2425382, 27.07.2011.
10. Najmeh Karimian, Mikhail Vagin, Mohammad Hossein Arbab Zavar, Mahmoud Chamsaz, Anthony P.F. Turner, Ashutosh Tiwari, An ultrasensitive molecularly-imprinted human cardiac troponin sensor. Biosensors and Bioelectronics 2013, 50, 492-498.
11. Najmeh Karimian, Anthony P.F. Turner, Ashutosh Tiwari, Electrochemical evaluation of troponin Τ imprinted polymer receptor. Biosensors and Bioelectronics 2014, 59, 160-165.
12. Cosimino Malitesta, Elisabetta Mazzotta, Rosaria A. Picca, Alessandro Poma, Iva Chianella, Sergey A. Piletsky, MIP sensors - the electrochemical approach. Anal. Bioanal. Chem. 2012, 402, 1827-1846.
1. Электрохимический биосенсор для прямой регистрации миоглобина в водных буферных растворах путем измерения высоты пика электровосстановления миоглобина методом квадратно-волновой вольтамперометрии, представляющий собой графитовый электрод, модифицированный углеродными нанотрубками и аналогом антител к миоглобину, представляющим собой молекулярно импринтированный для миоглобина полимер о-фенилендиамина.
2. Способ получения электрохимического биосенсора для прямой регистрации миоглобина по п. 1, заключающийся в том, что поверхность графитового электрода модифицируют суспензией углеродных нанотрубок, полученной методом ультразвуковой дезинтеграции углеродных нанотрубок в органическом растворителе, с последующей модификацией полученного электрода путем электрополимеризации о-фенилендиамина в присутствии миоглобина, осуществляемой на поверхности полученного модифицированного нанотрубками электрода, с последующей инкубацией полученного электрода в растворе, содержащем этанол и 0,25 М NaOH при их соотношении 2:1.