Восстановление кровотока в заблокированных артериях человека путем переноса наноинкапсулированного лекарственного средства посредством медицинских устройств, разработанных для этого, и высвобождения наноинкапсулированного лекарственного средства в артерии человека при уровне ph организма
Иллюстрации
Показать всеГруппа изобретений относится к медицине и касается медицинского устройства, вводимого в просвет части организма, для доставки лекарственного средства для лечения медицинского состояния, связанного с просветом части организма, а также способа лечения с использованием такого устройства при рН организма. К таким состояниям относятся рестеноз, атеросклероз и скопление бляшек в просвете части организма. Устройство может представлять собой стент, баллон, баллонный катетер, стент, установленный на баллоне, и имеет внешнюю поверхность, покрытую двумя или более наноносителями, имеющими множество средних диаметров. Множество наноносителей имеют средний диаметр, приемлемый для проникновения сквозь один и более слоев из двух или более слоев просвета части организма - интимы, среднего слоя, адвентициального слоя, сосуды сосудов. Наноноситель включает лекарственное средство, окруженное инкапсулирующей средой, которая включает одно или более из биологического средства, наполнителя на основе крови и фосфолипида, растворимых при рН менее 7,4. Группа изобретений обеспечивает высвобождение и контакт лекарственного средства только в тканях места назначения, с предотвращением фокального рестеноза, стабилизацию лекарственного средства инкапсулирующей средой, с улучшением аффинности носителей для тканей места назначения - улучшением целевой доставки при деградации инкапсулирующей среды. 2 н. и 24 з.п. ф-лы, 6 ил., 5 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0001] Изобретение в целом относится к медицинскому устройству для введения лекарственного средства в место назначения в просвете части организма. Более конкретно, изобретение относится к доставляющему лекарственное средство вводимому медицинскому устройству, покрытому наноносителями одного или нескольких лекарственных средств для эффективной доставки одного или нескольких лекарственных средств сквозь различные слои кровеносного сосуда.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Стенты и другие медицинские устройства используются для восстановления правильного кровотока в заблокированной артерии в интервенционных кардиологических процедурах, таких как чрескожная транслюминальная коронарная ангиопластика. Тем не менее, существующие интервенционные кардиологические процедуры и кардиологические медицинские устройства, используемые в этих процедурах, связаны с таким явлением как рестеноз. Для того, чтобы снизить случаи рестеноза, который возникает после ангиопластических процедур или установки стента, часто используют стенты с элюирующим лекарственным покрытием (DES). На существующие DES загружают лекарственные средства с помощью полимеров. Полимеры могут вызывать воспаление в месте, где DES имплантируются. В некоторых случаях воспаление, вызванное DES, может быть более тяжелым, чем воспаление, которое вызвано непокрытыми металлическими стентами, из-за присутствия полимеров в DES. Воспаление, вызванное полимерами, может, в свою очередь, приводить к формирования тромба из-за физиологического иммунного ответа организма. Сформированный таким образом тромб может быть острым тромбом или подострым тромбом. Тромб может далее увеличиваться, приводя к блокированию артерии. Кроме того, DES с неразлагаемыми полимерами связаны с поздними воспалительными реакциями, тем самым приводя к позднему формированию тромба. Таким образом, полимеры, используемые для загрузки лекарственных средств на DES, могут приводить к рестенозу.
[0003] Для того чтобы избежать воспаления, которое связано с использованием полимеров для загрузки лекарственного средства на стент, лекарственное средство может быть загружено на поверхность стента без использования полимеров. Тем не менее, способы для загрузки лекарственного средства на поверхность стента без использования полимеров, которые хорошо известны в данном уровне техники, основаны на модифицировании поверхности стента.
[0004] Кроме того, присутствие одного или нескольких лекарственных средств и полимеров на внутренней поверхности стента приводит к замедленному заживлению или неправильному заживлению повреждений по сравнению с непокрытыми металлическими стентами. Длительная антитромбоцитарная (например, клопидрогель) терапия, как правило, рекомендуется пациентам с замедленным заживлением или неправильным заживлением. Антитромбоцитарная терапия также связана с побочными эффектами и, таким образом, не рекомендуется на длительный период.
[0005] Далее, размер частиц лекарственных средств, а также полимеров, которые наносятся на DES, больше, чем размеры пор ткани в месте назначения. Следовательно, существенное количество лекарственных средств остается неабсорбированным. Неабсорбированные лекарственные средства могут вымываться в кровоток и могут вызывать побочные эффекты. Например, используемые в настоящее время DES загружаются с более чем 100 микрограмми лекарственного средства, из которых только 12 нанограмм - 25 нанограмм лекарственного средства проникают сквозь ткани артерии. Остаток лекарственного средства либо вымывается в кровоток с внутренней поверхности DES, либо высвобождается с течением времени.
[0006] Кроме того, используемые в настоящее время DES связаны с таким явлением как фокальный рестеноз и краевой рестеноз. Одной из главных причин фокального рестеноза является то, что некоторые участки повреждения снабжаются лекарственным средством в достаточной мере с помощью DES, тогда как некоторые участки повреждения (область, не покрытая DES) очень плохо или вообще не снабжаются лекарственным средством с помощью DES. Участки повреждения, которые снабжаются лекарственным средством в достаточной мере, могут вероятно оставаться менее предрасположенными к рестенозу по сравнению с участками повреждения, которые плохо снабжаются или не снабжаются вообще лекарственным средством.
[0007] В современных DES лекарственное средство наносят на металлическую поверхность. Количество лекарственного средства, которое достигает повреждения, как правило, равно соотношению металла к артерии. Соотношение металла к артерии для современных DES, как правило, находится в диапазоне от 10% до 20%. Таким образом, только 10% до 20% повреждения снабжается лекарственным средством. Тогда как оставшиеся 80%-90% повреждения либо очень плохо снабжаются лекарственным средством, либо вообще не снабжаются лекарственным средством. Кроме того, по причине большего размера частиц лекарственного средства, нанесенного на поверхность DES, оптимальная диффузия лекарственного средства в ткани артерии не достигается. Диффузия лекарственного средства в ткани артерии дополнительно зависит от свойств лекарственного средства. Например, сиролимус-элюирующие стенты проявляют низкую диффузию сиролимуса в ткани артерии из-за низкой растворимости, связанной с сиролимусом. Следовательно, сиролимус-элюирующие стенты могут проявлять фокальный рестеноз, который составляет вплоть до 71% общего рестеноза. Тогда как паклитаксел-элюирующие стенты могут проявлять фокальный рестеноз, который составляет вплоть до 56% общего рестеноза. Дополнительно, большинство лекарственных средств, которые вводят пациенту, используя современные DES, являются гидрофобными по природе и имеют меньшее сродство к тканям организма. В результате высокое количество лекарственного средства необходимо загрузить в DES для достижения желательного терапевтического эффекта.
[0008] Следовательно, существует необходимость в данной области техники в улучшенном доставляющем лекарственное средство вводимом медицинском устройстве, которое связано с уменьшенными случаями фокального рестеноза, краевого рестеноза, общего рестеноза, острого формирования тромба, подострого формирования тромба, позднего формирования тромба, замедленного заживления повреждений и неправильного заживления повреждений. Дополнительно, в данной области техники необходимо улучшенное доставляющее лекарственное средство вводимое медицинское устройство, которое может снижать длительность антитромбоцитарной терапии, которая в ином случае рекомендуется пациентам с замедленным заживлением повреждений и/или неправильным заживлением повреждений после установки DES. Кроме того, в данной области техники также необходимо улучшенное высвобождающее лекарственное средство медицинское устройство, которое обеспечивает усиленную биодоступность лекарственных средств, усиленную биосовместимость и доставку лекарственного средства к главному участку повреждения в кровеносном сосуде с оптимальной загрузкой лекарственным средством.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
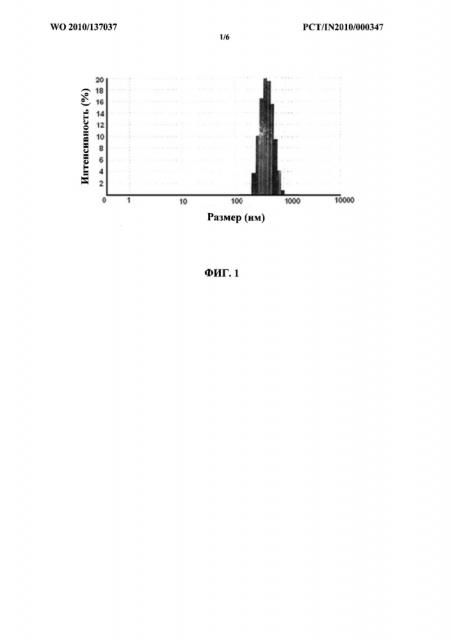
[0009] ФИГ. 1 иллюстрирует распределение по размерам наночастиц фосфолипида сои при определении с помощью Malvem ZS90 согласно Примеру 1.
[0010] ФИГ. 2 иллюстрирует распределение по размерам наноносителей при определении с помощью Malvem ZS90 согласно Примеру 1.
[ООН] ФИГ. 3 иллюстрирует хроматограмму для стандартного раствора согласно Примеру 2.
[0012] ФИГ. 4 иллюстрирует хроматограмму для раствора образца согласно Примеру 2.
[0013] ФИГ. 5 иллюстрирует хроматограмму для водного раствора наноносителей согласно Примеру 3.
[0014] ФИГ. 6 иллюстрирует процентное высвобождение сиролимуса из стентовой системы с покрытием для Дня 1 - Дня 39 согласно Примеру 4.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0015] Перед подробным описанием вариантов осуществления согласно изобретению следует отметить, что варианты осуществления заключаются в первую очередь в комбинациях компонентов медицинского устройства для лечения медицинского состояния, связанного с просветом части организма. Соответственно, компоненты были описаны с включением только тех конкретных деталей, которые имеют отношение к пониманию вариантов осуществления данного изобретения с тем, чтобы не затруднять понимание раскрытия деталями, которые будут очевидны специалистам в данной области, извлекающим пользу из приведенного в данном документе описания.
[0016] В этом документе выражения "включает", "включающий" или любая другая их вариация подразумеваются как охватывающие неисключающее включение так, что процесс, способ, изделие или аппарат, которые включают перечень элементов, не включает только такие элементы, но может включать другие элементы, не перечисленные конкретно или присущие такому процессу, способу, изделию или аппарату. Элемент, которому предшествует "включает..." не исключает, без больших ограничений, существование дополнительных идентичных элементов в процессе, способе, изделии или аппарате, который включает элемент.
[0017] Далее, перед подробным описанием вариантов осуществления согласно изобретению, следует отметить, что все научные и технические термины, используемые в данном документе для описания изобретения, имеют такие же значения, которые понятны специалисту в данной области техники.
[0018] Кроме того, перед подробным описанием вариантов осуществления согласно изобретению, следует отметить, что доставляющее лекарственное средство вводимое медицинское устройство может быть медицинским устройством, которое может быть введено в просвет части организма для доставки лекарственного средства к месту назначения в просвете части организма. Доставляющее лекарственное средство вводимое медицинское устройство может быть одним из, например, стента, баллона, стента, установленного на баллоне, (предварительно сжатый стент) и баллонного катетера. Доставляющее лекарственное средство вводимое медицинское устройство может быть любым другим медицинским устройством, используемым для проведения процедур чрезкожной транслюминальной ангиопластики, которая может доставить наноносители лекарственного средства к месту назначения, не отклоняясь от объема изобретения.
[0019] Стент может быть одним из, например, эндоваскулярного стента, периферического васкулярного стента, уретрального стента, простатического стента, стента-трансплантата, перманентно имплантируемого стента, временно имплантируемого стента и стента, изготовленного из одного или более чем одного или более из, но не ограничиваясь, металла, сплава, биоразлагаемого полимера и неразлагаемого полимера, SS316L, L605 сплава кобальта и хрома, и сплава никеля и титана, и любого стента, который может быть покрыт наноносителями лекарственного средства. Дополнительно, стент может быть любым стентом, покрытым одним или более из, но не ограничиваясь, разлагаемого полимера, биосовместимого полимера, биоразрушаемого полимера и неразлагаемого полимера.
[0020] Баллон может быть любым баллоном, изготовленным из эластомерного материала, который может быть расширен, используя пригодные средства для расширения в процедурах чрезкожной транслюминальной ангиопластики и который может быть покрыт наноносителями лекарственного средства для доставки двух или более наноносителей к месту назначения в просвете части организма. Баллон может быть одним из, например, баллона для ангиопластики и любого другого баллона, используемого для интервенционных процедур на сердечно-сосудистой системе.
[0021] Предварительно сжатый стент может быть стентом, установленным на баллоне, так что предварительно сжатый стент может быть покрыт наноносителями лекарственного средства, когда стент установлен на баллоне. Предварительно сжатый стент может дополнительно включать два или более из баллона, стента, установленного на баллоне, штифта и гипотрубки.
[0022] Дополнительно, доставляющее лекарственное средство вводимое медицинское устройство может быть одним из, например, спинального имплантата, чрескожного имплантата, устройства трансдермальной доставки лекарственного средства, зубного имплантата, любого хирургического имплантата и медицинского устройства, которое может быть введено в организм человека для доставки одного или более лекарственных средств в конкретное место в организме человека.
[0023] Следует отметить, что в дальнейшем наноносители лекарственного средства могут также называться как один или более из наноносителей, первого комплекта наноносителей, второго комплекта наноносителей, третьего комплекта наноносителей и двух или более наноносителей.
[0024] В общем, согласно различным вариантам осуществления раскрывается доставляющее лекарственное средство вводимое медицинское устройство для лечения медицинского состояния, связанного с просветом части организма. Медицинское состояние может быть одним из рестеноза, заблокированного просвета части организма, атеросклероза, инфаркта миокарда и скопления бляшек в просвете части организма. Просвет части организма может быть, например, кровеносным сосудом, уретрой, пищеводом, мочеточником и желчным протоком.
[0025] Доставляющее лекарственное средство вводимое медицинское устройство имеет внешнюю поверхность, покрытую двумя или более наноносителями. Внешняя поверхность доставляющего лекарственное средство вводимого медицинского устройства вступает в прямой контакт с местом назначения в просвете части организма, когда доставляющее лекарственное средство вводимое медицинское устройство накачивается или расширяется при установке в месте назначения. Наноноситель из двух или более наноносителей содержит лекарственное средство, окруженное инкапсулирующей средой. Так как лекарственное средство окружено инкапсулирующей средой, то поверхность наноносителей свободна от лекарственного средства. Инкапсулирующая среда содержит одно или несколько из биологического средства, наполнителя на основе крови и фосфолипида. Два или более наноносителей имеют два или более средних диаметров. Наноноситель из двух или более наноносителей имеет средний диаметр, приемлемый для проникновения сквозь один или более слоев из двух или более слоев просвета части организма. Когда доставляющее лекарственное средство вводимое медицинское устройство приближается к месту назначения в просвете части организма, два или более наноносителей высвобождаются с внешней поверхности. После этого Наноноситель из двух или более наноносителей проникает сквозь один или более слоев из двух или более слоев просвета части организма исходя из среднего диаметра. Таким образом, достигается зависимое от размера проникновение наноносителя сквозь один или более слоев из двух или более слоев просвета части организма.
[0026] В варианте осуществления доставляющее лекарственное средство вводимое медицинское устройство используется для лечения медицинского состояния, связанного с кровеносным сосудом. Кровеносный сосуд может быть одним из, например, коронарной артерии, периферической артерии, сонной артерии, почечной артерии, подвздошной артерии, артерий ниже колена и вены. Кровеносный сосуд имеет два или несколько слоев тканей. Два или несколько слоев тканей включают слой интимы, средний слой и адвентициальный слой. Слой интимы включает наиболее внутренний слой тканей кровеносного сосуда, который находится в прямом контакте с кровотоком через кровеносный сосуд. Средний слой включает слой тканей кровеносного сосуда, который находится под слоем интимы. Тогда как адвентициальный слой включает слой тканей кровеносного сосуда, который находится под средним слоем.
[0027] Внешняя поверхность доставляющего лекарственное средство вводимого медицинского устройства покрыта двумя или более наноносителями. В иллюстративном варианте осуществления, когда предварительно сжатый стент используется в качестве доставляющего лекарственное средство вводимого медицинского устройства, внешняя поверхность, такая как один или более участков аблюминальной поверхности предварительно сжатого стента и один или более участков баллона, которые выходили через предварительно сжатый стент, покрыты двумя или более наноносителями. Согласно различным вариантам осуществления только внешняя поверхность доставляющего лекарственное средство вводимого медицинского устройства покрыта двумя или более наноносителями. Тогда как внутренняя поверхность доставляющего лекарственное средство вводимого медицинского устройства, по сути, свободна от двух или более наноносителей. Соответственно, в иллюстративном варианте осуществления, когда доставляющее лекарственное средство вводимое медицинское устройство представляет собой стент, только аблюминальная поверхность стента покрыта двумя или более наноносителями. Тогда как люминальная поверхность стента, по сути, свободна от двух или более наноносителей. Такое селективное покрытие внешней поверхности может минимизировать случаи замедленного заживления.
[0028] Соответственно, когда доставляющее лекарственное средство медицинское устройство приближается к кровеносному сосуду, наноноситель из двух или более наноносителей может проникать сквозь один или более из слоя интимы, среднего слоя и адвентициального слоя исходя из среднего диаметра, связанного с наноносителем. Наноноситель проникает сквозь один или более из слоя интимы, среднего слоя и адвентициального слоя путем прохождения через одну или более из межтканевых пор, присутствующих в слое интимы, сосудах сосудов, связанных со средним слоем, и сосудах сосудов, связанных с адвентициальным слоем. Межтканевые поры, присутствующие в слое интимы, сосудах сосудов, связанных со средним слоем, и сосудах сосудов, связанных с адвентициальным слоем, имеют различные внутренние диаметры. Следовательно, проникновение наноносителя из двух или более наноносителей в один или более из слоя интимы, среднего слоя и адвентициального слоя зависит от среднего диаметра, связанного с наноносителем.
[0029] Два или более наноносителей, нанесенных на внешнюю поверхность доставляющего лекарственное средство медицинского устройства, имеют два или более средних диаметров. Два или более средних диаметров могут быть в диапазоне от 1 нм до 5000 нм.
[0030] В варианте осуществления доставляющее лекарственное средство медицинское устройство может быть покрыто первым комплектом наноносителей, вторым комплектом наноносителей и третьим комплектом наноносителей. Первый комплект наноносителей имеет первый средний диаметр, приемлемый для проникновения сквозь слой интимы через межтканевые поры, присутствующие в слое интимы. Второй комплект наноносителей имеет второй средний диаметр, приемлемый для проникновения сквозь средний слой через сосуды сосудов, связанные со средним слоем, и межтканевые поры, присутствующие в слое интимы. Третий комплект наноносителей имеет третий диаметр, приемлемый для проникновения сквозь адвентициальный слой через межтканевые поры, присутствующие в слое интимы, сосуды сосудов, связанные со средним слоем, и сосуды сосудов, связанные с адвентициальным слоем.
[0031] В варианте осуществления первый средний диаметр может быть в диапазоне от 800 нм до 1500 нм, второй средний диаметр может быть в диапазоне от 300 нм до 800 нм и третий средний диаметр может быть в диапазоне от 10 нм до 300 нм. В другом варианте осуществления первый средний диаметр составляет 1000 нм, второй средний диаметр составляет 700 нм и третий средний диаметр составляет 200 нм. Первый средний диаметр, второй средний диаметр и третий средний диаметр могут быть изменены, чтобы соответствовать конкретной терапевтической необходимости, не отклоняясь от объема изобретения.
[0032] Два или более наноносителей, нанесенные на доставляющее лекарственное средство медицинское устройство, могут включать 10%-60% первого комплекта наноносителей, 20%-60% второго комплекта наноносителей и 30%-80% третьего комплекта наноносителей. Альтернативно, два или более наноносителей могут быть нанесены так, чтобы включать от приблизительно 15% до 90% первого комплекта наноносителей, 10%-85% второго комплекта наноносителей и 5%-85% третьего комплекта наноносителей.
[0033] Соответственно, когда доставляющее лекарственное средство медицинское устройство приближается к месту назначения в кровеносном сосуде, два или более наноносителей, соответствующих одному или более из первого комплекта наноносителей, второго комплекта наноносителей и третьего комплекта наноносителей, высвобождаются с внешней поверхности доставляющего лекарственное средство вводимого медицинского устройства. Затем два или более наноносителей, высвобожденные таким образом, проникают сквозь один или более слоев кровеносного сосуда исходя из соответствующих средних диаметров, связанных с двумя или более наноносителями. Таким образом, достигается зависимое от размера проникновение двух или более наноносителей.
[0034] Кроме зависимого от размера проникновения двух или более наноносителей, скорость, при которой наноноситель высвобождается с внешней поверхности доставляющего лекарственное средство медицинского устройства, также контролируется с помощью среднего диаметра наноносителя. Наноноситель с маленьким средним диаметром быстро высвобождается доставляющим лекарственное средство медицинским устройством. Следовательно, время, необходимое для третьего комплекта наноносителей для высвобождения с внешней поверхности при приближении к месту назначения является меньшим, чем время, необходимое для второго комплекта наноносителей и первого комплекта наноносителей, чтобы высвободиться с внешней поверхности. Таким образом, третий комплект наноносителей проявляет быструю скорость высвобождения с внешней поверхности. Тогда как второй комплект наноносителей и третий комплект наноносителей проявляют более медленные скорости высвобождения с внешней поверхности по сравнению со скоростью высвобождения третьего комплекта наноносителей.
[0035] Как только два или более наноносителей высвобождаются и проникают сквозь один или более слоев кровеносного сосуда, лекарственное средство высвобождается из двух или более наноносителей в один или более из адвентициального слоя, среднего слоя и слоя интимы. Лекарственное средство высвобождается, когда инкапсулирующая среда растворяется. Таким образом, достигается внутритканевое высвобождение лекарственного средства в месте назначения. Дополнительно, один или более наноносителей, которые проникают в адвентициальный слой, могут оставаться в адвентициальном слое в течение пролонгированного периода времени. Другими словами, адвентициальный слой может действовать как резервуар лекарственного средства, из которого лекарственное средство медленно высвобождается в течение пролонгированного периода времени.
[0036] Дополнительно, лекарственное средство может дополнительно диффундировать сквозь один или более из адвентициального слоя, среднего слоя и слоя интимы в течение пролонгированного периода времени. В таком случае, лекарственное средство, которое диффундирует сквозь один или более из адвентициального слоя, среднего слоя и слоя интимы может обеспечивать внутритканевую диффузию лекарственного средства в течение пролонгированного периода времени. Таким образом, благодаря внутритканевому высвобождению лекарственного средства и внутритканевой диффузии лекарственного средства главный участок повреждений в месте назначения снабжается лекарственным средством. Следовательно, возможные шансы фокального рестеноза снижаются по сравнению с традиционными DES.
[0037] Кроме того, благодаря внутритканевому высвобождению лекарственного средства и внутритканевой диффузии лекарственного средства в течение пролонгированного периода времени случаи замедленного заживления и неправильного заживления повреждений в месте назначения минимизируются по сравнению с традиционными DES. В результате антитромбоцитарная терапия, которую приходится предоставлять пациентам с замедленным заживлением и/или неправильным заживлением повреждений, может также быть минимизирована.
[0038] Кроме того, так как инкапсулирующая среда включает одно или несколько из биологического средства, наполнителя на основе крови и фосфолипида, два или более наноносителей проявляют сродство к тканям места назначения. Такое сродство облегчает эффективный перенос двух или более наноносителей с внешней поверхности доставляющего лекарственное средство вводимого медицинского устройства к месту назначения с течением времени. В результате, по сути, каждый из первого комплекта наноносителей, второго комплекта наноносителей и третьего комплекта наноносителей высвобождается с внешней поверхности с течением времени. После этого внешняя поверхность доставляющего лекарственное средство вводимого медицинского устройства может становится, по сути, свободной от двух или более наноносителей с течением времени. В иллюстративном варианте осуществления, где доставляющее лекарственное средство вводимое устройство представляет собой стент, стент может становится, по сути, свободным от двух или более наноносителей в течение 7-45 дней после установки стента в месте назначения. В другом иллюстративном варианте осуществления стент может становится, по сути, свободным от двух или более наноносителей в течение приблизительно 30 дней от установки стента.
[0039] Кроме того, инкапсулирующая среда также поддерживает поверхность наноносителя свободной от любого свободного лекарственного средства. Это способствует устранению прямого контакта лекарственного средства с поверхностью доставляющего лекарственное средство вводимого медицинского устройства. Дополнительно, лекарственное средство вступает в контакт с тканями места назначения, только когда наноноситель проникает в один или более слоев кровеносного сосуда и инкапсулирующая среда растворяется. Таким образом, предотвращается прямое воздействие лекарственного средства на ткани места назначения и поверхность доставляющего лекарственное средство вводимого медицинского устройства.
[0040] Лекарственное средство может включать нанокристаллы лекарственного средства. Нанокристаллы лекарственного средства могут имеют средний диаметр, находящийся в диапазоне от 1 нм до 5000 нм. Дополнительно, нанокристаллы лекарственного средства могут иметь два или более различных средних диаметров. Альтернативно, лекарственное средство может быть одним или несколькими из наноразмерных частиц, наносфер, липосом, нанокапсул, дендримеррв и любой другой подобной формы лекарственного средства, которая имеет наноразмеры. Лекарственное средство может быть одним или несколькими, но не ограничиваясь, из антипролиферативного средства, противовоспалительного средства, антинеопластического средства, антикоагулянтного средства, антифибринового средства, антитромботического средства, антимитотического средства, антибиотика, противоаллергического средства и антиоксиданта, антипролиферативного средства, эстрогенов, ингибитора протеазы, антител, иммуносупрессорного средства, цитостатического средства, цитотоксического средства, блокатора кальциевого канала, ингибитора фосфодиэстеразы, ингибитора простогландина, пищевой добавки, витаминов, средства против агрегации тромбоцитов и генетически сконструированных эпителиальных клеток.
[0041] Лекарственное средство может быть одним или несколькими, например, но не ограничиваясь, из сиролимуса, паклитаксела, такролимуса, клобетазола, дексаметазона, генистеина, гепарина, 17 бета-эстрадиола, рапамицина, эверолимуса, этилрапамицина, зотаролимуса, АВТ-578, биолиму са А9, доцетаксела, метотрексата, азатиоприна, винкристина, винбластина, фторурацила, доксорубицина гидрохлорида, митомицина и его аналогов, миомицина, гепарина натрия, низкомолекулярного гепарина, гепариноида, гирудина, аргатробана, форсколина, вапипроста, простациклина, аналога простациклина, декстрана, D-phe-pro-arg-хлорметилкетона, дипиридамола, гликопротеина IIb/IIIа, рекомбинантного гирудина, бивалирудина, нифедипина, колхицинов, ловастатина, нитропруссида, сурамина, блокатора серотонина, стероида, ингибитора тиопротеазы, триазолопиримидина, оксида азота или донора оксида азота, супероксиддисмутазы, миметика супероксиддисмутазы, эстрадиола, аспирина, ангиопептина, каптоприла, цилазаприла, лизиноприла, пермироласта калия, альфа-интерферона, биологически активных RGD и любых их солей или аналогов.
[0042] Лекарственное средство окружено инкапсулирующей средой. Инкапсулирующая среда может быть одним или несколькими из биологического средства, наполнителя на основе крови и фосфолипида. Альтернативно, инкапсулирующая среда может быть одним или несколькими из одного или нескольких биологических средств, одного или нескольких наполнителей на основе крови, одного или нескольких фосфлипидов и одного или нескольких наполнителей. Биологическое средство может включать наночастицы биологического средства. Наночастицы биологического средства могут иметь средний диаметр, находящийся в диапазоне от 1 нм до 5000 нм. Дополнительно, наночастицы биологического средства могут иметь два или более различных средних диаметров. Альтернативно, биологическое средство может включать одно или несколько из наноразмерных частиц, наносфер, липосом, нанокапсул, дендримеров и любой другой подобной формы биологического средства, которая имеет наноразмеры.
[0043] Биологическое средство может быть одним или несколькими, но не ограничиваясь, из носителей лекарственного средства, наполнителей, компонентов крови, наполнителей, полученных из крови, встречающихся в природе фосфлипидов, твердых липидных наночастиц, фосфлипидов, полученных из живых животных, синтетически полученных фосфлипидов, липоидов, витаминов и молекул сахара. Биологическое средство может быть, например, но не ограничиваясь, стероидами, витаминами, эстрадиолом, эстерифицированными жирными кислотами, неэстерифицированными жирными кислотами, глюкозой, инозитом, L-лактатом, липопротеинами, углеводами, трикальцийфосфатом, осажденным фосфатом кальция, трехосновным фосфатом кальция, веществами, полученными из по меньшей мере одного из человека, яйца и сои, фосфолипоном ВОН, фосфолипоном 90Н, липоидами S75, липоидами Е80, интралипидом 20, липоидом ЕРС, липоидом Е75, липидами, полученными из яйца, липидами, полученными из сои, фосфатидилхолином, фосфатидилглицерином, фосфатидилинозитолом, фосфатидилсерином, фосфатидной кислотой, кардиолипином и фосфатидилэтаноламином.
[0044] Фосфолипид может включать наночастицы фосфолипида. Наночастицы фосфолипида могут иметь средний диаметр, находящийся в диапазоне от 1 нм до 5000 нм. Дополнительно, наночастицы фосфолипида могут иметь два или более различных средних диаметров. Альтернативно, фосфолипид может включать одно или несколько из наноразмерных частиц, наносфер, липосом, нанокапсул, дендримеров и любой другой подобной формы фосфолипида, которая имеет наноразмеры. Фосфолипид может включать одно или несколько из, но не ограничиваясь, липидов, полученных из яйца, липидов, полученных из сои, фосфатидилхолина, фосфатидилглицерина, фосфатидилинозитола, фосфатидилсерина, фосфатидной кислоты, кардиолипина и фосфатидилэтаноламина.
[0045] Наполнитель на основе крови может включать наночастицы наполнителя на основе крови. Наночастицы наполнителя на основе крови могут имеют средний диаметр, находящийся в диапазоне от 1 нм до 5000 нм. Дополнительно, наночастицы наполнителя на основе крови могут иметь два или более различных средних диаметров. Альтернативно, наполнитель на основе крови может включать одно или несколькими из наноразмерных частиц, наносфер, липосом, нанокапсул, дендримеров и любой другой подобной формы наполнителя на основе крови, которая имеет наноразмеры. Наполнитель на основе крови может быть одним или несколькими из, но не ограничиваясь, стероидов, витаминов, эстрадиола, эстерифицированных жирных кислот, неэстерифицированных жирных кислот, глюкозы, инозита, L-лактата, липидов, липопротеинов, фосфолипида, углеводов, трикальцийфосфата, осажденного фосфата кальция и трехосновного фосфата кальция.
[0046] Наполнитель на основе крови и биологическое средство растворимы при рН менее 7,4. Следовательно, когда два или более наноносителей вступают в контакт с тканями места назначения, то биологическое средство и наполнитель на основе крови становятся растворимыми в крови. Растворение биологического средства и наполнителя на основе крови приводит к высвобождению лекарственного средства из двух или более наноносителей в месте назначения. Таким образом, достигается рН-зависимое высвобождение лекарственного средства из двух или более наноносителей.
[0047] В иллюстративном варианте осуществления доставляющее лекарственное средство вводимое медицинское устройство представляет собой коронарный стент. Коронарный стент представляет собой, например, хромокобальтовый L-605 стент. Коронарный стент включает аблюминальную (внешнюю) поверхность, покрытую двумя или более наноносителями. Два или более наноносителей включают первый комплект наноносителей со средним диаметром приблизительно 1200 нм, второй комплект наноносителей со средним диаметром приблизительно 700 нм и третий комплект наноносителей со средним диаметром приблизительно 200 нм. Когда стент приближается к месту назначения, два или более наноносителей высвобождаются с аблюминальной поверхности стента. После этого первый комплект наноносителей проникает сквозь слой интимы через межтканевые поры, присутствующие в слое интимы. Второй комплект наноносителей проникает сквозь средний слой через сосуды сосудов, связанные со средним слоем, и межтканевые поры, присутствующие в слое интимы. Третий комплект наноносителей проникают сквозь адвентицию через сосуды сосудов, связанные с адвентициальным слоем, сосуды сосудов, связанные со средним слоем, и межтканевые поры, присутствующие в слое интимы.
[0048] В другом иллюстративном варианте осуществления доставляющее лекарственное средство вводимое медицинское устройство представляет собой баллон. Баллон представляет собой, например, ультратонкий баллон для ангиопластики. Баллон имеет внешнюю поверхность, покрытую двумя или более наноносителями. Два или более наноносителей включают первый комплект наноносителей со средним диаметром приблизительно 1200 нм, второй комплект наноносителей со средним диаметром приблизительно 700 нм и третий комплект наноносителей со средним диаметром приблизительно 200 нм. Когда баллон накачивают при приближении к месту назначения, два или более наноносителей высвобождаются с аблюминальной поверхности стента. После этого, первый комплект наноносителей проникает сквозь слой интимы через межтканевые поры, присутствующие в слое интимы. Второй комплект наноносителей проникает сквозь средний слой через сосуды сосудов, связанные со средним слоем, и межтканевые поры, присутствующие в слое интимы. Третий комплект наноносителей проникает сквозь адвентицию через сосуды сосудов, связанные с адвентициальным слоем, сосуды сосудов, связанные со средним слоем, и межтканевые поры, присутствующие в слое интимы. Баллон может быть покрыт двумя или более наноносителями, когда баллон находится в свернутой конфигурации или развернутой конфигурации.
[0049] В еще одном иллюстративном варианте осуществления доставляющее лекарственное средство вводимое медицинское устройство представляет собой предварительно сжатый стент (стент, установленный на баллоне). Например, предварительно сжатый стент представляет собой хромокобальтовый L-605 стент, установленный на ультратонком баллоне для ангиопластики. Предварительно сжатый стент покрыт двумя или более наноносителями. Наноноситель из двух или более наноносителей, нанесенный на предварительно сжатый стент, включает нанокристаллы сиролимуса, инкапсулированные с наночастицами одного или более из фосфолипида сои и трикальцийфосфата. Два или более наноносителей включают первый комплект наноносителей со средним диаметром 1200 нм, второй комплект наноносителе