Тиазолилфенилбензолсульфонамидопроизводные в качестве ингибиторов киназ
Иллюстрации
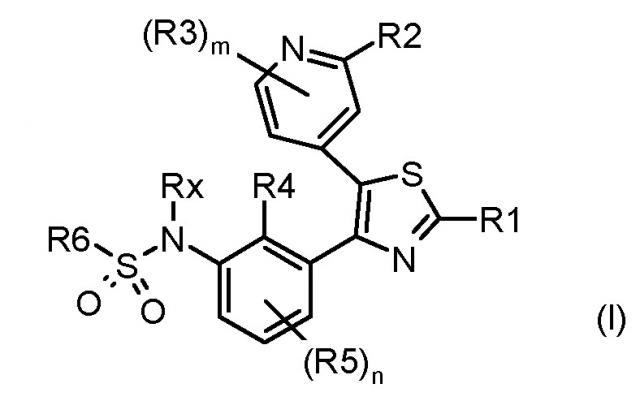
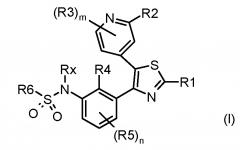
Показать всеИзобретение относится к соединению формулы (I), где каждый из n и m независимо равен 1; R1 представляет собой галоген или группу, выбранную из прямого или разветвленного (C1-C8)алкила и гетероциклила, выбранного из пиперидинила и тетрагидропиранила, где пиперидинил необязательно замещен (C1-C6)алкилом и (С3-С6)циклоалкилом; или R1 представляет собой NR7R8, где каждый из R7 и R8 независимо представляет собой водород или группу, выбранную из прямого или разветвленного (C1-C8)алкила, гетероциклила, выбранного из пиперидинила и необязательно замещенного метилом; или, взятые вместе с атомом азота, с которым они связаны, R7 и R8 могут образовывать необязательно замещенный 3-8-членный гетероциклил, необязательно содержащий один дополнительный гетероатом или гетероатомную группу, выбранные из О, N и NH, необязательно замещенный галогеном; каждый из R2 и R3 независимо представляет собой водород, галоген или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила и гетероциклила, выбранного из имидазолидина, замещенного -СОСН3, -С=O, -СН2-ОСН3, -СН3; или каждый из R2 и R3 независимо представляет собой NR17R18, где R17 и R18 независимо представляют собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (С1-С8)алкила, необязательно замещенного -NH-СОСН3, -NHCOOCH3, -N(CH3)2; или R17 представляет собой водород и R18 представляет собой COR22, где R22 представляет собой OR23 или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, где R23 представляет прямой или разветвленный (С1-С8)алкил, каждый из R4 и R5 независимо представляет собой водород или галоген; Rx представляет собой водород; R6 представляет собой фенил, необязательно замещенный галогеном; или его фармацевтически приемлемой соли. Изобретение относится к способу ингибирования in vitro активности семейства Raf, который включает контактирование указанного рецептора с эффективным количеством соединения, формулы (I). Соединение формулы (I) или его фармацевтически приемлемая соль предназначены для применения в качестве лекарственного средства или в составе фармацевтической композиции, с активностью, направленной против злокачественной опухоли. Технический результат – тиазолилфенилбензолсульфонамидопроизводные в качестве ингибиторов киназ семейства Raf. 5 н. и 5 з.п. ф-лы, 1 табл., 22 пр.
Реферат
Настоящее изобретение относится к определенным замещенным тиазолилфенилбензолсульфонамидо соединениям, которые модулируют активность протеинкиназ. Таким образом, соединения по настоящему изобретению могут быть использованы для лечения заболеваний, вызываемых нарушением регуляции активности протеинкиназ. Также настоящее изобретение относится к способам получения этих соединений, фармацевтическим композициям, содержащим эти соединения, и к способам лечения заболеваний с использованием фармацевтических композиций, содержащих эти соединения.
Классический каскад Ras, Raf, MEK (активируемая митогеном протеинкиназа/киназа регулируемой внеклеточным сигналом киназы), ERK (регулируемая внеклеточным сигналом киназа) играет центральную роль в регуляции различных клеточных функций, в зависимости от клеточного контекста, включая пролиферацию, дифференцировку, выживание, иммортализацию и ангиогенез клеток (рассмотрено в Peyssonnaux and Eychene, Biology of the Cell, 2001, 93, 3-62). В этом каскаде представители семейства Raf привлекаются к плазматической мембране при связывании с Ras, нагруженной гуанозинтрифосфатом (GTP), что приводит к фосфорилированию и активации белков Raf. Затем активированные Raf фосфорилируют и активируют MEK, которые в свою очередь фосфорилируют и активируют ERK. При активации ERK транслоцируются из цитоплазмы в ядро, что приводит к фосфорилированию и регуляции активности факторов транскрипции, таких как Elk-I и Myc. Описано, что Ras/Raf/MEK/ERK вносит вклад в онкогенный фенотип путем индукции иммортализации, роста, независимого от факторов роста, нечувствительности к ингибирующим рост сигналам, способности к инвазии и метастазированию, путем стимуляции ангиогенеза и путем ингибирования апоптоза (рассмотрено в Kolch et al., Exp. Rev. Mol. Med., 2002, 25 April, http://www.expertreviews.org/02004386h.htm). Действительно, фосфорилирование ERK повышено приблизительно в 30% всех опухолей человека (Hoshino et al., Oncogene, 1999, 18, 813-822). Это может быть результатом сверхэкспрессии и/или мутации ключевых представителей каскада.
Описаны три изоформы серин/треониновой протеинкиназы Raf: Raf-1/C-Raf, B-Raf и A-Raf (рассмотрено в Mercer and Pritchard, Biochim. Biophys. Acta, 2003, 1653, 25-40), гены для которых, как полагают, появились в результате дупликации гена. Все три гена Raf экспрессируются в большинстве тканей, но с отличиями: C-Raf экспрессируется повсеместно на высоких уровнях, в то время как экспрессия B-Raf на высоком уровне встречается в нейрональной ткани, а экспрессия A-Raf встречается в тканях мочеполовых путей. Высоко гомологичные представители семейства Raf имеют перекрывающиеся, но отличающиеся биохимические виды активности и биологические функции (Hagemann and Rapp, Expt. Cell Res. 1999, 253, 34-46). Экспрессия всех трех генов Raf требуется для нормального развития мышей, однако как C-Raf, так и B-Raf, требуются для завершения гестации. Мыши B-Raf -/- погибают на сроке E12,5 вследствие сосудистой геморрагии, вызываемой повышенным апоптозом эндотелиальных клеток (Wojnowski et al. Nature Genet., 1997, 16, 293-297). Описано, что B-Raf является главной изоформой, вовлеченной в пролиферацию клеток, и является первичной мишенью онкогенной Ras. Активирующие соматические миссенс-мутации были идентифицированы исключительно для B-Raf, встречающихся с частотой 66% в злокачественных меланомах кожи (Davies et al., Nature, 2002, 417, 949-954) и также присутствующих в широком диапазоне злокачественных опухолей человека, включая, но не ограничиваясь ими, папиллярные опухоли щитовидной железы (Cohen et al., J. Natl. Cancer Inst., 2003, 95, 625-627), холангиокарциномы (Tannapfel et al., Gut, 2003, 52, 706-712), рак толстого кишечника и рак яичника (Davies et al., Nature, 2002, 417, 949-954). Наиболее частой мутацией в B-Raf (80%) является замещение глутаминовой кислотой валина в положении 600. Эти мутации увеличивают базальную активность киназы B-Raf, и полагают, что они разобщают передачу сигнала Raf/MEK/ERK от вышележащих механизмов включения пролиферации, включая активацию Ras и рецепторов факторов роста, что приводит к конститутивной активации ERK. Мутантные белки B-Raf являются трансформирующими в клетках NIH3T3 (Davies et al., Nature, 2002, 15 417, 949-954) и меланоцитах (Wellbrock et al., Cancer Res., 2004, 64, 2338-2342) и также было показано, что они необходимы для жизнеспособности и трансформации клеток меланомы (Hingorani et al., Cancer Res., 2003, 63, 5198-5202). В качестве ключевого запускающего фактора каскада передачи сигнала Raf/MEK/ERK, B-Raf представляет собой возможную точку вмешательства в опухоли, зависимые от этого каскада.
Замещенные производные тиазола для лечения опосредуемых протеинкиназами заболеваний, таких как злокачественная опухоль, описаны в WO 2009/137391 на имя SKB & Co, в WO 2011/059610 на имя Glaxosmithkline LLC и в WO 2011/161216 на имя Novartis AG.
Авторы настоящего изобретения открыли, что соединения формулы (I), описанные ниже, являются ингибиторами киназ и, таким образом, пригодны в терапии в качестве противоопухолевых средств.
Таким образом, первой задачей настоящего изобретения является предоставление замещенного тиазолилфенилбензолсульфонамидо соединения, соответствующего формуле (I)
где:
каждый из n и m независимо равен 1 или 2;
R1 представляет собой водород, галоген, циано или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, (C3-C8)циклоалкенила, гетероциклила, арила и гетероарила; или R1 представляет собой NR7R8 или COR9,
где:
каждый из R7 и R8 независимо представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, (C3-C8)циклоалкенила, гетероциклила, арила и гетероарила; или, взятые вместе с атомом азота, с которым они связаны, R7 и R8 могут образовывать необязательно замещенный 3-8-членный гетероциклил, необязательно содержащий один дополнительный гетероатом или гетероатомную группу, выбранные из S, O, N и NH; или
R7 представляет собой водород и R8 представляет собой COR10,
где:
R10 представляет собой OR11, NR12R13 или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, (C3-C8)циклоалкенила, гетероциклила, арила и гетероарила, где:
R11 представляет собой необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила;
каждый из R12 и R13 независимо представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила; или, взятые вместе с атомом азота, с которым они связаны, R12 и R13 могут образовывать необязательно замещенный 3-8-членный гетероциклил или гетероарил, необязательно содержащий один дополнительный гетероатом или гетероатомную группу, выбранные из S, O, N и NH;
R9 представляет собой OR14 или NR15R16, где:
R14 представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила;
каждый из R15 и R16 независимо представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила; или, взятые вместе с атомом азота, с которым они связаны, R15 и R16 могут образовывать необязательно замещенный 3-8-членный гетероциклил или гетероарил, необязательно содержащий один дополнительный гетероатом или гетероатомную группу, выбранные из S, O, N и NH;
каждый из R2 и R3 независимо представляет собой водород, галоген, циано или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, (C3-C8)циклоалкенила, гетероциклила, арила и гетероарила; или каждый из R2 и R3 независимо представляет собой NR17R18, CONR19R20, OR21, SR21 или SO2R21,
где:
R17 и R18 независимо представляют собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила; или, взятые вместе с атомом азота, с которым они связаны, R17 и R18 могут образовывать необязательно замещенный 3-8-членный гетероциклил или гетероарил, необязательно содержащий один дополнительный гетероатом или гетероатомную группу, выбранные из S, O, N и NH; или
R17 представляет собой водород и R18 представляет собой COR22,
где:
R22 представляет собой OR23, NR24R25 или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, (C3-C8)циклоалкенила, гетероциклила, арила и гетероарила, где:
R23 представляет собой необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, (C3-C8)циклоалкенила, гетероциклила, арила и гетероарила, и
каждый из R24 и R25 независимо представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила: или, взятые вместе с атомом азота, с которым они связаны, R24 и R25 могут образовывать необязательно замещенный 3-8-членный гетероциклил или гетероарил, необязательно содержащий один дополнительный гетероатом или гетероатомную группу, выбранные из S, O, N и NH;
каждый из R19 и R20 независимо представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила; или, взятые вместе с атомом азота, с которым они связаны, R19 и R20 могут образовывать необязательно замещенный 3-8-членный гетероциклил или гетероарил, необязательно содержащий один дополнительный гетероатом или гетероатомную группу, выбранные из S, O, N и NH;
R21 представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, гетероциклила, арила и гетероарила;
или R2 и R3, взятые вместе, могут быть частью гетероциклила, арила или гетероарила, когда m равно 1, и R3 находится в положении 3 ядра пиридина;
каждый из R4 и R5 независимо представляет собой водород, галоген, трифторметил, трихлорметил, циано, OR26 или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила и (C3-C8)циклоалкила, где:
R26 представляет собой водород или необязательно замещенную группу, выбранную из прямого или разветвленного (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила и (C3-C8)циклоалкила;
Rx представляет собой водород, необязательно замещенный прямой или разветвленный (C1-C3)алкил, необязательно замещенную (C2-C6)ацильную группу или необязательно замещенную (C2-C6)алкоксикарбонильную группу;
R6 представляет собой необязательно замещенную группу, выбранную из прямого или разветвленного (C2-C8)алкенила, (C2-C8)алкинила, (C3-C8)циклоалкила, (C3-C8)циклоалкенила, гетероциклила, арила и гетероарила;
или его фармацевтически приемлемых солей.
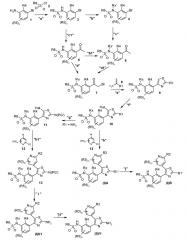
Также настоящее изобретение относится к способам получения замещенных тиазолилфенилбензолсульфонамидо соединений, соответствующих формуле (I), получаемых с помощью процесса, состоящего из стандартных синтетических преобразований.
Также настоящее изобретение относится к способу лечения заболеваний, вызываемых и/или ассоциированных с нарушением регуляции активности протеинкиназы, в частности, семейства Raf, ABL, ACK1, AKT1, ALK, AUR1, AUR2, BRK, BUB1, CDC7/DBF4, CDK2/CYCA, CHK1, CK2, EEF2K, EGFR1, EphA2, EphB4, ERK2, FAK, FGFR1, FLT3, GSK3-бета, Haspin, IGFR1, IKK2, IR, JAK1, JAK2, JAK3, KIT, LCK, LYN, MAPKAPK2, MELK, MET, MNK2, MPS1, MST4, NEK6, NIM1, P38-альфа, PAK4, PDGFR, PDK1, PERK, PIM1, PIM2, PKA-альфа, PKC-бета, PLK1, RET, ROS1, SULU1, Syk, TLK2, TRKA, TYK, VEGFR2, VEGFR3, ZAP70, более конкретно семейства Raf, который включает введение млекопитающему, нуждающемуся в этом, эффективного количества замещенного тиазолилфенилбензолсульфонамидо соединения, соответствующего формуле (I), как определено выше.
Предпочтительным способом по настоящему изобретению является лечение заболевания, вызываемого и/или ассоциированного с нарушением регуляции активности протеинкиназ, выбранного из группы, состоящей из злокачественной опухоли, нарушений пролиферации клеток, вирусных инфекций, аутоиммунных и нейродегенеративных нарушений.
Другим предпочтительным способом по настоящему изобретению является лечение конкретных типов злокачественной опухоли, включая, но не ограничиваясь ими: карциному, такую как карцинома мочевого пузыря, молочной железы, толстого кишечника, почки, печени, легкого, включая мелкоклеточный рак легкого, карциному пищевода, желчного пузыря, яичника, поджелудочной железы, желудка, шейки матки, щитовидной железы, предстательной железы и кожи, включая плоскоклеточную карциному; гемопоэтические опухоли лимфоидного ростка, включая лейкоз, острый лимфоцитарный лейкоз, острый лимфобластный лейкоз, B-клеточную лимфому, T-клеточную лимфому, лимфому Ходжкина, неходжскинскую лимфому, волосатоклеточную лимфому и лимфому Беркитта; гемопоэтические опухоли миелоидного ростка, включая острые и хронические миелогенные лейкозы, миелодиспластический синдром и промиелоцитарный лейкоз; опухоли мезенхимного происхождения, включая фибросаркому и рабдомиосаркому; опухоли центральной и периферической нервной системы, включая астроцитому, нейробластому, глиому и шванномы; другие опухоли, включая меланому, семиному, тератокарциному, остеосаркому, пигментную ксеродерму, кератоксантому, фолликулярный рак щитовидной железы и саркому Капоши.
Другим предпочтительным способом по настоящему изобретению является лечение определенных клеточно-пролиферативных нарушений, например, таких как доброкачественная гиперплазия предстательной железы, семейный аденоматоз, полипоз, нейрофиброматоз, псориаз, пролиферация гладкомышечных клеток сосудов, ассоциированная с атеросклерозом, фиброзом легких, артритом, гломерулонефритом и послеоперационным стенозом и рестенозом.
Другим предпочтительным способом по настоящему изобретению является лечение вирусных инфекций, в частности, профилактика развития СПИД у ВИЧ-инфицированных индивидуумов.
Другим предпочтительным способом по настоящему изобретению является лечение ассоциированных с иммунными клетками заболеваний и нарушений, таких как воспалительные и аутоиммунные заболевания, например, рассеянный склероз, системная красная волчанка, воспалительные заболевания кишечника (IBD), болезнь Крона, синдром раздраженной кишки, панкреатит, язвенный колит, дивертикулез, миастения gravis, васкулит, псориаз, склеродермия, астма, аллергия, системная склеродермия, витилиго, артрит, такой как остеоартрит, ювенильный ревматоидный артрит, анкилозирующий спондилит.
Другим предпочтительным способом по настоящему изобретению является лечение нейродегенеративных нарушений, таких как болезнь Альцгеймера, болезнь Паркинсона и болезнь Гентингтона.
Кроме того, способ по настоящему изобретению также предусматривает ингибирование ангиогенеза в опухоли и метастазирования опухоли, а также лечение отторжения трансплантата органа и реакции "хозяин против трансплантата".
В следующем предпочтительном варианте осуществления способ по настоящему изобретению дополнительно включает воздействие на млекопитающего, нуждающегося в этом, режима лучевой терапии или химиотерапии в комбинации по меньшей мере с одним цитостатическим или цитотоксическим средством.
Более того, изобретение относится к способу ингибирования in vitro активности белков семейства Raf, который включает контактирование указанного белка с эффективным количеством соединения формулы (I).
Также настоящее изобретение относится к фармацевтической композиции, содержащей одно или несколько соединений формулы (I) или их фармацевтически приемлемые солей и фармацевтически приемлемый эксципиент, носитель или разбавитель.
Кроме того, настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы (I), в комбинации с известным способом лечения злокачественной опухоли, таким как режим лучевой терапии или химиотерапии в комбинации с цитостатическими или цитотоксическими средствами, средствами типа антибиотиков, алкилирующими средствами, антиметаболитными средствами, гормональными средствами, иммунологическими средствами, средствами типа интерферонов, ингибиторами циклооксигеназы (например, ингибиторы COX-2), ингибиторами матриксной металлопротеиназы, ингибиторами теломеразы, ингибиторами тирозинкиназы, средствами против рецепторов факторов роста, средствами против HER, средствами против EGFR, антиангиогенными средствами (например, ингибиторы ангиогенеза), ингибиторами фарнезилтрансферазы, ингибиторами каскада передачи сигнала RAS-RAF, ингибиторами клеточного цикла, другими ингибиторами Cdk, связывающими тубулин средствами, ингибиторами топоизомеразы I, ингибиторами топоизомеразы II и т.п. Кроме того, изобретение относится к продукту или набору, содержащим соединение формулы (I) или его фармацевтически приемлемую соль, как определено выше, или их фармацевтические композиции и одно или несколько химиотерапевтических средств, в качестве комбинированного препарата для одновременного, отдельного или последовательного применения в терапии против злокачественной опухоли.
В другом аспекте изобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, как определено выше, для применения в качестве лекарственного средства.
Более того, изобретение относится к применению соединения формулы (I) или его фармацевтически приемлемой соли, как определено выше, для изготовления лекарственного средства с противоопухолевой активностью.
Наконец, изобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, как определено выше, для применения в способе лечения злокачественной опухоли.
Если нет иных указаний, при указании на соединения формулы (I) непосредственно, а также на любую их фармацевтическую композицию или на любое медикаментозное лечение, включающее их, настоящее изобретение включает все изомеры, таутомеры, гидраты, сольваты, комплексы, метаболиты, пролекарства, носители, N-оксиды и фармацевтически приемлемые соли соединений по настоящему изобретению.
Метаболит соединения формулы (I) представляет собой любое соединение, в которое это соединение формулы (I) преобразуется in vivo, например, при введении млекопитающему, нуждающемуся в этом. Как правило, но в качестве неограничивающего примера, при введении соединения формулы (I) это производное может преобразовываться в различные соединения, например, включающие более растворимые производные, такие как гидроксилированные производные, которые легко экскретируются. Таким образом, в зависимости от метаболического каскада, протекающего таким путем, любое из этих гидроксилированных производных может быть воспринято как метаболит соединений формулы (I).
Пролекарства представляют собой любые ковалентно связанные соединения, которые высвобождают in vivo активное исходное лекарственное средство формулы (I).
N-оксиды представляют собой соединения формулы (I), где азот и кислород связаны через донорно-акцепторную связь.
Если в соединении по настоящему изобретению присутствует хиральный центр или другая форма изомерного центра, подразумевается, что все формы такого изомера или изомеров, включая энантиомеры и диастереомеры, охватываются настоящим изобретением. Соединения, содержащие хиральный центр, можно использовать в качестве рацемической смеси или энантиомерно обогащенной смеси, или рацемическую смесь можно разделять с использованием хорошо известных способов и отдельный энантиомер можно использовать отдельно. В случаях, когда соединения имеют ненасыщенные углерод-углеродные двойные связи, как цис(Z)-, так и транс(E)-изомеры входят в объем настоящего изобретения.
В случаях, когда соединения могут существовать в таутомерных формах, предусматривается, что каждая форма включена в настоящее изобретение, существуя либо в равновесии, либо с преобладанием одной формы.
В случаях, когда соединения могут существовать в других таутомерных формах, таких как кето-енольные таутомеры, предусматривается, что каждая таутомерная форма включена в настоящее изобретение, существуя либо в равновесии, либо с преобладанием одной формы.
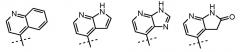
В случаях, когда m равно 1 и R3 находится в положении 3 ядра пиридина, R2 и R3, взятые вместе, могут быть частью гетероциклила, арила или гетероарила, так что в таком случае предусматривается группа, изображенная ниже:
Неограничивающими примерами таких групп являются:
Под термином "прямой или разветвленный (C1-C8)алкил" понимают любую из групп, например, такую как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втор-бутил, н-пентил, н-гексил, н-гептил, н-октил и т.п.
Под термином "прямой или разветвленный (C1-C6)алкил" понимают любую из групп, например, такую как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втор-бутил, н-пентил, н-гексил и т.п.
Под термином "прямой или разветвленный (C1-C3)алкил", понимают любую из групп, например, такую как метил, этил, н-пропил, изопропил.
Под термином "(C3-C8)циклоалкил" понимают, если нет иных указаний, 3-8-членное полностью углеродное моноциклическое кольцо, которое может содержать одну или несколько двойных связей, но не имеет полностью сопряженной π-электронной системы. Примерами циклоалкильных групп являются, но не ограничиваясь ими, циклопропан, циклобутан, циклопентан, циклопентен, циклогексан, циклогексен и циклогексадиен.
Под термином "гетероциклил" понимают 3-8-членное насыщенное или частично ненасыщенное карбоциклическое кольцо, где один или несколько атомов углерода заменены гетероатомами, такими как азот, кислород и сера. Неограничивающими примерами гетероциклильных групп являются, например, пиран, пирролидин, пирролин, имидазолин, имидазолидин, пиразолидин, пиразолин, тиазолин, тиазолидин, дигидрофуран, тетрагидрофуран (THF), 1,3-диоксолан, пиперидин, пиперазин, морфолин и т.п.
Под термином "(C2-C8)алкенил" понимают алифатическую (C2-C8)углеводородную цепь, содержащую по меньшей мере одну углерод-углеродную двойную связь, и которая может быть прямой или разветвленной. Репрезентативные примеры включают, но не ограничиваются ими, этенил, 1-пропенил, 2-пропенил, 1- или 2-бутенил и т.п.
Под термином "(C2-C8)алкинил" понимают алифатическую (C2-C8)углеводородную цепь, содержащую по меньшей мере одну углерод-углеродную тройную связь, и которая может быть прямой или разветвленной. Репрезентативные примеры включают, но не ограничиваются ими, этинил, 1-пропинил, 2-пропинил, 1- или 2-бутинил и т.п.
Термин "арил" относится к моно-, би- или поли-карбоциклическому углеводороду с 1-4 кольцевыми системами, необязательно дополнительно конденсированными или связанными друг с другом одинарными связями, где по меньшей мере одно из карбоциклических колец является "ароматическим", где термин "ароматический" относится к системе с полностью сопряженной π-электронной связью. Неограничивающими примерами таких арильных групп являются фенильная, α- или β-нафтильная или бифенильная группы.
Термин "гетероарил" относится к ароматическим гетероциклическим кольцам, как правило, 5-8-членным гетероциклам с 1-3 гетероатомами, выбранными из N, O или S; гетероарильное кольцо может быть необязательно дополнительно конденсированным или связанным с ароматическими и неароматическими карбоциклическими и гетероциклическими кольцами. Неограничивающими примерами таких гетероарильных групп являются, например, пиридил, пиразинил, пиримидинил, пиридазинил, индолил, имидазолил, тиазолил, изотиазолил, пирролил, фенилпирролил, фурил, фенилфурил, оксазолил, изоксазолил, пиразолил, тиенил, бензотиенил, изоиндолинил, бензоимидазолил, хинолинил, изохинолинил, 1,2,3-триазолил, 1-фенил-1,2,3-триазолил, 2,3-дигидроиндолил, 2,3-дигидробензофуранил, 2,3-дигидробензотиофенил; бензопиранил, 2,3-дигидробензоксазинил, 2,3-дигидрохиноксалинил и т.п.
В соответствии с настоящим изобретением и если не предусмотрено иное, любая из указанных выше групп Rx, R1, R2, R3, R4, R5 и R6 может быть необязательно замещенной в любом из ее свободных положений одной или несколькими группами, например 1-6 группами, независимо выбранными из: галогена, нитро, оксогруппы (=O), циано, (C1-C8)алкила, полифторированного алкила, полифторированного алкокси, (C2-C8)алкенила, (C2-C8)алкинила, гидроксиалкила, арила, арилалкила, гетероарила, гетероарилалкила, гетероциклила, гетероциклилалкила, (C3-C8)циклоалкила, гидрокси, алкокси, арилокси, гетероциклилокси, метилендиокси, алкилкарбонилокси, арилкарбонилокси, циклоалкенилокси, гетероциклилкарбонилокси, алкилиденаминоокси, карбокси, алкоксикарбонила, арилоксикарбонила, циклоалкилоксикарбонила, гетероциклилалкилоксикарбонил-амино, уреидо, алкиламино, диалкиламино, ариламино, диариламино, гетероциклиламино, формиламино, алкилкарбониламино, арилкарбониламино, гетероциклилкарбониламино, аминокарбонила, алкиламинокарбонила, диалкиламинокарбонила, ариламинокарбонила, гетероциклиламинокарбонила, алкоксикарбониламино, гидроксиаминокарбонилалкоксиимино, алкилсульфониламино, арилсульфониламино, гетероциклилсульфониламино, формила, алкилкарбонила, арилкарбонила, циклоалкилкарбонила, гетероциклилкарбонила, алкилсульфонила, арилсульфонила, аминосульфонила, алкиламиносульфонила, диалкиламиносульфонила, ариламиносульфонила, гетероциклиламиносульфонила, арилтио, алкилтио, фосфоната и алкилфосфоната. В свою очередь, когда это является пригодным, каждый из описанных выше заместителей может быть дополнительно замещен одной или несколькими из упомянутых выше групп.
Под термином "галоген" понимают фтор, хлор, бром или иод.
Под термином "циано" понимают остаток -CN.
Под термином "нитро" понимают группу -NO2.
Под термином "полифторированный алкил" или "полифторированный алкокси" понимают любую из указанных выше прямых или разветвленных (C1-C8)алкильных или алкоксигрупп, которые замещены более чем одним атомом фтора, например, такую как трифторметил, трифторэтил, 1,1,1,3,3,3-гексафторпропил, трифторметокси и т.п.
Под термином "гидроксиалкил" понимают любой из указанных выше (C1-C8)алкилов, имеющий гидроксильную группу, например, такой как гидроксиметил, 2-гидроксиэтил, 3-гидроксипропил и т.п.
Из вышесказанного специалисту в данной области очевидно, что любая группа, название которой является составным названием, как например, ариламино, традиционно следует толковать по частям, из которых она происходит, например, как аминогруппа, которая дополнительно замещена арилом, где арил является таким, как определено выше.
Аналогично, любой из терминов, например, такой как алкилтио, алкиламино, диалкиламино, алкоксикарбонил, алкоксикарбониламино, гетероциклилкарбонил, гетероциклилкарбониламино, циклоалкилоксикарбонил и т.п., включает группы, где алкильная, алкокси, арильная, (C3-C8)циклоалкильная и гетероциклильная части являются такими, как определено выше.
Фармацевтически приемлемые соли соединений формулы (I) включают кислотно-аддитивные соли с неорганическими или органическими кислотами, например, азотной, хлористоводородной, бромистоводородной, серной, перхлорной, фосфорной, уксусной, трифторуксусной, пропионовой, гликолевой, молочной, щавелевой, фумаровой, малоновой, яблочной, малеиновой, виннокаменной, лимонной, бензойной, коричной, миндальной, метансульфоновой, изотионовой и салициловой кислотой.
Фармацевтически приемлемые соли соединений формулы (I) также включают соли с неорганическими или органическими основаниями, например, щелочными или щелочноземельными металлами, особенно гидроксиды, карбонаты или бикарбонаты натрия, калия, кальция, аммония или магния, ациклические или циклические амины, предпочтительно метиламин, этиламин, диэтиламин, триэтиламин, пиперидин и т.п.
Предпочтительным классом соединений формулы (I) являются соединения, где:
R1 представляет собой NR7R8 или необязательно замещенный гетероциклил, где R7 и R8 являются такими, как определено выше.
Более предпочтительным классом соединений формулы (I) являются соединения, где:
R2 представляет собой водород или группу NR17R18, где R17 и R18 являются такими, как определено выше.
Еще более предпочтительным классом соединений формулы (I) являются соединения, где:
R2 представляет собой группу NR17R18, где R17 представляет собой водород и R18 представляет собой COR22, где R22 является таким, как определено выше.
Наиболее предпочтительным классом соединений формулы (I) являются соединения, где:
R3 представляет собой водород, R4 представляет собой галоген и R5 представляет собой водород или галоген.
Следующим наиболее предпочтительным классом соединений формулы (I) являются соединения, где:
Rx представляет собой водород и R6 представляет собой необязательно замещенную фенильную группу.
Предпочтительные конкретные соединения (cmpd.) формулы (I) или их фармацевтически приемлемые соли представляют собой соединения, приведенные ниже:
1) N-{3-[2-амино-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2,4-дифторфенил}-2,5-дифторбензолсульфонамид;
2) N-{2,4-дифтор-3-[2-(метиламино)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}-2,5-дифторбензолсульфонамид;
3) N-{3-[2-(диэтиламино)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2,4-дифторфенил}-2,5-дифторбензолсульфонамид;
4) N-(2,4-дифтор-3-{2-[(2-метилпропил)амино]-5-(пиридин-4-ил)-1,3-тиазол-4-ил}фенил)-2,5-дифторбензолсульфонамид;
5) N-(2,4-дифтор-3-{2-[(2-метоксиэтил)амино]-5-(пиридин-4-ил)-1,3-тиазол-4-ил}фенил)-2,5-дифторбензолсульфонамид;
6) N-{2,4-дифтор-3-[2-(пиперидин-4-иламино)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}-2,5-дифторбензолсульфонамид;
7) N-(3-{2-[циклогексил(метил)амино]-5-(пиридин-4-ил)-1,3-тиазол-4-ил}-2,4-дифторфенил)-2,5-дифторбензолсульфонамид;
8) N-{2,4-дифтор-3-[2-(4-метилпиперазин-1-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}-2,5-дифторбензолсульфонамид;
9) N-{2,4-дифтор-3-[2-(пиперидин-1-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}-2,5-дифторбензолсульфонамид;
10) N-(3-{2-[4-(диметиламино)пиперидин-1-ил]-5-(пиридин-4-ил)-1,3-тиазол-4-ил}-2,4-дифторфенил)-2,5-дифторбензолсульфонамид;
11) N-{3-[2-(1,4-диокса-8-азаспиро[4.5]дец-8-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2,4-дифторфенил}-2,5-дифторбензолсульфонамид;
12) N-{2,4-дифтор-3-[2-(4-оксопиперидин-1-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}-2,5-дифторбензолсульфонамид;
13) N-{2,4-дифтор-3-[2-(4-гидроксипиперидин-1-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}-2,5-дифторбензолсульфонамид;
14) N-{3-[2-(4,4-дифторпиперидин-1-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2,4-дифторфенил}-2,5-дифторбензолсульфонамид;
15) N-{2,4-дифтор-3-[2-(морфолин-4-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}-2,5-дифторбензолсульфонамид;
16) N-{3-[2-(диэтиламино)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
17) N-{3-[2-(1,4-диокса-8-азаспиро[4.5]дец-8-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
18) N-{3-[2-(4,4-дифторпиперидин-1-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
19) 2,5-дифтор-N-{2-фтор-3-[2-(1-метилпиперидин-4-ил)-5-(пиридин-4-ил)-1,3-тиазол-4-ил]фенил}бензолсульфонамид;
20) 2,5-дифтор-N-{2-фтор-3-[5-(пиридин-4-ил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-4-ил]фенил}бензолсульфонамид;
21) N-{3-[2-(1-циклопропилпиперидин-4-ил)-5-(пиридин-4-ил)- 1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
22) N-{3-[5-(2-аминопиридин-4-ил)-2-(1-циклопропилпиперидин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
23) N-{4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(1-метилпиперидин-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}ацетамид;
24) N-{3-[5-(2-аминопиридин-4-ил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
25) 2,5-дифтор-N-(2-фтор-3-{5-[2-(метиламино)пиридин-4-ил]-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-4-ил}фенил)бензолсульфонамид;
26) 2,5-дифтор-N-{2-фтор-3-[2-(1-метилпиперидин-4-ил)-5-(2-метилпиридин-4-ил)-1,3-тиазол-4-ил]фенил}бензолсульфонамид;
27) 2,5-дифтор-N-{2-фтор-3-[5-(2-фторпиридин-4-ил)-2-(1-метилпиперидин-4-ил)-1,3-тиазол-4-ил]фенил}бензолсульфонамид;
28) 2,5-дифтор-N-{2-фтор-3-[5-(2-метилпиридин-4-ил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-4-ил]фенил}бензолсульфонамид;
29) N-{4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(1-метилпиперидин-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}-2-метилпропанамид;
30) N-{4-[2-(1-циклопропилпиперидин-4-ил)-4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-1,3-тиазол-5-ил]пиридин-2-ил}ацетамид;
31) N-{3-[2-(1-циклопропилпиперидин-4-ил)-5-(2-метилпиридин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
32) N-{3-[2-(1-циклопропилпиперидин-4-ил)-5-(2-фторпиридин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
33) N-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2,6-дифторфенил)-5-(пиридин-4-ил)-1,3-тиазол-2-ил]ацетамид;
34) 2,5-дифтор-N-{2-фтор-3-[5-(3-фторпиридин-4-ил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-4-ил]фенил}бензолсульфонамид;
35) N-{4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}ацетамид;
36) N-[2-({4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}амино)этил]ацетамид;
37) N-(3-{2-(1-циклопропилпиперидин-4-ил)-5-[2-(метиламино)пиридин-4-ил]-1,3-тиазол-4-ил}-2-фторфенил)-2,5-дифторбензолсульфонамид;
38) 2,5-дифтор-N-(2-фтор-3-{5-[2-(метиламино)пиридин-4-ил]-2-(1-метилпиперидин-4-ил)-1,3-тиазол-4-ил}фенил)бензолсульфонамид;
39) N-{3-[5-(2-аминопиридин-4-ил)-2-(1-метилпиперидин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
40) N-{3-[5-(2-{[2-(диметиламино)этил]амино}пиридин-4-ил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
41) метил [(2S)-1-({4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(тетрагидро-2H-пиран-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}амино)пропан-2-ил]карбамат;
42) N-{4-[2-трет-бутил-4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-1,3-тиазол-5-ил]пиридин-2-ил}ацетамид;
43) N-{3-[2-трет-бутил-5-(пиридин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
44) N-{4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(пиперидин-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}ацетамид;
45) метил [(2S)-1-({4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(1-метилпиперидин-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}амино)пропан-2-ил]карбамат;
46) 2,5-дифтор-N-{2-фтор-3-[5-(3-фторпиридин-4-ил)-2-(1-метилпиперидин-4-ил)-1,3-тиазол-4-ил]фенил}бензолсульфонамид;
47) N-{4-[4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-2-(1-этилпиперидин-4-ил)-1,3-тиазол-5-ил]пиридин-2-ил}ацетамид;
48) метил [(2S)-1-({4-[2-(1-циклопропилпиперидин-4-ил)-4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-1,3-тиазол-5-ил]пиридин-2-ил}амино)пропан-2-ил]карбамат;
49) N-{3-[2-(1-циклопропилпиперидин-4-ил)-5-(3-фторпиридин-4-ил)-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
50) N-{3-[5-(2-аминопиридин-4-ил)-2-трет-бутил-1,3-тиазол-4-ил]-2-фторфенил}-2,5-дифторбензолсульфонамид;
51) N-(3-{2-трет-бутил-5-[2-(метиламино)пиридин-4-ил]-1,3-тиазол-4-ил}-2-фторфенил)-2,5-дифторбензолсульфонамид и
52) метил [(2S)-1-({4-[2-трет-бутил-4-(3-{[(2,5-дифторфенил)сульфонил]амино}-2-фторфенил)-1,3-тиазол-5-ил]пиридин-2-ил}амино)пропан-2-ил]карбамат.
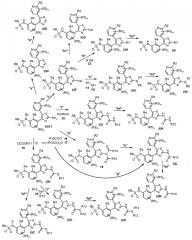
Также настоящее изобретение относится к способу получения соединения формулы (I), как определено выше, с использованием путей реакций и синтетических схем, описанных ниже,