Агонисты рецепторов нейротрофинов и их применение в качестве лекарственных средств
Иллюстрации
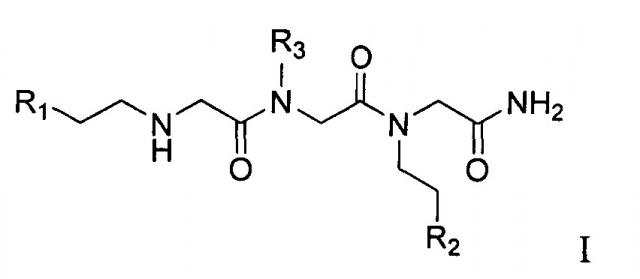
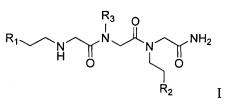
Показать всеИзобретение относится к соединениям, имеющим формулу II, или их фармацевтически приемлемым солям, которые обладают активностью агонистов рецепторов нейротрофинов. В формуле II R1 представляет собой фенил, замещенный галогеном или трифторметилом и дополнительно возможно замещенный одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-6алкила, (C1-6)алкокси и галоген(C1-6)алкила; R2 представляет собой 2-оксопирролидин-1-илметил или сульфамоилфенил. Изобретение относится также к фармацевтической композиции, способу ее получения, применению указанных соединений в качестве активного ингредиента для получения лекарственного средства для предотвращения или лечения различных заболеваний, в том числе для предотвращения или лечения гибели или повреждения нервных клеток, способам предотвращения или лечения гибели или повреждения нервных клеток, нейропротекции, регенерации нервных клеток, стимулирования активности рецептора нейротрофинового фактора, способам предотвращения или лечения различных заболеваний, в том числе восприимчивых к стимулированию активности фактора роста нервов или рецептора фактора роста нервов, нейротрофинового фактора или рецептора нейротрофинового фактора. 22 н. и 35 з.п. ф-лы, 14 ил., 17 пр.
Реферат
УРОВЕНЬ ТЕХНИКИ
[0001] Настоящая заявка испрашивает приоритет по более ранней дате подачи предварительной заявки на патент США №61/378823, поданной 31 августа 2010 года, полное содержание которой включено в настоящее описание посредством ссылки.
Область техники
[0002] Настоящее изобретение относится к области терапии неврологических, психических расстройств и старения. В частности, оно относится к нейропротекторному эффекту низкомолекулярных агонистов рецепторов нейротрофинов (фактора роста нервов (ФРН, NGF) или нейротрофического фактора головного мозга (BDNF)) и применению указанных агонистов в качестве лекарственных средств.
Уровень техники
[0003] Старение, неврологические и психические расстройства вызывают гибель и повреждение нервных клеток. Частые и соответствующие повреждения нервной системы могут возникать, среди прочего, в результате дегенерации нейронов, ишемии, воспаления, иммунных ответов, травмы и рака. Как следствие этого, нервные клетки могут погибнуть в течение минут или часов или пережить это первичное повреждение в пораженном состоянии, которое активирует нейродегенерацию и, равным образом, приводит к клеточной гибели.
[0004] С учетом важной роли нервной системы в обеспечении основных двигательных функций и восприятия, существует заинтересованность в поиске терапевтических средств для защиты нервной системы.
[0005] Нейропротекция ориентирована на сохранение, восстановление, лечение или регенерацию нервной системы, ее клеток, структуры и функции (Vajda et al., 2002). Целью нейропротекции является предотвращение или минимизация эффектов первоначального повреждения нервной системы или предотвращение или минимизация последствий эндогенных или экзогенных вредоносных процессов, вызывающих повреждение аксонов, нейронов, синапсов и дендритов.
[0006] В общем случае стратегии лечения часто основаны на модулировании единственного предполагаемого поражающего фактора. Несмотря на то, что была показана эффективность таких способов лечения в весьма ограниченных животных моделях, они с гораздо меньшей вероятностью окажутся эффективными в более сложном случае расстройства у человека, включающем более вариабельные степени тяжести поражения в генетически разнообразной популяции (Faden and Stoica, 2007). Важно отметить, что поскольку предполагаемые механизмы гибели нейронов являются сложными и многообразными, например, окислительный стресс, митохондриальная дисфункция, агрегация белков, апоптоз и воспаление (Youdim et al., 2005), желательно получение индивидуальных соединений, обладающих полипотентным действием на множественные механизмы поражения.
[0007] В стадии исследования находятся несколько нейропротекторных лекарственных средств, включая следующие классы: противовоспалительные агенты, NMDA-антагонисты (антагонисты N-метил-D-аспартатного (NMDA) рецептора), АМРА-антагонисты (антагонисты рецептора α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты (АМРА)), дексанабинол, блокаторы натриевых каналов, тиреотропин-рилизинг-гормон (ТРГ), факторы роста, глюкокортикоиды, кофеинол, антагонисты опиоидных рецепторов, ингибиторы апоптоза, ловушки/скэвенджеры свободных радикалов, эритропоэтин, блокаторы кальциевых каналов, сульфат магния и статины.
[0008] Способность этих фармакологических агентов ограничивать вторичное биохимическое повреждение и гибель клеток не оправдала надежд (Faden and Stoica, 2007).
[0009] Нейротрофины представляют собой факторы роста, которые регулируют развитие и поддержание периферической и центральной нервных систем (Lewin and Barde, 1996). Фактор роста нервов (ФРН) является первым обнаруженным и лучше всего изученным представителем семейства нейротрофинов, включающего другие структурно родственные белки, такие как нейротрофический фактор головного мозга (BDNF). Фактор роста нервов (ФРН) представляет собой гомодимерный белок из семейства нейротрофинов, который играет ключевую роль в выживаемости, дифференцировке и росте нейронов (Levi-Montalcini, 1987) и связывает два различных клеточных рецептора; тирозинкиназный рецептор TrkA и рецептор р75 (Chao, 2003). Связывание ФРН с TrkA активирует внутреннюю тирозинкиназную активность рецептора, вызывая фосфорилирование тирозина TrkA и связанных партнеров в сигнальном пути, что приводит к стимулированию выживания или дифференцировки клеток (Kaplan and Miller, 2000). Рецептор р75 является представителем суперсемейства рецепторов фактора некроза опухоли. В зависимости от клеточного окружения и типа лиганда, р75 может действовать в качестве трансдуктора сигналов выживания, апоптоза или дифференцировки (Barker, 1998; Rabizadeh et al., 1999; Zaccaro et al., 2001; Saragovi and Zaccaro, 2002). Соответственно, в зависимости от метаболического пути, связывание либо с рецептором TrkA, либо с рецептором р75 может запускать сигналы, в зависимости от рассматриваемого типа клеток, непонятным образом связанные с дифференцировкой и/или выживаемостью клеток. Нейротрофины действуют посредством двух основных сигнальных путей: пути фосфатидилинозитол-3-киназа (PI3K)-AKT и пути митоген-активируемая протеинкиназа (MAPK)-MEK (оба пути вовлечены в ингибирование апоптоза). Нейротрофические факторы, как известно, действуют также на зрелые нейроны и, в частности, на пораженные и дегенеративные клетки (Lindvall et al. 1994; Tuszynski and Gage 1995; Lykissas et al. 2007; Song et al. 2009).
[0010] Потенциал ФРН в качестве терапевтического средства для ряда заболеваний был показан несколькими исследователями. Такие заболевания включают нейродегенеративные расстройства, воспаления нервов и некоторые типы рака, рассеянный склероз, нейромиелит зрительного нерва, боковой амиотрофический склероз (БАС), болезнь Паркинсона, болезнь Альцгеймера, атаксию Фридрейха, болезнь Хантингтона, деменцию с тельцами Леви, спинальную мышечную атрофию, большое депрессивное расстройство, шизофрению, глаукому или периферические невропатии (диабетическую невропатию или невропатию при СПИДе) (Longo et al, 2007; Schulte-Herbruggen, 2007; Shi, 2007; Hellveg, 2008; Shoval, 2005; Apfel, 2002; Anand, 2004). ФРН обладает значительными иммунорегуляторными свойствами при воспалениях в ЦНС, участвуя в сохранении иммунной привилегии ЦНС (Villoslada and Genain, 2004). В модели экспериментального аутоиммунного энцефаломиелита (ЭАЭ) на мартышках ФРН подавлял развитие клинических симптомов при интрацеребровентрикулярном введении путем непрерывной инфузии, по-видимому, вследствие своей способности индуцировать иммуносупрессивное микроокружение в ЦНС, которое приводит к пониженной инфильтрации ЦНС (Villoslada et al., 2000). Тот факт, что ФРН вызывает подавление иммунного ответа при аутоиммунной демиелинизации в дополнение к его нейропротекторным свойствам в нейронах и олигодендроцитах делает его отличным кандидатом для лечения воспалительных заболеваний ЦНС, таких как рассеянный склероз (PC). Однако ФРН не является идеальным кандидатом на роль лекарственного средства из-за его неспособности проникать через гематоэнцефалический барьер (ГЭБ) (Poduslo and Curran, 1996), короткого периода полувыведения и побочных эффектов (Apfel, 2002). Было приложено много усилий для поиска малых молекул, обладающих активностью агонистов рецепторов ФРН, с улучшенными фармакокинетическими свойствами и меньшими побочными эффектами. Для достижения этой цели были опробованы различные подходы (Poduslo and Curran, 1996; Longo et al., 1997; Maliartchouk et al., 2000a; Maliartchouk et al., 2000b; Peleshok and Saragovi, 2006).
[0011] Таким образом, существует насущная потребность в обеспечении лекарственных средств, в частности миметиков ФРН, с нейропротекторными свойствами, имеющих предпочтительно полипотентное действие, но без присущих ФРН недостатков. Авторами настоящего изобретения было разработано семейство соединений, отличных от уже известных в данной области техники. Семейство соединений согласно изобретению представляет собой пептидомиметики нейротрофинов (ФРН, BDNF) и агонисты специфичных рецепторов TrkA, TrkB и р75. Некоторые из соединений согласно изобретению стимулируют, например, выживание клеток даже в более высокой степени, чем сам ФРН. Соединения согласно изобретению рассматриваются в качестве пептидомиметиков нейротрофинов, и все они имеют общую структуру N-алкилглициновых тримеров.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0012] Настоящее изобретение относится к применению пептоидных соединений нижеприведенных Формул I-V и их фармацевтически приемлемых солей и пролекарств в качестве агонистов рецепторов нейротрофинов и, в частности, рецепторов фактора роста нервов (ФРН) и рецепторов нейротрофического фактора головного мозга (BDNF).
[0013] Соединения, подходящие согласно настоящему изобретению, ранее не были описаны в литературе. Таким образом, один аспект настоящего изобретения относится к новым соединениям Формул I-V, а также их фармацевтически приемлемым солям и пролекарствам.
[0014] Другой аспект изобретения относится к применению соединений любой из Формул I-V и их фармацевтически приемлемых солей и пролекарств в качестве агонистов рецепторов ФРН. Другой аспект изобретения относится к применению соединений любой из Формул I-V и их фармацевтически приемлемых солей и пролекарств в качестве агонистов рецепторов BDNF.
[0015] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения в качестве лекарственного средства. В одном аспекте изобретения лекарственный препарат предназначен для применения для предотвращения или лечения гибели или повреждения нервных клеток. В одном аспекте изобретения лекарственное средство предназначено для применения для нейропротекции. В одном аспекте изобретения лекарственное средство предназначено для применения для регенерации нервных клеток. В одном аспекте изобретения лекарственное средство предназначено для применения для усиления когнитивных функций. В одном аспекте лекарственное средство предназначено для применения для предотвращения или лечения неврологического или психического заболевания. В одном аспекте изобретения лекарственное средство предназначено для применения для предотвращения или лечения заболевания, выбранного из группы, состоящей из неврологического заболевания, предпочтительно нейродегенеративного расстройства (такого как боковой амиотрофический склероз (БАС), болезнь Паркинсона, болезнь Альцгеймера, атаксия Фридрейха, болезнь Хантингтона, деменция с тельцами Леви и спинальная мышечная атрофия), воспаления нервов (такого как рассеянный склероз и нейромиелит зрительного нерва), большого депрессивного расстройства, шизофрении, глаукомы, периферической невропатии (такой как диабетическая невропатия или невропатия при СПИДе) и рака (такого как глиобластома, астроцитома, медуллобластома, невринома, нейробластома, менингиома, рак толстой кишки, рак поджелудочной железы, рак молочной железы, рак предстательной железы, лейкоз, острый лимфоцитарный лейкоз, остеосаркома, гепатоцеллюлярная карцинома, карцинома яичника, аденокарцинома легкого и карцинома пищевода).
[0016] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения в качестве лекарственного средства для лечения рассеянного склероза.
[0017] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения в качестве лекарственного средства, при этом лекарственное средство представляет собой лекарственное средство для лечения нейродегенеративных заболеваний.
[0018] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения в качестве лекарственного средства, при этом лекарственное средство представляет собой иммуномодулятор.
[0019] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения в качестве лекарственного средства, при этом лекарственное средство обладает комбинированным нейропротекторным и иммуномодулирующим действием.
[0020] Согласно следующему аспекту настоящего изобретения предложена фармацевтическая композиция, содержащая терапевтически эффективное количество по меньшей мере одного соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства и фармацевтически приемлемый носитель.
[0021] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения лекарственного средства для предотвращения или лечения гибели или повреждения нервных клеток.
[0022] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения лекарственного средства для обеспечения нейропротекции.
[0023] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения лекарственного средства для регенерации нервных клеток.
[0024] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения лекарственного средства для предотвращения или лечения неврологического заболевания или психического заболевания.
[0025] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения лекарственного средства для предотвращения или лечения заболевания, выбранного из группы, состоящей из неврологического заболевания, предпочтительно нейродегенеративного расстройства (такого как боковой амиотрофический склероз (БАС), болезнь Паркинсона, болезнь Альцгеймера, атаксия Фридрейха, болезнь Хантингтона, деменция с тельцами Леви и спинальная мышечная атрофия), воспаления нервов (такого как рассеянный склероз и нейромиелит зрительного нерва), большого депрессивного расстройства, шизофрении, глаукомы, периферической невропатии (такой как диабетическая невропатия или невропатия при СПИДе) и рака (такого как глиобластома, астроцитома, медуллобластома, невринома, нейробластома, менингиома, рак толстой кишки, рак поджелудочной железы, рак молочной железы, рак предстательной железы, лейкоз, острый лимфоцитарный лейкоз, остеосаркома, гепатоцеллюлярная карцинома, карцинома яичника, аденокарцинома легкого и карцинома пищевода).
[0026] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения лекарственного средства для предотвращения или лечения рассеянного склероза.
[0027] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения нейрорегенеративного лекарственного средства.
[0028] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения иммуномодулятора.
[0029] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения лекарственного средства, обладающего комбинированным нейропротекторным и иммуномодулирующим действием.
[0030] Согласно следующему аспекту изобретения предложено применение соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства для получения нейростимулирующего лекарственного средства.
[0031] Согласно следующему аспекту изобретения предложен способ предотвращения или лечения гибели или повреждения нервных клеток, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства или эффективного количества фармацевтической композиции, содержащей соединение любой из Формул I-V или его фармацевтически приемлемую соль или пролекарство.
[0032] Согласно следующему аспекту изобретения предложен способ обеспечения нейропротекции, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства или эффективного количества фармацевтической композиции, содержащей соединение любой из Формул I-V или его фармацевтически приемлемую соль или пролекарство.
[0033] Согласно следующему аспекту изобретения предложен способ обеспечения иммуномодулирования, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства или эффективного количества фармацевтической композиции, содержащей соединение любой из Формул I-V или его фармацевтически приемлемую соль или пролекарство.
[0034] Согласно следующему аспекту изобретения предложен способ регенерации нервных клеток, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства или эффективного количества фармацевтической композиции, содержащей соединение любой из Формул I-V или его фармацевтически приемлемую соль или пролекарство.
[0035] Согласно следующему аспекту изобретения предложен способ предотвращения или лечения заболевания, выбранного из группы, состоящей из неврологического заболевания, предпочтительно нейродегенеративного расстройства (такого как боковой амиотрофический склероз (БАС), болезнь Паркинсона, болезнь Альцгеймера, атаксия Фридрейха, болезнь Хантингтона, деменция с тельцами Леви и спинальная мышечная атрофия), воспаления нервов (такого как рассеянный склероз и нейромиелит зрительного нерва), большого депрессивного расстройства, шизофрении, глаукомы, периферической невропатии (такой как диабетическая невропатия или невропатия при СПИДе) и рака (такого как глиобластома, астроцитома, медуллобластома, невринома, нейробластома, менингиома, рак толстой кишки, рак поджелудочной железы, рак молочной железы, рак предстательной железы, лейкоз, острый лимфоцитарный лейкоз, остеосаркома, гепатоцеллюлярная карцинома, карцинома яичника, аденокарцинома легкого и карцинома пищевода), включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства или эффективного количества фармацевтической композиции, содержащей соединение любой из Формул I-V или его фармацевтически приемлемую соль или пролекарство.
[0036] Согласно следующему аспекту изобретения предложен способ предотвращения или лечения рассеянного склероза, болезни Альцгеймера, болезни Паркинсона или глаукомы, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства или эффективного количества фармацевтической композиции, содержащей соединение любой из Формул I-V или его фармацевтически приемлемую соль или пролекарство.
[0037] Согласно следующему аспекту изобретения предложен способ лечения заболевания, восприимчивого к стимулированию активности нейротрофинов или рецептора нейротрофинов, у млекопитающего, страдающего от недостаточного стимулирования указанной активности, включающий введение эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства.
[0038] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения для стимулирования активности нейротрофинов или рецептора нейротрофинов.
[0039] Согласно следующему аспекту настоящего изобретения предложен способ стимулирования активности рецепторов нейротрофинов у субъекта, нуждающегося в этом, включающий введение указанному субъекту соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства. В одном варианте реализации рецептор нейротрофинов представляет собой рецептор TrkA, рецептор TrkB или рецептор р75.
[0040] Согласно следующему аспекту изобретения предложен способ лечения заболевания, восприимчивого к стимулированию активности фактора роста нервов или рецептора фактора роста нервов, у млекопитающего, страдающего от недостаточного стимулирования указанной активности, включающий введение эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства.
[0041] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения для стимулирования активности фактора роста нервов или рецептора фактора роста нервов.
[0042] Согласно следующему аспекту настоящего изобретения предложен способ стимулирования активности рецептора фактора роста нервов у субъекта, нуждающегося в этом, включающий введение указанному субъекту соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства. В одном варианте реализации рецептор фактора роста нервов представляет собой рецептор TrkA или рецептор р75.
[0043] Согласно следующему аспекту изобретения предложен способ лечения заболевания, восприимчивого к стимулированию активности нейротрофического фактора головного мозга или рецептора нейротрофического фактора головного мозга, у млекопитающего, страдающего от недостаточного стимулирования указанной активности, включающий введение эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства.
[0044] Согласно следующему аспекту изобретения предложено соединение любой из Формул I-V или его фармацевтически приемлемая соль или пролекарство для применения в стимулировании активности нейротрофического фактора головного мозга или рецептора нейротрофического фактора головного мозга.
[0045] Согласно следующему аспекту настоящего изобретения предложен способ стимулирования активности рецептора нейротрофического фактора головного мозга у субъекта, нуждающегося в этом, включающий введение указанному субъекту соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства. В одном варианте реализации рецептор фактора роста нервов представляет собой рецептор TrkB или рецептор р75.
[0046] Согласно следующему аспекту настоящего изобретения предложен способ получения фармацевтической композиции, включающий смешивание эффективного количества соединения любой из Формул I-V или его фармацевтически приемлемой соли или пролекарства с фармацевтически приемлемым носителем.
[0047] Дополнительные варианты реализации и преимущества изобретения частично изложены в описании ниже и следуют из описания или могут быть обнаружены при реализации изобретения. Варианты реализации и преимущества изобретения будут осуществлены и достигнуты посредством элементов и комбинаций, отдельно указанных в прилагаемой формуле изобретения.
[0048] Следует понимать, что и вышеприведенное краткое описание, и последующее подробное описание представлены исключительно в качестве примера и пояснения и не ограничивают заявленное изобретение.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ/ФИГУР
[0049] ФИГ.1 иллюстрирует результаты согласно Примеру 2 для соединений G79, G80 и G81 в анализе влияния величины дозы на дифференцировку на линии клеток PC12. На ФИГ.1A показаны изображения клеток PC12, дифференцировавшихся в присутствии соединения G79. На ФИГ.1B показаны изображения клеток PC12, дифференцировавшихся в присутствии соединения G80. На ФИГ.1C показаны изображения клеток PC12, дифференцировавшихся в присутствии соединения G81. ФИГ.1D иллюстрирует количество дифференцированных клеток в анализе влияния величины дозы на дифференцировку. ФИГ.1E иллюстрирует процент дифференцированных клеток, рассчитанный относительно ФРН-индуцированной дифференцировки. Данные представляют собой средние значения ± среднеквадратическое отклонение из по меньшей мере трех экспериментов, каждый из которых был проведен в двух повторностях.
[0050] ФИГ.2 иллюстрирует действие соединений G79, G80 и G81 по стимулированию выживания клеток RN22. Представлены средние значения ± среднеквадратическая ошибка из трех экспериментов, каждый из которых был проведен в двух повторностях. *p<0,05, **p<0,01 (дисперсионный анализ; ANOVA) относительно контроля, подвергнутого стрессу.
[0051] ФИГ.3 иллюстрирует действие соединений G79, G80 и G81 в анализе стимулирования секреции (ФИГ.3A), в анализе синергической активности (ФИГ.3B), в анализе активации TrkA (ФИГ.3C), в анализе ингибирования передачи сигналов в присутствии ингибитора PI3K LY294002 (ФИГ.3D) и в анализе ингибирования передачи сигналов в присутствии ингибитора киназы MAPK PD98059 (ФИГ.3E). ФИГ.3F-3J иллюстрируют действие, показанное на ФИГ.3A-3E, соответственно, в виде процентов дифференцированных клеток, рассчитанных относительно ФРН-индуцированной дифференцировки.
[0052] ФИГ.4 иллюстрирует результаты для соединения G79 в модели глаукомы. ФИГ.4A иллюстрирует подсчет ганглионарных клеток сетчатки для контроля, плацебо, ФРН в концентрации 200 мкг/мл, соединения G79 в концентрации 200 мкг/мл и соединения G79 в концентрации 400 мкг/мл. ФИГ.4B иллюстрирует срезы сетчатки после обработки контролем, плацебо, ФРН в концентрации 200 мкг/мл, соединением G79 в концентрации 200 мкг/мл и соединением G79 в концентрации 400 мкг/мл. ФИГ.4C иллюстрирует подсчет ганглионарных клеток сетчатки для контроля, плацебо, соединения G79 в концентрации 200 мкг/мл, противоглаукомного препарата Тимолол и соединения G79 в концентрации 200 мкг/мл и Тимолола.
[0053] ФИГ.5 иллюстрирует результаты для соединений G79, G80 и G81 в модели болезни Паркинсона (ФИГ.5A) и в модели окислительного стресса (ФИГ.5B).
[0054] ФИГ.6 иллюстрирует полученные методом флуоресцентной детекции изображения результатов анализа посредством Вестерн-блоттинга клеток PC12, обработанных соединением G79 в концентрации 100 нг/мл.
[0055] ФИГ.7 иллюстрирует внутриклеточный сигнальный путь, активируемый путем фосфорилирования рецепторной тирозинкиназы (РТК).
[0056] ФИГ.8 иллюстрирует действие соединения G79 и BDNF на уровни активации фосфопротеинов ATF-2, HSP-27, JNK и STAT-1, исследованное с применением технологии Luminex.
[0057] ФИГ.9 иллюстрирует действие соединения G79 в цитометрическом анализе связывания согласно Примеру 13. ФИГ.9A иллюстрирует среднеканальную флуоресценцию (СКФ) в анализе конкурентного связывания на клетках PC12 (ФРН/G79-ФИТЦ). ФИГ.9B иллюстрирует СКФ в анализе конкурентного связывания на клетках PC12 (ФРН/G79-ФИТЦ) с применением антител против TrkA. ФИГ.9C иллюстрирует СКФ в анализе конкурентного связывания на клетках PC12 (ФРН/G79-ФИТЦ) с применением антител против р76. ФИГ.9D иллюстрирует СКФ в анализе конкурентного связывания на клетках SH-SY5Y (BDNF/G79-ФИТЦ).
[0058] ФИГ.10 иллюстрирует результаты для соединений G79, G80 и G81 в модели бокового амиотрофического склероза (БАС) in vitro.
[0059] ФИГ.11 иллюстрирует результаты для соединения G79, амида гарциниевой кислоты (Gambogic amide) и препарата Ксалипроден при профилактическом применении в модели PC in vivo после и.п. введения соединения G79 или амида гарциниевой кислоты (ФИГ.11A) и после перорального введения Ксалипродена (ФИГ.11B).
[0060] ФИГ.12 иллюстрирует результаты для соединения G79, амида гарциниевой кислоты и препарата Ксалипроден при лечебном применении в модели PC in vivo после перорального введения.
[0061] ФИГ.13 иллюстрирует действие соединения G79 в индукции фермента индуцибельной NO-синтазы (iNOS) в течение 48 часов.
[0062] ФИГ.14 иллюстрирует результаты для соединения G79 в модели нейровоспаления in vitro. ФИГ.14A иллюстрирует выработку ФНОα в органотипической культуре; мозжечка, а ФИГ.14B иллюстрирует выработку ИЛ-1β в органотипической культуре мозжечка.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0063] Один аспект изобретения основан на применении соединений Формул I-V и их фармацевтически приемлемых солей и пролекарств в качестве агонистов рецепторов нейротрофинов и, в особенности, агонистов рецепторов фактора роста нервов (ФРН) и рецепторов нейротрофического фактора головного мозга (BDNF). Благодаря указанному свойству, соединения Формул I-V и их фармацевтически приемлемые соли и пролекарства подходят для предотвращения или лечения заболеваний, отвечающих на стимулирование рецепторов нейротрофинов и, в особенности, фактора роста нервов или рецептора фактора роста нервов или нейротрофического фактора головного мозга или рецептора нейротрофического фактора головного мозга.
[0064] Соединения любой из Формул I-V демонстрируют достаточную ФРН-подобную активность "in vitro" посредством индукции дифференцировки клеток PC12 и стимулирования выживания клеток RN22 и, таким образом, обладают нейропротекторными свойствами.
[0065] Соединения согласно этому аспекту изобретения представляют собой соединения Формулы I:
и их фармацевтически приемлемые соли и пролекарства, где
[0066] R1 представляет собой фенил, замещенный галогеном или трифторметилом и дополнительно возможно замещенный одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-6алкила, (C1-6)алкокси и галоген(C1-6)алкила; или
[0067] R1 представляет собой пирролидин-1-ил;
[0068] R2 представляет собой 2-оксопирролидин-1-илметил или сульфамоилфенил; и
[0069] R3 выбран из пропила, 1-метилэтила, бутила, 2-метилпропила, пентила, 1-метилбутила, 2-метилбутила, гексила, 4-метилпентила, 3-метилпентила, 2-метилпентила и 1-метилпентила.
[0070] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R1 представляет собой фторфенил. В одном варианте реализации фторфенильная группа представляет собой 2-фторфенил, 3-фторфенил или 4-фторфенил. Предпочтительно, R1 представляет собой 2-фторфенил. В одном варианте реализации фторфенильная группа дополнительно замещена одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-6алкила, (C1-6)алкокси и галоген(C1-6)алкила; предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-4алкила, (C1-4)алкокси и галоген(C1-4)алкила; более предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, метила, этила, пропила, изопропила, метокси, этокси, фторметила и трифторметила.
[0071] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R1 представляет собой хлорфенил. В одном варианте реализации хлорфенильная группа представляет собой 2-хлорфенил, 3-хлорфенил или 4-хлорфенил. В одном варианте реализации R1 представляет собой 2-хлорфенил. В одном варианте реализации хлорфенильная группа дополнительно замещена одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-6алкила, (C1-6)алкокси и галоген(C1-6)алкила; предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-4алкила, (C1-4)алкокси и галоген(C1-4)алкила; более предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, метила, этила, пропила, изопропила, метокси, этокси, фторметила и трифторметила.
[0072] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R1 представляет собой бромфенил. В одном варианте реализации бромфенильная группа представляет собой 2-бромфенил, 3-бромфенил или 4-бромфенил. В одном варианте реализации R1 представляет собой 2-бромфенил. В одном варианте реализации бромфенильная группа дополнительно замещена одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-6алкила, (C1-6)алкокси и галоген(C1-6)алкила; предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-4алкила, (C1-4)алкокси и галоген(C1-4)алкила; более предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, метила, этила, пропила, изопропила, метокси, этокси, фторметила и трифторметила.
[0073] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R1 представляет собой йодфенил. В одном варианте реализации йодфенильная группа представляет собой 2-йодфенил, 3-йодфенил или 4-йодфенил. В одном варианте реализации R1 представляет собой 2-йодфенил. В одном варианте реализации йодфенильная группа дополнительно замещена одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-6алкила, (C1-6)алкокси и галоген(C1-6)алкила; предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-4алкила, (C1-4)алкокси и галоген(C1-4)алкила; более предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, метила, этила, пропила, изопропила, метокси, этокси, фторметила и трифторметила.
[0074] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R1 представляет собой трифторметилфенил. В одном варианте реализации трифторметилфенильная группа представляет собой 2-трифторметилфенил, 3-трифторметилфенил или 4-трифторметилфенил. Подходящие соединения включают те, в которых R1 представляет собой 2-трифторметилфенил. В одном варианте реализации трифторметилфенильная группа дополнительно замещена одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-6алкила, (C1-6)алкокси и галоген(C1-6)алкила; предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, C1-4алкила, (C1-4)алкокси и галоген(C1-4)алкила; более предпочтительно одним или двумя заместителями, выбранными из группы, состоящей из галогена, метила, этила, пропила, изопропила, метокси, этокси, фторметила и трифторметила.
[0075] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R1 представляет собой пирролидин-1-ил.
[0076] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R2 представляет собой 2-оксопирролидин-1-илметил.
[0077] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R2 представляет собой сульфамоилфенил. В одном варианте реализации сульфамоилфенильная группа представляет собой 2-сульфамоилфенил, 3-сульфамоилфенил или 4-сульфамоилфенил. Предпочтительно, R2 представляет собой 4-сульфамоилэтил.
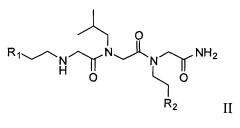
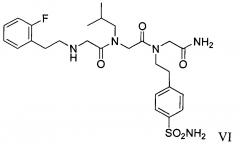
[0078] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формулы I, где R3 представляет собой 2-метилпропил, имеющие Формулу II:
и их фармацевтически приемлемые соли и пролекарства, где R1 и R2 имеют значения, определенные выше для Формулы I.
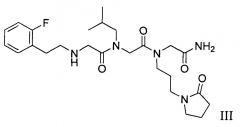
[0079] В одном варианте реализации соединения, подходящие согласно настоящему изобретению, представляют собой соединения Формул I-II и их фармацевтически приемлемые соли и пролекарства, где R1 представляет собой 2-фторфенил или пирролидин-1-ил и R2 представляет собой 2-оксопирролидин-1-илметил или 4-сульфамоилфенил, как указано ниже:
или
или
[0080] Предпочтительные соединения в соответствии с настоящим изобретением представляют собой соединения Формулы I, име