Способ синтеза наночастиц полупроводников
Иллюстрации
Показать всеИзобретение относится к коллоидной химии и нанотехнологии и может быть использовано в производстве люминесцентных материалов, сверхминиатюрных светодиодов, источников белого света, одноэлектронных транзисторов, нелинейно-оптических устройств, фоточувствительных и фотогальванических устройств. Синтезируют нанокристаллы из прекурсоров, содержащих халькоген и металл II или IV группы, в присутствии растворителя при комнатной температуре «двойным капельным методом», для чего указанные прекурсоры вводят одновременно по каплям при перемешивании. В качестве растворителя используют ионную жидкость или смесь ионных жидкостей в сочетании с одним или несколькими низкокипящими органическими растворителями. Реакционную смесь, содержащую ядра полупроводниковых квантовых точек, облучают УФ-светом и обрабатывают ультразвуком. Получают наночастицы халькогенидов металлов II или IV группы с дисперсией среднего размера не более 10 %, обладающие высокой фотостабильностью и агрегативной устойчивостью, способные диспергироваться как в полярных, так и в неполярных растворителях без дополнительных стадий обработки. При синтезе не используют токсичные растворители. 8 ил., 11 пр.
Реферат
Изобретение относится к получению наночастиц, полупроводниковых квантовых точек методом коллоидного синтеза в ионной жидкости, обладающих высокой агрегативной устойчивостью, фотостабильностью, дисперсией среднего размера наночастиц не более 10%, способных к диспергации, как в полярных, так и в неполярных растворителях без дополнительной обработки.
Данное изобретение может найти применение в производстве различных люминесцентных материалов, а также в качестве основы для производства сверхминиатюрных светодиодов, источников белого света, одноэлектронных транзисторов, нелинейно-оптических устройств, фоточувствительных и фотогальванических устройств.
На сегодняшний день широко применяются в основном три способа получения квантовых точек:
1. метод электронно-лучевой эпитаксии;
2. мосгидридная газофазовая эпитаксия;
3. метод коллоидного синтеза, и т.д.
Метод коллоидного синтеза обладает рядом преимуществ:
- возможность контролировать процесс роста наночастиц, например с помощью варьирования температурных параметров;
- возможность получать наночастицы в виде порошка;
- относительно невысокие температуры синтеза;
- метод позволяет синтезировать наночастицы с небольшим разбросом геометрических параметров (дисперсия среднего размера 5-10%);
Основой для современных способов коллоидного синтеза квантовых точек можно считать способ, предложенный в 1993 году Бавенди с соавторами (JACS, 115, 8706 (1993)). В типичном синтезе в реакционную колбу помещают координирующий растворитель - триоктилфосфиноксид, нагревают до 300°С в атмосфере аргона, а затем через септу шприцом вводят смесь диметилкадмия и триоктилфосфин селенида.
Недостатком способа является низкий квантовый выход флуоресценции за счет дефектности поверхности нанокристаллов, что приводит к появлению энергетических уровней, лежащих внутри запрещенной зоны. Эти уровни действуют как ловушки для электронов и дырок, что ухудшает люминесцентные свойства квантовых точек. Второй недостаток - применение токсичных органометаллических реагентов, самопроизвольно воспламеняющихся на воздухе.
Известен способ получения квантовых точек (RU №2497746, опубл 10.11.2013 г.), состоящий из нескольких стадий: смешивание амфифильного полимера, растворенного в некоординирующемся растворителе, с первым предшественником для получения карбоксилатного предшественника, смешивание карбоксилатного предшественника со вторым предшественником для получения ядра квантовой точки, смешивание ядра квантовой точки с предшественником, выбранным из группы, состоящей из: третьего предшественника, четвертого предшественника и их комбинации, для получения покрытия квантовой точки на ядре квантовой точки с образованием квантовой точки, где квантовая точка включает слой амфифильного полимера, размещенный на поверхности квантовой точки. Изобретение обеспечивает лучший контроль кинетики роста, возможность конструирования ширины запрещенной зоны и получение большого диапазона для испускания.
Недостатками данного способа являются высокая температура синтеза (от 200°С до 350°С), быстрое впрыскивание (нагнетание) одного из предшественников, зависимость рН раствора от применяемого некоординирующегося растворителя, применение токсичных органометаллических реагентов.
Также известен способ получения полупроводниковых квантовых точек, включающий высокотемпературный синтез нанокристаллов из прекурсора халькогенида VI группы и прекурсора металла II или IV группы с использованием органического растворителя и модификатора поверхности (US №7105051, 2006 г.). Это изобретение лучше предшественников, так как в нем не используются органометаллические прекурсоры, которые токсичны и пирофорны. При этом получаются квантовые точки высокого качества, малого размера и с узким распределением по размеру. При синтезе используется некоординирующий растворитель.
Недостатком способа является то, что несмотря на значительные успехи в совершенствовании оптических свойств КТ (квантовый выход, ширина пика флуоресценции) не удавалось добиться достаточной фотостабильности синтезируемых нанокристаллов. Предполагается, что при облучении полученных вышеописанными способами нанокристаллов УФ светом на воздухе произойдет значительное падение флуоресценции. Исключение - квантовые точки состава CdSe/ZnS, но при этом обязательно используются токсичные и пирофорные органометаллические прекурсоры. Это не позволяет проводить крупномасштабный синтез, что существенно снижает возможность широкого применения КТ в различных областях науки и техники.
Известен способ получения наночастиц методом синтеза в ионных жидкостях (RU 2404024, опубл. 20.11.2010 г.). Способ получения наночастиц включает введение ионной жидкости в камеру осаждения; вакуумирование камеры осаждения для образования вакуума в интервале от 1 и 7 микрон ртутного столба; распыление одного или более катодов в камере осаждения для направления одного или более материалов по направлению к ионной жидкости для образования наночастиц в ионной жидкости.
Недостатком данного способа является сложность технологического процесса, необходимость использования высокого вакуума, а также применение токов высокого напряжения и мощности.
В качестве ближайшего аналога (прототипа) выбран способ синтеза квантовых точек на основе халькогенидов металлов II или IV группы, включающий синтез ядер нанокристаллов из прекурсора, содержащего халькоген, и прекурсора, содержащего металл II или IV группы, с использованием органического растворителя и модификатора поверхности, в качестве которого используют (аминоалкил) триалкоксисиланы (RU №2381304, опубл. 10.02.2010). Синтез ядер осуществляют при постоянной температуре в пределах от 150 до 250°С в течение от 15 с до 1 часа и дополнительно проводят обработку реакционной смеси, содержащей ядра нанокристаллов, УФ-светом в течение 1÷10 мин и ультразвуком в течение 5÷15 мин.
К недостаткам ближайшего аналога (прототипа) следует отнести поддержание постоянной температуры в пределах 150-230°С, использование в качестве модификатора поверхности (3-аминопропил)триметоксисилан, (3-аминопропил)триэтоксисилан, а в качестве органического растворителя непредельные высококипящие углеводороды, например октадецен, сквален, а также дифенилы, терфенилы, дифениловый эфир или их производные.
Во всех вышеописанных способах в процессе синтеза квантовых точек используются высококипящие токсичные органические растворители, а также существует необходимость поддержания высоких температур (150-250°С) для получения квантовых точек.
Задачей изобретения, направленной на устранение отмеченных недостатков, является получение методом коллоидного синтеза при низких температурах с использованием малотоксичных растворителей, обладающих высокой агрегативной устойчивостью, фотостабильностью, полупроводниковых квантовых точек с дисперсией среднего размера наночастиц не более 10%, способных диспергироваться как в полярных, так и в неполярных растворителях без дополнительных стадий обработки.
Поставленная задача решается за счет того, что заявленный способ получения полупроводниковых квантовых точек на основе халькогенидов металлов II или IV группы включает синтез нанокристаллов из прекурсора, содержащего халькоген, и прекурсора, содержащего металл II или IV группы, в присутствии растворителя с дополнительным облучением УФ-светом и воздействием ультразвука. При этом синтез наночастиц осуществляют при комнатной температуре «двойным капельным методом». В качестве растворителя используют ионную жидкость или смесь ионных жидкостей в сочетании с одним или несколькими низкокипящими органическими растворителями.
Технический результат заключается в сокращении числа необходимых для синтеза реагентов, времени синтеза, проведении синтеза при комнатной температуре, в получении наночастиц, дисперсия среднего размера которых не более 10%.
Сущность изобретения поясняется чертежами, на которых изображено:
На фиг. 1 - представлены данные по размерам наночастиц сульфида цинка, рассчитанные из УФ-спектров поглощения, где D - диаметр частиц ZnS, нм; Cm(ZnS) - молярная концентрация частиц ZnS в золе, моль/л.
На фиг. 2 - представлены спектры поглощения наночастиц сульфида цинка 1, где D - оптическая плотность, относит. ед.; λ - длина волны излучения, нм.
На фиг. 3 представлены данные по размерам наночастиц сульфида цинка полученные методом динамического светорассеяния (ДСР), где D - диаметр частиц ZnS; Accumulation time - время накопления, с.
На фиг. 4 представлен рельеф поверхности наночастиц сульфида цинка, полученных в ионной жидкости - N-децилпиридиний тетрафторборате.
На фиг. 5 представлены данные динамического светорассеяния золей квантовых точек, полученные в ионной жидкости.
На фиг. 6 представлены данные динамического светорассеяния золей квантовых точек, полученные в ионной жидкости - N-децилпиридиний метилсульфате.
На фиг. 7 представлены данные динамического светорассеяния золей квантовых точек, полученные в ионной жидкости - 1-бутил-3-метилимидазолий тетрафторборате.
На фиг. 8 представлены данные динамического светорассеяния золей квантовых точек, полученные в ионной жидкости - N-децилпиридиний тетрафторборате.
Суть предложенного метода заключается в том, что синтез проводится по «двойному капельному методу» с использованием ионных жидкостей. «Двойной капельный метод» кардинально отличается от известных аналогов тем, что прекурсоры для синтеза наночастиц вводятся в реакционную смесь одновременно по каплям при интенсивном перемешивании в отличие от известных вышеописанных аналогов, где прекурсоры вводятся последовательно. Благодаря использованию ионных жидкостей в совокупности с «двойным капельным методом» достигается технический результат.
Готовят смесь, содержащую ионную жидкость (тетрафторборат N-децилпиридиния), ацетон и этилацетат. Реагенты (ZnSO4 и Na2S) в виде водных 0.5М растворов добавляют в реакционную смесь при комнатной температуре по каплям при постоянном перемешивании. За счет образования нерастворимого соединения (наночастиц) реагенты выводятся из реакционного объема. Поэтому синтез каждой новой порции частиц происходит в одинаковых условиях при низкой концентрации прекурсоров, и при этом удается достичь высокой концентрацию наночастиц полупроводника в золе.
Достижение высокой устойчивости золей наночастиц и дисперсии среднего размера наночастиц не более 10%, сохранение или повышение квантового выхода вызвано наличием в молекулярной структуре ионных жидкостей упорядоченных структур (домены, цепочки и др.). При введении прекурсоров (например, водных растворов ZnSO4 и Na2S) в раствор ионной жидкости взаимодействие между ионами Zn2+ и S2- происходит преимущественно в полярных областях (доменах) молекулярной структуры ионной жидкости, которая имеет наномасштабные размеры. Протекание реакции в таких областях (доменах) приводит к тому, что рост наночастиц образующегося ZnS ограничен размерами этих доменов. Кроме того, в этих условиях сильно затруднено взаимодействие наночастиц друг с другом, и, как следствие, для золей полученных в растворах ионных жидкостей наблюдается высокая агрегативная устойчивость.
В качестве реагентов для синтеза наночастиц полупроводников (халькогениды металлов II или IV группы) в данном изобретении используется прекурсор, содержащий халькоген, и прекурсор, содержащий металл II или IV группы. В качестве среды для синтеза наночастиц используется широкий ряд ионных жидкостей в присутствии различных низкокипящих органических растворителей.
В отдельных случаях, в качестве прекурсоров металла II или IV группы используют прекурсоры цинка, кадмия, ртути, свинца.
В частном случае, в качестве прекурсора, содержащего халькоген, используют прекурсоры, содержащие серу, селен, теллур.
При синтезе наночастиц полупроводников проводится дополнительное облучение УФ-светом с длинной волны 254 нм и мощностью 30 Вт, а использование ультразвука с мощностью 150 Вт и частотой 25 кГц позволяет повысить квантовый выход и фотостабильность. Облучение УФ-светом снижает количество дефектов на поверхности полупроводниковой квантовой точки, а обработка ультразвуком позволяет достичь более высокой степени дезагрегации ядер полупроводниковых квантовых точек, что, в свою очередь, приводит к более однородному нарастанию оболочки. Это позволяет получать более однородные по размерам полупроводниковые квантовые точки с более высокой фотостабильностью.
В качестве органических растворителей в синтезе наночастиц полупроводников в дополнение к ионной жидкости используются различные полярные низкокипящие органические растворители в качестве сорастворителя. Выбор сорастворителя зависит от природы и структуры ионной жидкости, а также от ее физико-химических параметров (вязкость, плотность и др.). В качестве сред для синтеза наночастиц полупроводников могут выступать смеси ионных жидкостей.
Примеры используемых сорастворителей: низшие алифатические спирты (например, метанол, этанол), низшие кетоны (например, ацетон, метилэтилкетон), сложные эфиры ароматических и алифатических кислот и низших спиртов (например этиловый эфир уксусной кислоты), диметилформамид, диметилсульфоксид, хлороформ, четыреххлористый углерод, ацетонитрил и другие.
Ионные жидкости - это соли, полностью состоящие из ионов, жидкие при комнатной температуре или близкие к ней температуре, как правило, с объемными органическими катионами и неорганическими анионами. Они могут быть использоваться как высокополярные растворители в препаративной химии, как катализаторы, каталитические среды, растворители для синтеза полимеров. В состав ионной жидкости входит объемный органический катион аммония, пиридиния, фосфония, сульфония, имидазолия, пиперидиния, морфолиния, гуанидиния, пирролидиния, холиния, пиперазиния и др. и моно- или полиатомные анионы типа: Cl-, Br-, I-, FeCl4- ClO4-, NO3-, BF4-, PF6-, SbF6-, RSO3-, Al2Cl7- и др.
Количество ионных жидкостей, описанных в литературе, в настоящее время очень велико (около 500). К числу ионных жидкостей можно отнести и все известные поверхностно-активные вещества катионного типа, имеющие не симметричное строение, хотя до настоящего времени их так не называли.
Повышенное внимание к ионным жидкостям, прежде всего, определяется их негорючестью, невзрывоопасностью, нетоксичностью и этим обусловливается отсутствие вредного воздействия на окружающую среду, кроме того, они нелетучие (в силу давления насыщенного пара, близкого к нулю), что позволяет их многократно использовать. Ионные жидкости имеют широкий интервал жидкого состояния (>300°С) и низкие температуры плавления (<100°С); для сравнения вода и органические растворители находятся в жидком состоянии в значительно узком диапазоне - около 100°С, что затрудняет их использование.
Важным свойством ионных жидкостей является их высокая удельная электропроводность; хорошая растворяющая способность по отношению к разнообразным неорганическим, металлоорганическим и органическим соединениям; каталитическая активность, обуславливающая повышение селективности органических реакций и выход целевого продукта.
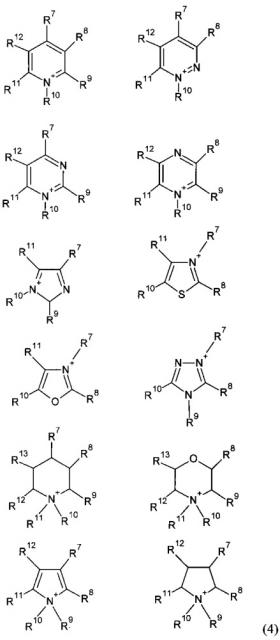
В качестве ионной жидкости для синтеза наночастиц полупроводников могут выступать соединения следующего состава и структуры:
Органические катионы в составе ионной жидкости:
где R1 и R2 - алкильные группы с количеством углеродных атомов от 1 до 16, могут быть одинаковыми, а могут отличаться по длине друг от друга, или атомы водорода.
где R3, R4, R5, R6 независимы друг от друга и представляют собой алкильную группу, арильную, гетероциклическую и алкиларильную соответственно. Группы R3, R4, R5, R6 каждая может содержать заместитель и гетероатом в структуре; R3, R4, R5, R6 могут быть соединены друг с другом с образованием одного или более колец, и, кроме того, R3, R4, R5, R6 могут быть связаны с R3, R4, R5, R6 соседнего катиона, образуют полимерную форму.
Примеры алкильной группы включают линейные разветвленные алкильные группы, или цепь, имеющую не более 30 атомов углерода, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутиловый, трет-бутил, пентил, гексил, гептил, октил, нонил и децил. Примеры арильной группы включают фенил, нафтил, толил и ксилил; арильная группа может иметь один или несколько заместителей, таких как атомы галогена (F, Cl, Br, I), гидроксильную группу, алкокси-группу (такую, как метокси, этокси, пропокси и бутокси), карбоксильную группу, ацетильную группу, пропаноильную группу, тиольную группу, алкилтиогруппы (например, метилтио, этилтио, пропилтио и бутилтио), аминогруппы, алкиламиногруппы и диалкиламиногруппы. Примеры гетероциклических групп включают пиридил, тиенил, имидазолил, пиразолил, оксазолил, изоксазолил, пирролидинил, пиперазинил и морфолил. Примеры арилалкильной группы включают бензил и фенетил. Кроме того, R3, R4, R5, R6 могут быть кольцом, таким как пирролидиний и пиперидиний, образованным связыванием между R3, R4, R5, R6 в одной молекуле, и дополнительно может быть цепь, такая, например, как структура (3).
В представленных выше формулах (4) R7-R13 могут быть одинаковыми или отличными друг от друга; R7-R13 непосредственно связаны одинарной или двойной связью, и независимо друг от друга один или несколько заместителей могут быть замещены на атом водорода или атомы галогенов. В алкильной группе может быть частично или полностью замещены атомы водорода на другие алкильные или арильные группы или атомы галогена.
Примеры алкильной группы включают линейные разветвленные алкильные группы, или цепь, имеющую не более 30 атомов углерода, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутиловый, трет-бутил, пентил, гексил, гептил, октил, нонил и децил. Примеры арильной группы включают фенил, нафтил, толил и ксилил; арильная группа может иметь один или несколько заместителей, таких как атомы галогена (F, Cl, Br, I), гидроксильную группу, алкокси-группу (такую, как метокси, этокси, пропокси и бутокси), карбоксильную группу, ацетильную группу, пропаноильную группу, тиольную группу, алкилтиогруппы (например, метилтио, этилтио, пропилтио и бутилтио), аминогруппы, алкиламиногруппы и диалкиламиногруппы. Примеры гетероциклических групп включают пиридил, тиенил, имидазолил, пиразолил, оксазолил, изоксазолил, пирролидинил, пиперазинил и морфолил. Примеры арилалкильной группы включают бензил и фенетил.
В качестве примеров органических катионов можно привести следующие: триметилгексиламмоний, триметилфениламмоний, триметилциклогексиламмоний, диметилэтилгексиламмоний, тетраэтиламмоний, триметилбензиламмоний, триметилвиниламмоний, триметил(метоксикарбонилметил)аммоний, триметилэтиламмоний, триметил(гидроксиэтил)аммоний, триэтилметиламмоний, диэтилметилгексиламмоний, триметил(пентаметилфенил)аммоний, триэтилбензиламмоний, N-метил-N-бутилпиперидиний, N,N-диметилпиперидиний, N-метил-N-пропилпиперидиний, N-метил-N-бутилпирролидиний, N-метил-N-пропилпирролидиний, N,N-диметилпирролидиний, триметилгексилфосфоний, триметилфенилфосфоний, триметилциклогексилфосфоний, диметилэтилгексилфосфоний, тераэтилфосфоний, триметилбензилфосфоний, N-делилпиридиний, N-метил-N-гексилморфолиний и соли фосфония, представленные ниже (5):
где R14 и R15 одинаковые или разные алкильные заместители с длинной углеродной цепью от 1 до 12 атомов, R14 или R15 могут быть водородными атомами.
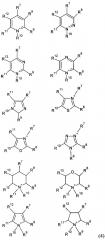
В качестве анионов в ионных жидкостях, используемых для синтеза наночастиц полупроводников, могут выступать следующие:
В структуре (6) заместители R16 и R17 содержат галоген, связанный с концевым атомом в заместителе. Заместители R16 и R17 содержат фтор, хлор или бром. Особенно предпочтительным является наличие атома фтора. Кроме того, когда R16 и R17 представляют собой галогенированный алкил, предпочтительным является галогенированный алкил, имеющий от 1 до 3 атомов углерода, и специфические примеры предпочтительных галогенированных алкильных групп включают трифторметильную группу, пентафторэтильную группу и группу гептафторпропил. Галогенированные алкильные группы могут быть одинаковыми или отличными друг от друга. Примерами таких анионов могут служить структуры (7)
где R18 представляет собой атом водорода, C1-С10-алкильную группу, С3-С10-циклоалкильную группу, фенильную группу, гидроксильную группу, меркаптогруппу, аминогруппу, карбоксильную группу, тетразолил или группу сульфоновой кислоты, и каждая из групп, за исключением атома водорода, может иметь один или несколько заместителей.
где R18 и R19 представляют собой атом водорода, C1-С10-алкильную группу, С3-С10-циклоалкильную группу, фенильную группу, гидроксильную группу, меркаптогруппу, аминогруппу, карбоксильную группу, тетразолил или группу сульфоновой кислоты, и каждая из групп, за исключением атома водорода, может иметь один или несколько заместителей.
Анион в структуре ионной жидкости может быть и неорганической природы: NO3- CN-, SCN-, NO2-, Hal-, PF6-, BF4-, B4O72-, [B(OR)4]-, PO43-, HPO42-, H2PO4-, O=P(OR)2O-, S2-, HS-, SO42-, ClO4-, SbF6-, HSO4-, MeHal4-, MeHal42-,
где Hal-: F, Cl, Br, I,
Me: Al, Fe, Ni, Co, Mn, Cu, Zn,
R - алкильные заместители одинаковые или разные с длиной углеродного фрагмента от 1 до 12 атомов.
В способе получения квантовых точек (RU №2381304, опубл. 10.02.2010) был изменен метод получения квантовых точек с «метода горячего впрыска» на «двойной капельный метод», а кремнийорганические модификаторы, высококипящие и токсичные, например, (3-аминопропил)триметоксисилан, были заменены на ионные жидкости.
Синтез наночастиц осуществляется «двойным капельным методом» при комнатной температуре в течение 30 сек - 3 мин, в качестве растворителя используется ионная жидкость в сочетании с низкокипящими органическими растворителями, затем проводится облучение УФ-светом в течение 2-х мин при длине волны 254 нм и мощности 30 Вт, далее 3 мин воздействуют ультразвуком с мощностью 150 Вт и частотой 25 кГц.
Возможность осуществления заявляемого изобретения подтверждается следующими примерами.
Пример 1. Синтез наночастиц ZnS в ионной жидкости N-децилпиридиний тетрафторборате.
В круглодонную колбу на 50 мл снабженную механической мешалкой помещают 15 мл ионной жидкости (N-децилпиридиний тетрафторбората), которую растворяют в 15 мл смеси ацетона и этилацетата. В данную смесь по каплям при постоянном перемешивании и температуре 25°С одновременно приливают свежеприготовленные водные 0,5М растворы сульфата цинка и сульфида натрия. Реакционная смесь, содержащая ядра полупроводниковых квантовых точек, подвергается обработке УФ-светом1 (2 мин) и ультразвуком2 (3 мин). Далее полученные квантовые точки диспергируются в неполярный или полярный растворитель.
Зависимость размеров цинксодержащих квантовых точек от концентрации частиц в золе представлена на Фиг. 1. Спектры поглощения цинксодержащих квантовых точек приведены на Фиг. 2. Максимумы в спектрах поглощения соответствуют размерам квантовых точек 5,5-6,0 нм. Данные динамического светорассеяния золей квантовых точек представлены на Фиг. 3. Рельеф поверхности квантовых точек, выделенных из золя путем осушки последнего, представлен на Фиг. 4.
[1Обработка УФ-светом осуществляется при помощи ультрафиолетовой лампы, длина волны 254 нм, мощность 30 Вт.
2Обработка ультразвуком осуществляется при помощи ультразвуковой мойки Techpan TYPE UM-2, рабочая частота 25кГц, мощность 150 Вт].
Пример 2. Синтез наночастиц ZnS в ионной жидкости N-децилпиридиний метилсульфате.
Выполняется аналогично примеру 1, но в качестве ионной жидкости берется N-децилпиридиний метилсульфат, в качестве органических растворителей используется смесь хлороформа с диэтиловым эфиром.
Данные динамического светорассеяния золей квантовых точек представлены на Фиг. 5. Размер наночастиц 5,5 нм.
Пример 3. Синтез наночастиц CdS в ионной жидкости 1-бутил-3-метилимидазолий гексафторфосфате.
Выполняется аналогично примеру 1, но в качестве ионной жидкости берется 1-бутил-3-метилимидазолий гексафторфосфат, в качестве реагента, содержащего ион металла, - хлорид кадмия (II), в качестве органических растворителей используется смесь ацетонитрила с ацетоном.
Данные динамического светорассеяния золей квантовых точек представлены на Фиг. 6. Размер наночастиц 3,5 нм.
Пример 4. Синтез наночастиц CdS в ионной жидкости 1-октил-3-бутилимидазолий тетрафторборате.
Выполняется аналогично примеру 1, но в качестве ионной жидкости берется 1-октил-3-бутилимидазолий тетрафторборат, в качестве реагента, содержащего ион металла, - хлорид кадмия (II), в качестве органических растворителей используется смесь метанола с диметилформамидом.
Пример 5. Синтез наночастиц ZnSe в ионной жидкости 1-бутил-3-метилимидазолий тетрафторборате.
Выполняется аналогично примеру 1, но в качестве ионной жидкости берется 1-бутил-3-метилимидазолий тетрафторборат, в качестве реагента, содержащего халькоген, - селенид натрия (II), в качестве органических растворителей используется смесь метилэтилкетона и этилацетата. Данные динамического светорассеяния золей квантовых точек представлены на Фиг. 7. Размер наночастиц 6,5 нм.
Пример 6. Синтез наночастиц PbS в ионной жидкости N-децилпиридиний тетрафторборате.
Выполняется аналогично примеру 1, но в качестве реагента, содержащего металл, используется нитрат свинца (II), в качестве органических растворителей используется смесь диметилсульфоксида с этанолом. Данные динамического светорассеяния золей квантовых точек представлены на Фиг. 8. Размер наночастиц 5,0 нм.
Пример 7. Синтез наночастиц PbSe в ионной жидкости 1-октил-3-бутилимидазолий тетрафторборате.
Выполняется аналогично примеру 1, но в качестве ионной жидкости берется 1-октил-3-бутилимидазолий тетрафторборат, в качестве реагента содержащего металл используется нитрат свинца (II), в качестве реагента, содержащего халькоген, - селенид натрия (II), в качестве органического растворителя используется ацетонитрил.
Пример 8. Синтез наночастиц ZnSe в ионной жидкости 1-додецил-β-пиколиний тетрафторборате.
Выполняется аналогично примеру 1, но в качестве ионной жидкости берется 1-додецил-β-пиколиний тетрафторборат, в качестве реагента, содержащего металл, используется сульфат цинка (II), в качестве реагента, содержащего халькоген, - селенид натрия (II), в качестве органического растворителя используется ацетонитрил. Размер наночастиц 4,5-5,0 нм.
Пример 9. Синтез наночастиц ZnTe в ионной жидкости 1-додецил-β-пиколиний гексафторфосфате.
Выполняется аналогично примеру 1, но в качестве ионной жидкости берется 1-додецил-β-пиколиний гексафторфосфат, в качестве реагента, содержащего металл, используется сульфат цинка (II), в качестве реагента, содержащего халькоген, - телурид натрия, в качестве органического растворителя используется метилэтилкетон. Размер наночастиц 5,0-5,5 нм.
Пример 10. Синтез наночастиц CdS в смеси ионных жидкостей 1-октил-3-бутилимидазолий тетрафторбората и N-децилпиридиний тетрафторбората.
Выполняется аналогично примеру 1, но используется смесь ионных жидкостей 1-октил-3-бутилимидазолий тетрафторбората и N-децилпиридиний тетрафторбората, в качестве реагента, содержащего ион металла, - хлорид кадмия (II), в качестве органических растворителей используется смесь ацетона с этилацетатом. Размер наночастиц 6,0-6,5 нм.
Пример 11. Синтез наночастиц ZnS в смеси ионных жидкостей 1-бутил-3-метилимидазолий гексафторфосфата и N-децилпиридиний гексафторфосфата.
Выполняется аналогично примеру 1, но используется смесь ионных жидкостей 1-бутил-3-метилимидазолий гексафторфосфата и N-децилпиридиний гексафторфосфата, в качестве реагента, содержащего ион металла, - сульфат цинка (II), в качестве органических растворителей используется смесь ацетона с этилацетатом. Размер наночастиц 6,0 нм.
Приведенные примеры показывают возможность получения наночастиц полупроводников в присутствии ионных жидкостей и одного или нескольких низкокипящих органических растворителей. При этом синтез наночастиц проводников существенно не зависит от вида низкокипящих растворителей.
Полученные описанным способом наночастицы полупроводников позволяют сделать вывод об эффективности предложенного метода синтеза. Возможно получение субкилограммовых количеств наночастиц.
Наночастицы полупроводников, полученные описанным способом, могут быть использованы для производства фотодетекторов в инфракрасной области, солнечных батарей, источников белого света, одноэлектронных транзисторов и нелинейно-оптических устройств, сверхминиатюрных светодиодов, а также в медицине в качестве оптических сенсоров, флуоресцирующих меток.
Способ получения полупроводниковых квантовых точек на основе халькогенидов металлов II или IV группы, включающий синтез нанокристаллов из прекурсора, содержащего халькоген, и прекурсора, содержащего металл II или IV группы, в присутствии растворителя с облучением УФ-светом, обработкой ультразвуком, отличающийся тем, что синтез наночастиц осуществляют при комнатной температуре «двойным капельным методом», в качестве растворителя используют ионную жидкость или смесь ионных жидкостей в сочетании с одним или несколькими низкокипящими органическими растворителями.